4
ю
4
оо оо




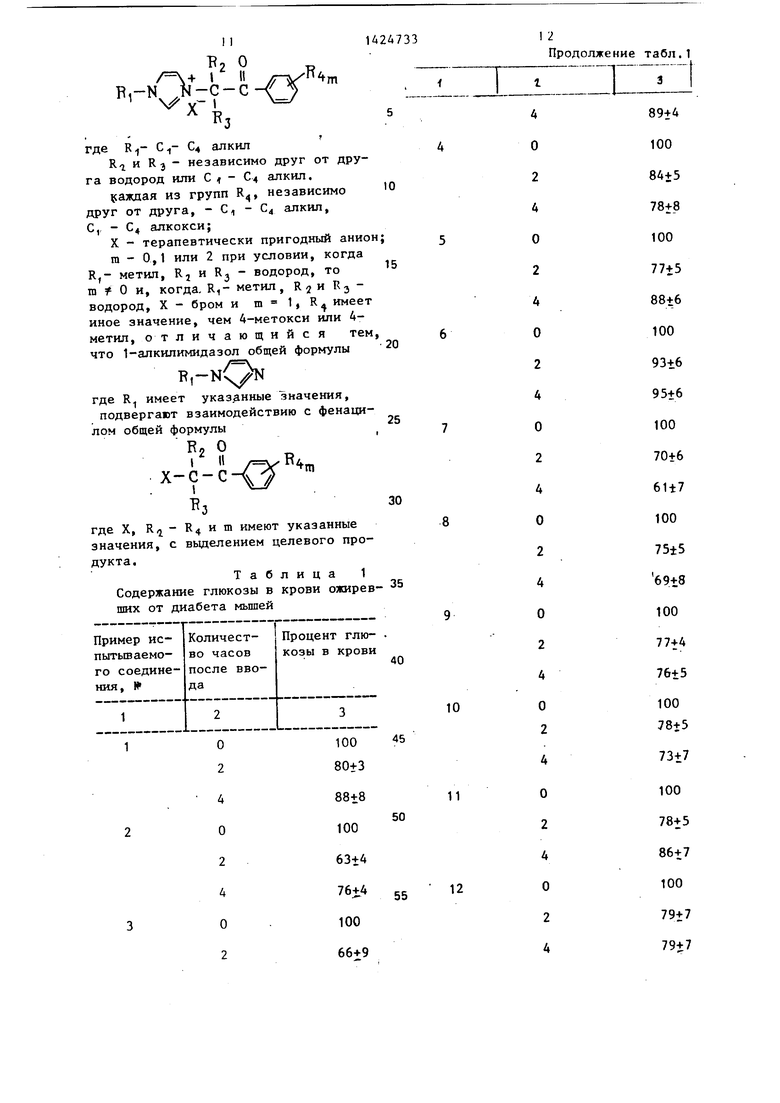

Изобретение относится к способу получения солей имидазола формулы .. Г B,-N ..Л-С-С R l,, V V- I в. с, R И R J не- или алкил независигде Kj - алкил v., - t., r, зависимо друг от друга - И С,- 64; каждая из групп R МО друг от друга С - С алкил, С i С4 алкокси, X - терапевтически пригодный анион; m равно 0,1 или 2, когда R, - метил, R иRj-H, то когm имеет значение иное. 3 чем О и, да RI - метил; R и R - Н; X - Вг и m равно 1, R., имеет иное значение, чем 4-метокси или 4-метил, которые могут быть использованы в медицине. Получение целевых соединений ведут взаиь одействием 1-алкилимидазола и фенацила с выделением целевого продукта. 2 табл. «о СП
СП
Изобретение относится к способу получения новых солей имидазола, которые могут быть использованы для лечения диабета.
Цель изобретение - получение новы солей имидазола, которые Б отличие от структурного аналога обладают гипогликемическнм действием.
Пример 1. 1-Метил-3-Г2-(А- метилфенил)-2-оксоэтил -1Н-имидазол- бромид.
В раствор 10,6 г (0,05 моль) 1- бром-2-(А-метилфенил)-2-оксоэтана в 150 мл простого дизтилового эфира вводят 4,18 г (0,051 моль) 1-метил- имидазола. Реакционную смесь перемешивают примерно 3 ч при комнатной температуре и выпавший в осадок твердый продукт извлекают путем фильтра- ции. nony4etrHoe гигроскопическое твердое вещество перекристаллизовыва- ется из смеси метанол-этилацетат и в результате получается 4,82 г 1- метил-3-Г2-(4-метилфенил)-2-оксоэтил -1Н-имидазолбромида в виде твердого вещества. Вторая порция продукта получается из фильтрата, и дополнительный выход этого продукта составляет 5,8 г.
Выход 72%, т. пл. 148-15ГС.
Рассчитано,%: С 52,90; Н 5,12; N 9,49.
С,,,Н jBrNjO.
Найдено,%: С 52,73; Н 4,95; N 9,26.
Пример 2, 1-Метил-3-Г2(-3- метоксифенил)-2-оксоэтил -1Н-имида- золбромид.
Раствор 4,58 г (0,02 моль) 1-бром -2-(3-метоксифенил)-2-оксоэтана в 100 мл простого диэтилового эфира фильтруют, фильтрат оборабатывают 1,82 г (0,022 моль) 1,-метш1Ими,цазола Полученную реакционную смесь перемешивают при комнатной температуре приблизительно 19 ч, после чего раствор декантируют и осадок промывают простым диэтиловым эфиром. Этот осадок растворяют в горячем ацетонитри- ле и после охлаждения из раствора осаждаются темные иглы. Полученное твердое вещество извлекают и двукратно перекристаллизовывают из смеси ацетонитрил/этилацетат, в результате чего получается 2,1 г 1-метил-З- 2- (3-метоксифенил)-2-оксоэтил -1Н-ими- дазолбромида в виде белых игл.
Выход 34%, т. пл. 1б7-17Гс.
g
5 0 5 0
0 5
5
0
5
Рассчитано,%: С 50,18; Н 4,86; N 9,00; Вг 25,68.
С,зН ,BrN,Oj.
Найдено,%: С 49,89; Н 4,75; N 8,98; Вг 25,56.
Н р и м е р 3. 1-Метш1-3-Г2(3- этoкcифeнил)-2-oкcoэтилJ-1H имидазол- бромид.
Раствор 2,9 г (0,012 моль) 1-5ром- 2-(3-этоксифенил)-2-оксоэтана в 20 мл ацетоиит рила смешивают с 1 ,03 г (0,013 моль) 1-метилимидазола и полученную смесь перемешивают при комнатной температуре примерно 18 ч. Смесь разбавляют метанолом и летучие вещества испаряются при пониженном давлении до объема примерно 15 ьш. Дан- ньй раствор разбавляют этилацетатом и твердый коричневый осадок извлекают путем фильтрации. Извлгченное твердое веществр промывают этилацетатом и растворяют в ацетонитриле. Смесь очищают древесным углем, и после охлаждения извлекают твердое вещество. Это твердое вещество перекристаллизовывают из смеси ацетонит- рил/простой диэтиловый эфир и в результате получают две порции, которые смешивают и перекристаллизовывают три раза Из изопропилового спирта, D результате чего получают 0,27 г 1-метил-3-Г2-(3-этоксифенил)-2-оксоэтил - 1Н-имидазолбромида в виде бледно-желтых хлопьев.
Выход 7%, т. пл. 137-138°С.,
Рассчитано,%: С 51,71; Н 5,27; N 8,61; Вг 24,57.
С Н Н п BrN 0 .
Найдено,%: С 51, 54; Н 5,01; . N 8,40; Вг 24,80.
Пример 4. |-Метил-3-(1,1-ди- метил-2-фенил-2-оксоэтил)-1Н-имида- золбромид.
Раствор 4,6 г (0,02 моль) с -бром- изобутирофенона и 1,8 г (0,022 моль) 1-метилимидазола в 30 мл простого диэтилового эфира перемешивают при комнатной температуре примерно 48 ч. Растворитель декантируют и полученное масло суспензируют в этилацетате. Растворитель снова декантируют и осадок растворяют в ацетонитриле до ввода небольшого количества этилаце- тата. Полученный белый осадок извлекают путем фильтрации и перекристал- лизовывшот из смеси метанол/этилаце- тат, в результате чего получают 3,88 г 1-метил-3-(151-диметил-2да в виде блестяп1их белых чешуек.
Выход 63%, т. пл. 137-140°С.
Рассчитано,%: С 54,38; II 5,54; N 9,06; Вг 25,84.
C,,H,, .
Найдено,%: С 54,25; Н 5,82; N 8,87; Вг 25,67.
Пример 5. 1-Метил-3-Г2-(4- этилфеиил)-2-оксоэтил -1Н-имидазол- бромид.
Раствор 4,41 г (0,019 моль)1-бром 2-(4-этилфенил)-2-оксоэтана и 1,65 г (0,02 моль) 1-метилимидазола в 40 мл простого диэтилового эфира перемешивают при комнатной температуре приблизительно 18 ч. Растворитель реакционной смеси декантируют и осадок промывагот прос:тым диэтиловым эфиром и растворяют в небольшом количестве ацетонитрила. Полученный в результате раствор разбавляют небольшим количеством этилацетата, после чего образуется коричневьш осадок. Твердое вещество извлекают и перекристал лизоБывают из смеси ацетонитрил/этил- Iацетат, в результате чего получают 2,26 г 1-метил-3-.2-(4-этилфепил - 2-оксо-этил -1Н-имидазолбромида в виде тонких желто-коричневых игл.
Выход 38%, т. пл. 177--:79 С.
Рассчитано,%: С 54,38; Н 5,54; N 9,06; Вг 25,54.
С,,Н,,Вг
Найдено,%: С 5,13; Н 5,81; N 9,04; Вг 26,05.
Пример 6. 1-Метил-3- 2-(2- метилфенил)-2-оксоэтш1 J-1В-имидазол- бромид.
Раствор 4,22 г (0,02 моль) 1-бром 2-2-метилфепил-2-оксоэтана, 2,64 (0,032 моль) 1-метили1-1Идазсла и 60м простого диэтилового эфира перемешивают при комнатной температуре примерно 17 ч. Растворитель реакционной смеси декантируют и осадок промывают простым диэтиловым эфиром. Этот осадок растворяют в горячем ацетонитри- ле и полученный раствор охлаждают и разбавляют простым диэтиловым эфиром Твердый продукт извлекают и его двукратно перекристаллизовывают из смеси ацетонитрил/простой диэтиловый эфир, в результате чего получают 1,99 г 1-метил-З- 2-(2-метилфенил)- 2-оксоэтил }-1Н-имидазолбромида в виде белых игл.
Выход 34%, т. пл. 152-154 с.
N 9,49; Вг 27,07.
.
Найдено,%: С 52,82; Н 5,28; N 9,54; Вг 27,14.
Пример 7. 1-Метил-3-(1- метил-2-фенил-2-оксоэтил)-1Н-имида- золбромид,
0 Раствор 8 мл (0,047 моль) 90%- ного чистого 1-фенил-l-OKCo-2-бром- пропана и 4,25 г (0,052 моль) 1- метилимидазола в 100 мл простого диэтилового эфира перемешивают при ком- 5 натной температуре примерно 24 ч. Осажденное твердое вещество извлекают путем фильтрации, промывают простым диэтиловым эфиром и растворяют в метаноле. Этот раствор разбавляют Q простым диэтиловым эфиром и полученное белое твердое вещество извлекают путем фильтрации. Данное твердое вещество перекристаллизовывают из смеси метанол/простйй диэтиловый 5 эфир, в результате чего получают
7,65 г 1-метил-3-(1-метил-2-фенил-2- оксоэтил)-1Н-имидазолбромида в виде белых кристаллов.
Выход 55%, т. пл. 1б7-170°С.
Рассчитано,%: С 52,90; Н 5,12;
0
N 9,49.
С,Н .
0
1 15
Найдено,%: С 52,73; Н 4,95; N 9,26.
Пример 8. 1-Метил-З-П- метил-2-(4-метилфенил)-2-оксоэтил - 1Н-имидазолбромид.
Раствор 2,24 г (0,01 моль)1-(4- метилфенил)-1-оксо-2-бромпропана и 0,9 г (0,011 моль)1-метилимидазола в 50 мл простого диэтилового эфира перемешивают при комнатной температуре приблизительно 18 ч. Растворитель реакционной смеси декантируют и осадок промывают простым диэтиловым эфиром и растворяют в ацетонитриле. Полученный раствор разбавляют простым диэтиловым эфиром, -и осажденный твердый продукт извлекают путем фильтраьщи. Этот твердый продукт перекристалпизовывают из смеси ацетонитрил/простой диэтиловый эфир и в результате получают 0,33 г 1-метил- 3- 1-метил-2-(4-метилфенил)-2-оксо- / эт11л 1 Н-имидазолбромида в виде твер- 5 дого вещества.
Выход 11%, т. пл. 175-177°С.
Рассчитано,%: С 54,38; Н 5,54; N 9,06.
5
0
С,Н ,, .
Найдено,%: С 54,09; Н 5,54;
N 9,17.
Вторую порцию продукта получают из фильтрата, и дополнительный выход данного продукта составляет 0,4г. Т. пл. 174-178 С.
Пример 9. 1-Метил-3- 2-(2,4 диметилфенил)-2-оксоэтил -1Н имида- эолбромид,
Раствор 4,76 г (0,021 моль)1-бром 2-(2,4-диметилфенил)-2-оксоэтана и 1,76 г (0,021 моль)1-метнлимидазола в 50 мл простого диэтилового эфира перемешивают при комнатной температуре примерно 21 ч. Растворитель реакционной смеси декантируют. Осадок промывают простым диэтиловьм эфиром. Этот осадок перекристаллиэовы- вают из смеси ацетонитрил/этилаце- тат. В результате получают 3,32 г целевого продукта в виде белых кристаллов .
Выход 51%, т. пл. 179-18ГС.
Рассчитано,%: С 54,38; Н 5,54; N 9,09; Вг 25,84.
С ,H, . ,
Найдено,%: С 54,18; Н 5,46; N 8,86; Вг 25,96.
Пример 10. 1-Метил-3- 2-(3- метилфенил)-2-оксозтрш -1Н-имидазол- бромид.
Раствор 5,16 г (0,024 моль)1-бром 2-(3-метилфенил)-2-оксозтана и 2,15 (0,026 моль)1-метилимидазола в примерно 30 мл простого диэтилового эфира перемешивают при комнатной температуре примерно 19 ч. Растворитель реакционной смеси декантируется. Полученный коричневый осадок промывают простым дизтиловым эфиром. Этот осадок пр.омывают горячим ацетонитри- лом и двукратно перекристаллизовыва- ют из смеси ацетонитрил/диэтиловьш простой эфир, в результате чего получают 1,74 г 1-метгш-3- 2-(3-метил- фенил)-2-оксоэтил -1Н-им1Хдазолбро- мида в виде белых игл.
Выход 25%, температура пл. 185- 187 С.
Рассчитано,%: С 52,90; Н 5,12; N 9,49; Вг 27,07.
С iiH, .
Найдено,%: С 53,11; Н 5,08; N 9,43; Вг 26,96.
Нижеследующие примеры иллюстрируют дополнительные соединения, используемые в изобретении, которые получа
4247336
ются общепринятыми описанными способ,1МИ.
Рассчитано,%: С 49,28; Н 5,02; N 8,21; Вг 23,42. 10 0,4 Hi,.
Найдено,%: С 49,05; Н 4,98; N 8,08; Вг 23,14.
Пример 12. 1-н-пропш1-3-(2- фенил-2-оксоэтил)-1Н-имидазолхлорид, 15 т. пл. 143-150°С.
Рассчитано,%: С 63,51; Н 6,47; N 10,58.
Найдено,%: С 64,81; Н 6,77; 20 N 9,86.
Приме;) 13. 1-Метил-3-С2-(2- метоксифенил)-2-оксоэтил - 1Н-имида- золбромид, т. rin. 165-167 С.
Рассчитано,%: С 50,18; Н 4,86; 25 N 9,00; Вг 25,68.
С 1 H,5BrN202.
Найдено,%: С 49,95; Н 4,97; N 8,78; Вг 25,92.
Пример 14. 1-Метил-3-С2- 30 (3,5-диметоксифенил)-2-оксо-этил -1Н- имидазолбромид, т. пл. 239-241°С (с разложением).
Рассчитано,%: С 49,28; Н 5,02; N 8,21; Вг 23,42.
С14Н„ВгЫ20з.
Найдено,%: С 49,33; Н 4,98; R 7,97; Вг 23,34.
Пример 15. 1-Метил-3-С2-(4- этоксифенил)-2-оксоэтил -1Н-имидазол- бромид, т. пл. 143-146 С.
Рассчитано,%: С 51,71; Н 5,27; N 8,61; Вг 24,57.
Ci4H nBrNjOt
Найдено,%: С 51,49; Н 5,39; N 8,42; Вг 24,45.
Пример 16. 1-Метил-3-Г2- (3,4-диметилфенш1)-2-оксоэтил 1-1Н- имидазолбромид, т. пл. 163-165 С.
Рассчитано,%: С 54,38; Н 5,54; N 9,09; Вг 25,84.
C H BrNiO
Найдено,%: С 54,61; Н 5,49; N 9,17; Вг 25,90.
Пример 17. 1-Метил-3- 2-(4- метоксифенш1)-2-оксоэтил-1Н-имидазол- бромид, т. пл. 156-159 с.
Рассчитано,%: С 50,18; Н 4,86; N 9,00; Вг 25,68.
Cn,H,jBrNjO35
40
45
50
Найдено,: С 49,98; И 5,11; N 8,82; Вг 25,95.
Пример. 18. 1-Метил-3-(2- фенил-2-оксоэтил)-1Н-имндазолхлорид, т. рл. 104-108 С.
Рассчитано,,: С 60,89; И 5,53; N 11,84; С1 14,98.
Найдено,%: С 59,63; И 5,35; N 11,37; С1 14,33,
Пример 19. 1-(1-мeтилэтил)- (3-мeтoкcифeни.п) -2-оксозтил J-1 Н имида 3 олб р омид.
Данное соединение получается при существлении следующей процедуры. Перемешанный раствор 1-(3-метокси- фенил)имидазола(1,08 г) в 20 мл аце- тонитрила подвергают обработке 2- бромпропаном при комнатной температуре в течение семи дней. Растворитель удаляется в вакууме и остаточный продукт, представляющий собой коричневое стекловидное вещество, перемешивается с растиранием с тетрагидро- фураном, при этом получается беловатый порошок. После перекристаллизации из смеси метанол-тетрагидрофуран получается продукт в виде тонких белых игл с т. 1Ш. 177-179 С (с разложением) .
Рассчитано,%: С 53,11; И 5,65; N 8,26.
С ijH .iBr
Найдено,%: С 52,91; И 5,39; N 8,35.
Осуществлял процесс таким образом получают продукты примеров 20 и 21.
Пример 20. 1-Метил-3-С2--(3 оксифенил)-2-оксоэтил -1Н-имидазол-4 метилбензолсульфонат, т. пл. 96-98 С (с. разложением) .
Рассчитано,%: С 58,75; И 5,19; N 7,21; S 8,25.
C HioNcjOsS
Найдено,%: С 58,54; Н 4,91; N 7,22; S 8,02.
П р и м е р 21. 1-Метил-3- 2-(3- трифторметилфенил)-2-оксоэтил -1Н- имидазолиодид, т. пл. 184-186 С (с разложением).
Рассчитано,%: С 39,41; Н 3,05; N 7,07.
С ijiioi N-iOF я
Найдено, %: с 39,65; Н 3,26; N 7,02.
Изобретение охватывает способ понижения содержания глюкозы в крови млекопитаю Ц1-1х животных, заключающийся в воде в организм млекопитающих животных эффективного количества нового имидазольного соединения. Под
термином эффективное количество имеется в виду количество соединения необходимое для достижения гипо- г. П кемического эффекта после впсзда препарата, предпочтительно в оргакизм млекопитающих животных с диабетом в зрелом возраста.
Данные активные соединения эффективны в широком пределе доз. Например, дневные дозы составляют примерио от 0,5 до 500 мг/кг песа. При
лечет-1и взрослых людей предпочтительный предел дозы составляет примерно от 0,5 до 500 мг/кг веса тела и вводится в виде единичной или разделенной дозы. Однако количество соединения, фактически вводимого в организм, должно определяться лечащим врачом и это связано с такими обстоятельствами, как состояние пациента, подвергаемого лечению, выбор соеди нения, которое должно вводит:ся в организм, возраст, вес пациента, реакция каждого пациента, острота симптом пациента, выбранный способ ввода препарата
в организм. Следовательно, пределы указанной дозы не ограничивают объем изобретения. Хотя соединения по предлагаемому способу вводятся предпочтительно орально для снижения содержания глюкозы в крови млекопитающих животных, но эти соединения могут также вводиться и различными другими путями, например трансдермально, подкожно, в нос, внутримьщ1ечно, внутривенно.
Соединения, к .пользуемые согласно предлагаемому способу, действуют иным образом, чем сульфонилмочевина, и повышают стойкость к инсулину. Следовательно, соединения по предлагаемому способу наиболее подходят для лечения диабета типа II, диабета, проявляющегося у людей зрело го возраста, поскольку многие пациенты имеют достаточно хорощо циркулирующий инсулин но сами невосприимчивы к инсулину. Однако точный механизм, согласно которому функционируют данные соединения, пока еще неизвестен и изобретение не
органичивается каким-либо принципом действия.
Соединения согласно предлагаемому способу вводятся орально в организм пациента. Хотя можно вводить соедине91424
ния по изо)ретенню ттепосредстпсино без приготовления рецептуры, однако жслатйлько их 1спользо1з чть в форме фармацевтическог о препарата, включающего фармацевтически пригодный носи
тель, разбавитель пли эксципиенти сое- динение, от11ечаш11;ео изобретению. Таки композиции содержат примерно от 0,1 до 90 % данного соединения.
При приготовлении композиций согласно предо агаемому способу активной ингредиент обычно смеигивается с носителем или разбавляется носителем, или покрывается носителем, которьп может иметь форму капсул, пузырьков, бумажной обертки и другую форму. Когда носитель служит 13 качество разбавителя, он может быть твердым, полутвердым -ши жидким веществом, который действует как носитель, эксципиент или среда для активного ингредиента. Так, композиция можут иметь форму таблеток
, порошков, лепешек, пузырьков капсул, эликсиров, эмульсий, растворов, сироггов, суспензий, аэрозолей (как в твердой, так и в жидкой среде и мягких и твердых желатиновых капсул,
Примерами подходящих для данной цели носителей, эксципиентов ij разбавителей могут являться лактоза, декстроза, сахароза, сорбит, маннит, крахмал, камеденосная акация, фосфит кальция, ггльгинаты, силикат кальция, микрокристаллическая целлюлоза, поли- винилпирролидон, це::люлоза, трагакант желатин, сироп, метилцеллюлоза, метил и пропил-оксибензоаты, тальк, стеарат магния, вода и минеральное масло. Данные рецептуры мог ут включать смачивающие реагенты, эмульсирующие и суспензирующие веп(ества, предохраняющие средства, подслащивающие или аро- матизируюпсие реагенты. Рецептуры, отвечающие изобретению, могут приготовлены образом, что обеспечивают быстрое, непрерывное или за- ме.цленное выделерще активного ингредиента после ввода в- организм патгиен- та путем испол.ьзонания уже известт1ы : приемов.
Для орального ввода в организм соединение, отвечающее изобретению, может быть идеальным образом смешано с носителями и разбавителями и может быть сформовано в таблетки шш заключено в желатиновые капсулы.
Длнпые композиции прш отаплинают- ся предпочтительно в форме единичной доты, и каждая единичная доза содер500 мг, чаще
жит примерно от 1 до примерно от 5 до 300 мг активного ингредиента. Под понятием форма единичной дозы имеются в виду физически дискретные единичные лекарственные препараты, пригодные как унитарные дозы для ввода в организм людей и других млекопитающих животных, и такой каждый единичньш лекарственный препарат содержит предварительно заданное количество активного материала, рассчитанное таким образом, что
бы достигался желаемый терапевтичес- киГг эффект, при комбинировании его с фармацевтическим носителем,
Гипогликемическая актив1;ость соединений, отвечающих изобретению, определяется путем испытания на эффективность действия рецептур, включающих данные соединения, в условиях, нн вино на жизнеспособньп ожиревших от диабета желтых мьпнах. Методика 1спытания описана Hiime .
Проведение эксперимента.
Испытываемые рецецтуры приготовли- ваются путем растворения подвергаемого испь танию соединения в солевом растворе, содержащем 2% эмульс лора (поверхностно-активное веи;ество, представляющее собой полиоксиэтилирован- ное растительное масло, поставляемое фирмой GAF CORP) , так что получаемая дозированная форма составляет 100 мг/кг. Каждая испытыв -емая рецептура вводится в организм шести жизнеспособных ожиревших от диабета желтых мышей путем их насильственногокормле- )ця . Содержание глюкозы в крови определяли по прошествии О, 2 и 4 ч после ввода рецептуры. Брали среднее значение шести испытаний.
Данные представлень в табл. 1,
Некотор)1е из этих соединений под- вертчзлись также исп)танию на действие против диабета типа II на крысах и бьио установлено. чтс1 они способны также понижать содерл;ание глюкозы в крови эт}гх животных.
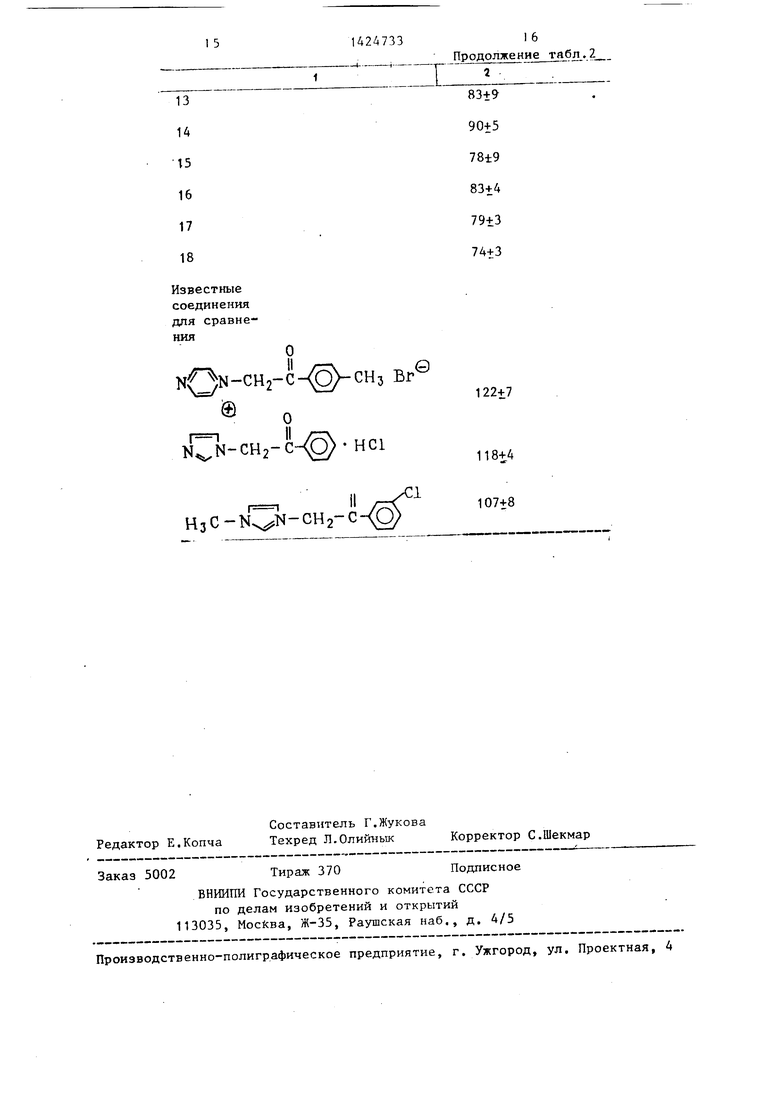
Сравнение предлагаем.ix соединений с аналогичньми по известными соединениями приведено в табл. 2.
Формула изобретения
Способ получения солей имидазола обще формулы
Т
1 1/ 2Д733
Продолжение табл.1
3:::znzi:
о100
283+9
А101+11
О100
290t5
А108+5
О100
278±9
4103+5
Соединение
Предлагаемые соединения по примеру
1
2 3 4 5 6 7
9 10 11 12
Продолжение табл. I
1
100
83+А
95±Д
100
79±3
93+7
100
74+4
71 + 7
Таблица 2
Процентное содержание глюкозы в крови через 2ч после введения
2
80+3 63+4 66+9 84+5 77+5 93+6 70+6 75+5 77+4 78+5 78+5 79+7
К ы-сНг-с
N N-CH2-C-4O - НС1
H3C-N N-CH2-C- Q
122+7
118+4 107+8
| ЭльдерфилдР | |||
| Гетероциклические соединения | |||
| М,: Изд-во И.П, 1954, т | |||
| V, с | |||
| Прибор для запора стрелок | 1921 |
|
SU167A1 |
Авторы
Даты
1988-09-15—Публикация
1985-11-11—Подача