Изобретение относится к новым химическим соединениям в ряду 1,2,4-триазоло [l, 5-a] бензимидазола, обладающим гипотензивной активностью.
Цель изобретения - новые вещества, обладающие большей чем дибазол, (структурный аналог) гипотензивной активностью.
Пример 1. Дигидрохлорид 4 - β -диэтиламиноэтил-2-метил -1,2,4-триазоло [l, 5-а] бензимидазола (1а).
Стадия 1. Хлорид 1,2-диамино-3-(β-диэтиламиноэтил)-бензимидазола (IIа).
Раствор 2,96 г (0,02 моль) 1,2-диаминобензимидазола и 3,5 г (0,025 моль) β -диэтиламиноэтилхлорида в 30 мл спирта кипятят 1,5 ч. Охлаждают, осадок представляющий собой побочный продукт-дихлорид тетраэтилпиперазина (0,6 г) отфильтровывают.
Маточный раствор упаривают до половины объема и осадок соли Па высаживают эфиром. Выход 4,65 г (69%). Бесцветные кристаллы; т. пл. 223-225°С (из спирта с эфиром).
ИК-спектр 1640, 1690 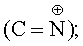
Найдено, %: С 46,1; Н 8,1; С1 10,4; N 20,7.
C13H22ClN5·3H2O.
Вычислено, %: С 46,2; Н 8,3;
С1 10,5; N 20,7.
Стадия 2. Раствор 3,87 г. (0,01 моль) четвертичной соли IIа в 20 мл уксусного ангидрида кипятят в присутствии 0,7 г (0,005 моль) поташа 5 ч. Охлаждают, осадок неорганических солей отфильтровывают, уксусный ангидрид отгоняют под уменьшенным давлением. Остаток обрабатывают 3 мл конц. NH4OН, после испарения аммиака растворяют в 15 мл хлороформа и очищают хроматографированием через колонку с А12O3, элюент хлороформ, отделяя фракцию с Rf0,65. Хлороформ отгоняют досуха, маслянистый остаток растворяют в 20 мл ацетона и обрабатывают конц. НС1 до рН 1. Выделяющийся бесцветный осадок отфильтровывают и промывают ацетоном. Выход 2,7 г (78%); т.пл. 227-228°С (из спирта с эфиром).
ИК-спектр 1660 (С=N); 2300-2700 см-1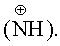
Найдено, %: С 52,5; Н 6,9; С1 20,9; N 20,6.
С15Н21N5·2НС1.
Вычислено, %: С 52,3;Н 6,7; С1 20,6; N 20,3.
Пример 2. Дигидрохлорид 4-β-морфолиноэтил-2-метил-1,2,4-триазоло [1,5-а] бензимидазола (Iб).
Стадия 1. Хлорид 1,2-диамино-3-β-морфолиноэтилбензимидазолия (IIб) получен аналогично соли IIа, (пример 1, стадия 1) с выходом 90%.
Бесцветные кристаллы; т.пл. 257-259°С (из спирта).
ИК-спектр 1640, 1690 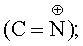
Найдено, %: С 52,5;,Н 6,5; С1 11,7; N 23,2. C13H20ClN5O.
Вычислено, %: С 52,4; Н 6,7; С1 11,9; N 23,5.
Стадия 2. Триазолобензимидазол 1б получен аналогично соединению Iа с выходом 81%. Бесцветные кристаллы; т.пл. 245-248°С (из спирта с этилацетатом), растворимые в воде.
ИК-спектре 1650, (C=N); 2100-2500 см-1 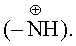
Найдено, %: С 50,5; Н 5,9; С1 19,9; N 19,5.
С15Н 19O52HC1.
Вычислено, %: С 50,3; Н 5,9; С1 19,8; N 19,6.
Пример3. Гидрохлорид 4-β-пиперидиноэтил-2-фенил-1,2,4-триазоло [1,5-а]бензимидазола (Iв).
Стадия 1. Хлорид 1,2-диамино-3- β-пиперидиноэтилбензимидазолия (IIв) прлучен аналогично четвертичной соли IIа (пример 1, стадия 1). Выход 62%. Бесцветные иглы; т.пл. 208-209°С (из спирта).
ИК-спектр: 1700 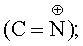
Найдено, %: С 56,7; Н 7,4; С1 11,8; N 23,6.
С14Н22С1N5.
Вычислено, %: С 56,9; Н 7,4; СI 12,0; N 23,7.
Стадия 2. Смесь 2,95 г (0,01 моль) соли IIв и 0,7 г (0,005 моль) поташа в 5 г (0,022 моль) бензойного ангидрида нагревают при 180-190°С 3 ч. Охлаждают, добавляют 10 мл воды и подщелачивают 40% КОН до рН 10. Экстрагируют хлороформом (3×20 мл), упаривают до объема 20 мл и пропускают через колонку с А120з (элюент хлороформ), отделяя фракцию с Rf 0,6, Хлороформ испаряют досуха, остаток растворяют в 30 мл ацетона и подкисляют конц. НС1 до рН 1. Выделяющийся осадок отфильтровывают и промывают ацетоном. Выход 3,2 г (80%). Бесцветные кристаллы; т.пл. 271-273°С (разложение из спирта).
ИК-спектр: 1600 (C-N); 2450-2700 см-1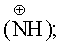
Найдено, %: С 63,3; Н 6,8; С1 9,2; N 17,6.
С21Н23N5·НС1·Н2О.
Вычислено, %: С 63,1; Н 6,5; С1 8,9; N 17,5.
Действие соединений на системное артериальное давление изучают в острых опытах на наркотизированных (нембутал 40 мг/кг, внутрибрюшинно) белых беспородных крысах массой 160-190 г общепринятым методом. Исследуемые вещества вводят внутривенно медленно. Артериальное давление измеряют в сонной артерии с помощью ртутного манометра. Показателем влияния вещества на артериальное давление принимают величину ЕД20 доза (мг/кг), в которой вещество снижает артериальное давление на 20%. ЕД20 рассчитывают по графику доза-эффект. Активность соединений сравнивают с действием дибазола. Для расчета терапевтического индекса (ЛД50 /ЕД20) определяют величину острой токсичности (ЛД50). ЛД50 вещества определяют в опытах на беспородных белых мышах массой 16-19 г при его внутрибрюшинном введении. Гибель животных определяют через 24 ч. При подсчете величины ЛД50 используют метод Миллера и Тейтнера (Беленький М.А. Элементы количественной оценки фармакологического эффекта, 1963, с.67-80). В отдельной серии опытов на наркотизированных (нембутал, 40 мг/кг внутрибрюшинно) кошках массой от 2 до 5кг изучали влияние соединений Iб и Iв на показатели центральной гемодинамики: системное артериальное давление (САД), минутный объем крови (МОК), частоту сердечных сокращений (ЧСС), общее периферическое сопротивление (ОПС), ударный объем крови (УО) и работу левого желудочка (РЛЖ). Минутный объем крови определяют методом терморазведения (Fegger et. al. 1954, 39, 154-164) в модификации Гуревича М.М. с соавторами (ФИЗИОл, ж. СССР, 1967, с. 350) и Ванькова Д.Е. и Цибина Ю.Н. (Физиол. ж. СССР, 1973, № 1, с. 179-180), Частоту сердечных сокращений подсчитывают по электрокардиограмме, записанной во 2-ом стандартном отведении. УО рассчитывают делением МОК на ЧСС. Общее периферическое сопротивление определяют по формуле, описанной Wigger s Kirculatory dinamics, гл. 4, 5, 1954.
Результаты исследований представлены в табл. 1-3.
Влияние новых производных триазоло [1,5-а]бензимидазола на системное артериальное давление крыс (ЕД20 доза, мг/кг, при внутривенном введении, снижающая артериальное давление в течение 30-60 мин опыта на 20%)
Влияние соединения Iб (в дозе.10 мг/кг при внутривенном введении) на основные показатели гемодинамики наркотизированных кошек (М+m)
Влияние соединения 1в (доза 10 мг/кг при внутривенном введении) на основные показатели гемодинамики наркотизированных кошек (M±m)
Таким образом, установлено, что соединения Ia-в обнаруживают гемодинамический механизм гипотензивного действия, причем по абсолютной величине гипотензивного действия (ЕД20) они превосходят дибазол в 3,5-5 раз, а по величине терапевтического индекса (ЛД50/ЕД20) в 2,6-7,4 раза.
| название | год | авторы | номер документа |
|---|---|---|---|
| N-КАРБАМОИЛМЕТИЛ-4-ФЕНИЛ-2-ПИРРОЛИДОН, ОБЛАДАЮЩИЙ ГИПОТЕНЗИВНОЙ АКТИВНОСТЬЮ | 1979 |
|
SU797219A1 |
| КАРДИОТОНИЧЕСКОЕ И ГИПЕРТЕНЗИВНОЕ СРЕДСТВО, ДЛИТЕЛЬНО ПОВЫШАЮЩЕЕ ДАВЛЕНИЕ, И ЛЕКАРСТВЕННЫЕ ФОРМЫ НА ЕГО ОСНОВЕ | 1999 |
|
RU2181286C2 |
| ПРОИЗВОДНЫЕ НИТРОФУРАНА, ОБЛАДАЮЩИЕ АНТИБАКТЕРИАЛЬНЫМ ДЕЙСТВИЕМ | 2009 |
|
RU2425044C2 |
| 2,6-ДИМЕТИЛ -3,5-БИС (АЛКОКСИКАРБОНИЛ) -4-[ПОЛИФТОРАЛКОКСИ(МЕТОКСИ) -ФЕНИЛ] -1,4-ДИГИДРОПИРИДИНЫ, ПРОЯВЛЯЮЩИЕ КАРДИОТОНИЧЕСКОЕ И ГИПЕРТЕНЗИВНОЕ ДЕЙСТВИЕ | 1992 |
|
RU2036907C1 |
| 1-Дифторнитроацетил-2-арилгидразины,обладающие гипотензивной активностью | 1986 |
|
SU1432052A1 |
| ПРОТИВОСУДОРОЖНЫЕ СРЕДСТВА | 1994 |
|
RU2108094C1 |
| ГИДРОХЛОРИДЫ ПРОИЗВОДНЫХ 5-ФЕНОКСИМЕТИЛ-1,2,4-ОКСАДИАЗОЛА, ОБЛАДАЮЩИЕ β И a -АДРЕНОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 1982 |
|
SU1132505A1 |
| 1-ФЕНИЛ-5- (2′- ОКСИФЕНИЛ)-3-СТИРИЛ-1,2,4-ТРИАЗОЛЫ, ОБЛАДАЮЩИЕ ТРАНКВИЛИЗИРУЮЩИМ ДЕЙСТВИЕМ | 1983 |
|
SU1124558A1 |
| ОКСАЛАТЫ 2-[1-(3-АЛКИЛАМИНО-2-ОКСИПРОПИЛОКСИИМИНО)ЭТИЛ]1,4-БЕНЗОДИОКСАНОВ, ОБЛАДАЮЩИЕ β -АДРЕНОБЛОКИРУЮЩЕЙ АКТИВНОСТЬЮ | 1981 |
|
SU1009051A1 |
| ГИДРОХЛОРИДЫ N-АЛЛИЛ- И N-[3-(3,4-ДИМЕТОКСИ)-ФЕНИЛ]-2-ПРОПЕНИЛИЗОХРОМАНИЛ-1-МЕТИЛАМИНОВ, ОБЛАДАЮЩИЕ КОРОНАРОРАСШИРЯЮЩЕЙ АКТИВНОСТЬЮ | 1983 |
|
SU1137734A1 |
Изобретение касается гетероциклических соединений, в частности гид-рохлоридов 4-β-диалкиламиноэтил 1,2,4-триазоло [1,5-а]бензимидазолов общей формулы
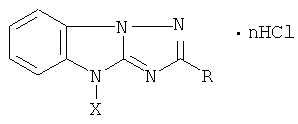
где X - группа формулы - (CH2)2NR1R2, при a) R - СН3; R1 = R2 - C2H5; n = 2; б) R = СН3; R4 + R2 - морфолил; n = 2; в) R - C6H5; R1 + R2 - пиперидил; n = 1, обладающих гипотензивной активностью, что может быть использовано в медицине. Цель - создание новых более активных веществ указанного класса. Синтез целевых веществ ведут реакцией 1,2-днаминобензимидазола и β -диэтиламино -, или β -молфолино-, или β -пиперидино-этилхлорида в среде спирта при кипячении 1,5 ч. Полученные соединения обрабатывают поташом и уксусным или бензойным ангидридом при кипячении или 180-190°С в течение 3-5 ч. Выход %; т.пл. °С; брутто формула: а) 78; 227-228; С15Н24N5·2HC1; б)81; 245-248; C15H19N5O·2НС1; в) 80; 271-273 (разл.); С21H23N5·HCl·Н2O. Новые соединения по гипотензивной активности превосходят дибазол в 3,5-5 раз, а по величине терапевтического индекса в 2,6-7,4 раза при токсичности ЛД50 230-550 мг/кг, 3 табл.
Гидрохлориды 4- β -диалкиламиноэтил-1,2,4-триазоло [l,5-а] бензимидазолов общей формулы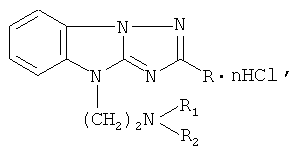
где Ia; R - CH2, R1 = R2 - C2H5; n=2; Iб: R - CH3, R4 + R2 - остаток морфолина;
n - 2;
Iв: R - C6H5, R4+ R2 - остаток пиперидина; n=l, обладающие гипотензивной активностью.
Авторы
Даты
2014-06-27—Публикация
1987-02-05—Подача