1
4 4ib
00
со
i4
Изобретение относится к усовершенствованному способу получения аллени- ловых эфиров формулы:
,
где ,, ,C.jHj; n-CjH7, СН -СНиСН П-С4Н5; 1-C4H9J которые могут найти применение как мономеры и полупродук
ты для тонкого органического синтеза. . Цель изобретения - упрощение про- цесса и расширение ассортимента целевых продуктов.
Изобретение иллюстрируется следующими примерами.
Пример 1. 8 г (0,114 М) метилпропаргилового эфира, 4 г (0,071 М) КОН и 20 мл (0,282 М)диме тилсульфоксида (ДМСО), соотношение реагентов 1,6:1:4, перемешивают в течение 15 мин при 20°С, После чего реакционную колбу присоединяют в вакуумной системе и при давлении
рт.ст. отгоняют метоксиаллен в ловушку, охлажденную до -70° I, выход продукта 7,2 г (90%), чистота 99,9%.
Найдено, %: С 68,40; Н 8,53;
C4Hg,0
Вычислено, %: С 68,57; И 8,57.
Спектр ПМР ((Г, М.Д.): 6,76 Г6,68 лит т (1Н, СН); 5,47 5,-40 д (2Н, CH,)i 3,40 с (ЗН, СНз), j 5,6 Гц ИК спектр (V, ):1952, 1964 пл.
(c,), 1053 (л)5 ) 1210 ( } С-О-С).
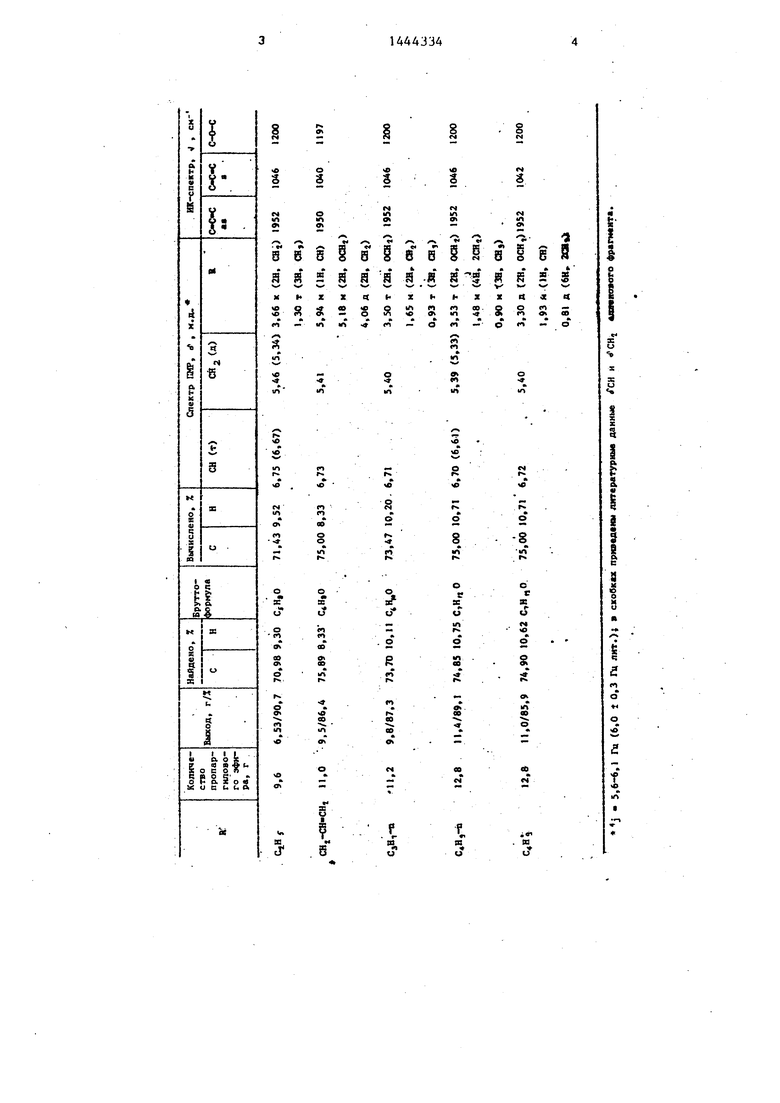
Другие аллениловые эфиры получены аналогично. Время реакции во всех случаях 15 мин, количества КОН 4 г, ДМСО 20 мл, чистота получаемых продуктов 99,9%.
Количество исходного пропаргипового эфира, выходы алленов, данные их элементного анализа, ПМР- и ИК-сп.ектров приведены в таблице.
514443346
Пример 2. 3,8г (0,054 М)спектры получены на приборе Specord- метилпропаргилового эфира, 2 г КОН75IR в чистой жидкости - (0,038 М) в 20 мл (0,282 М) ДМСО, Таким образом, данный способ полусоотношение 1,4:1:8, перемешивают причения аллениловых эфиров позволяет комнатной температуре (23°С) в течение быстро (в течение 0,5 ч) получать их
15 мин. В вакууме 2 мм рт.ст. отгоняют метоксиаллен, выход 2,1 г (55,6%), чистота 67,8%.
Пример 3. 3,8 г (0,054 М) метилпропаргилоэого эфира, 4 г (О.,071 М) КОН в 20 мл (0,282 М) ДМСО,, соотношение 0,76:1:4, перемешивают ,. при 24°С в течение 15 мин. В вакууме 3 мм рт.ст. отгоняют метоксиаллен, выход 3 г (78,9%), чистота 99,9%.
П р и м е р 4. 10 г (0,143 М) мётилпропаргилового эфира, 2 г (0,038 М) КОН в 10 мл (0,141 М) ДМСО, соотношение 4:1:4, перемешивают при в течение 15 мин. В вакууме 2 мм рт.ст. отгоняют метоксиаллен, выход 8,26 г (82,6%), чистота 90,7%.
Пример 5. 7 г (0,1 М) мётилпропаргилового эфира, 2 г (0,038 М) .КОН в 10 мл (0,141 М) ДМСО, соотношение 3:1:4, перемешивают при в течение 15 мин. В вакууме 4 мм рт.ст. ; отгоняют метоксиаллен, выход 6 г (86%), чистота 98%.
Чистота получаемых аллениловых эфиров контролировалась методом ГЖХ на приборе Хром-4 (детектор-катаро- метр, газ-носитель - гелий, колонка 3700 3,5 мм, твердая фаза Инертон AW (0,2-0,25 мм), пропитанньй 15% Carbowax 20М, температура колонки 80-90 С). Спектры ПМР сняты на спектрометре Tesla BS-487B (80 МГц) в СС14. Внутренний стандарт ГМДС. ИК-
с чистотой 99,9% и выходом 85-90% в мягких условиях (без дополнительного нагрева реакционной массы), используя
10 дешевые и доступные реагенты (ДМСО и КОН), тогда как в известном способе реакцию ведут при повышенной температуре () в течение 2-3 ч с использованием труднодоступных реагентов
15 (t-BuOK) (ка тиевая соль трет-бутило- вого спирта).
Кроме того, данный способ позволяет получать новые алленйловые эфиры R-0-CH C CH ;, где R - CHj-CH CH2,
20 jH - С4Нд .
Формула изобретения
Способ получения аллениловых зфи- ров общей формулы
25
35
ROCH-C CH,
где R - CHj, C-jHj, п - СэН, п - С4Нд; i - ,
30 прототропной изомеризацией соответствующих пропаргиловых эфиров в присутствии основания, отличающийся тем, что, с целью упрощения процесса и расширения ассортимента целевых продуктов, в качестве основания используют безводную гидроокись калия в сухом диметил ульфокси- де, процесс ведут при 20-25°С и молярном соотношении реагентов пропарги40 ловый эфир:гидроокись калия:диметил- сульфоксид, равном (О, 76-4,0): I: (4-8),
с чистотой 99,9% и выходом 85-90% в мягких условиях (без дополнительного нагрева реакционной массы), используя
дешевые и доступные реагенты (ДМСО и КОН), тогда как в известном способе реакцию ведут при повышенной температуре () в течение 2-3 ч с использованием труднодоступных реагентов
(t-BuOK) (ка тиевая соль трет-бутило- вого спирта).
Кроме того, данный способ позволяет получать новые алленйловые эфиры R-0-CH C CH ;, где R - CHj-CH CH2,
jH - С4Нд .
Формула изобретения
Способ получения аллениловых зфи- ров общей формулы
25
ROCH-C CH,
где R - CHj, C-jHj, п - СэН, п - С4Нд; i - ,
прототропной изомеризацией соответствующих пропаргиловых эфиров в присутствии основания, отличающийся тем, что, с целью упрощения процесса и расширения ассортимента целевых продуктов, в качестве основания используют безводную гидроокись калия в сухом диметил ульфокси- де, процесс ведут при 20-25°С и молярном соотношении реагентов пропаргиловый эфир:гидроокись калия:диметил- сульфоксид, равном (О, 76-4,0): I: (4-8),

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 3-диалкиламино-2-бутеналей | 1990 |
|
SU1770318A1 |
| Способ получения производных алкилтиоэтиниламина | 1983 |
|
SU1097616A1 |
| Способ получения винилоксиаллена | 1986 |
|
SU1442515A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИС-1,2-ДИ-(АЛКИЛСЕЛЕНО)ЭТЕНОВ | 1991 |
|
SU1833615A3 |
| 2-[4-(4-Транс-Алкилциклогексил)-фенил]-5-(4-транс-алкилциклогексил)-пиридины в качестве компонентов жидкокристаллического материала для электрооптических устройств и жидкокристаллический материал для электрооптических устройств | 1987 |
|
SU1710556A1 |
| Способ получения -ацетиленовых спиртов | 1977 |
|
SU745888A1 |
| Способ получения водорастворимых пропаргиловых эфиров полисахарида арабиногалактана | 2016 |
|
RU2650544C2 |
| Способ получения ди(пропен-1-ил)сульфида | 1983 |
|
SU1114675A1 |
| Способ получения 1-галоген-2-триалкилсилилалкенилалкиловых эфиров | 1983 |
|
SU1122661A1 |
| Способ получения производных @ -дигалоидвинилциклопропана | 1978 |
|
SU1075972A3 |
Изобретение касается производства простых эфиров, в частности получения аллениловых эфиров общей ф-лы R-0-CH C CH, где R - п-С -С -алкил, СН j-CH CHj ,изо-С4Н g - мономеров или полупродуктов органического синтеза. Процесс ведут прототропной изомеризацией соответствующих пропаргнловых эфиров в присутствии основания. В качестве последнего используют безводную КОН в сухом диметилсульфоксиде при молярном соотношении эфира, КОН и диметилсульфоксида, равном (0,76-4) :1:(4-8). Эти условия позволяют расширить ассортимент целевых веществ с выходом 90% и чистотой 99,9% с использованием дешевых и доступных реагентов и мягких условий (20°С). 1 табл. §

| Hoff S., Brandsma L | |||
| J.F.Arens | |||
| Rep | |||
| trav.chiffl, 1968, v.87, IP 9, p.916-924. |
Авторы
Даты
1988-12-15—Публикация
1987-03-25—Подача