сн
Изобретение относится к способу получения новых производных 1,3-ди- гидро(4,5-Ъ)хинолин-2-о нов, о бладающих лекарственными свойствами и свойствами, вьфажающимися в воздействии на биологические объекты, а, более конкретно, они являются ингибиторами фосфодиэстеразы, антиагре- гаторами тромбоцитов крови и кардио- тоническими агентами.
Цель изобретения - синтез новых производных имидазохинолин-2-онов, обладакяцих биологической активностью не характерной для данного ряда соединений.
Пример 1. 8-Хлор-1,3-дигид- ро-2Н-имидазо(4,5-Ъ)хинолин-2-он.
5- (2-Хлор-6-нитрофенил)метю1 - 2,4-имидазолидиндион (2 г, 7,4 ммоль в диметилформамиде (40 мл) гидрировался над 10%-ным палладием на древесном угле (0,2 г))1При давлении 60 фунт/кв. дюйм (4,219 кг/см ) до тех пор, пока не прекратилось потреб ление водорода. Реакционная смесь нагревалась на паровой бане в течение 2 ч, фильтровалась через фильтр из инфузорной земли и концентрировалась в вакууме, давая твердое вещество. Кристаллизация игз метанола давала гидратированный 8-хлор-1,3-дигидро- 2Н-имидазо(4,5-Ъ)хинолин-2-он (1,20 г, 36%), Т.Ш1. 860 С.
Вычислено; С 52,24; Н ,82; N 18,9§; С1 16,01; 0,81,
НбСто-о,1НсО
Найдено: С 54,18; Н 2,93; N 18,93 С1 15,76; HtO Q,75.
ЯМР (flMCO-dgh от 7,44 до 7,65 (2, мультиплет), 7,69 (1, синглет), 7,80 (1, двойной дублет, 3 Гц, 6 Гц 11,18 (, широкий синглет), 11,70 . (1, щирокий сингле -).
П р и м е р 2. 7-ФТОР-1,3-дигидро 2Н-имидазр(4,5-Ъ)хинолин-2-он
Н
N
К
5-(5-Фтор-2-нитрофенил)метш17- 2,4-имидазолидиндион (6 г, 23 ммоль) в диметилформамиде (120 мл) гидрировался над 10%-ным палладием на. древесном угле (0,6 г) при давлении 4,219 кг/см до тех пор, пока не прекратилось потребление водорода.
s
0 5
g
0
5
0
0
5
Реак1щонная смесь кагревалась на паровой бане в течение 2,5 ч, фильтровалась через фильтр из инфузорной земли и концентрировалась в вакууме, давая твердое вещество, которое суспендировалось в кипящем метаноле (750 мл). Через 18 ч горячая смесь фильтровалась и растворитель упаривался до получения твердого вещества, которое растворялось в кипящем метаноле. (500 мл), и добавлялся йод (2,0 г, 7,9 ммоль) двумя равными порциями. Спустя 15 мин растворитель упаривался, и остаток обрабатывался раствором тиосульфата натрия (10 г) в воде (100 мл) и карбонатом натрия (5 г) в воде (50 мп). Песочно-коричневое твердое вещество (2,80 г) отфильтровывалось и растворялось в ди- метилсульфоксиде (30 мл). Добавление дихлорметана осаждало 7-фтор-1,3-ди- гидро-2Н-имидазяэ (4,5-Ъ) хинолин- 2-он в виде дихлорметан-диметилсульфоксид- ного сольвата гидрата (2,18 г, 45%, т.пл. 360°С).
Вычислено; С 56,72; Н 3,19; N 19,55; НаО 1,68,
CeHeFNj О 0,2НгО 0,05CHeClq- 0,05С2НбОЗ
Найдено: С 57,01; Н 3,09; N 19,24; НеО 1,66.
ЯМР (WCO-dfi): 2,60 (щирокий син- ), 5,74 (синглет, CHj-CHe) 7,20-7,95 (4, мультиплет); 11,30 (2, щирокий синглет).
ПримерЗ, 8-Метип-1,3-дигид- ро-2Н-имидазо(4,5-Ъ)хинолин-2-он.
5-П 2-Метил-6 -нитрофенил )метил7- 2,4-имидазолидиндион (5 г, 20 ммоль) в диметилформамиде (200 мл) гидрировался над 10%-ным палладием на угле (0,5 г) при давлении 4,219 кг/см до тех пор, пока не прекратилось потребление водорода. Реакционная смесь нагревалась на паровой бане в течение 2 ч,фильтровалась через фильтр из инфузорной земли и растворитель упаривался. Остаток в, виде твердого вещества суспендировался в кипящем метаноле, и йод (4 г, 15 ммоль) добавлялся равными четырьмя порциями в течение 10 мин. Смесь нагревалась с обратным холодильником в течение 10 мин концентрировалась в вакууме, и остаток обрабатывался раствором тиосульфата натрия (45 г) в. воде ( 150 мл) и раствором карбоната натрия (13 г) в воде (150 мл). Нерастворимое твер1
дое лещество i4,/j т ()1фил1 тровыпа- лось и растр(рялось в I ОА-НОМ хлористом водороде в метаноле. Добавление простого эфира приводит к образованию остатка в виде гидрата 8-метил- 1,3-дигидро-2Н-имидазо(4,5-Ъ)хино- лин-2-она (3,38 г, 71%), т.пл. 350- (разл.).Вычислено: С 54,60; Н 4,46;
N 17,37; С1 14,61; НдО 2,6Ь
Сц НдКзО-НС1 0,35НгО :
Найдено: С 54,30; Н 4,15; N 17,49 С1 1Д,54;.Н2.0 0,38.
ЯМР (ЛМСО-dj): 2,62(3, синглет), 7,35 (1, дублет, 8 Гц), 7,54 {|, дублет, 8 Гц), .7,80 (1, синглет), 7,83 (1, дублет, 8 Гц), 9,72 (1, широкий синглет), 11,70(1, широкий синглет)
П р и м е р 4, 7-Метил-1,3-дигидро 2Н-имидазо(4,5-Ъ)хинолин-2-он.
5-(5-Метил-2-нитрофенил)}-метил - 2,4-имидазолидиндион (5 г, 20 ммоль) в диметилформамиде (200 мл) гидрировался над 107,-ным палладием на угле (0,5 г) при 4,219 кг/см до тех пор, пока не закончится потребление водорода. Реакционная смесь нагревалась на паровой бане в течение 2ч, фильтровалась через инфузорную землю и концентрировалась в вакууме. Твердое вещество остатка обрабатьшалось кипящим метанолом (300 мл) и добавлялся двумя равными порциями йод (4 г, 15 ммоль) в течение 10 мин. Нагрева- ние с обратным холодильником продолжалось в течение последующих 25 мин перед тем, как растворитель упаривался и остаток обрабатывался раствором тиосульфата натрия (17 г)в йо- де (170 мл) и раствором карбоната натрия (10 г) в воде (100 мл). Светло-коричневое твердое вещество отфильтровывалось (4,09 г) и растворялось в 10%-ном хлористом водороде в метаноле. Добавление простого эфира приводило к осаждению 7-метил-1,3- дигидро-2Н-имидазо(4,5-Ъ) хинолин-2- она в виде гидрата гидрохлорида (3,60 г, 74%), т.пл. ,
Вычислено: С 54,81; Н 4,43; N 17,43; С1 14,71; HgO 2,24.
Cf, HgNgO HCl-0,3HaO
Найдено: С 55,15; Н 4,56; N 17,16 С1 14,03; 0,69.
ЯМР (ЛМСа-de): 2,45 (З, синглет), 7,44 (, дублет, 8 Гц), 7,75 (2, синглет), 7,90 (1, дублет, 8 Гц), 11,0
46
(1, широкий синглет), 11,62 (1, широкий синглет).
П р и м е р 5. 7-Хлор-1,3-дигид- po-2H-имидaзo(4,5-b)xинoлин-2-oн.
5- ( 5-Хлор-2-нитрофенил)метил - 2,4-имидазолидиндион (3 г, 11,1 ммоль в диметилформамиде (60 мл) гидрировался над 10%-ным палладием на угле (0,3 г) при 4,219 кг/см до тех пор, пока не прекратится потребление водорода. Реакционная смесь нагревалась на паровой бане в течение 2ч, фильтровалась инфузорную землю и концентрировалась примерно до 10 мл. Добавление дихлорэтана давало гидра тированный 7-хлор-1,3-дигидро-2Н-ими- да30(4,5-Ъ)хинолин-2-он (1,22 г, 50%) т.пл. :7360°С,
Вычислено; С 54,24; Н 2,82; N 18,98; С1 16,0 ; HjO 0,8Ь
СчоНйСШа,0«0,1НсО
Найдено: 54,36; Н 2,83; N 18,88; С1 15,29; Н«0 0,52.
ЯМР (ДМСО-саб): 7,46 (1, двойной дублет, 2 Гц, 9 Гц), 7,59 (1, син-. глет), 7,79 (1, дублет, 9 Гц), 7,99 (1, дублет, 2 Гц), 11,10 (1, широкий синглет), 11,50 (1, широкий синглет).
П р и м е р 6. I,3-Дигидро-6,7- диметил-2Н-имидазо(4,5-Ь)хинолин-2-он
Раствор 5-(4,5-диметил-2-нитро- фенил)метил -2,4-имидазолидиндиона (3 г, 11,4 ммоль) в диметилформамиде (100 мл) гидрировался над 10%-ным палладием на угле (0,3 г) до тех пор пока не прекратилось потребление водорода. Реакционная смесь нагревалась на паровой бане з течение 3 ч перед тем, как она профильтровывалась через инфузорную землю. Упаривание растворителя давало масло, которое растворялось в кипящем метаноле (150 мл) и обрабатывалось йодом (2 г, 7,5ммоль) двумя равными порциями в течение 15 мин. После дополнительных 15 мин нагревания с обратным холодильником растворитель упаривался и добавлялся раствор карбоната натрия (9 г) и тиосульфата натрия (9 г) в воде (180 мл) Бледно-желтое твердое вещество от- фильтровьшалось и растворялось в 10%-ном хлористом водороде в метаио- ле. Растворитель упаривался и остаток кристаллизовался из метанола, давая 1,З-дигидро-6,7-диметил-2Н-имидазо (4,5-Ъ)хинолин-2-он в виде гидрата гидрохлорида (1,04 г, 47%), т.пл, 360°С.
N
Вычислено: C57jlO|H4,91; 16,65; Н2.0 1 ,07.
C4iH( N O-HCl-OjlSHgO Найдено С 57,04; Н 5,01; N 16,57;
1,02.
ЯМР (ДМСО-de): 2,36 (З, синглет), 2,39 (3, синглет)J 7,70 (З, синглет-). П р и м е р 7. 1,З-Дигидро-7,8-ди- метил-2Н-имидазо(4,5-Ъ)хинолин-2-он, а) Хпоргидрат 1,3-дигидpo 7,8-ди- мвтил-2H-имидaзo (4,) ХИНОЛИН-2-ОН, 5- С( 2,3-Диметил-бН-нитрофенил )ме- тил1-2,4-имидазолидиндион (2,15 г.
Через 66 ч смесь разбавлялась диме- тилформамидом (300 мл), нагревалась для того, чтобы вьтавдее в осадок ве- с щество растворилось, обрабатьшалась древесным углем, фильтровалась через инфузорную землю и концентрировалась. Остаточное вещество суспендировалось в кипящем метаноле (2л) и порциями 10 добавлялся йод (38,7 г, 0,15 моль) в течение 30 мин. Нагревание с обрат- ньм холодильником продолжалось в течение дополнительных 10 мин, смесь концентрировалась до объему при8,2 ммоль) в диметилформамиде (30 мл) 15 близительно 400 мл и добавлялся раст- гидрировался над 10%-ным палладием вор тиосульфата натрия (60 г) и кар- на угле (0,2 г) при давлении 55фунт/кв, боната натрия (60 г) в воде (600 мл). дийм (3,867 кг/см). Спустя 4 ч добавлялся 10%-ный палладий на угле (0,2 г) и гидрирование продолжалось. 20 Спустя 18 ч реакционная смесь нагреОсадок собрфался, промывался водой и метанолом и затем растирался с водой (500 мл). Растертое твердое вещество собиралось, .суспендировалось
в кипящем метаноле (200 мл),охлаждалось и фильтровалось, давая гидрати- рованный 1,3-дигидpo-7,8-димeтил-2H- 25 имидазо(4,5-Ъ)хинолин 2-он (29,44 мг, 88%), т.пл, 7310°С.
залась на паровой бане в течение 1,5 ч, охлаждалась, фильтровалась чрез инфузорную землю и растворитель упаривался. Оставшеейя твердое вещество суспендировалось в кипящем метаноле (100 мл) и обрабатывалось йодом (1 г). Через 30 мин реакционная смесь концентрировалась до объема приблизительно 30 мл и добавлялся растрор тиосульфата натрия (ДО г) и кар(боната натрия (Ю г) в воде (100 мл). Коричневое тв.ердое вещество отфильтровывалось, промьгоалось вдой и метанолом и обрабатывалось 10%-ным хлористым водородом в метаноле. Нерастворимое коричневое твердое вещество суспендировалось в кипящем метаноле и фильтровалось, давая 1,3-дигидоо-7,8-диметил-2Н-йми- дазо(Д,5-Ъ)кинолин-2-он в виде гидрата гидрохлорида (1,0 г, 49%), т,п 360°С,
Вычислено С 56,90; И 4,93; и 16,59} НЮ 1,42.
HaO.HCi 0,2HtO
Найдено: С 57,01; Н 4,89 j Ы 16,3 ЙФО 1,07.
ЯМР (даСО-ав); CFgCO H : 2,41 (3, сияглет), 2,52 (З, синглет), 7, (2, АВ квартет, 9 Гц), 7,89 (1, син шеН, .11,50 (3, щирокий синглет).
б) Гидрат 1,3-днгидро-7,8-димети 2Н-имидазо(4,5-Ъ)хинолин-2-он.
5-t(2,3-Димвтил-6-нитрофенил)-ме тилЗ-2,4-имидазолидин (40,18 г, 0,15 -моль) в диметилформамиде (500 мл) гидрировался над 10%-ным
палладием на угле (6 г) при 4,219 кг
;
.
4507466
Через 66 ч смесь разбавлялась диме- тилформамидом (300 мл), нагревалась для того, чтобы вьтавдее в осадок ве- с щество растворилось, обрабатьшалась древесным углем, фильтровалась через инфузорную землю и концентрировалась. Остаточное вещество суспендировалось в кипящем метаноле (2л) и порциями 10 добавлялся йод (38,7 г, 0,15 моль) в течение 30 мин. Нагревание с обрат- ньм холодильником продолжалось в течение дополнительных 10 мин, смесь концентрировалась до объему при) 15 близительно 400 мл и добавлялся раст- вор тиосульфата натрия (60 г) и кар- в, боната натрия (60 г) в воде (600 мл). 20
близительно 400 мл и добавлялся раст- вор тиосульфата натрия (60 г) и кар- боната натрия (60 г) в воде (600 мл).
Осадок собрфался, промывался водой и метанолом и затем растирался с водой (500 мл). Растертое твердое вещество собиралось, .суспендировалось
т.пл. т ЗбО ,
в кипящем метаноле (200 мл),охлаждалось и фильтровалось, давая гидрати- рованный 1,3-дигидpo-7,8-димeтил-2H- имидазо(4,5-Ъ)хинолин 2-он (29,44 мг, 88%), т.пл, 7310°С.
Вычислено; С 66,47; Н 5,3Q; N 19,38; 1,66Ci4tH N/iO 0,2H.iO
Найдено: С 66,14; Н 5,12; N 19,32; НеО 1,0.
ЯМР (даСО-авЬ 2,41 (З, синглет), 2,49 (3, синглет), 7,45 (2, АВ квартет, 9 Гц), 7,62 (f, синглет), 10,90 (1, синглет), 11,30 (1, широкий син- . глет).
Пример 8. 1,3-Дигидро-7-хлор- 6-метил-2Н-имидазо(4,5-Ъ)хинолин-2он,
5-Ц5-ХлЬр-4-метил-2-нитрофенил) метш11-2,4-имидазолидиндион (2,г, 7 ммоль) в диметилформамиде (30 мл) гидрировался над 6%-ным палладием йа
угле (0,4 г) при 55 фунт/кв. дюйм (3,867 кг/см) до тех пор, пока не прекратится потребление водорода. Смесь нагревалась на паровой бане в течение 2ч, концентрировалась в вакууме и йстаток обрабатывался горячим Ч90 с) диметилсульфоксидом. Фильтрация через инфузорную землю и упаривание растворителя давало твердое вещество, которое промывалось простын зфиром и суспендировалось в кипящем метаноле. Фильтрация давала 1,3- дигидро-7-хлор6-метил-2Н-имидазо (4,5-Ь) ХИНОЛИН-2-ОН (1,40 г, 84%),
10
Вычислено; С 56,55; Н 3,45; N 17,88; С1 15,17.
C HgClNgO
Найдено:С 56,34; Н3,42; N 17,71; С1 .
ЯМР (ДМСО-(1б),: 2,45 (3, синглет), 7,55 (1, синглет), 7,72 (1, синглет), 7,98 (1, синглет).
П р и м е р 9. 1,3-Дигидро-8-мет- окси-2Н-имидазо(4,5-Ъ)хинолин-2-он,
Это соединение приготавливалось в соответствии с примером 7(1) из 5- (2-метокси-6-нитрофенил)метил -2,4- имидазолидиндиона. Целевой продукт получался в виде гидрата (91%), т.пл. ЗОО С.
Вычислено: С 60,13; Н 4,36; И 19,13; HgO .
С HgNjOg- 0,25Н40,.
Найдено: С 59,85; Н 4,12; N 18.,78; %0 1,26.
ЯМР (CO-dg): 3,97 (3, сингле), 6,88 (1, двойной дублет, 4 Гц, 5 Гц), 7,35-7,50 (2, мультиплет), 7,71 (1, синглет), 10,98 (1, широкий синглет), 11,45 (1, пюрокий сингле ).
Примерю. 1,3-Дигидро-8- хлор-7-метил-2Н-имидазо(4,5-Ъ)хино- ЛИИ-2-ОН.
Это соединение приготавливалось аналогично примеру 2 из 5-|( 2г-хлор- З-метил-6- нитрофенил)метил 2,4-ими- дазолидиндиона. Целевой продукт по- лзгчался в виде гидрата (5%) т.пп. 7 360°С.
Вычислено: С 55,69v Н 3,57; N 17,71; НаО 1,52.
CH H8ClNjO-0,2He.O
Найдено: С 54,61; Н3,47; N 17,11; 1,43.
ЯМР (flMCO-dgb 2,50 (3, синглет), 7,57 (2, АВ квартет, 8 Гц) 7,69 (1, синглет), 11,10 (1, широкий синглет), 11,60 (1, широкий синглет).
Ц р и м е р II. 7-Хлор- 1,3-дигид- ро -б, 8-диметш1-2Н-имидазо (4,5-Ъ) хи- НОЛИН-2-ОН.
Это соединение было получено аналогично примеру 8 из 5-(2,4-диметил-50 К 17,13. 3-хлор-6-нитрофенил)метид -2,4-ямида-С аНцКар
Пример 12. 7-Метокси-1,3-ди- гидро-2Н-имидазо(4,5-Ъ)хинолин-2-он.
Раствор 5- (2-нитро-5-метоксифе- нил)метилен -2,4-имидазолидиндиона (4,5 г, 17 ммоль) в диметилформамиде (120 мл) гидрировался над 10%-ным палладием на угле (0,45 г) при 4,219 кг/см . Через 42 ч смесь фильтровалась через инфузорную землю и растворитель упаривался, давая коричневое твердое вещество. Смесь этого вещества и метанола (150 мл) нагревалась с обратным холодильником и порци- 15 ями в нее Дьбавлялся йод (3,65 г, 14 ммрль) в течение 15 мин. Реакционная смесь на гревалась с обратным холодильником в течение 45 мин, охлаждалась и концентрировалась до 20 мл 20 перед добавлением раствора тиосульфата натрия (10 г) и карбоната натрия (10 f) в воде (100 мл), воды (200 мл) и фильтровалась. Перекристаллизация из водного диметилформамида давала 25 7-метокси-1,3-дигидро-2Н-имидазо (4,5-Ъ)хинолин-2-он (1,61 г, 43%), т.пл. 360°С.
Вычислено; С 61,39; Н 4,22; N 19,53.
C iHqNftOe
Найдено: С 61,21; Н 4,27; N 19,53.
ЯМР (ДМСО-аб):. 3,79 (З, синглет), 7,10 (1, двойной дублет, 3 Гц, 9 Гц), 7,28 (1, дублет, 3 Гц), 7,48 (1, синглет), 7,65 (1, дублет, 9 Гц), 10,90 (1, широкий синглет)i 11,32, (1, широкий сннглет).
П р и м е р 13. 1 ,3-ди141дро-6,7- 40 диметокси-2Н-имидазо(4,5-Ъ)хннолян-2- он.
30
35
Это соединение приготавливалось
аналогично примеру 7(Ъ) из 5-(4,5- 45 диметокси-2-нитрофенил),4- имидазолидиндиона. Целевой продукт
получался в виде белого пороипса (б4%),
т.пл. 320 С.
Вычислено: С 58,77; Н 4,52;
Найдено: С 58,38; Н 4,55; В 17.09. ЯМР (flMCO-dg): 3,88 (6, сингяет), 7,20 (1, синглет), 7,30 (1, сингяет), 55 7,49 (1, синглет), 10-50-11,50 (2, широкий синглет).
П р и м е р 14. 7-Бром-1,3-днгкдyil LX -- J J. «-у- -- - /у « .,
2,93 (3, синглет), 7,84 (1, сингле), ро-6,8-диметил-2Н-имидазо(4,5-Ъ)хи- 8,90 (1, синглет). .. нрлин-2-он.
золидиндиона (70%), т.пл. С
Вычислено: С 58,19; Н 4,07; N 16,97.
ClNgO
Найдено: С 57,92; Н 4,10.; N 17,03.
ЯМР (): 2,73 (З,-синглет).
10
,
.
.
;
, ,
450746
Пример 12. 7-Метокси-1,3-ди- гидро-2Н-имидазо(4,5-Ъ)хинолин-2-он.
Раствор 5- (2-нитро-5-метоксифе- нил)метилен -2,4-имидазолидиндиона (4,5 г, 17 ммоль) в диметилформамиде (120 мл) гидрировался над 10%-ным палладием на угле (0,45 г) при 4,219 кг/см . Через 42 ч смесь фильтровалась через инфузорную землю и растворитель упаривался, давая коричневое твердое вещество. Смесь этого вещества и метанола (150 мл) нагревалась с обратным холодильником и порци- 15 ями в нее Дьбавлялся йод (3,65 г, 14 ммрль) в течение 15 мин. Реакционная смесь на гревалась с обратным холодильником в течение 45 мин, охлаждалась и концентрировалась до 20 мл 20 перед добавлением раствора тиосульфата натрия (10 г) и карбоната натрия (10 f) в воде (100 мл), воды (200 мл) и фильтровалась. Перекристаллизация из водного диметилформамида давала 25 7-метокси-1,3-дигидро-2Н-имидазо (4,5-Ъ)хинолин-2-он (1,61 г, 43%), т.пл. 360°С.
Вычислено; С 61,39; Н 4,22; N 19,53.
C iHqNftOe
Найдено: С 61,21; Н 4,27; N 19,53.
ЯМР (ДМСО-аб):. 3,79 (З, синглет), 7,10 (1, двойной дублет, 3 Гц, 9 Гц), 7,28 (1, дублет, 3 Гц), 7,48 (1, синглет), 7,65 (1, дублет, 9 Гц), 10,90 (1, широкий синглет)i 11,32, (1, широкий сннглет).
П р и м е р 13. 1 ,3-ди141дро-6,7- 40 диметокси-2Н-имидазо(4,5-Ъ)хннолян-2- он.
30
35
50 К 17,13. С аНцКар
Это соединение приготавливалось
аналогично примеру 7(Ъ) из 5-(4,5- 45 диметокси-2-нитрофенил),4- имидазолидиндиона. Целевой продукт
получался в виде белого пороипса (б4%),
т.пл. 320 С.
Вычислено: С 58,77; Н 4,52;
Это соединение приготавливалось, в соответствии с примером 5 из 5- 0 И 4-диметил-3-бром-6-нитрофенил) метил -2,4-имидазолидиндиона (74%), т.пл, .
исчислено; С 49,34; Н 3,45; N I4,38i
,oBrN,0
Найдено: С 49,27; Н 3,50; N 14,42, . ЯМР (CFjCO jH): 2,76 (3, синглет), 2,09 (3, синглет), 7,81.
Пример 15, Дополнительные соединения указанной формулы получались восстановлением соответственно замещенного гидантоина согласно вышеприведенным примерам.
П р и м е р 16. 7-Бром-1,5-дигид- ро-2Н-имидазо(4,5-Ъ)хинолин-2-он, - I Используя методику примеров, -щолучают 7-бром-1,3-дигидро-2Н-имидазо |(4,5-Ъ)хинолин-2-он (8,45 г, 90%), ;т,го1. выше .
Вычислено: С 45,49; Н 2,30; Н 15,92.
С НбВгК,0 .
Найдено: С 45,69; Н 2,42; N 15,85.
ЯМР (flMCO-dfi):-дельта 7,61 (1Н, двойной дублет, Гц, Гц, ароматический Н), 7,62 «Н, синглет), 7,71 Он, дублет, Гц), 8,15 (Ш, дублет, 2 Гц).
П р и.м е р 17. 1,3-Дигидро-7-(1- ьйтилэтокси)-2Н-имидазо(4,5-Ъ)кино- лин-2-ttH.
Данное соединение (описанное в примере 15-6) приготавливалось аналогично примеру 12 из 5-(5-(1-метил14507А610
, ,
этокси)-2-нитро)метиленЗ-2,4-имида- золидиндиона (39%), т.пл. выше 320 С. Вычислено: С 64,19; Н 5,39; 17,27.
N
C,H,,.,..
Найдено: С 64,31; Н 5,40; N 17,11. ЯМР (ДМСО-(1б): дельта 1,35 (6Н,
дублет, ,5 Гц,
4,68 (1Н,
5
0
5
0
45
0
мультиплет, ОСН), 7,16 (IH, дублет, Гц, ароматический орто по отно- 5 шению к -0-), 7,35 (Ш, синглет), 7,59 (Ш, синглет, ароматический Н орто к NCO), 7,76 (1Н, .дублет ,1 ароматический Д орто к -0-), ГГ,04 (1Н, широкий синглет, NH), 11,45 (1Н, Q широкий синглет, NH).
Пример 18. 1,3-Дигидpo-6,7,8- тpимeтoкcи-2H-имидaзo (4,5-Ъ)хинолии- 2-он. ,
Данное соединение получалось аналогично примеру 12 из ,5,6-тримет- окси-2-нитрофенилметилен)-2,4-ииида- эолидиндиона (выход 61%), т.пл. выше .
Вычислено: С 56,73; Н 4,76; 15,27.
N
C«H«N,04
Найдено: С 56,90; Н 4,73; N 15,20.
ЯМР (ДИСО-с1б): дельта 3,83 (ЗН, синглет, ОСДэ), 3,90 (5Н, синглет, ОСН,), 3,95(ЗН, синглет, ОСН,), 7,08 (1Н, синглет, ароматический Н. орто к ОСИ,) 7,51 (1Н, синглет, ароматический Н.ОРТО к N00), 10,89 ( Ш, сииглет, Ш), 11,42 (Ш, синглет,
ВД).
Пример 19. 1,З-Дигидро-6- (трифторметил)-2Н-имидазо(4,5-Ъ)хи- нрлин-2-он.
Используя методику примера 12, бьшо получено названное соединение в виде твердого вещества, которое собиралось и сушилось в вакууме, давая I,З-дигидро-6-(трифторметил)-2Н-ими- дазо(4,5-Ъ)хинолин-2-он (1,38 г, 83%), т.пл. вьште 250°С.
Вычислено: С 52,18; Н 2,39; N 16,60.
i
Найдено: С 52,04; Н 2,43; N 16,64.
Пример 20. 1,3-Дигидро-1,8- димeтил-2Hrимидaзo (4,5-Ъ)хинолин-2- он.
Данное соединение, полученное в виде частично гидратированной гидроII
хлорндной соли, приготавливалось аналогично примеру 7Ь из 1-метил-5- L(2-метил-6-нитрофенил)метилен -2,4- имидазолидиндиона (выход 49%), т.пл. 340-341 С (разл.).
Вычислено: С 57,31; Н 4,89; N 16,71 .
,, N,0 HCl-0,lHjO.
Найдено: С 57,11; Н 4,75; N 16,57
ЯМР (flMCO-dg): дельта 2,66 (ЭЙ, синглет, ароматический СН.э), 3,41 (ЗН, синглет, N-CH), 7,19 (IH, дублет, Гц, ароматический Д орто к
(Ш), 7,45 (1Н, триплет, ароматичес- is N 18,49
145074612
ческий Н, синглет, орто к NHCO), 7, (1Н, дублет, Гц, ароматический ji. мета к ОСИ,).
Пример 23. 1,3-дигидро-1,7, триметил-2Н-имидазо(4,5-Ъ)хинолин-2 он.
Данное соединение приготавливало аналогично примеру 7б из 5-(2,3-ди 10 метш1-6-нитрофеннл)метилен -2,4-ими дазолидиндиона (выход 73%), т.пл, выше 300 С (кристаллизованное из ди метилацетамида).
Вычислено: С 68,70; Н 5,77;
кий Н мета к CHj), 7,71 (IH, дублет Гц, ароматический Н пара к СД), 7,87 (IH, синглет, ароматический Н. орто к ИН-СО).
П р и м е р 21. 1,3-Дигидро-1,7- диметил- 2Н-имидаз о ( 4 , 5-Ъ ) хинолин-2- он.
Данное соединение получалось аналогично примеру 7 из 1-метип-5-f(5CftH,,N,0. Найдено: С 68,36; Н 5,78; N 18,4 ЯМР (ДМСО-йб): дельта 2,42 (ЗН, синглет, СН), 2,55 (ЗН, синглет, 20 Щэ), 3,39 (ЗН, синглет, N-CH,), 7, (IH, дублет, ,5 Гц, ароматический Н. орто к СН), 7,67 (Ш, дублет, j ,5 Гц), 7,86 (1Н, синглет, аромат ческий « мета к CHj), 11,62 (1Н, си
метил-2-нитрофёнил)метилен -2,4-ими- 25 глет, NH), бензальдегид (32,08 г.
дазолидиндиона (выход 46%), т.пл. вьше 320 С.
Вычислено: С 67,36; Н 5,22; W 19,63.
С«2:Н„НзО 0,04НгО
Найдено: С 67,04; Н 5,21;11 19,64
ЯМР (ДМСО-а): дельта 2,46 (ЗН, синглет, ароматический СН,), 3,36 (ЗН, синглет, N-CH,), 7,35 (IH, дублет, Гц, ароматический Д орто к CHjj), 7,62 (1Н, синглет, ароматический П) f 7,65 (1Н, сннглет лроматичес- кий Д), 7,70 (1Н, дублет, j«7 Гц, ароматический Д мета к CMj).
Пример 22. 1 З-Дигидро-7-мет- до древесном угле (3 г) при 60фунт. окси-1-метил-2Н-имидазо(4,5-Ъ)хино- на кв. дюйм в аппарате гцдрнрова- ЛИН-2-ОН.ния Парра. После того, как поглощеДанное соединение, полученное в ние водорода прекращалось, смесь виде частичного гидрата, приготавли- фильтровалась через кизельгуц / и валось по примеру 76 из 5-(5- еток- д растворитель упарив ался, оставляя си-2-нитрофенил)метилен -1-метил-2,4- имидазолидиндиона (:виход 54%), т.пл. выше 310 С.
Вычислено: С 62,77; Н 4,85; N 18,30; 0,157
C гEцЩQз (),02Eyp.
Найдено: С 62,43; Н 4,85; N 18,14;
93%). Аналитический образец пригота ливался с помощью кристаллизации из дииз о пропил о во го эфира, т.пл. 66-68
Вычислено: С 60,33; Н 5,06; 30 N 7,82.
C,H,N,
Найдено: С 6Q,19; Н 5,27; N 8,27
Пример 24, 1,3-Дигидро-7,8- диметил-2Н-имидазо(4,5-Ъ)хинолин-2- он.
5-t(2,5-Диметил-6-нитрофенил)-не тилен -2,4-имидазолидиндион (19,95 76 ммоль) в диметилформамиде (350 мл гидрировался над 10%-ным палладием
50
HjO 0,094.
ЯМР (ДИСО-dg): дельта 3,34 (ЗН, синглет, Кен,), 3,86 (ЗН, сииглет, ОСН), 7,18(1Н, дублет, Гц, ароматический Н орто к ОСЦз), 7,30 (Н, синглет,.ароматический Ц. орто к ОСДз) 7,66 (1Н, синглет, ароматитвердое вещество, которое суспенди- ровалось в кипящем с обратным холог дильником метаноле (1 л). Порцияьш добавлялся йод (19,4 г, 76 ммоль) иа протяжении 5 мин и смесь нагревалась с обратным холодильником в течеиие 15 мин перед тем, как она ковдеитри- ровалась в вакууме до-примерно 100 м При этом энергичгном перемешивании gg добавлялся раствор тиосульфата натрия (21 г) и карбоната натрия (II г в воде (300 мл), давая бежевый осадок, который собирался, промывался водой и сушился на воздухе, давая
is N 18,49
5074612
ческий Н, синглет, орто к NHCO), 7,71 (1Н, дублет, Гц, ароматический ji. мета к ОСИ,).
Пример 23. 1,3-дигидро-1,7,8- триметил-2Н-имидазо(4,5-Ъ)хинолин-2- он.
Данное соединение приготавливалось аналогично примеру 7б из 5-(2,3-ди- 10 метш1-6-нитрофеннл)метилен -2,4-ими- дазолидиндиона (выход 73%), т.пл, выше 300 С (кристаллизованное из ди- метилацетамида).
Вычислено: С 68,70; Н 5,77;
CftH,,N,0. Найдено: С 68,36; Н 5,78; N 18,46, ЯМР (ДМСО-йб): дельта 2,42 (ЗН, синглет, СН), 2,55 (ЗН, синглет, Щэ), 3,39 (ЗН, синглет, N-CH,), 7,34 (IH, дублет, ,5 Гц, ароматический Н. орто к СН), 7,67 (Ш, дублет, j 8,5 Гц), 7,86 (1Н, синглет, ароматический « мета к CHj), 11,62 (1Н, синглет, NH), бензальдегид (32,08 г.
5 глет, NH), бензальдегид (32,08 г.
93%). Аналитический образец приготавливался с помощью кристаллизации из дииз о пропил о во го эфира, т.пл. 66-68 С;
Вычислено: С 60,33; Н 5,06; 0 N 7,82.
C,H,N,
Найдено: С 6Q,19; Н 5,27; N 8,27.
Пример 24, 1,3-Дигидро-7,8- диметил-2Н-имидазо(4,5-Ъ)хинолин-2- он.:
5-t(2,5-Диметил-6-нитрофенил)-не- тилен -2,4-имидазолидиндион (19,95 г, 76 ммоль) в диметилформамиде (350 мл) гидрировался над 10%-ным палладием
ние водорода прекращалось, смесь фильтровалась через кизельгуц / и растворитель упарив ался, оставляя
твердое вещество, которое суспенди- , ровалось в кипящем с обратным холог i . дильником метаноле (1 л). Порцияьш добавлялся йод (19,4 г, 76 ммоль) иа протяжении 5 мин и смесь нагревалась с обратным холодильником в течеиие 15 мин перед тем, как она ковдеитри- ровалась в вакууме до-примерно 100 мл« При этом энергичгном перемешивании добавлялся раствор тиосульфата натрия (21 г) и карбоната натрия (II г) в воде (300 мл), давая бежевый осаок, который собирался, промывался водой и сушился на воздухе, давая
3
15,7 г вещества. Оно объединялось р неочищенным материалом от экспериметов, проведенных с 40 и 4,16 г исходного вещества, суспендировалось горячей () воде, фильтровалось, суспендировалось в кипящем с обратным холодильником метаноле и фильтровалось. Кристаллизация из диметил ацетамида давала 1,З-дигидро-7,8-ди метил-2Н-имидазо(4,5-Ъ) хинолин-2-он (53,4 г, 65%), т.пл. выше .
Вычислено; С 67,59; Н 5,20; N 19,71.
СиН,НэО
Найдено: С 67,20; Н 5,20; N 19,5
ЯМР (ДМСО-ае): дельта 2,41 (ЗН, синглет, СН), 2,48 (ЗН, синглет, СН,), 7,31 (1Н, ку&пет, Гц, ароматический Н), 7,55 (1Н, дублет, j 8 Гц, ароматический Н) и 7,61 (Ш, синглет, ароматический Н).
П р и м е р 25, 1,З-Дигидро-7- этокси-2Н-имидазо(4,5-Ъ)хинолин-2-о t .Данное соединение (описанное в примере 15-7).приготавливалось аналгично примеру 2 из 5-П 5-этoкcи-2- нитpoфeнил )метилен -2,4-имидазолиди диона (43%), т.пл. выше .
Вычислено: С 62,88; Н 4,84; N 18,33.
0(2 Н
II N,0.2Таким образом, предложенные соединения которые обладают антитромбо-г генными свойствами (ингибируют агрегирование тромбоцитов крови) и свойствами ингибировать фосфодиэстеразу, полезны при профилактике или лечении заболеваний, при которых имеет место склеивание тромбоцитов и тромбозы.
Считается, что предложенные соединения обладают интиместазным потеи- 40 циалом в виду их свойств ингибирова- ния тромбоцитов.
Фармакологические свойства предложенных соединений могут быть продемонстрированы с помощью обычных био- 45 логических испытаний ин-витро и ин- виво.
Ингибирование ин-витро агрегирования тромбоцитов.
Для оценки активности ин-витро
35
Найденов С 62,68; Н 4,92; Н 18,16.
ЯМР (ДМСО-dg): дельта 1,36 (ЗН, триплет, Гц, ОСН2СНз 4,04 (2Н, кв. ), 6,97 (1Н, дублет, j 9 Гц, ,6 Гц, ароматический Н ор- то к Gift), 7,08 (1Н, дублет, ,6 Гц ароматический Н орто к OlHi), 7,26.. (Ш, синглет ароматический Н орто к NCO), 7,64 (1Н, дублет, Гц, ароматический Н мета к OEt).
Предложенные соединения или их фармацевтически приемлемые соли обладают фармакологическими свойствами, которые делают их особенно полезными в качестве ингибиторов фосфоди - эстеразы, антиагрегаторов тромбоцитов крови и/или кардиотонических агентов. Учитывая последнее, предложенные сое- 50 различных соединений в отношении ин- динения селективно усиливают сокраще гибиройания аденозин-дифосфата (АДФ) ние миокарда (сердечной мьшщы), с и агрегирования тромбоцитов, вызван- помощью которого сердце нагнетает кровь на периферию. Таким образом, предложенные соединения являются полезными при лечении или профилактике сердечных состояний, таких как мио- кардиальная недостаточность, когда необходима положительная инотропная
ного коллагеном, использовался метод измерения агрегирования Ббрна, 55 модифицированным автором Mustard, и др. Плазма, богатая тромбоцитами (РРР), отделялась от смеси крови кро лика и лимонной кислоты (3,8%). Для индуцирования агрегирования исполь14
0
5
активность. Предпочтительные соединения увеличивают силу сокращения, не увеличивая при этом чрезмерно сердечный ритм.
Агрегирование (скопление) тромбоцитов считается частью сложного физиологического механизма образования тромбов в сосудистой системе. Явле- Q ние тромбоэмболии, например образованием тромбов, имеет место при гемостазе (свертьшании крови) и ряде болезненных состояний млекопитающих, включающих тромбофлебит, флемботром- 5 боз, церебральный тромбоз, коронарный тромбоз и тромбоз сосудов сетчатки глаз. Увеличение склонности к агрегированию тромбоцитов, назьюае- мому иногда склеиванием тромбоцитов, наблюдается после родов, хирургических операций, таких как частичная хирургия венечной артери, трансплан- тацци органов, пластической хирургии, на сосудах, пересадки протезного сердечного клапана и при ишемических сердечных заболеваниях, атеросклерозе, рассеянном склерозе, внутричерепных опухолях, тромбоэмболизме и ги- перлипемии.
Таким образом, предложенные соединения которые обладают антитромбо-г генными свойствами (ингибируют агрегирование тромбоцитов крови) и свойствами ингибировать фосфодиэстеразу, полезны при профилактике или лечении заболеваний, при которых имеет место склеивание тромбоцитов и тромбозы.
Считается, что предложенные соединения обладают интиместазным потеи- 40 циалом в виду их свойств ингибирова- ния тромбоцитов.
Фармакологические свойства предложенных соединений могут быть продемонстрированы с помощью обычных био- 45 логических испытаний ин-витро и ин- виво.
Ингибирование ин-витро агрегирования тромбоцитов.
Для оценки активности ин-витро
0
35
50 различных соединений в отношении ин- гибиройания аденозин-дифосфата (АДФ) и агрегирования тромбоцитов, вызван-
различных соединений в отношении ин- гибиройания аденозин-дифосфата (АДФ) и агрегирования тромбоцитов, вызван-
ного коллагеном, использовался метод измерения агрегирования Ббрна, модифицированным автором Mustard, и др. Плазма, богатая тромбоцитами (РРР), отделялась от смеси крови кролика и лимонной кислоты (3,8%). Для индуцирования агрегирования использовался АДФ с конечной концентрацией 0,5 мкг/мл или 0,05 мл суспензии коллагена, полученной согласно извест- ной методике.
Различные испытьгоаемые соединения растворялись в диметилсульфоксиде (ДИСО) так, чтобы 5 мкп, добавленных к плазме, богатой тромбоцитами, давали требуемую испытываемую концентрацию. Продельшались контрольные опыты с носителем и сравнивались с опытами агрегирования, вызванного в богатой тромбоцитами плазме, содержащей различные концентрации испытываемых соединений. Получены бьши кривые ответной реакции на дозу и вычислялись величины эффективной концентрации (ECjj). В данном опыте величины для дипиридамола, используемого в клиниках антитромбогенного агента, составляют более 512 мкг/мл по сравнению с АДФ и 245 мкг/мл по сравнению с коллагеном.
Ингибирование агрегирования тромбоцитов после орального назначения.
Данное испытание иногда называют в технике как метод экс-виво. Анализ в основном осуществляется следующим образом.
Агрегометрия проводится ин-витро на пробах плазмы, богатой тромбоцитами, полученной от крыс, которым бьши даны дозы или испытывае &1х соедине- : НИИ или носителей. Во всех случаях активность определяется через 2 ч ; после назначения лекарства орально в различных дозах путем кормления че- рез. зонд в виде суспензии в 0,9% воды плюс несколько капель Твин-20. Активность лекарства вьфажается в виде БД50(это доза, требуемая для ин- гибирования вызванного агрегирования на 50%), вычисленной по результа
в пробирках для культуры. Данная реакция заканчивается путем погружения пробирок в кипящую водяную баню, после чего они помещаются на лед и в каждую пробирку добавляется алик- вота змеиного яда. Данная реакция при еще одном инкубировании превращает 5 AMP в аденозин. Для связывания остающегося циклического AMP добавляется ионообменная смола. Пробирки центрифугируются для осаждения смолы, а часть прозрачного плавающего сверху слоя (который содержит ра5 диоактивный аденозил) просчитывается в жидкостном сцинтилляциоином счетчике. Активность ингибирования сАМР фосфодизстеразы испытываемого агента определяется с помощью предваритепь0 ного инкубирования РДЕ ферментного препарата с испытываемым агентом.Получаются значения ответной реакции на дозу, и активность испытьгеаемого агента приводится в виде молярной концентрации испытьшаемого агента, ингибирующей 50% активности РДЕ (iCyo). В данном опыте значение ICjo милринона, агента, составляет
Инотропная активность ин-витро. Основной анализ представляет собой модификацию известного анализа. Морских свинок умерщвляют путем шейного смещения и быстро открывают серД це. На левое предсердие налагаются соединительные швы из щелковой нити, затем предсердия удаляются из животных и крепятся в тканевьк ваннах, где они стимулир.уются электротоком. После начального периода равновесия
5
0
0
известного инотропного 20 10 моль.
5
предсердия обрабатываются пропанолом в концентрации 10 моль. Это подавляет их натичную силу сокращения, но также делает их более чувствитепьны









Изобретение относится к гетероциклическим соединениям, в частности к получению производных 1,3-дигидро- 2Н-ймидазо(4,5-Ъ)хинолин-2-онов фор- мулй где Б - галоген нязпий алкил, ииз- ший алкокси, трифто 1етип; Rt - Н, галоген, низший алквл, низший алкок- си; В - Н, галоген, низший алкил, ннзший алкокси; В - Н или низпмй алкил, или их фармацевтически приемлемых солей, которые обладают лекарств енньми свойствами. Цель - выявление новых соединений указанного класса, обладающих данными свойствами. Получение целевых продуктов ведут из соответствующих замещенных гидаято- ина восстановлением и в случае необходимости восстановленный продукт обрабатывают окислителем. 2 табл. СО С
там, полученным на группах из -10 жи- 5 позитивные инотропным воздействотных, подвергнутых лечению различными дозами испытываемого соединения, в сравнении с отдельными контрольными
группами.
ВИЯМ ингибиторов фосфодизстеразы. Спо собность лекарств увеличивать силу сокращения предсердия оценивается. Получают кривые ответных реакций на
В данном опыте величина ЕДудДИпири- д дозы испытываемых соединений и резульдамола составляет больше, чем
100 мг/кг, а анагралида - 4,9 мг/кг.
Ингибирование циклической AMP фос- фодиэстеразы.
Меченый тритием циклический аде- нозин-монофосфат (сАМР) инкубируется с фосфодиэстеразой (РДЕ) ферментом, полученным из тромбоцитов человека, который превращает часть сАМР в 5 AMP
55
таты даются в виде процента от контрольного значения пропанола,. . Когда это необходимо, может также анализироваться хронотропная ответная реакция правого предсердия, которое бьется самопроизвольно.
Инотропн-ая активность ин-виво.
Испытание проводится на африканских хорьках следующим образом. Содер позитивные инотропным воздейстВИЯМ ингибиторов фосфодизстеразы. Способность лекарств увеличивать силу сокращения предсердия оценивается. Получают кривые ответных реакций на
5
таты даются в виде процента от контрольного значения пропанола,. . Когда это необходимо, может также анализироваться хронотропная ответная реакция правого предсердия, которое бьется самопроизвольно.
Инотропн-ая активность ин-виво.
Испытание проводится на африканских хорьках следующим образом. Содер11
жащиеся в голоде анестезированные хорьки оборудовались приборами для исследования гемодинамических парамеров, а также силы сокращения правого желудочка с использованием незамкнутой тензометрической арки. Лекарства назначались интрадуоданально в виде растворов в ДМСО (1 мл или менее), и действие на силу сокращения миокарда и другие параметры контролировались в течение 50 .мин после введения лекарства. Изменения силы сокращения в ответ на введение лекарства выражаются в виде процентного изменения по сравнению с контролем до введения дозы препарата.
В данном испытании милринон дает при 3 мг/кг увеличение силы сокращения правого желудочка на 52%.
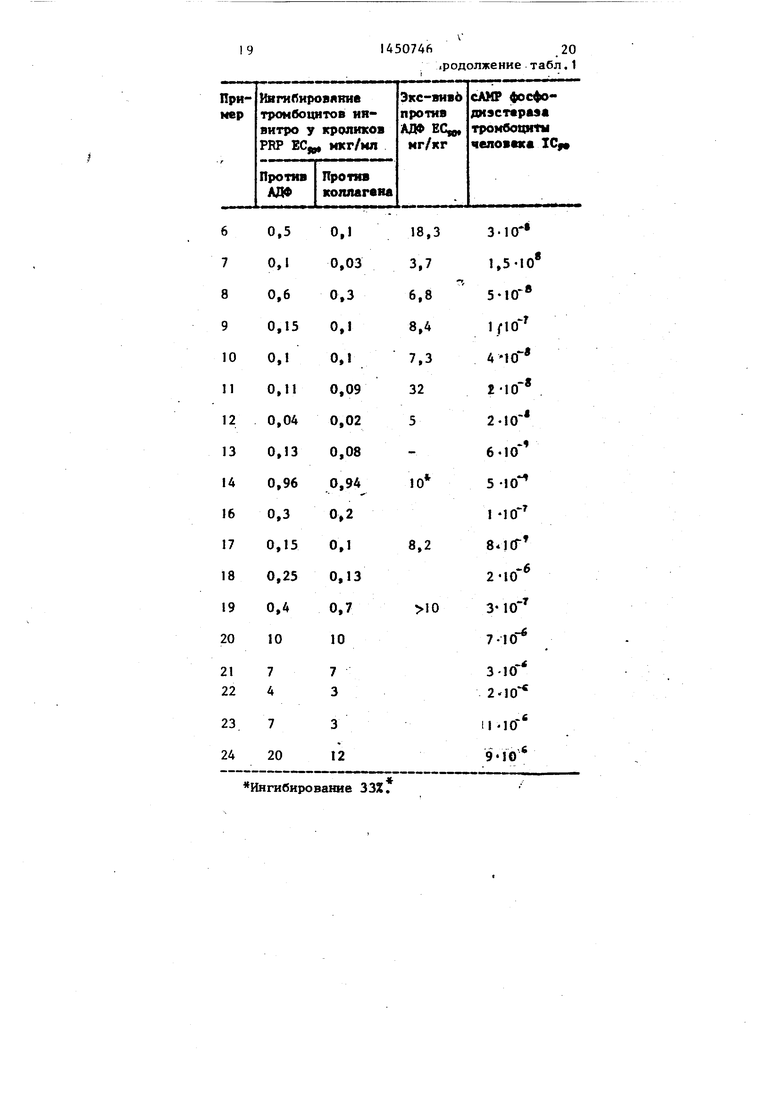
Ингибирование агрегирования тром- боЦитов и сАМР фосфодизстеразы приведено в табл. 1 .
Инотропная активность приведена в табл. 2.
I Формула изобретения
I
Способ получения производных 1,3-дигидро-2Н-имидазо(4,5-Ь)хино- ЛИН-2-ОНОВ формулы
07461Н
где R, - галоген, низший алкил, ни--- ший алкокси, трифторметил; . - водород, галоген, низший л
кил, низший алкокси; R- - водород, галоген, низгаий ал
кил, низший алкокси; R4 - водород или низший алкил, или их фармацевтически приемлемых солей, отличающийся тем, что замещенный гидантоин формулы
ЩОЙ
а
где а и Ъ
R
jR
- водород или вместе представляют ковалентную связь;
и R имеют указанные значения,
восстановлению и в случае необходимости восстановленный продукт обрабатывают окислителем. Приоритет по признакам:
одвергают
алкил, низший
алкокси;
водород, галоген,
низший алкил,
низший алкокси;
водород.
26,02.86 при трифторметил;
R, R, водород, галоген, низший алкил, низший алкокси; низший алкил.
Таблица 1
Ингибирование 33%.
21
1450746
Примечание: 1, Активность - увеличение силы сокращения: О - незначительная при 1СГ М; + - 50%-ное увеличение при 1, М; н- - 50%-ное увеличение при 10 Jtr w j
+++ - 50%-иое увеличение при 10 10- М{
++++ - 50%-ное увеличение при ниже
.
Редактор В.Данко Техред М.Ходанич Корректор М.Васильева
Заказ 6983/59 Тираж 370Подписное
ВПИШИ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб., д. 4/5
22 Та6лица2
| Kozak, et al., Bull | |||
| Intern | |||
| Acaol | |||
| Polanaise, 1930, A 432-438 (Chem | |||
| Abs., 25, 5400). |
Авторы
Даты
1989-01-07—Публикация
1986-04-24—Подача