шего спирта на трет-бутоксикарбонил- аминогруппу; К,-трет-бутоксигруппа и 3 4 С« йлкил, замещенный трет-бу- токсикарбониламиногруппой, проводят гидролиз с НС1 и получают R,- ОН и К С -С -алкиламин, Целевой продукт выделяют либо в свободном виде, либо в виде гидрохлорида. Новые соединения малотоксичны и при концентрации 0,1-1 мкмоль ингибируют фермент превращения ангиотензина I на 91-100% и реакцию вызванную ангиотензиноМ I при оральном введении в дозе 10 мг/кг после 20 мин на 82-98%, а при внутривенном введении в дозе 300 мкг/кг после 5 мин на 99-100%, 7 табл.
















Изобретение касается производных 2,3,4,5-тетрагидро-1,5-бензоксазе- пин-4-она, в частности получения веществ формулы I 6Н СН-СН-СН-(Ь-0- -CH -CrNH-CHR3-C(0)ORil-C(0)-t} -СН-г -С(0)К„ где R,-ОН, 1-трет-бутокси- карбонил-2-фенилэтиламино-, 1-кар- бокси-2-фенилэтнламино-, бензилокси- или трет-бутокси-группа; R/(- Н, , й-бутил, зтоксикарбонилметил или бензил; R,- Н, н- или изо-С-,-С9-алкил, этил (он замещен ,-циклоалкилом, , толилом, 4-тетрагидропиранилом или 4-тиенилом), С -С -алкил (он замещен 4-пиперидилом или 1-бензш1ОК- сикарбонш1-4-пиперидш10м) . кил (он замещен NH, трет-бутокси- карбониламино- или фталимидо-группой), или их гидрохлоридов, которые обладают гипотензивной активностью, что может быть использовано в медицине. Цель изобретения - создание способа получения нового класса гетероциклических веществ. Их синтез ведут ре- акцией соединений формул- II и III (::н сн-сн н-с.с-о-сн;-с(ш ;))-N СНг-С(О)R ;j(II) 1ти .его гидрохло- рида с СгНу-0-С(0)-С(0)-К (III), где R, - бензил-, окси- или трет-бу- токсигруппа, R в котором -алкил может быть замещен только фтал имидогруппой. Процесс ведут в среде низшего спирта в присутствии циан- боргидрида щелочного металла. При необходимости продукт: R,-бeнзилoкcи- группа и/или Rj-C -C -апкил, замещенный 1-бензилоксикарбонил-4-пипериди- лом, гидрируют над РА/С в среде спирта или (для Rj), обрабатывают НВг и получают R,вOHи Rз C -C -aлкил, замещенный 4-пиперидилом; R,- ОН, обрабатывают трет-бутиловым сложным эфиром фенилаланина в присутствии диэтилфос- форцианидата в среде диметилформамида при 0°С и получают R,- 1-трет-буток- сикарбонш1-2-фениламиногруппа; последнюю гидролизуют НС1 и получают R,- 1-карбокси-2-фенш1аминогруппа; R,- ОН или трет-бутоксигруппа и Rj- , последнюю отщепляют гидроокисью щелочного металла и вводят бензил- или этоксикарбонилметил- или н-бутилгруп- пу с помощью соответствующего гало- генида в среде диметилформамида в при- бутствии KI; R,-тpeт-бyтoкcигpyппoй и RJ- , первую гидролизуют НВг или НС1; и/или Rj- -алкил, замещенный фталимидогруппой, последнюю замещают с помощьюгидразингидрата и ди-трет-бутилкарбоната в среде низСО 4 сд 00 о 00 см

j Изобретение относится к способу получения новых производных 2,3,4,5- -тетрагидро-1,5-беизоксазепин-4-она Или их гидрохлоридов, которые облада- 1от антигипертонической активностью и Йогут найти применение в медицине. : Цель изобретения - разработка способа получения нового класса конденси Ьованных семичленных циклических соединений, обладающих антигипертоничес- Кой активностью при низкой токсичности.
Пример 1. В 30 мл этанола | астворяют 2 г бензил 3(8)-амино-4-ок со-2,3,4,5-тетрагидро-1,5-бензокса- эепин-5-ацетата гидрохлорида и в раствор вводят 0,45 г ацетата натрия 0,35 г уксусной кислоты, 0,45 г этил- 2-оксо-4-фенилбутирата и 10 г молекулярного сита 4А. После перемешива- мия смеси при комнатной температуре в течение 30 мин в смесь вводят по каплям раствор 0,34 г цианборгидрида натрия в 30 мл этанола в течение 3 ч. После дополнительного ввода в смесь раствора цианборгидрида натрия в 30 мл этанола в течение 1 ч реакционную смесь концентрируют при пониженном Давлении. В остаточный продукт концентрирования вводят 100 мл воды и 200 мл зтилацетата и смесь перемешивают. После удаления нерастворенного Б1ещества путем фильтрации этилацетат- Н1ЫЙ слой высушивают над безводным сульфатом магния и концентрируют при пониженном давлении. После ввода в остаточный продукт 50 мл простого этилового эфира и 1 г щавелевой кислоты смесь взбалтывают и разбавляют 300 мл петролейного эфира. Получен- ную смесь выстаивают в течение ночи. Вспльшший слой удаляют путем декантации и в осадок добавляют 50 мл воды и 300 мл этилацетата, после чего осуществляют нейтрализацию избытком бикарбоната натрия, Этилацетатный слой высушивают над безводным сульфатом магния и концентрируют при- пониженном давлении. Полученное масло отделяют и очищают в хроматографи- ческой колонке, наполненной силика- гелем (при элюировании смесью гекса этилацетат в отношении 5:1 - 2:1) и в результате первоначально получают бензил 3(3)(К)-этоксикарбо- нил-З-фенилпропил амино74-оксо-2,3,- 4,5-тетрагидро-1,5-бензоксазепин-5- ацетат в виде масла. Этот продукт растворяют в смеси 100 мл петролейного эфира и 20 мл простого диэтило- вого эфира,-в раствор вводят 1 мл раствора хлористый водород - этилаце тат (5 н.) и в результате получают 0,9 г гидрохлорида данного продукта в виде бесцветного порошка. Рассчитано, %: С 65,15 Н 6,01; N 5,07.
Cj,
Найдено, %: С 64,65; Н 6,17; N 4,94. 1
1-о -86,9 (csO,5 в метаноле).
Из последующих вьщеляющихся фракций бензил 3(3)- П(S)-этoкcикapбoнил -3-фeнилпpoпил амино-4-оксо-2,3,4,5- -тетрагидро-1,5-бензоксазепин-5-аце- тат получают в виде бесцветного масла. Этот продукт превращают в его гидрохлорид в виде бесцветного порошка (выход 1,3 г) таким же образом, как описано вьше.
Рассчитано, %: С 65,15, Н 6,01; N 5,07.
СэоНэгН О НС1
Найдено, %: С 64,97,; Н 6,18, N 4,99./
С(ЛУ- 62,(,5 в метаноле).
Пример 2. В 100 мл этанола растворяют 0,7 г бензил 3(S)(R)- -этоксикарбонил-3-фенилпропил амино- -4-ОКСО-2,3,4,5-тетрагидро-1,5-бен- зоксазепин-5-ацетата, гидрохлорида, полученного в примере 1, и осуществ- ю ляют каталитическое восстановление при нормальной температуре и при атмосферном давлении с использованием 0,5 г 10%-ного палладия на углероде (с содержанием 50% влаги) в качестве 15 катализатора; когда абсорбция водорода прекращается, катализатор отфильт- ровьшают и фильтрат концентрируют при пониженном давлении. В остаточный продукт концентрирования вводят 20 петролейный эфир и в результате Получают 0,53 г (8)-С1(К)-этоксикарбо- нил-3-фенилпропил Замино-4-оксо-2,3,- 4,5-тетрагидро-1,5-бензоксазепин-Зэтиловый эфир и полученную смесь выстаивают. Выпавшие в осадок кристаллы фильтруют и фильтрат обрабатывают раствором хлористый водород - этил- ацетат, выпавший в осадок порошок из влекают путем фильтрации и в результате получают 3(s)-И(8)-этоксикарбо нил-3-фенилпропил7 амино-4-оксо-2,3,- 4,5-тетрагидро-1,5-бензоксазепин-5- -уксусную кислоту, гидрохлорид, кото рый имеет более высокую оптическую чистоту.
, -103 (с-0,5 в метаноле).
П р-и м е р 4. В смеси 1 мл этано ла и 4 мл раствора (1 н.) гидроокиси натрия растворяют 0,15 г 3(S)(R) -этоксикарбонш1-3-фенилпропил амино- -4-ОКСО-2,3,4,5-тетрагидро-1,5-бенз- оксазепин-5-уксусной кислоты гидрохлорида, полученного в примере 2,полученную смесь выстаивают в течение 2 ч и слабо подкисляют 1 н. соляной кислотой. Осажденный порошок извле-уксусной кислоты, гидрохлорида в ви- 25 кают путем фильтрации, высушивают и
растворяют в 10 мл этанола. Нераство ренное вещество отфильтровывают и фильтрат высушивают при пониженном давлении, в результате чего получают 30 0,03 г 3(3)(Ю-карбокси-3-фенил- пропил амино-4-оксо-2,3,4,5-тетрагидро- 1,5-бензоксазепин-5-уксусной кислоты в виде бесцветного порошка.
де бесцветного порошка.
Рассчитано, %: С 57,44; Н 6,08, N 5,83.
C jH N jO -HCl- Найдено, %:С 57,39i Н 5,97; N 5,74.
,6 (свО,6 в метаноле), П р и м е р 3. Осуществляют каталитическое восстановление 1,1 бензил 3(S)-C1(S)-этoкcикapбoнил-3-фeнил- пpoпил амино-4-оксо-2,3,4,5-тетрагидро- 1 ,5-бензоксазепин-5-ацетата гидрохлорида, полученного в примере 1 таким же образом, как описано в примере 2, и в результате получают 0,8 г 3(S)-СК S)-этоксикарбонил-З-фенилпро пиламино-4-оксо-2,3,4,5-тетрагидро- -1,5-бензоксазепин-З-уксусной кислоты, гидрохлорида в виде бесцветного
;:С 58,54i Н 5,98;
порошка.
Рассчитано, N 5,94.
CijOi NiOf НС1 - 1/2
Найдено, %: С 58,45-, Н 6,08; N 5,71.
«( (,6 в метаноле) .
К данному продукту добавляют 10 мл воды и раствор экстрагируют три раза этилацетатом каждый раз порциями по 50 мл. Экстракт высушивают над безводным сульфатом магния и концентрируют при пониженном давлении. К маслянистому остаточному продукту концентрирования добавляют простой диэтиловый эфир и полученную смесь вы стаивают. Выпавшие в осадок кристаллы фильтруют и фильтрат обрабатывают раствором хлористый водород - этил- ацетат, выпавший в осадок порошок извлекают путем фильтрации и в результате получают 3(s)-И(8)-этоксикарбо- нил-3-фенилпропил7 амино-4-оксо-2,3,- 4,5-тетрагидро-1,5-бензоксазепин-5- -уксусную кислоту, гидрохлорид, который имеет более высокую оптическую чистоту.
, -103 (с-0,5 в метаноле).
П р-и м е р 4. В смеси 1 мл этанола и 4 мл раствора (1 н.) гидроокиси натрия растворяют 0,15 г 3(S)(R)- -этоксикарбонш1-3-фенилпропил амино- -4-ОКСО-2,3,4,5-тетрагидро-1,5-бенз- оксазепин-5-уксусной кислоты гидрохлорида, полученного в примере 2,полученную смесь выстаивают в течение 2 ч и слабо подкисляют 1 н. соляной кислотой. Осажденный порошок извлеают путем фильтрации, высушивают и
растворяют в 10 мл этанола. Нераствоенное вещество отфильтровывают и ильтрат высушивают при пониженном авлении, в результате чего получают 0,03 г 3(3)(Ю-карбокси-3-фенил- пропил амино-4-оксо-2,3,4,5-тетрагидро- 1,5-бензоксазепин-5-уксусной кислоты в виде бесцветного порошка.
Рассчитано, %: С 59,29; Н 5,92; N 6,59.
- 3/2 HiO
Найдено, %:С 59,63; Н 5,64; N 6,73.
112° (с 0,3 в метаноле). .
П р и м е р 5. Гидролиз 0,16 г 3 ( S) -{I ( S) -этоксикарбонил-3-фенилпро- пил амино-4-оксо-2,3,4,5-тетрагидро- -1,5-бензоксазепин-5-уксусной кислоты гидрохлорида, полученного в примере 3, осуществляют таким же образом, как описано в примере 4. Полученные кристаллы перекристаллизовывают из этанола и в результате получают 0,1 г 3(S7- 1(5)-карбокси-3-фенилпропил амино-4-оксо-2,3,4,5-тетрагидро-1,5- -бензоксазепин-5-уксусной кислоты в виде бесцветных призм, с т.ш1.127- 130°С.
Рассчитано, %: С 60,57; Н 5,81; 6,73.
CiiH,,N Oi HiG
Найдено, 60,44; Н 5.,69; 6,68.
,5(с 0,4 в метаноле).
10
Примере. Бензил 3(3)-амино -4-ОКСО-2,3,4,5-тетрагидро-1,5-бен- зоксазепин-5-ацетат гидрохлорид (1,5 г) и этил 4-циклоге1{скл-2-оксобутират (2,63 г) подвергают реакции восстановительного алкилирования аналогично тому как описано в примере 1 и пфдукт очищают в хроматографичес- кф колонке, наполненной силикагелем ( использовании в качестве элюен- та; смеси гексан - этилацетат в отношении 5:1 - 4:1). Из первой фракции получают 0,4 г бензил 3(S)-{1(R)- -э|гоксшсарбонил-3-циклогексилпропил - д амйно-4-оксо-2,3,4,5-тетрагидро-1,, 5-- -бензооксазепин-5-ацетат в виде бес- цв(тного масла.
; Рассчитано, %: С 68,94; Н 7,33: N $,36.
jC oHjjN.O, ;Найдено, % N $,57.
:М 110 (с
С 69,03; Н 7,27;1 в метаноле).
;Вторая фракция дает 0,4 г бензил 3($)-f1(5)-этоксикарбонил-3-циклогек- си пропил амино-4-оксо-2,3,4,5-тетрагидро- 1 ,5-бензоксазепин-5-ацетата в виде бесцветного масла,
Рассчитано, %: С 68,94 Н 7.33; N 5,36.
Н
CjoHj N O,
Найдено, %: С 69,08; Н 7,35; 5,60.
Пример 7. Осуществляют каталитическое восстановление бензил 3(S)- (Ю-этоксикарбонил-3-циклогексил- пропил; амино-4-оксо-2,3,4,5-тетрагид- ро-1,5-бензоксазепин-5-ацетат (0,35 г),4о полученного в примере 6, с использованием 10%-ного палладия на углероде в качестве катализатора, таким же образом, как описано в примере 2.Маслянистый продукт растворяют в простом эфире и в раствор вводят по каплям 0,5 мл раствора (5 н.) хлористого водорода - этилацетата, в результате чего получают 0,18 г (S) ЧКЮ-этокП р и м е р 8. Осуществляют каталитическое восстановление бензил 3(5)-П(8)-этоксикарбонил-3-цикло- гексилпрошш амино-4-оксо-2,3,4 5- -тетрагидро-1,5-бензоксазепин-5-аце- тата (0,35 г), полученного в примере 6, таким же образом, как описано в примере 2. В маслянистый продукт добавляют 0,31 г 3(s) (8)-этокси- карбонш1-3-циклогексш1пропил амино-4- -оксо-2,3,4,5-тетрагидро-1,5-бенз- оксазепин-5-уксусной кислоты в виде бесцветных призм, т.пл. 135-139 С.
Рассчитано, %:С 62,57; Н 7,53: N 6,34.
Ca3H32N20 1/2 HjO Найдено, %: С 62,7j Н 7,38: N 6,30. 20 М /-128 (с 0,5 в метаноле).
Данный продукт перекристаллизовы- вают дважды из смеси этилацетата с петролейным эфиром и в результате получают 3(S)(8)-этоксикарбонил-3- 25 -циклогексилпропил амино-4-оксо-2,3- 4,5-тетрагидро-1,5-бензоксазепин-5- -уксусную кислоту в. виде бесцветных призм, имеющих более высокую оптическую чистоту и т.пл. 146-148°с. 30 Рассчитано, %: С 63,87; Н 7,46; N 6,48.
CjjHj.N.O
Найдено, %:С 64,07; Н 7,64; N 6,45.
c/J;j-166 (с и 0,6 в метаноле). Пример 9, В 10 мл Ы,Ы-диме- . тилформамида растворяют 0,3 г 3(8)- -Г1(5)-этоксикарбонил-3-фенилпропил - амино-4-оксо-2,3,4,5-тетрагидро-1,5- -бензоксазепин-5-уксусной .кислоты гидрохлорида,.полученного в примере 3, и в раствор вводят трет-бутилфенил- апанинат (0,3 г). В данную смесь вводят раствор 0,13 г дизтилфосфоро- 45 цианидата в Н,К-диметилформамиде (по каплям) при температуре ледяной бани. После перемешивания полученной смеси в течение 10 мин вводят по-каплям раствор 0,14 г триэтиламина в
35
„„„,„.. , - H°v-iDUi/ и, 14 1- триэтиламина в
сикарбонил-3-циклогексилпропил амино- о N,N -диметилформамиде при температу- ц-ОКСО-2 .3. «. т-ТРФПЯГ-МППГ -1 Ч -rtatio- .„ -
-4-0КСО-2,3,4,5-тетрагидро-1,5-бенз- оксазепин-5-уксусной кислоты, гидрохлорида в виде бесцветного порошка.
Рассчитано, %: С 58,91; Н 7,09; N 5,97.
55
N
Найдено, %: С 58,89j Н 7,23; 5,82. (с, в; 0,5 В метаноле).
ре ледяной бани и смес1 перемешивают в течение 30 мин. В реакционную смесь вводят 200 мл этилацетата и полученную смесь промывают последовательно 50 мл воды, 50 МП 0,1 н. соляной кислоты (дважды), 50 мл 0,1 н. раствора гидрата окиси натрия и 50 мл воды. Этилацетатный слой высушивают над безводным сульфатом магния и концентN,N -диметилформамиде при температу .„ -
ре ледяной бани и смес1 перемешивают в течение 30 мин. В реакционную смесь вводят 200 мл этилацетата и полученную смесь промывают последовательно 50 мл воды, 50 МП 0,1 н. соляной кислоты (дважды), 50 мл 0,1 н. раствора гидрата окиси натрия и 50 мл воды. Этилацетатный слой высушивают над безводным сульфатом магния и концентрируют при пониженном давлении, в результате чего ползгчают 0,4 г трет-бу- тил 3(8)-t1(8)-этоксикарбонил-3-фе- нил-пропил амино-4-оксо-2,3,4,5-тет- рагидро-1,5-бензоксазепин-5-Ш1-Н-аце- тил-о -фенилаланината в виде бесцветного масла.
ИК
4uf.tct
СМ
1730
„«, .. . (Ш);
(сложный эфир); 1680; 1690 (амид), , Пример 10. В 100 мл5 и.раствора хлористого водорода в этилаце- тате растворяют 0,4 г трет-бутил 3(8)1(8)-этоксикарбонил-3-фенилпро- пил амино-4-оксо-2,3,4,5-тетрагидро- -1,5-бензоксазепин-5-ил-Ы-ацетил- -с -фенилаланината, полученного в примере 9, и раствор выстаивают в течение 4 ч. Реакционный раствор концентрируют при пониженном давлении и в остаточный продукт концентрирования вводят 50 мл простого эфира. Полученную смесь экстрагируют дважды насыщенным раствором бикарбоната натрия (по 70 мл в каждой экстракции) и водный слой экстрагируют 50 мл простого эфира. Водный слой нейтрализуют 1 н. соляной кислотой и экстрагируют 100 мл этилацетата. Этилацетатный слой высушивают над безводным сульфатом магния и концентрируют при пониженном давлении. Маслянистый продукт растворяют в 10 мл простого эфира и в раствор вводят 0,5 мл 5 н. раствора хлористого водорода в этилацетате, в результате получают 0,2 г 3(8)- -t1(8)-этоксикарбонил-3-фенилпропил - амино-4-оксо-2,3,4,5-тетрагидро-1,5- -бензоксазепин-5-ил-К-ацетил-о -фе- нилаланина гидрохлорида в виде бесцветного порошка.
Cod D -53,3 (с 0,5 в метаноле).
Рассчитано, 7,: С 63,00; Н 5,95; N 6,89.
Сз,Н,,НзО,.НС1
Найдено, %: С 62,75 Н 5,93, N 6,84.
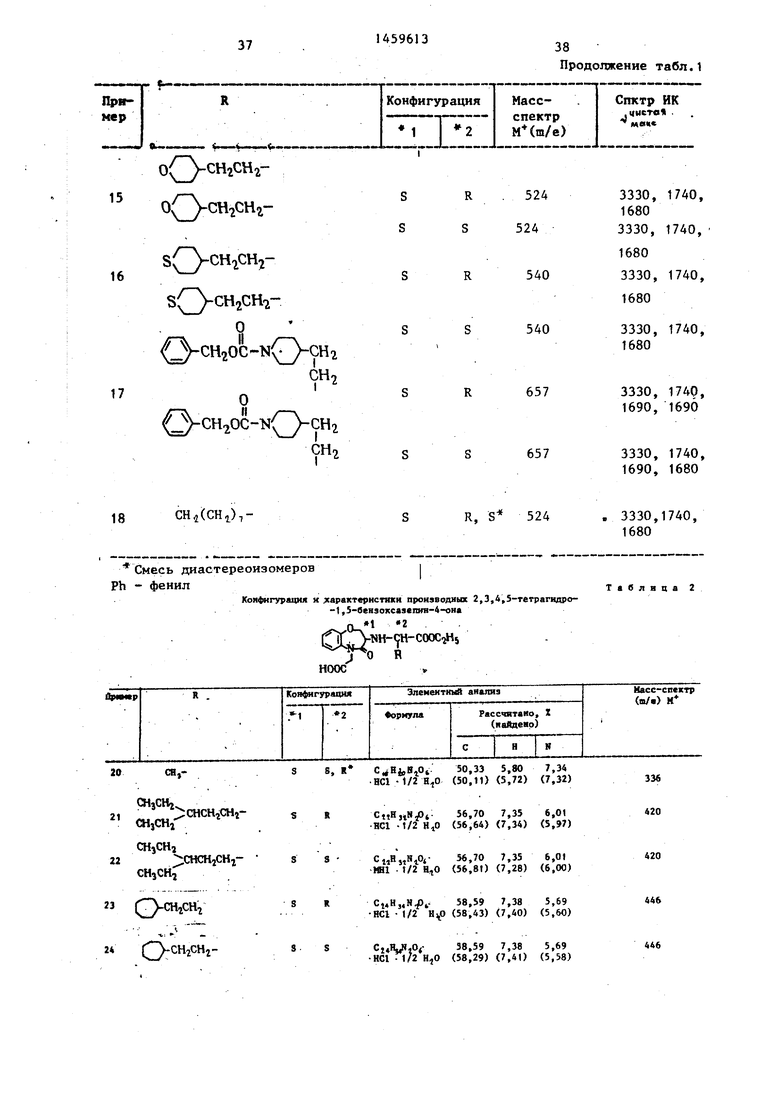
П р и м е р ы 11-18. ензил 3(8)- -амино-4-оксо-2,3,4,5-тетрагидро- -1,5-бензоксазепин-5-ацетаты, гидрохлориды, подвергают взаимодействию с этилпируватом или сложным о -кето- эфиром, аналогично тому, как описано в примере 1, и в результате получают соответствующие целевые соединения в виде масла, приведенные в табл.1.
Пример 19. По методике примера 1 получают продукт, который очи
15
20
° щают в хроматографической колонке, наполненной силикагелем (при элюи- ровании смесью гексан - этилацетат в отношении 4:3), и в результате получают 0,2Й г бензил 3(8)-этокси- карбонилметиламино-4-оксо-2,3,4,5- -тетрагидро-1,5-бензоксазепин-5-аце- тата в виде бледно-желтого масла.
ИК ., : , см- : 3330 (NH)i 1740;
MrtKC
1680 (С-р)
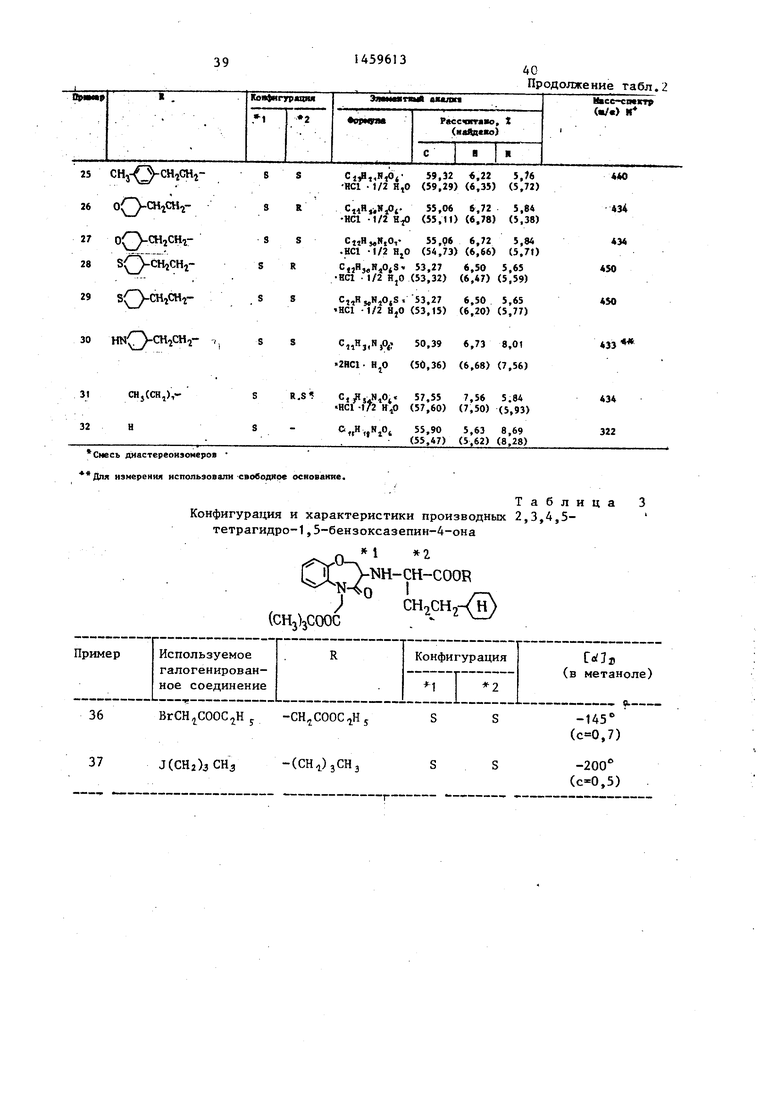
Масс-спект (ш/е): 412 (М) . C-S JD-148 (с 0,4 в метаноле). Примеры 20-32. Осуществляя каталитическое восстановление бензил- 1,5-бензоксазепин-5-ацетатного производного, полученного в примерах 11-18 с использованием 10%-ного палладия на углероде в качестве катализатора, таким же образом, как описано в примере 2, получают производные 1,5-бен- зоксазепин-5-уксусной кислоты, представленные в табл.2.
П р и м е р 33. Осуществляют вза25 имодействие 9,5 г трет-бутил 3(8)- -амино-4-оксо-2,3,4,5-тетрагидро-1,5- -бензоксазепин-5,-ацетата с этил-4-- -циклогексил-2-оксобутиратом в восстановительных условиях таким же об-
30 разом, как описано в примере 1, и полученный продукт очищают в хроматографической колонке, наполненной силикагелем (при элюировании смесью гексан-этилацетат в отношении 5:1).
25 Из первой фракции получают 2,3 г трет-бутил 3(S)-ri(R)-этоксикарбо- нил-3-циклогексилпропил амино-4-оксо- -2,3,4,5-тетрагидро-1,5-бензоксазе- пин-5-ацетата в виде бесцветного мас40 ла.
%: С 66,37; Н-8,25;
4В
50
55
Рассчитано, N 5,73.
C iH4oN Ot
Найдено, %: С 66,57; Н 8,57; N 5,48.
Масс-спектр (т/е): 488 (МО.
-112 (с 0,5 в метаноле).
Из второй фракции получают 3,2 г трет-бутил 3(8)(8)этоксикарбонил- -3-циклогексилпропил aминo-4-oкco- -2 , 3 , 4 , 5-тетрагидро-1,5-бензоксазе- пин-5-ацетата в виде бесцветного масла.
Рассчитано, %: С 66,37-, Н 8,25; N 5,73.
,,(, Найдено, %: 5,82.
С 66,72; Н 8,72;
1459613
Масс-спектр (m/e)j 488 (М)
)(с в 0,4 в метаноле). П р и м е р 34. В 100 мл этанола растворяют 1,5 г трет-бутил 3(8)- -I1(S)-этоксикарбонил-3 циклогексил- пропил}амино-4-оксо-2,3,4,5-тетра- Гидро-1,5-бензоксазепин-5-ацетата, полученного в примере 33, вводят по Каплям 1 н. раствор гидрата окиси натрия в течение 15 мин. После перевешивания в течение 3 ч раствор разбавляют водой (200 мл) и экстрагируют :)1ростым этиловым эфиром (100 мл).Вод- слой слабо подкисляют 1 н. соля- «ой кислотой и осаждаются кристаллы. ;|анный продукт извлекают путем фильтрации и высушивают и в результате по- Лучают 1,2 г трет-бутил 3(S)(S)- - кapбoкcи-3-циклoгeкcилnpoпилIaминo- -4-ОКСО-2,3,4,5-тетрагидро-1,5-бенз- оксазепин-5-ацетата в виде бесцветных игл, с т.пл. 180-183 С.
Рассчитано, %: С 65,20; Н 7,88 N 6,08.
; С 65,18; Н 7,83$ (с 0,5 в метаноле).
., Найдено, °/. N 6,14.
ro(D-122
П р и м- е р 35. В 10 мл Н,Н-диме- тилформамида растворяют 0,25 г трет- -бутил 3(S)-Cl(8)-карбокси-3-цикло- гексилпропил амино-4-оксо-2,3,4,5- -Гетрагидро-1,5-бензоксазепин-5-аце- тата, полученного в примере 34, ив Рйствор вводят бензилбромид (0,14 г), бикарбонат натрия (0,7 г) и йодид калия (0,05 г). Реакционный раствор перемешивают при комнатной температуре в течение 6ч., разбавляют водой (too мл) и экстрагируют этилацетатом. кстракт промывают последовательно 1 н, соляной кислотой и водой, высуивают над безводным сульфатом маг- кя и концентрируют при пониженном авлении. Маслянистый продукт очищают хроматографической колонке, наполенной силикагелем (при отношении ексан : этилацетат 5 : 1), в реультате чего получают 0,25 г трет- бутил 3(S)(5)-бензилоксикарбонил- 3-циклогексилпропил амино-4-оксо- 2,3,4,5-тетрагидро-1,5-бензоксазе- иМ-5-ацетат в виде бесцветного маса,
ИК см- : 3330 (NH); 1740} 680 (С-0)
«/Зв -155 (с «г 0,6 в метаноле). Масс-спектр (га/е): 550 (М)
10
Примеры 36-37. Осуществляя реакцию трет-бутил 3(S)(8)-карб- окси-3-циклогек силпропил амино-4-ок- со-2,3,4,5-тетрагидро-1,5-бензоксазе- пин-5-ацетата с соответствующим гало- генидом, аналогично примеру 34, получают бензоксазепиновые производные, приведенные в табл.3.
10
П р и м е р 38. В 10 мл 5 н. раствора хлористый водород-этилацетат растворяют 0,5 г трет-бутил 3(8)1(8)- -этоксикарбонил-З-циклогексилпропилЛг 15 амино-4-оксо-2,3,4,5-тетрагидро-1,5- -бензоксазепин-5-ацетата, полученного в примере 33, и раствор выстаивают при комнатной температуре в течение 4 ч. В раствор вводят 200 мл петро- 20 лейного эфира и полученную смесь тщательно взбалтывают. После удаления всплывшего слоя путем декантации ос- - таток разбавляпот 50 мл врды и трехкратно экстрагируют этилацетатом пор- 25 циями по 100 мл. Экстракт промывают водой, высушивают над безводным сульфатом магния и концентрируют при пониженном давлении. В вязкий остаточный продукт вводят простой этиловый 30 эфир и в результате получают 0,37 г 3- (s) -{1 (8)-этоксикарбоЯил-3-цикло- гексилпропил амино-4-оксо-2,3,4,5- -тетрагидро-1,5-бен:зоксазепин-5-ук- сусной кислоты в виде бесцветных кристаллов с т.пл. 135-139 С.
t JD-144 (с «: 0,3 в метаноле). Данный продукт перекристаллизо- вывают из этилацетата и петролейно- го эфира и в результате получают 40 3(3)-Г1(8)-этоксикарбонил-3-цикло- гексилпропил амино-4-оксо-2,3,4,5- -тетрагидро-1,5-бензоксазепин-5-ук- сусную кислоту в виде бесцветных призм, которая идентична соединению, 5 получаемому путем перекристаллизации в примере 8.
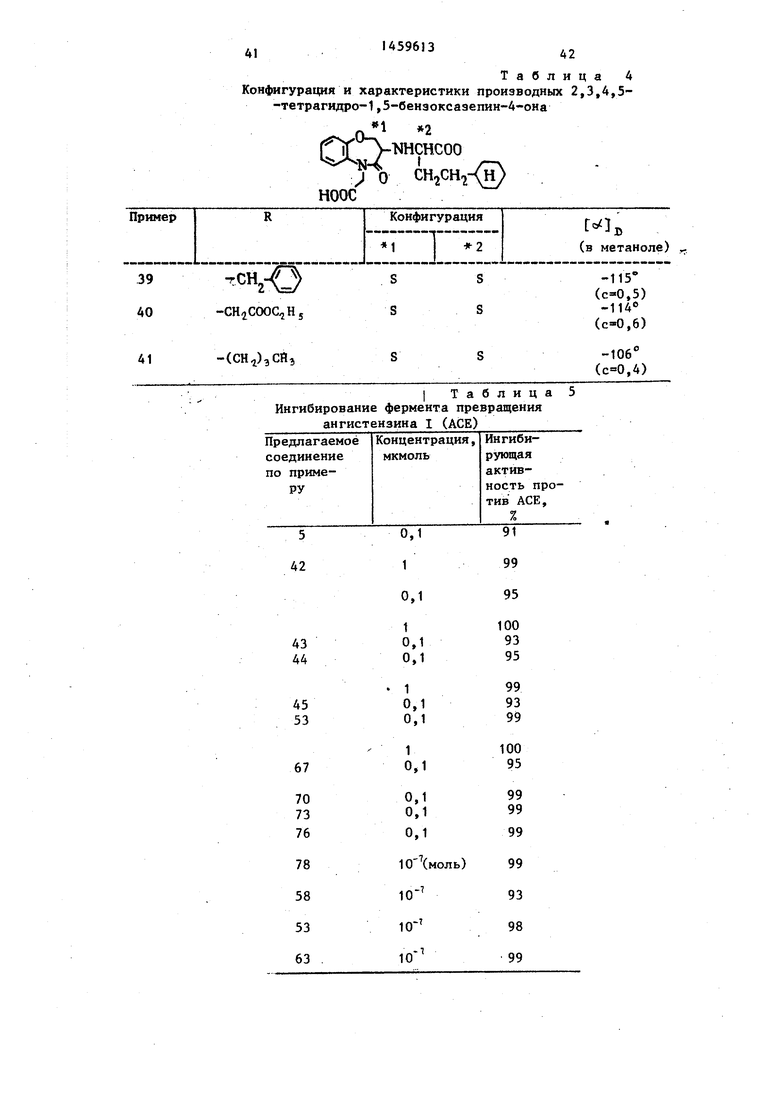
Пример 39-41. Производные трет-бутилового сложного эфира бенз- оксазепин-5-уксусной кислоты, полу- 0 ченные в примерах 35-37, подвергают обработке хлористым водородом аналогично описанию примера 38, в результате чего получают производные бензоксазепин- 5-уксусной кислоты, g приведенные в табл.4.
П р и м е р 42. В 1 мл этанола растворяют 0,2 г 3(S)(5)-этокси- карбонил-3-циклогексилпропил амино- -4-ОКСО-2,3,4,5-тетрагидро-1,5-бенз35
11
оксазепин-5-уксусной кислоты, полученной в примере 38, и в раствор вводят 3 мл 1 н. раствора гидрата окиси натрия. После перемешивания при комнатной температуре в течение 2 ч раствор слабо подкисляют 1 н. соляной кислотой. Осажденные кристаллы извлекают путем фильтрации, промывают водой, высушивают и перекристалли- зовьшают из этанола. Получают 0,14 г 3(S)- 1(S)-карбокси-3-циклогексил- пропил Замино-4-оксо-2,3,4,5-тетра- гидро-1,5-бензоксазепин-5-уксусной кислоты в виде бесцветных кристаллов с т.пл. 202-205 С.
Рассчитано, %: С 59,70;Н 7,16 N 6,63.
C,(.. HjO
N
Найдено, %: С 59,81; Н 7;03;
6,68.
Сс/ о-131° (с г 0,4 в метаноле).
Пример 43. ВЗмл 1 н. раствора гидрата окиси натрия растворяют 0,2 г 3 (S)-C1 (5)-этоксикарбонил- -3-(3,4,5,6-тетрагидро-2Н-пиран-4- -ил)пропил амино-4-оксо-2,3,4,5- -тетрагидро-1,5-бензоксазепин-5-ук- сусной кислоты, гидрохлорида, полученного в примере 2,7, и раствор выстаивают при комнатной температуре в течение 1 ч. Раствор нейтрализуют 1,5 мл уксусной кислоты и очищают в хроматографической колонке, наполненной Амберлитом XAD-2 (при элюировани смесью ацетон - вода в отношении 1:1 Элюат концентрируют при пониженном давлении и лиофилизируют. Получают 0,16 г 3(8)(5)-карбокси-3-(3,4,5-, 6-тетрагидро-2Н-пиран-4-ил)пропил - амино-4-оксо-2,3,4,5-тетрагидро-1,5- -бензоксазепин 5-уксусной кислоты в виде бесцветного порошка. Рассчитано, Z: С 57,82; Н 6,55;
6,74.
C,H,(N,Ov1/2 Н,0
Найдено, %: С 57,41; Н.6,01; 6,36.
Гв(3о- 128° (с в 0,4 в метаноле).
П р и м е р 44. 3(3)-С1(8)-Этокси карбонш1-3-(4-пиперидил)пропил амино -4-ОКСО-2,3,4,5-тетрагидро-1,5-бенз- оксазепин-5-уксусную кислоту, полученную в примере 30, подвергают гидролизу таким же образом, как описано в примере 43, очищают и люфилизирую Получают 3(S)-t1(3)-карбокси-3-(4-пи перидил)-пропил1амино-4-оксо-2,3,4,5 -тетрагидро-1,5-бензоксазепин-5-ук
N
N
2 виде
бесцветного по10
15
20
25 N зо -д). до
45
- до - ggт. - - сусную кислоту в рошка.
.JD -132°(с «0,6 в метаноле). Масс-спектр (т/е): 406 ().
П р и м е р 45. 3(S)-ri(S)-Этокси- карбонил-3-(4-тианил)пропил амино- - -оксо-2,3,4,5-тетрагидро-1,5-бензок- сазепин-5-уксусную кислоту, гидрохлорид, полученный в примере 29, подвергают гидролизу таким же образом,как описано в примере 43, и очищают в хроматографической колонке, наполненной Амберлитом XAD-2. Элюат концентрируют при пониженном давлении и в результате получают 3(S)-t1(S)- -карбокси-3-(4-тианил)про1Шл амино-4- -оксо-2,3,4,5-тетрагидро-1,5-бензок- сазепин-5-уксусную кислоту в виде кристаллов.
Рассчитано, %: С 54,53t Н 6,41; N 6,36.
C,,0,
с 54,12;
Найдено, %: С 54,12; Н 6,32; 6,30.
Пример46. В150мл ацето- нитрила растворяют 5 г бензил 3(8)- амино-4-оксо-2,3,4,5-тетрагидро-1,5- бензоксазепин-5-ацетата гидрохлорида и 13 г этил 2-бром-5-фталимидогек- саноата и в раствор вводят 3,2 г три- этиламина. После нагревания при 80°С в течение 4 дней раствор концентрируют при пониженном давлении, разбавляют 100 мл воды и экстрагируют 150 мл этила1;етата. Этилацетатный слой высушивают над безводным сульфатом магния и концентрируют при пониженном давлении, Этилацетат (15 мл) и щавелевую кислоту (3 г) вводят в остаточный продукт. В раствор вводят пет-, ролейный эфир (200 мл) и полученную смесь взбалтывают. После выстаивания всплывший слой отделяют путем декантации и в осадок добавляют 100 мл воды и 150 мл этилацетата. Полученную смесь нейтрализуют бикарбонатом натрия, Этилацетатный слой высушивают над безводным сульфатом магния и концентрируют при пониженном давлении.
Полученное в результате масло отделяют и очищают в хроматографической колонке, наполненной силикаге- лем (при элюировании смесью гек ан- этилацетат в отношении 2:1 - 3:2), в результате чего сначала получают 2,3 г бензил 3 (S)(К)-этоксикарбо- нил-5-тфталимидопентил амино-4-оксо13
-2,3,4,5-тетрагидро-1,5-бенэоксазе- Йин-5-ацетата в виде бесцветного масла.
ИК vZr , см- 3330 (NH)j - jl770i 1740; 1720,- t680 (С«0). i - 104°(в метаноле). j Из следующей фракции получают ензил 3(S)1(8)-этоксикарбонил-51А59613
14
-7-фталимидогептил амино-4-оксо-2,3,- -4,5-тетрагидро-1, 5ih6eH30Kca3enHH-5- -ацетата.
ИК см- 3340 (Н); 177S; 1740.; 1720, 1680, ()
метаноле).
Пример 49. В5мл5н. раствора хлористого водорода-этилацетата
фталимидопентил амино 4-оксо-2,3,4,-,Q растворяют 0,12 г трёт-бутил 3(8)- -тетрагидро-1,5-бензоксазепин 5-аце- -d (Ю-этоксикарбонил-7-фталимидогеп- faT в виде бесцветного масла, f , см- 3330 (Ш);
J760- 1710; 1680 (OOj. Co(Jo ОО (в метаноле).
Пример 47. В 20 мл этанола
тил амино-4-оксо-2,3,4,5-тетрагидро- -1дЗ-бензоксазепин-З-ацетата, полученного в примере 48, и раствор выстаи- 15 вшот при комнатной температуре в течение 3 ч, В раствор вводят петролей астворяют 0,15 г бензил 3(S)(S) 7этоксикарбонил-5-фталимидопентш1 - 4мино-4-оксо-2,3,4,5-тетрагидро-1,5- 4бензоксазепин-5-ацетата, полученно- о в примере 48, и осуществляют каталитическое восстановление при нор- 1|альной температуре и при атмосфер- Ном давлении при использовании 0,1 г 10%-ного палладия на углероде в качестве катализатора. После прекращения потребления водорода катализатор Отфильтровывают и фильтрат концентрируют при пониженном давлении. Маслянистый продукт растворяют в 3 мл простого этилового эфира, и в раствор вводят 0,5 Nm 5 н. раствора хлористого вОдорода-этилацетата. Получают 0,12 г 3(3)(5)-этоксикарбонилный эфир (100 мл) и выпавший осадок высушивают при пониженном давлении. Получают 0,08 г 3(8)-С1(Ю-этоксикар20 бонил-7-фталимидогептил амино-4-оксо- -2,3,4,5-тетрагидро-1,5-бензоксазё- пин-5-уксусной кислоты гидрохлорида, в виде бесцветного порошка. иЗр- 128(в метаноле).
25 Рассчитано, %: С 58, Н 5,90, N 7,03.
С,НззКэОг-НС1 - 1/г Найдено, % С 58,25 Н 5,75; N 7,08.
30 Пример 50. В 5 мл 5 н. раствора хлористого водорода - этилацета- та растворяют 0,11 г трет-бутил 3(8)- -tl(8)-этоксикарбонил-7-фталимидогеп- Ttm амино-4-оксо-2,3,4,5-тетрагидро-5-фталимидопентил амино-4-оксо-2,3, 35 -и5-бензоксазепин-5-ацетата, полу4,5-тетрагидро-1,5-бенз оксазепин-5 уксусной кислоты, гидрохлорида, в
виде бесцветного порошка.
Рассчитано, % С 56,07; Н 5,61;
К 7,54.
,- НС1 1/2 Найдено, %:С 56,19; Н 5,31;
N 7,44.
ченного в примере 48, и раствор выстаивают при комнатной температуре в течение 3 ч. В раствор вводят пет- ролейный эфир (100 мл) и осажденный 40 осадок высушивают при пониженном дав- Лении. Получают 0,095 г 3(8)(8)- -этоксикарбонил-7-фталимидогептил - амино-4-оксо-2,3,4,5-тетрагидро-1,5- бензоксазепин-5-уксусной кислоты.
Г. 104° (в метаноле).гидрохлорида, в виде бесцветного поПриме р 48. По методике приме- - „„тя-а ра 1 получают маслянистый продукт, отделяют и очищают в хроматографичес- кой колонке, наполненной силикагелем. Получают 1,5 г трет-бутил 3(8)(R)- -этоксикарбонил-7-фталимидогептил - амино-4-оксо-2,3,4,5-тетрагидро-1,5- -бензоксазепин-5-ацетата из первой
рошка,
Рассчитано, % С 58,34; Н 5,90; N 7,03.
C gHjjNjGj . НС1 -1/2
50
фракции.
WK ,1 ЧКСта - .
МС.КС см
1740; 1710; 1670 (). Г(п- 104 (в метаноле).
Из второй фра1едии получают 1,7 г трет-бутил 3(8)-t1(8)-этоксикарбонилНайдено, % С 58,43; Н 6,02j Ы 6,80.
104° (в метаноле). Пример 51. ВЮмл этанола
См«1 177П растворяют 0,7 г трет -бутил-3(8)- JJ4U i.iNH;, I//U, (S)-этoкcикapбoнил-7-фтaлимидoгeп- тил амино-4-оксо-2 ,3,4,5-тетрагидро- 1 ,5-бензоксазепин-5-ацетата,полученного в примере 48, и в раствор вводят 0,29 г гидразин гидрата. Пос14
-7-фталимидогептил амино-4-оксо-2,3,- -4,5-тетрагидро-1, 5ih6eH30Kca3enHH-5- -ацетата.
ИК см- 3340 (Н); 177S; 1740.; 1720, 1680, ()
метаноле).
Пример 49. В5мл5н. раствора хлористого водорода-этилацетата
растворяют 0,12 г трёт-бутил 3(8)- -d (Ю-этоксикарбонил-7-фталимидогеп-
растворяют 0,12 г трёт-бутил 3(8)- -d (Ю-этоксикарбонил-7-фталимидогеп-
тил амино-4-оксо-2,3,4,5-тетрагидро- -1дЗ-бензоксазепин-З-ацетата, полученного в примере 48, и раствор выстаи- вшот при комнатной температуре в течение 3 ч, В раствор вводят петролейный эфир (100 мл) и выпавший осадок высушивают при пониженном давлении. Получают 0,08 г 3(8)-С1(Ю-этоксикарбонил-7-фталимидогептил амино-4-оксо--2,3,4,5-тетрагидро-1,5-бензоксазё- пин-5-уксусной кислоты гидрохлорида, в виде бесцветного порошка. иЗр- 128(в метаноле).
Рассчитано, %: С 58, Н 5,90, N 7,03.
С,НззКэОг-НС1 - 1/г Найдено, % С 58,25 Н 5,75; N 7,08.
Пример 50. В 5 мл 5 н. раствора хлористого водорода - этилацета- та растворяют 0,11 г трет-бутил 3(8)- -tl(8)-этоксикарбонил-7-фталимидогеп- Ttm амино-4-оксо-2,3,4,5-тетрагидро-и5-бензоксазепин-5-ацетата, полученного в примере 48, и раствор выстаивают при комнатной температуре в течение 3 ч. В раствор вводят пет- ролейный эфир (100 мл) и осажденный осадок высушивают при пониженном дав- ении. Получают 0,095 г 3(8)(8)- -этоксикарбонил-7-фталимидогептил - амино-4-оксо-2,3,4,5-тетрагидро-1,5- бензоксазепин-5-уксусной кислоты.
гидрохлорида, в виде бесцветного по„„тя-а
рошка,
Рассчитано, % С 58,34; Н 5,90; N 7,03.
C gHjjNjGj . НС1 -1/2
Найдено, % С 58,43; Н 6,02j Ы 6,80.
10
ле отстаивания в течение ночи раствор концентрируют при пониженном давлении, разбавляют 50 мл воды и экстрагируют пять раз 30 мл (в каждой экстракции) этилацетата. В этилацетат- ный слой добавляют 50 мл воды и 0,7 мл бикарбоната натрия и в полученную смесь при одновременном перемешивании вводят по каплям 0,38 г ди-трет-бутилдикарбоната.После перемешивания смеси при комнатной температуре в течение 0,5 ч этилацетат- ный слой высушивают над безводным сульфатом магния и концентрируют при пониженном давлении. Остаточный продукт концентрирования очищают в хро- матографической колонке, наполненной силикагелем (при элюировании смесью гексан-этилацетат в отношении 2:1), и в результате получают 0,51 г трет- -бутил 3 ( S) -{7 -трет-бутоксикарбонил- амино-t(З)-этоксикарбонилгептилЗами- , НО-4-ОКСО-2,3,4,5-тетрагидро-1,5-бенз- оксазепин-5-ацетата в виде бесцвёт- 25 ного масла.
ИК Vlij c i 1740 1710; 1680 ().
- 122 (в метаноле).
пониженном давлении и лиофилизируют. Получают 0,31 г 3(8)-Г7-амико-1(S)- -кapбoкcигeптилJ-aминo-4-oкco-2,3,4,- 5-тeтpaгидpo- 1,5-бензоксазепин-5-ук- сусной кислоты в виде бесцветного порошка.
159 (в метаноле).
Масс-спектр (га/е) : 394 (МН).
П р и м е р 54. По методике примера 1, используя соответствующие исходные продукты, получают целевой продукт в виде маслянистого остатка,который подвергают разделение в хрома- 15 тографической колонке, наполненной силикагелем, с использованием для элюирования смеси гексан-этилацетат в отношении 2:1 - 1:1. После выпаривания первой фракции получают трет- бутил 3(S)-Cl-(R)-этоксикарбонил-6- -фталимидогексил амино-4-оксо-2,3,4,5- -тетрагидро-1,5-бензоксазепин-5-аце- тат (0,65 г) в виде бесцветного масла.
ИК ;:,Д7 см- : 3330 (NH)i 1770; 1740; 1710i 1680 ().
11 О(в метаноле).
Масс-спектр (га/е): 593 (М).
После выпаривания второй фракции
20
Пример 52. В 10 мл 5 н. раст- зо получают трет-бутил 3(8)С1(5)-этоксикарбонил-6-фтапимидогексил амино-4--оксо-2,3,4,5-тетрагидро-1,5-бензокса- зепин-5-ацетат (0,75 г) в виде бесцветного масла.
вора хлористого водорода - этилацетата растворяют 1,1 г трет-бутил- -3(8)- 7-трет-бутоксикарбониламино- -1(8)этоксикарбонилгептилДамино-4- -оксо-2,3,4,5-тетрагидро-1,5-бензок- сазепин-5-ацетата, полученного в примере 51, ,и раствор выстаивают при комнатной температуре в течение 3 ч. В раствор вводят петролёйный эфир и осадок высушивают при пониженном давлении. Получают 0,9 г 3(5)- 7-ами- но-1(S)-этоксикарбонилгептил7 амино- -4-ОКСО-2,3,4,5-тетрагидро-1,5-бенз- оксазепин-5-уксусной кислоты, гидрохлорида в виде бесцветного порошка. todj -108 (в метаноле). П р и м е р 53. В 15 мл 1 н. раствора гидрата окиси натрия растворяют 0,5 г 3(8)- 7-амино-1(8)-этоксикарбо- нилгептил -амино-4-оксо-2,3,4,5-тетрагидро- 1 ,5-бензоксазепин-5-уксусной кислоты дигидрохлорида, полученного в примере 52, и раствор выстаивают при комнатной температуре в течение 30 мин. В раствор вводят уксусную кислоту (3,5 мл), и смесь очищают в хроматографической колонке, наполненной Амберлитом XAD-2 (отношение мета- нол:вода 1:2).Элюат концентрируют при
0
25
пониженном давлении и лиофилизируют. Получают 0,31 г 3(8)-Г7-амико-1(S)- -кapбoкcигeптилJ-aминo-4-oкco-2,3,4,- 5-тeтpaгидpo- 1,5-бензоксазепин-5-ук- сусной кислоты в виде бесцветного порошка.
159 (в метаноле).
Масс-спектр (га/е) : 394 (МН).
П р и м е р 54. По методике примера 1, используя соответствующие исходные продукты, получают целевой продукт в виде маслянистого остатка,который подвергают разделение в хрома- 5 тографической колонке, наполненной силикагелем, с использованием для элюирования смеси гексан-этилацетат в отношении 2:1 - 1:1. После выпаривания первой фракции получают трет- бутил 3(S)-Cl-(R)-этоксикарбонил-6- -фталимидогексил амино-4-оксо-2,3,4,5- -тетрагидро-1,5-бензоксазепин-5-аце- тат (0,65 г) в виде бесцветного масла.
ИК ;:,Д7 см- : 3330 (NH)i 1770; 1740; 1710i 1680 ().
11 О(в метаноле).
Масс-спектр (га/е): 593 (М).
После выпаривания второй фракции
0
о получают трет-бутил 3(8)С1(5)-этоксикарбонил-6-фтапимидогексил амино-4--оксо-2,3,4,5-тетрагидро-1,5-бензокса- зепин-5-ацетат (0,75 г) в виде бесцветного масла.
ИК л)Ч: в1с см- : 3320 (Ш); 1770 1740; I710i 1670 ().
Wlfl 123(в метаноле).
Масс-спектр (т/е): 593 (М).
Приме р 55. Смесь 5 н. раство- . ра хлористого водорода-зтилацетата
5
5
0
5
(5 мл) и трет-бутил 3(S)-Cl(8)-эток- сикарбонил-б-фталимидогексил амино- -4-ОКСО-2,3,4,5-тетрагидро-1,5-бенз- оксазепин-5-ацетата (О,1 г) выстаивают при комнатной температуре в течение 3 ч. Эту смесь разбавляют петро- лейным эфиром (80 мл) и осаждают бесцветный порошок, который извлекают и высушивают в вакууме. Получают 3(S)-t1(8)-этоксикарбонил-6-фталими- догексил амино-4-ОКСО-2,3,4,5-тетрагидро- 1,5-бензоксазепин-5-уксусную кислоту, гидрохлорид (0,08 г). jj - 108°(в метаноле). Рассчитано, %: С 57,68; Н 5,53 N 7,21., ,
CjjH 3,N 0,-HCl - 1/2 Найдено, %: С 57,65; Н 5,65; N 7,13.
Пример 56,.Смесь трет-бутил 3(S)-П(S)-этоксикарбонил-6-фтали- мидогексил амино-4-оксо-2,3,4,5-тет- рагидро-1,5-бенэоксаэепин-5-ацетата (0,65 г)5 гидразин гидрата (0,27 г) и. этанола (10 мл) выстаивают в течение ночи при комнатной температуре. Сйесь концентрируют в вакууме, раз- б вляют водой (50 мл) и экстрагируют амилацетатом (50 мл х 4). В смесь органического экстракта, воды (50мл и бикарбоната натрия (0,65 г) вво- ло каплям ди трет-бутилдикарбо нфт (0,36 г) с одновременным пере- мфшиванием при комнатной температу- рф. После перемешивания смеси в те- чфние 30 мин этиладетатный слой от- дфляют, высушивают над безводным сульфатом магния и концентрируют в вфкууме. Остаточный продукт концентрирования подвергают разделенрда в Х1|оматографической колонке, наполнен ной силикагелем, с использованием сйеси гексан-этилацетат в отношении 2s1 - 1;1 для элюирования, и.в результате получают трет-бутил 3(5)- - 6-трет-бутоксикарбониламино-1(S)- -Этоксикарбонилгексил амино-4-оксо- -2,3,4,5-тетрагидро-1,5-бензоксазе- пин-5-ацетат (0,54 г) в виде бесцветного масла.
ИК . см : 1740 1720 1680 (С-0).
128 (в метаноле).
Масс-спектр (т/е) : 563 (М) ,
Приме р 57. Раствор трет-бу- тил-3(8)-Гб-трет-бутоксикарбонилами- но-1(5)-этоксикарбонилгексил амино- -4-ОКСО-2,3,4,5-тетрагидро-1,5-бенз- оксазепин-5-ацетата (0,5 г) в 5 н. растворе хлористого водорода-этил- ацетата (10 мл) выстаивают в течение 3,5 ч при комнатной температуре. В раствор вводят петролейный эфир (80 мл), образзтощийся осадок извлекают и высушивают в вакууме. Получают 3(5)-Гб-амино-1 (8)-этоксикарбонш1- гексил амино-4-оксо-2,3,4,5-тетра- ги,цро-1,5-бензоксазепин-5-уксусную кислоту, дигидрохлорид (0,4 г), в виде бесцветного порошка.
118°(в метаноле). Масс-спектр (т/е) : 407 (М) . П р и м емр 58. Раствор 3(S) -a)№iHo-1 (S) -этоксикарбонилгексил ами- но- 4-оксо-2,3,4,5-тетрагидро-1,5-бенз океазепин-5 уксусной кислоты,дигидро- хлорида (0,35 г), в 1 н, растворе
гидрата окиси натрия (10 мл) выстаивают в течение 30 мин при комнатной температуре. После добавления уксус- ной кислоты (2,5 мл) смесь подвергают разделению в хроматографической колонка, наполненной Амберлитом XAD-2, с использованием для элюирования смеси метанол-вода в отношении 1:10. Элюат 0 концентрируют при пониженном давлении и лиофилизируют, Получают 3(3)Сб-ами- но-1(S)-карбоксигексил амино-4-оксо- -2,3,4,5-тетрагидро-1,5-бензоксазепин- 5-уксусную кислоту (0,17 г) в виде 5 бесцветного порошка.
,- 157° (в метаноле). Масс-спектр (га/е) : 380 (МН). Г(5)-карбоксиоктил амино-4-оксо- -2,3,4,5-тетрагидро-1,5-бензоксазеш1н- 0 5-уксусная кислота (0,2 г) в виде бесцветного порошка.
Рассчитано, %:С 56,46 Н 7,34; 9,87.
.gNjO.-HiO
Найдено, %:С 56,61; Н 6,86; 9,85.
Id If 147 (в метаноле).
Спектр SIMS (т/е): 408 (МН).
П р и м е Р 59. По методике приме- 0 Р 1 используя соответствующие исходные продукты, получают т слянистый остаток целевого продукта, который подвергают хроматографическому разделению в колонке, наполненной силика5
N
N
5
0
элюента смеси гексан-этилацетат в отношении 2:1. После вьшаривания первой фракции получают трет-бутил 3(S) -(К)-этоксикарбонил-9-фталимидононил - амино-4-оксо-2,3,4,5-тетрагидро-1,5- -бензоксазепин-5-ацетат (0,45 г) в виде бесцветного масла.
ИК
чмстао мс«с
СМ- : 3320 (Н)., 1770;
5
0
5
1740; 1740; ().
Го(ц- 100 (в метаноле).
Масс-спектр (т/е): 635 (М).
Из второй фракции получают трет-бутил 3(S)(8)-этоксикарбонил-9-фтал- ИМИДОНОНШ1 j амино-4-оксо-2,3,4,5-тетрагидро-1 ,5-бензоксазепин-5-ацетат (0,55 г) в виде бесцветного масла.
ИК л1 см- : 3320 (NH)i 1770,- 1740; 1710; 1680 ().
- 98 (в метаноле).
Масс-спектр (т/е) : 635 (М) .
П р и м е р 60. Смесь трет-бутил 3(S)-tl(8)-этоксикарбонил-9-фталимидо- нонил амино-4-оксо-2,3,4,5-тетрагидро- 1,5-бензоксазепин-5-ацетата (0,08 г)
19
и 5 н, раствора хлористого водорода этилацетата (5 мл) выстаивают при комнатной температуре в течение 3 ч. Смесь разбавляют петролейным эфиром (80 мл), в результате осалщается бесцветный порошок, который извлекают и высушивают при пониженном давлении. Получают 3(8)(5)-этокси- карбонш1-9-фталимидононил амино-4- -оксо-2,3,4,5-тетрагидро-1,5-бензок- сазепин-5-уксусную кислоту, гидрохлорид (0,066 г).
CO IB - 101° (в метаноле). Рассчитано, %: С 58,56; Н 6,29; N 6,72.
Сз,Нз7Кз02-1/2 Н-гр Найдено, %: С 39,29; Н 6,48; N 6,51.
П р и м е р 61. Смесь трет-бутил 3(3)(8)-этоксикарбонил-9-фталими- дононил амино-4-оксо-2,3,4,5-тетра- гидро-1,5-бензоксазепин-5-ацетата (0,47 г), гидразингидрата (0,18 г) и этанола (10 мл) выстаивают в течение ночи при комнатной температуре. Смесь концентрируют при пониженном давлении, разбавляют водой (50 мл) и экстрагируют этилацетатом (50 мл х X 4). В органический экстракт вводят воду (50 мл) и бикарбонат натрия (0,5 г) и к полученной смеси добавляют по каплям с од новременным перемешиванием ди-трет-бутилдикарбонат (0,24 г). После перемешивания в течение 30 мин при комнатной температуре этилацетатный слой высушивают над .безводным сульфатом магния и концентрируют в вакууме. Остаточный продукт концентрирования очищают в хромато- графической колонке, наполненной силикагелем, с использованием в качестве элюента смеси гексана с этил- ацетатом в отношении 2:1, и в результате получают трет-бутил 3(S) -трет-бутоксикарбонилам11Но-1 (5)-эток сикарбонилнонил амино-4-оксо-2,3,4,5 -тетрагидро-1,5-бензоксазепнн-5-аце- тат (0,35 г) в виде бесцветного масла.
ИК м 1740i 1710i 1680 ().
Масс-спектр (т/е): 605 (М) . 1 16 (в метаноле).
П р и м е р 62. Смесь трет-бутил 3(S)- 9-трет-бутоксикарбониламино- -1(8)-этоксикарбонилнонил амино-4-ок- со-2,3,4,5-тетрагидро-1,5-бензокса- зепин-5-ацетата (0,33 г) и 5 н. раст1459613
20
вора хлористого водорода - этилацетата (8 мл) выстаивают в течение 2,5 ч при комнатной температуре. Смесь разбавляют петролейным эфиром (80 мл), в результате чего осазкдается бесцветный порошок, которЬ1Й извлекают и высушивают при пониженном давлении. Получают 3(8)- 9-амино-1(5)-этоксикарО бонилнонил амино-4-оксо-2,3,4,5-тет- рагидро-1,5-бензоксазепин-5-уксусную кислоту, дигидрохлорид (0,25 г).
Рассчитано, %:С 51,11} Н 7,26, N 7,77.
5 С1зНзуНзО -2НС1-
Найдено, %: С 51,17; Н 7,57-, N 7,34.
110 (в метаноле).
0 Пример 63. Раствор 3(S) -амино-1(S)-этoкcикapбoнилнoнилJaми- НО-4-ОКСО-2,3,4,5-тетрагидро-1,5-бенз- оксазепин-5-уксусной кислоты, ди- гидрохлорида (0,2 г) в 1 н. растворе
5 гидрата окиси натрия (6 мл) выстаивают в течение 30 мин при комнатной температуре. Ввводят уксусную кислоту (1,5 мл) и полученную смесь подвергают разделению в хроматографической
0 колонке, наполненной Амберлитом XAD-2, с использованием в качестве элюента смеси метанол-- вода в отношении 1:2. Элюат концентрируют в вакууме, и лио- . филизируют. Получают 3(8)- 9-амино- -1 (S)- карбоксинонил -амино-4-оксо-- -2,3,4,5-тетрагидро-1,5-бензоксазе- пин-15-уксусную кислоту (0,15 г) в виде бесцветного порошка.
Рассчитано, %: С 57,39; Н 7,57;
0 N 9,56.
Сг,Н j,N,,20 Найдено, %:С 57,42; Н 7,27; N 9,58.
)- 142° (в метаноле).
5 Спектр SIMS (m/e): 422 (МН).
П р и м е р 64. Смесь бензил 3(8)- -амино-4-оксо-2,3,4,5-тетрагидро-1,5- бензоксазепин-5-ацетата,гидрохлорида (2,5 г), этанола (30 мл), ацетата натg рия (0,57 г), уксусной кислоты (0,4 г), этил 5-(1-бензилоксикарбонил-4-пипе- ридил)-2-оксовалерата (2,5 г) и молекулярного сита ЗА(10 г) перемешивают в течение 10 мин при комнатной темпеg ратуре. К перемешанной смеси добавляют по каплям раствор цианборгидрида натрия (0,4 г) в этаноле (50 мл) в течение 2 ч. После выстаивания в течение ночк при комнатной температуре смесь
5
концентрируют в вакууме и разбавляют смесью воды (300 мл) и этилацетата (300 мл). Полученную смесь тщательно перемешивают и фильтруют, Этилацетат нйй слой отделяют, высушивают над безводным сульфатом магния и концент р|фуют в вакууме. Остаточный продукт растворяют в смеси этилацетата (20 мл с| щавелевой кислотой (2 г,). Данный pjacTHop разбавляют петролейным эфи- ррм (300 мл) и всплывший слой уда- путем декантации. К осадку до- б вляют воду (100 мл), этилацетат (|200 мл) и избыточное количество би- к рбоната натрия, Этилацетатный слой р -деляют, высушивают над безводным с гльфатом магния w выпаривают в ва . Маслянистый остаточный продук пЬдвергают разделению в-хроматогра- ф 1ческой колонке, наполненной силика гёлем, с использованием в качестве эЛюента смеси гексана с этилацетатом в отношении . После выпаривания первой фракции получают бензил 3(5)- (1-бензилоксикарбонил-4-пипери- дйл)-1 (Ю-этоксикарбонил амино-4-ок- со-2,3,4,5-тетрагидро-1,5-бензокса- зепин-5-ацетат (0,65 г) в виде бесцветного масла.
Ж чмсгпя Ма Kf
„-г
СМ-: 3320 (Ш); 1740 1690J 1680 (С-0).
Масс-спектр (т/е): 671 (М).
Из второй фракции получают бензил 3(S)-t4-(1-бензилоксикарбонил-4-пипе- ридил)-1(8)этоксикарбонил-бутил3ами- НО-4-ОКСО-2,3,4,5-тетрагидро-1,5-бенз оксазепин-5-ацетат (0,75 г) в виде бесцветного масла.
ИК , 3320 (NH), 1740, 1690, 1680 (С«0).
Масс-спектр (т/е): 671 (М).
П р и м е р 65. Раствор бензил 3 S) - Г4-( 1 -бензилоксикарбонил-4-пипе- рндил)-1 (Ю-этоксикарбонилбутилЗами НО-4-ОКСО-2,3,4,5-тетрагидро-1, 5- бензоксазепин-5-ацетата (0,65 г) в этаноле (50 мл) подвергают каталитическому гидрогенолизу над 10%-ным пйлладием на углероде (1 г, 50% влаги) при комнатной температуре и атмосферном давлении. После прекращения потребления водорода катализатор удаляют путем фильтрации и фильтрат выпаривают в вакууме. Остаточный продукт растирают четырехкратно с простым этиловым эфиром (100 мл) и затем растворяют в этаноле (5 мл). К данному раствору добавляют 5 н.
раствор хлористого водорода - этил- ацетата (1 мл) и полученную смесь разбавляют простым эфиром.Получают в осадке 3(8)-Г1 (Ю-этоксикарбонил- -4-(4-пиперидил)бутиламино-4-оксо- -2,3,4,5-тетрагидро-1,5-бензоксазе- пин-5-уксусную кислоту, дигидрохло- рид (0,12 г) в виде бесцветного порошка.
; Рассчитано, %: С 49,64; Н 7,06 N 7,55.
,
5 N
2НС1
С 49,17;
2НгО
Н 6,99,
0
5
0
5
Найдено, : 7,52.
CWJi)- 121 (в метаноле). П р и м ер 66. Раствор бензил 3(S)-t 4-(1-бензилоксикарбонил-4-пипе- ридил)-1-(5)этоксикарбонилбутил ами- НО-4-ОКСО-2,3,4,5-тетрагидро-1,5-бенэ- оксазепин-5-ацетата (0,75 г) в этаноле подвергают каталитическому гидрогенолизу над 10%-ным палладием на углероде (1 г, 50% влаги) при нормаль- ной температуре и под давлением до тех пор, пока не прекращается потребление водорода. После удаления катализатора путем фильтрации фильтрат концентрируют и разбавляют простым этиловым эфиром (30 мл), в результате осаждается бесцветный порошок,который извлекают путем фильтрации и затем растворяют в этилацетате (10мл). К раствору добавляют 5 н. раствор хлористого водорода - этилацетата (2 мл) и полученную смесь разбавляют простым этиловым эфиром (50 мл), в результате чего осаждается бесцветный порошок, который извлекают путем 0 фильтрации. Получается 3(S)(S)- -этоксикарбонил-4-(4-пиперидил)бутил амин0-4-оксо-2,3,4,5-тетрагидро- 1 ,5-бензоксазепин-5-уксусную кислоту, дигидрохлорид (0,45 г).
Рассчитано, %: С 49,64 Н 7,06j 7,55.
C-i;H jjNjOi . 2НС1 2Н.20 Найдено, %: С 49,83; Н 7,07; 7,29.
o/jj)- 93 (в метаноле). Пример 67. Раствор 3(S)(S)- -этоксикарбонш1-4-(4 пиперидил)бутил -амино-4-оксо-2,3,4,5-тетрагидро- -155-бензоксазепин-5-уксусной кисло- g ты, дигидрохлорида (0,35 г) в 1 н. растворе гидрата окиси натрия (8 мл) .выстаивают в течение 30 мин при комнатной температуре, После добавления уксусной кислоты (1,5 мл)
5
N
N
0
N
N
смесь подвергают разделению в хрома- тографической колонке, наполненной гелем МС1 (СНР 20Р 150-300 мк, Mitsubishi Chemical) с использованием в качестве элюента смеси вода - метанол в отношении 2:1. Элюат концентрируют в вакууме и лиофилизируют. Получают 3(S) (8)-карбокси-4-(;4-пипери- дил)бутил амино-4-оксо-2,3,4,5-тет- рагидро-1,5-бензоксазе1шн-5-уксусную кислоту (0,2 г) в виде бесцветного порошка.
Рассчитано, %: С 56,49 Н 7,22j 9,41.
С2,Н,НзО. 3/2 HjO Найдено, %: С 56,86; Н 7,31; 9,41.
idJ-D- 133(в метаноле). Масс-спектр (т/е): 420 (MH Пример 68. Смесь бензил 3(S)-амино-4-оксо-2,3,4,5-тетрагидро- -1,5-бензоксазепин-5-ацетата, гидрохлорида (3,4 г), этанола (30 мл), ацетата натрия (0,77 г), уксусной кислоты (0,56 г), этил 6-(1-бензил- оксикарбонш1-4-пиперидил)-2-оксогек- саноата (4,4 г) и молекулярного сита ЗА (10 г) перемешивают в течение 10 мин при комнатной температуре. К перемешанной смеси добавляют по каплям раствор цианборгидрида натрия (0,6 г) в этаноле (50 мл) в течение 3ч. После выстаивания в течение ночи при комнатной температуре смесь концентрируют в вакууме и разбавляют смесью РОДЫ (100 мл) и этилацетата (200 мл). Полученную смесь тщательно перемешивают и фильтруют. Этилацетат- ный слой отделяют, высушивают над безводным сульфатом магния и концентрируют в вакууме. Остаточный продукт концентрирования растворяют в смеси этнлацетата (20 мл) и щавелевой кислоты (3 г). Этот раствор разбавляют петролейным эфиром (100 мл) и поверхностный слой удаляют путем декантации. К осажденному продукту добавляют воды (50 мл),этилацетат (200 мл) и избыточное количество бикарбоната натрия. Этилацетатный слой отделяют, высушивают над безводным сульфатом магния и выпаривают в вакууме.Маслянистый остаточный продукт выпаривания подвергают разделению в хроматографи- ческой колонке, наполненной силика- гелем, с использованием в качестве элюента смеси гексан - этилацетат-в отношении 2:1. После выпаривания
первой фракции получают бензил 3(5)- -С5-(1-бензш1оксикарбонш1-4-пипери- дил)-1-(R)-этоксикарбонилпентил ами- НО-4-ОКСО-2,3,4,5-тетрагидро-1,5-бенз- оксазеш1Н-5-ацетат (0,35 г) в виде бесцветного масла.
3320 (Ш); 1730,
иь- чистя ИК ,
1680 (СвО).
Масс-спектр (га/е), 685 (М). . Из второй фракции получают бензил 3(8)(1-бензилоксикарбонш1-4-пи- перидил)-1-(8)-этоксикарбонилпентил - амино-4-оксо-2,3,4,5-тетрагидро-1,5- -бензоксазепин-5-ацетат (0,65 г) Р виде бесцветного масла.
ЧКСтая мвкс
СМ- : 3330 (NH); 1730,
ик
1680 ().
Масс-спектр (т/е), 685 (М).
П р и м е р 69. Раствор бензил 3(5)(1-бензилоксикарбонил-4-пи- перидил)-1(R)этоксикарбонилпентил ами- НО-4-ОКСО-2,3,4,5-тетрагидро-1,5-бенз-
оксазепин-5-ацетата (0,35 г) в этаноле (20 мл) подвергают каталитическому гидрогенолизу над 10%-ным палладием на углероде (0,5 г, 50% влаги) при комнатной температуре и при
повьш1енном давлении до тех пор, пока не прекращается потребление водорода. После удаления катализатора путем фильтрации фильтрат концентрируют. К остаточному продукту концентрирования добавляют 5 н. раствор хлористого водорода - этилацетата (1 мл) и полученную смесь разбавляют простым этиловым эфиром (50 мл), в результате чего осаждается 3(S)-C1(R)-этоксикарбонил-5-(4-пиперидил)пен- тил3-амино-4-оксо-2,3,4,5-тетрагид- ро-1,5-бензоксазепин-5-уксусная кислота, дигидрохлорид (0,25 г) в виде бесцветного осадка. Эту кислоту растворяют в 1 н. растворе гидрата окиси- натрия (10 мл) и полученный раствор выстаивают в течение 30 мин при комнатной температуре. После добавления уксусной кислоты (2 мл) смесь подвергают разделению в хроматографической колонке, наполненной гелем МС1, с использованием смеси вода - метанол (2:1) в качестве элюента. Элюат кон-, центрируют в вакууме и лиофилизируют.
Получают 3(8)-С1-(К)-карбокси-5-(4- -пиперидил)пентил амино-4-оксо-2,3,- 4,5-тетрагидро-1,5-бензоксазепин-5- -уксусную кислоту (0,15 г) в виде бесцветного порошка.
25
Рассчитано, %: С 57,38; Н 7,44: N 9,13.
Ci,H,.N, О,
1459613
26
нил-4-пиперидил)-2-оксогептаноата (3,2 г) и молекулярного сита ЗА (Юг) перемешивают в течение 10 мин. К перемешанной .смеси добавляют по каплям раствор цианборгидрида натрия (0,51 г) в этаноле (50 мл) в течение 3 ч при комнатной температуре. После выстаивания в, течение ночи при комнатной
3/2 НгО
Найдено, %: С 57,39; Н 7,62; N 9,06.
D/JB- 149(в воде). Масс-спектр (m/ejl: 434 (МН).
n.3rUtл ч ч:ял.е. л, «vv -1,-ъ -л&гдч0 3,ft. i . i rH,J
3(5)-1;5-(1-бензилоксикарбонш1-4-пипе- ig температуре смесь концентрируют в ридил)-1(3)этоксикарбонилпентил7ами- вакууме и разбавляют смесью воды НО-4-ОКСО-2,3,4,5-тетрагидро-1,5-бенэ- оксазепин-5-ацетата (0,65 г) в этаноле (40 мл) подвергают каталитическому гидрогенолизу над 10%-ным дием на углероде (1 г, 50% влаги) при комнатной температуре и при по- вьшенном давлении -до тех пор, пока не прекращается потребление водорода. После удаления катализатора путем фильтрации фильтрат концентрируют. В остаточный продукт концентрирования вводят 5 Н. раствор хлористого водорода - этилацетата (2 мл)и полученную смесь разбавляют простым этиловьм эфиром (50 мл). Осаждается 3-(S)(8)-этоксикарбонил-5-(4-пи- перидил)пентил амино-4-оксо-2,3,4,5- -тетрагидро-1,5-бензоксазепин-5-ук- сусная кислота, дигидрохлорид (0,45 г) в виде бесцветного осадка. Эту кислоту растворяют в 1 н. растворе гидрата окиси натрия (15 мл) и полученный раствор выстаивают в течение 30 мин при комнатной температуре. После добавления уксусной кислоты (3 мл) смесь подвергают разделению в хроматографической колонке,наполненной силикагелем МС1, с использованием в качестве элюента смеси- вода - метанол в отношении 2:1. Элю- ат концентрируют в вакууме и лиофили- зируют. Получают 3(S)-Cl-(S)-Kap6oK- си-5-(4-пиперидил)пентил амино-4-ок(50 мл) и этилацетата (200 мл). Полученную смесь тщательно перемешивают и фильтруют. Этилацетатньй слой промь - палла- 15 вают последовательно 0,1 н. соляной кислотой, 0,1-н. раствором гидрата окиси натрия и водой, высушивают над безводным сульфатом магния и концентрируют в вакууме. Маслянистый остаточ2Q ный продукт концентрирования подвергают хроматографическому разделению в колонке, наполненной силикагелем, с использованием в качестве элюента смеси гексан-этилацетат в отношении
25 2:1. После выпаривания первой фракции получают трет-бутил 3(S)-C6-(1- -бензилоксикарбонил-4-пиперидил)-1(S)- -этоксикарбонш1гексил амино-4-оксо- -2,3,4,5-тетрагидро-1,5-бензоксаз-е30 пин-5-ацетат (0,35 г) в виде бесцветного масла.,
К J , см- : 3320 (Ш); 1730; 1680 ().
Из второй фракции получают трет35 бутил 3(3)-Гб-(1-бензилоксикарбонил- -4-пиперидил)-1(8)-этоксикарбонилгек- сил амино-4-оксо-2,3,4,5-тетрагидро- -1,5-бензоксазепин-5-ацетат (0,5 г) в виде бесцветного масла.
40
ИК , см- : 3320 (NH), 1730, 1680 ().
Масс-спектр (т/е) : 665 (М).
Пример 72. К раствору трет- бутил 3(5)-Сб-(1-бензш1оксикарбонилсо-2,3,4,5-тетрагидро-1,5 бензоксазе- 5 -4-пиперидил)-1(Ю-этоксикарбонилпин-5-уксусную кислоту (0,3 г) в виде бесцветного порошка.
Рассчитано, %: С 57,38 Н 7,44; N 9,13.
Найдено, %: С 57,01; Н 7,76; N 9,00.
toijj,- (в воде).
Масс-спектр (га/е): 434 (МН).
П р и м е.р 71. Смесь трет-бутил 3(5)-амино-4-оксо-2,3,4,5-тетрагидро- 1 ,5-бензоксазепин-5 ацетат (2,4 г), этанола (30 мл), уксусной кислоты (0,5 г), этил 7-(1-бензилоксикарбогексил амино-4-оксо-2,3,455-тетра- гидро-1,5-бензоксазепин-5-ацетата (0,35 г) в уксусной кислоте (1 мл) добавляют 30%-ный раствор бромистого
50 водорода - уксусной кислоты (2 мл). Полученную смесь выстаивают в течение 1 ч при комнатной температуре и затем разбавляют простым этиловым эфиром (100 мл). Поверхностный слой
55 удаляют путем декантации и образующийся осадок растворяют в 1 н. растворе гидрата окиси натрия (10 мл). Раствор выстаивают в течение 60 мин при комнатной температуре, После до1459613
26
нил-4-пиперидил)-2-оксогептаноата (3,2 г) и молекулярного сита ЗА (Юг) перемешивают в течение 10 мин. К перемешанной .смеси добавляют по каплям раствор цианборгидрида натрия (0,51 г) в этаноле (50 мл) в течение 3 ч при комнатной температуре. После выстаивания в, течение ночи при комнатной
.е. л, «vv -1,-ъ -л&гдч0 3,ft. i . i rH,J
температуре смесь концентрируют в вакууме и разбавляют смесью воды
ig температуре смесь концентрируют в вакууме и разбавляют смесью воды
40
ИК , см- : 3320 (NH), 1730, 1680 ().
Масс-спектр (т/е) : 665 (М).
Пример 72. К раствору трет- бутил 3(5)-Сб-(1-бензш1оксикарбонил 5 -4-пиперидил)-1(Ю-этоксикарбонилгексил амино-4-оксо-2,3,455-тетра- гидро-1,5-бензоксазепин-5-ацетата (0,35 г) в уксусной кислоте (1 мл) добавляют 30%-ный раствор бромистого
водорода - уксусной кислоты (2 мл). Полученную смесь выстаивают в течение 1 ч при комнатной температуре и затем разбавляют простым этиловым эфиром (100 мл). Поверхностный слой
удаляют путем декантации и образующийся осадок растворяют в 1 н. растворе гидрата окиси натрия (10 мл). Раствор выстаивают в течение 60 мин при комнатной температуре, После до27
бавления уксусной кислоты (1 мл) смесь подвергают разделению в хрома- тографической колонке, наполненной гелем МС1, с использованием в качестве элюента смеси вода - метанол в отношении 1:2. Элюат концентрируют в вакууме и лиофилизируют и в результате получают 3(S)-C1(R)-кapбoкcи-6- -(4-пипepилил)гeкcкл aминo-4-oкco- -2 , 3 , 4 , 5-тетрагидро-1,5-бензоксазе- пин-5-уксусную кислоту (0,13 г) в виде бесцветного порошка. - 139 {в воде). Масс-спектр (т/е): 448 (МН), ПримерТЗ. В раствор трет- -бутил 3(S)-С 6-1-бен зилоксикарбонил- -4-пиперидШ1)-1(З -этоксикарбонилгек CHJij амино-4-оксо-2,3,4,5-тетрагидро- -1,5-бензоксазепин-5-ацетата (0,5 г) в уксусной кислоте (1 мл) вводят 30%-ный раствор бромистого водорода - уксусной кислоты (2 мл). Полученную смесь выстаивают в течение 1 ч при
в виде бесцветного масла.
см - : 3320 (NH); 1740;
ик V -7f
1690; 1680 ().
комнатной температуре и затем разбав- 25 гептил амино-4-оксо-2,3,4,5-тетрагид- ляют простым этиловьм эфиром (100 мл). ро-1,5-бензоксазепин-5-ацетат (0,35 г) Поверхностный слой удаляют путем декантации и осадок растворяют в 1 н. растворе гидрата окиси натрия (20:мл). Раствор выстаивают при комнатной тем- зо I пературе в течение 30 мин. После введения уксусной кислоты (4 мл) смесь подвергают хроматографическому разделению в колонке, наполненной МС1, с использованием в качестве элюента- смеси вода - метанол в отношении 1:2. Элюат концентрируют в вакууме и лиофилизируют. Получают 3(S)(S)- -карбокси-6-(4-пиперидил)гексил амиНО-4-ОКСО-2,3,4,5-тетрагидро-1,5- -бензоксазепин-5-уксусную кислоту (0,23 г) в виде бесцветного порошка.
to/li)- 133 (в воде).
Масс-спектр (т/е) , 448 (МН) .
П р и м е р 74. Смесь трет-бутил 3(S)-амино-4-оксо-2,3,4,5-тетрагидро- -1,5-бензоксазепин-5-ацетата (2 г), этанола (10 мл), уксусной кислоты
Пример 75. В раствор трет-бутил 3(5) -(1-бензш10ксикарбонил- -4-пиперидш1)-1 (Ю-этоксикарбонилгеп- тил амино-4-оксо-2,3,4,5-тетрагидро35 -1,5-бензоксазепин-5- ацетата(0,35 г) в уксусной кислоте (1,5 мл) добавляют 30%-ный раствор бромистого водорода - уксусной кислоты (1,5 мл). Полученную смесь выстаивают в тече40 ние 0,5 ч при комнатной температуре, разбавляют в течение 0,5 ч при комнатной температуре простым этиловым эфиром (100 мл). Поверхностный слой удаляют путем декантирования и оса45 док растворяют в 1 н. растворе гидрата окиси натрия (10 мл). Раствор выстаивают в течение 30 мин при комнатной температуре. После ввода уксусной кислоты (2 мл) смесь подвергают
(0,49 г), этил 8-(1-бензилоксикарбо- 50 хроматографическому разделению в
нил-4-пиперидил)-2-оксооктаноата (3 г) и молекулярного сита ЗА (10 г) перемешивают в течение 10 мин. К перемешанной смеси добавляют по каплям
колонке. Наполненной Амберлитом XAD-2, с использованием в качестве элюента смеси вода - метанол в отношении 1:1. Элюат концентрируют в вакууме и лиораствор цианборгидрида натрия Х0,47г)55филизируют. Получают 3(S)(К)-карбв этаноле (40 мл) в течение 3 ч приокси-7-(4-пиперидил)-гептил амино-4комнатной температуре. После выстаи--оксо-2,3,4,5-тетрагидро-1,5-бензоквания в течение ночи при комнатнойсазепин-5-уксусную кислоту (0,1 г)
температуре смесь концентрируют в на-в виде бесцветного порошка.
28
кууме и разбавляют смесью воды (100 мл)к этилацетата (200 мл). Полученную смесь тщательно перемешивают и фильтруют. Этилацетатный слой промывают водой, высушивают над безводным сульфатом магния и концентрируют в вакууме. Маслянистый остаток подвергают хроматографическому разделе Q нию в колонке, наполненной силика- гелем, с использованием в -качестве элюента смеси гексана с этилацетатом в отношении 5:2 - 2:1. После вьтари- вания первой фракции получают трет 5 бутил 3(5)-С7-(1-бензилоксикарбонил- -4-пиперидш1)-1 (Ю-этоксикарбонилгеп- тил амино-4-оксо-2,3,4,5-тетрагидро- -1,5-бензоксазепин-5-ацетат (0,35 г) в виде бесцветного масла.
20 ИК , см- : 3320 (NH),- 1740-, 1700; 1680 (ОО).
Из второй фракции получают трет- -бутил 3(S)(1-бензилоксикарбонил- -4-пиперидил)-1-(S)-зтоксикарбонилв виде бесцветного масла.
см - : 3320 (NH); 1740;
ик V -7f
1690; 1680 ().
гептил амино-4-оксо-2,3,4,5-тетрагид- ро-1,5-бензоксазепин-5-ацетат (0,35 г
гептил амино-4-оксо-2,3,4,5-тетрагид- ро-1,5-бензоксазепин-5-ацетат (0,35 г)
Пример 75. В раствор трет-бутил 3(5) -(1-бензш10ксикарбонил- -4-пиперидш1)-1 (Ю-этоксикарбонилгеп- тил амино-4-оксо-2,3,4,5-тетрагидро-1,5-бензоксазепин-5- ацетата(0,35 г) в уксусной кислоте (1,5 мл) добавляют 30%-ный раствор бромистого водорода - уксусной кислоты (1,5 мл). Полученную смесь выстаивают в течение 0,5 ч при комнатной температуре, разбавляют в течение 0,5 ч при комнатной температуре простым этиловым эфиром (100 мл). Поверхностный слой удаляют путем декантирования и осадок растворяют в 1 н. растворе гидрата окиси натрия (10 мл). Раствор выстаивают в течение 30 мин при комнатной температуре. После ввода уксусной кислоты (2 мл) смесь подвергают
колонке. Наполненной Амберлитом XAD-2, с использованием в качестве элюента смеси вода - метанол в отношении 1:1. Элюат концентрируют в вакууме и лиоГ-Лц- воде).
Масс-спектр (ш/е): 462,(МН).
Пример 76. В раствор трет- бутил 3(8)-Г7-(1-бензилоксикарбонил- -4-пиперидил)-1(8)-этоксикарбонилгеп- тилjaMHHo-4-OKCo-2,3,4,5-тетрагидро- -1,5-бензоксазепин-5-ацетата (0,35 г) в уксусной кислоте (1,5 мл) вводят 30%-ный раствор бромистого водорода уксусной кислоты (1,5 мл). Полученную смесь выстаивают в течение 0,5 ч при комнатной температуре и затем разбавляют простым этиловым эфиром
в уксусной кислоте. Образовавшейся смеси дают постоять в течение 1,5 ч при комнатной температуре, а затем ее разбавляют 100 мл этилового эфира. Верхний слой удаляют декантацией, а осадок растворяют в 20 мл 1 н. раствора гидрата окиси натрия. Раствору дают постоять в течение 30 мин при комнатной температуре. После добавления 4 мл уксусной кислоты смесь подвергают хроматографической обработке на геле МС1 с использованием смеси воды с метанолом в соотноше(100 мл) .Поверхностный слой удаляют нии 1:1 в, качестве элюента. Элюат кон
тем декантации и осадок растворяют в 1н, растворе гидрата окиси натрия (10 мл) Раствор выстаивают в течение 30 мин при комнатной температуре. После добавления уксусной кислоты (2 мл) смесь подвергают хроматографическому разделению в колонке, наполненной гелем МС1, с использованием в качестве элюента смеси вода - метанол в отношении 1:1. Элюат концентрируют в вакууме и лиофшшзируют. Получают 3(5)-Cl(5)-карбокси-7-(4-пиперидил)- гептил}амино-4-оксо-2,3,4,5-тетра- гидро-1,5-бензоксазепин-5-уксусную кислоту (0., 15 г) в виде бесцветного порошка.
Ы1в- 108° в воде).
Масс-спектр (т/е); 462 (МН).
Пример 77. По методике примера 1 из соответствующих исходных продуктов получают маслоподобный остаток, который очищают хроматографической обработкой в колонке с силика- гелем (гексан:этилацетат в соотношении 2:1), в результате чего в виде бесцветного маслоподобного продукта получают 0,75 г трет-гбутил 3(5) -(1-бензш1оксикарбонил-4-пиперидил)- -1 (Ю-этоксикарбонилпентил амино-4- -оксо-25 354,5-тетрагидро-1,5-бензок- сазепин-5-ацетата. Из последующей фракции в виде бесцветного маслоподобного продукта получают 0,7 г трет- бутил 3(8)(1-бензилоксикарбонил- -4-пиперидил)-1-(S)-этоксикарбонил- пентил амино-4-оксо-2,3,4,5-тетрагид- ро-1,5-бензоксазепин-5-ацетата.
Пример 78. В раствор 1,5 г трет-бутил 3(8)(1-бензилоксикар- бонш1-4-пиперидил)-1(З)-этоксикарбо- нилпентил амино-4-оксо-2,3,4,5-тет- рагидро-1,5-бензоксазепин-5-ацетата в 5 мл уксусной кислоты добавляют 5 мл 30%-ного раствора бромистого водорода
20
25
30
35
40
45
50
55
центрируют в вакууме и лиофилизируют с получением в виде бесцветного порошка 0,71 г 3(S)(S)-кapбoкcи- - 5- ( 4-пиперидил) пен тил амино-4-оксо- -1,3,4,5-тетрагидро-1,5-бензоксазе- пин-5-уксусной кислоты.
Изучение антигипертонической активности новых производных 2,3,4,5- -тетрагидро-1,5-бензоксазепин-4-она.
Эксперимент 1. Исследование инги- бирования фермента превращения ан - гистензина I (АСЕ).
Методика эксперимента.
Эксперимент проводили при использовании гиппурил-Ь-гистидил-Ь- лейцина (HHL) в качестве основу, а ингиби- рующую активность АСЕ выражали в процентах ингибирования на количество гиппуровой кислоты, образуемой АСЕ, при вводе предлагаемого соединения. Раствор соединения,получаемого по предлагаемому способу, растворенного в буферном растворе 0,02-0,5% диме- тилсульфоксида - 100 ммоль бората - НС1 (рН 8,3, с содержанием 300 ммоль Елористого натрия), вводили в 100 мкл АСЕ (концентрация белка 20 мг/мл) и 100 мкл НН (1,25 ммоль). В данном эксперименте в качестве контроля использовали буферный раствор борат - НС1, содержащий и диметилсульфоксид, концентрацией равной концентрации испытываемого раствора. После нагревания раствора при 37 С в течение 1 ч в него вводили 150 мкл 1 н. соляной кислоты для завершения реакции. После ввода 0,8 мл этилацетата раствор подвергали центрифугированию со скоростью 11500 об/мин в течение 2 мин. Аликвоту в количестве 0,5 мл отделяли от этилацетатного слоя и высушивали при температуре ниже 40°С в струе газообразного азота. Остаточный продукт тщательно перемешивали с 4,5 мл
в уксусной кислоте. Образовавшейся смеси дают постоять в течение 1,5 ч при комнатной температуре, а затем ее разбавляют 100 мл этилового эфира. Верхний слой удаляют декантацией, а осадок растворяют в 20 мл 1 н. раствора гидрата окиси натрия. Раствору дают постоять в течение 30 мин при комнатной температуре. После добавления 4 мл уксусной кислоты смесь подвергают хроматографической обработке на геле МС1 с использованием смеси воды с метанолом в соотношении 1:1 в, качестве элюента. Элюат кон
0
5
0
5
0
5
0
5
центрируют в вакууме и лиофилизируют с получением в виде бесцветного порошка 0,71 г 3(S)(S)-кapбoкcи- - 5- ( 4-пиперидил) пен тил амино-4-оксо- -1,3,4,5-тетрагидро-1,5-бензоксазе- пин-5-уксусной кислоты.
Изучение антигипертонической активности новых производных 2,3,4,5- -тетрагидро-1,5-бензоксазепин-4-она.
Эксперимент 1. Исследование инги- бирования фермента превращения ан - гистензина I (АСЕ).
Методика эксперимента.
Эксперимент проводили при использовании гиппурил-Ь-гистидил-Ь- лейцина (HHL) в качестве основу, а ингиби- рующую активность АСЕ выражали в процентах ингибирования на количество гиппуровой кислоты, образуемой АСЕ, при вводе предлагаемого соединения. Раствор соединения,получаемого по предлагаемому способу, растворенного в буферном растворе 0,02-0,5% диме- тилсульфоксида - 100 ммоль бората - НС1 (рН 8,3, с содержанием 300 ммоль Елористого натрия), вводили в 100 мкл АСЕ (концентрация белка 20 мг/мл) и 100 мкл НН (1,25 ммоль). В данном эксперименте в качестве контроля использовали буферный раствор борат - НС1, содержащий и диметилсульфоксид, концентрацией равной концентрации испытываемого раствора. После нагревания раствора при 37 С в течение 1 ч в него вводили 150 мкл 1 н. соляной кислоты для завершения реакции. После ввода 0,8 мл этилацетата раствор подвергали центрифугированию со скоростью 11500 об/мин в течение 2 мин. Аликвоту в количестве 0,5 мл отделяли от этилацетатного слоя и высушивали при температуре ниже 40°С в струе газообразного азота. Остаточный продукт тщательно перемешивали с 4,5 мл
дистиллированной воды и смесь подвергали колориметрическому воздействию при длине волны 228 им.
Результаты испытаний приведены в табл.5.
Исследование влияния предлагаемых соединений против гипертонического действия ангиотензина I.
В качестве экспериментальных животных использовали крысы-самцы (Sprague Dawley) весом 250-350 г, имеющие свободный доступ к воде и пище. Этих крыс анестезировали путем внутрибркипинного ввода пентабарбита- ла натрия (50 мг/кг) за день до проведения испытания и в бедренную арте- рмо вводили полиэтиленовую трубку для измерения кровяного давления, а в
25
30
35
ствия. Затем путем внутривенной инъек ции вводили 300 мк/кг предлагаемого соединения в виде солевого раствора, через 5,10,30,60,90 и 120 мин после этого вводили ангиотензии I и II повторно для определения гипертонических реакций. При расчете процента ингибирования гипертонической активности ангиотензина I величину процента ингибирования корректировали с учетом изменения со временем гипертонической реакции за счет ангиотензина II.
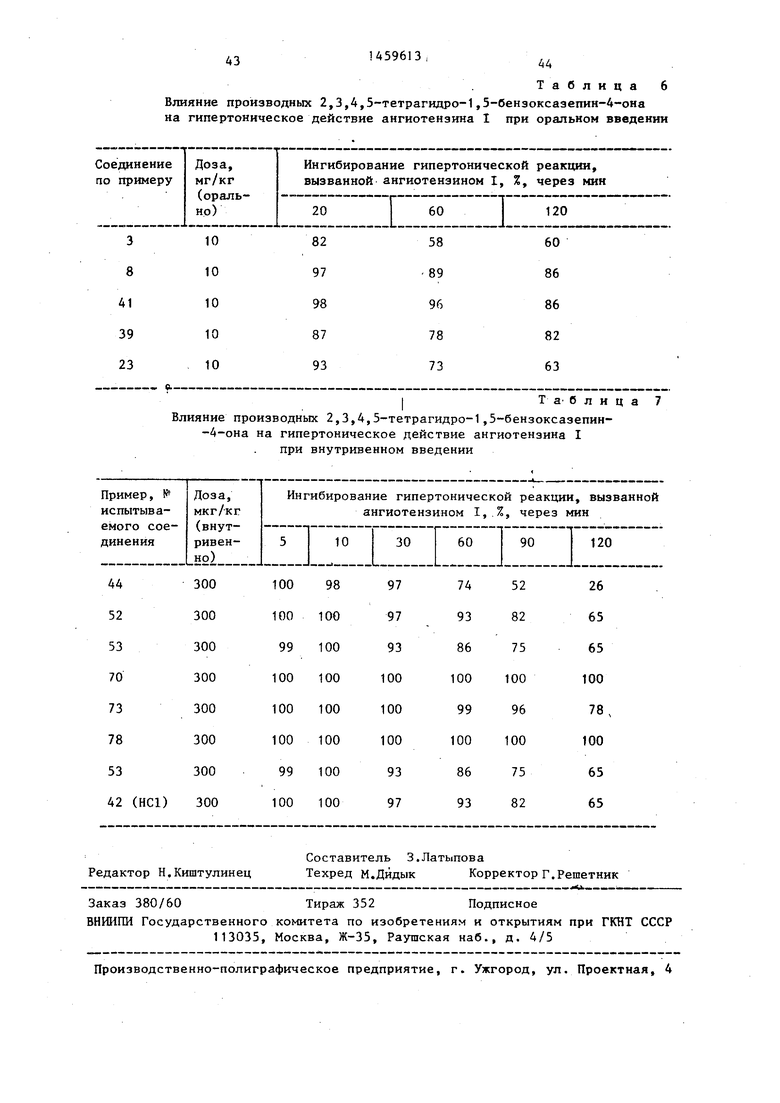
Результаты испытаний приведены в табл.7.
бедренную вену вводили такую же труб- 20 f измерения гипертонического дей- ку для инъекции ангиотензина I и II. Трубки закрепляли неподвижно.
В день испытания измеряли среднее кровяное давление в контрольной фазе посредством электрического гемодина- моментра (модели MPU 0,5-290-0-Ш, изготавливаемой NEC - Sanei, Япония) и регистрировали посредством полиграфа (NEC - Sanei, типа 365, или Nippon Kohden типа RM-45), затем через бедренную вену вводили гиотензин I, а затем ангиотензин II в дозе 300 и 100 мкг/кг соответственно для измерения гипертонического действия. Затем вводили через рот 10 мг/кг предлагаемого соединения, в виде водного раствора или водной суспензии аравийской камеди, через 20, 60 и 120 мин после такого ввода повторно вводили антиотензин I и ангиотензин II для того, чтобы проследить гипертонические реакции. При расчете процента ингибирования гипертонического действия ангиотензина I величину процента ингибирования корректировали с учетом изменения со временем гипертонической реакции, вызванной ангиотензином II.
Результаты испытаний приведены в табл.6.
Исследование влияния предлагаемых соединений против гипертонического действия ангиотензина I.
В качестве экспериментальных животных использовали крысы-самцы (Sprague Dawley) весом 300-400 г,которые имели свободный доступ к воде и пище. Крыс анестезировали путем внутрибрюшинного ввода пентабарбитаПредлагаемые соединения подвергали испытанию на токсичность на мйшах при оральном введении в дозе 40 300 мг/кг. Мьвпей обследовали через неделю (группа из 5 животных).
Все мыши остались живы, признаки токсичности не наблюдались. Следовательно предлагаемые соединения не 45 обладают токсичностью в испытуемых дозах.
Таким образом, предлагаемый способ позволяет получать новые производные 2,3,4,5-тетрагидро-1,5-бенз- 50 оксазепин-4-она, которые являются
перспективными для создания низкоток , сичных противогипертонических препаратов.
55 Формула изобретения
Способ получения производных 2,3,4,5-тетрагидро-1,5-бензоксазе- пин-4-она формулы
5
ла натрия (50 мг/кг; за день до проведения испытания: в бедренную артерию вставили полиэтиленовую трубку для измерения кровяного давления, а в венную артерию вставили такую же трубку для ввода ангиотензина I и II. Трубки закрепляются неподвижно.
В день испытания измеряли среднее кровяное давление в контрольной фазе посредством электрического гемодинамо- метра (модели MPU 0,5-290-0-Ш, изготавливаемой NEC - Sanei,Япония) и регистрировали с помощью полиграфа (NEC - Sanei типа 365 или Nippon Kohden типа RM-45). Затем вводили ангиотензин I, а после этого ангио- тензин II через бедренную вену в дозе соответственно 300 и 100 мк/кг
твия. Затем путем внутривенной инъекции вводили 300 мк/кг предлагаемого соединения в виде солевого раствора, через 5,10,30,60,90 и 120 мин после этого вводили ангиотензии I и II повторно для определения гипертонических реакций. При расчете процента ингибирования гипертонической активности ангиотензина I величину процента ингибирования корректировали с учетом изменения со временем гипертонической реакции за счет ангиотензина II.
Результаты испытаний приведены в табл.7.
измерения гипертонического дей-
Предлагаемые соединения подвергали испытанию на токсичность на мйшах при оральном введении в дозе 40 300 мг/кг. Мьвпей обследовали через неделю (группа из 5 животных).
Все мыши остались живы, признаки токсичности не наблюдались. Следовательно предлагаемые соединения не 45 обладают токсичностью в испытуемых дозах.
Таким образом, предлагаемый способ позволяет получать новые производные 2,3,4,5-тетрагидро-1,5-бенз- 50 оксазепин-4-она, которые являются
перспективными для создания низкоток , сичных противогипертонических препаратов.
55 Формула изобретения
Способ получения производных 2,3,4,5-тетрагидро-1,5-бензоксазе- пин-4-она формулы
33
л
,МНСНСООВ2
14596
Го(« е
CHjCORi
де RI ОКСИ-, 1-трет-бутоксикарбо- нил -2-фенилэтиламино-, : 1-кар6окси-2-фенилэтиламино-,. бензилокси- или трет-буток- сигруппа
R. - водород, этил, н-бутил.
этоксикарбонилметил или бензил;
R, 15
20
водород, линейный или разветвленный С,-С2-алкил,этил, который замещен С -Су-цикло- алкилом, фенилом, толилом, 4-тетрагидропиранилом или 4-тианилом, С -С -алкил, который замещен 4-пипериди- лом или 1-бензилоксикарбо- нил-4-пиперидилом, или C -Cj-алкил, который замещен 35 амино-, трет-бутоксикарбо- ниламино- или фталимидогруп- пой,
и их гидрохлоридов, отличаюийся тем, что осуществляют вза- одействие соединения формулы
(II)
где R - бензилокси- или трет-бутокси группа, или его гидрохлорида с соединением формулы
О О (III) , II II
Rj
где R J - водород, линейный или разветвленный С -С -алкил, этил который замещен ,-цикло- алкилом, фенилом, толилом, 4-тетрагидропиранилом или 4-тианш1ом, С -С -алкил, который замещен 1-бензил- оксикарбонил-4-пиперидилом, или С С -алкил который замещен фталимидогруппой, в среде низшего спирта в присутствии цианборгидрида щелевого металла при комнатной температуре, и ,в случае необходимости, в полученном продукте, в котором R , - бензилоксигруппа, удаляют бензильную группу каталити1459613
34
е
5
0
5
5
0
5 o g
ческим гидрогенолизом над палладием на углероде в среде спирта с получением целевого продукта, в котором оксигруппа, и/или в целевом продукте, в котором R - Cj-Cg-алкил, который замещен 1-бензилоксикарбо- нш1-4-пиперидилом, удаляют бензил- оксикарбонильную группу каталитичес КИМ гидрогенолизом над палладием на углероде в среде спирта или путем обработки раствором бромистоводород- ной кислоты с получением целевого продукта, в котором R.,- С С -алкил, который замещен 4-пиперидилом, и/или
целевой продукт,в котором Rr,- оксигруппа, подвергают взаимодействию с трет-бутиловым сложным эфиром фе- нилаланина в присутствии диэтилфос- форцианидата в среде диметилформами- да, охлажденного до , с получением целевого продукта, в котором 1 -тpeт-бyтoкcикapбoнилr2-фeнил- этилaминoгpyппa, случае необходимости,
целевой продукт, в котором R,-тpeт-бyтoкcикapбoнил-2-фeнилэтил- аминогруппа, подвергают кислотному гидролизу путем обработки раствором хлористоводородной кислоты с получением целевого продукта, JB котором 1-карбокси-2-фенилэтиламиногруп- па, или
целевой продукт, в которой ок- си- или трет-бутоксигруппа, Rj-этил, подвергают щелочному гидролизу раствором гидроокиси щелочного металла с получением целевого продукта, в котором окси или трет, -бутокси- группа, а водород, и в случае необходимости,
целевой продукт, в котором Rj - водород, подвергают взаимодействию с бензилгалогенидом, этоксикарбонилме- тилгалогенидом или н-бутилгалогени- дом в среде диметилформамида в присутствии йодида калия с получением целевого продукта, в котором R -бензил, зтоксикарбонилметил или н-бутил, или
целевой продукт, в котором R- трет- -бутоксигруппа, а этил, подвергают кислотному гидролизу раствором бромистоводородной кислоты или хло- ристоводородной кислоты с получением целевого продукта, в котором R , - оксигруппа, а R - этил, и/или
целевой продукт, в котором Rj - С4.-С g-алкил, который замещен фтал35
иьшдогруппой, подвергают взаимодей- ствию с гидразингидратом и ди-трет- Нбутилкарбонатом в среде низшего спирта при комнатной температуре с получением целевого продукта, в котором % С -С -алкил, который замещен трет-бутоксикарбониламиногруппой, и, в случае необходимости,
целевой продукт, в котором R,- -трет-бутоксигруппа, а R,- C4-Cg-an- кил, который замещен трет-бутоксикар- бониламиногруппой, подвергают кислотному гидролизу раствором хлористово36, Приорите т по признакам
5 водород, этил н-бутил или бензил) Rg - водород, линейный или разветвленный ,-алкил или этил, который замещен С -С -циклоалкилом, фенилом или толилом.
го продукта, в котором R , - окси- группа, а R - С -С -алкил, который замещен аминогруппой,
и вьщеляют целевой продукт в свободном виде или в виде его гидрохлорида.
20
или 1-бензилоксикарбонш1-4-пипериди- лом, или С С -алкил, который замещен амино-, трет-бутоксикарбонилами- но- или фталимкдогруппой; или R.iHR имеют указанные в формуле изобретения значения и этоксикарбонилм(втил.
Таблица 1
Конфигурация и характеристики производных 2,3,4,5-тетрагидро- -1,5-бензоксазепин-4-она
2 NH-CH-COOCoH
СНзСН2
« хCHjCHCHjCH2
CH2CH2
Г УсНгСН2 СНСН 2СН2
:СНСН2СН2V/
,
14 CH -O CH CH
сНз О-сн сн 59613
36, Приорите т по признакам
5 водород, этил н-бутил или бензил) Rg - водород, линейный или разветвленный ,-алкил или этил, который замещен С -С -циклоалкилом, фенилом или толилом.
R510
. S510
R536
S536
R.530
S530
3330, 1730, 1680
3330, 1740, 1670
3320, 1730, 1670 3330, 1740,
1670
3330, 1740, 1680
3330, 1740, 1680
37
20ся,CHjCH,
2, CHjCHi
CHjCHj
22;; cHCHjCHiСНзСН,
- я
1,1 .- ..
24(CHjCHjs
S, R CrfHfcHtOi.50,335,807,34
.HC1-1/2H,0(50,11)(5,72)(7,32)
КCi,H,tN.Ot-56,707,356,01
-HCl -1/2 (56,64)(7,34)(5,97)
S Ct,Hj,,707,356,01
№1 . t/2 (56,80(7,28)(6,00)
RCt4Hj,HJ),597,385,69
HCl -1/2 (58,43)(7,40)(5,60)
C,4H.JJ.O(-38,59 7,38 5,69
HC1-1/2H O (58,29) (7,4O (3,58)
1459613
38 Продолжение табл.1
CrfHfcHtOi.50,335,807,34
.HC1-1/2H,0(50,11)(5,72)(7,32)
Ci,H,tN.Ot-56,707,356,01
-HCl -1/2 (56,64)(7,34)(5,97)
Ct,Hj,,707,356,01
№1 . t/2 (56,80(7,28)(6,00)
Ct4Hj,HJ),597,385,69
HCl -1/2 (58,43)(7,40)(5,60)
C,4H.JJ.O(-38,59 7,38 5,69
HC1-1/2H O (58,29) (7,4O (3,58)
28S CBjCH 29s()-CHiCH730HN (}-CH,CH2- ,|
31CHjCCH,),32H
SR
SS
CMH,,H,OJS 53,276,505,65
HCl .1/2 H,0 (53,32)(6,47)(5,59)
C,,H5,HiO,S. 53,27 6,505,65
HCl -1/2 BjO (53,15)(6,20)(5,77)
.NjOjj «2HC1. HjO
50,39 6,73 8,01 (50,36) (6,68) (7,56)
R.S«
84 93)
Ci s+NtOj. 57,55 7,56 5.1 «HCl -172 (57,60) (7,50) (5,
0„Н HjOj 55,90 5,63 8,69 . (55,47) (5,62) (8,28)
450 450
433
434 322
Снесь диастереоиэомеров Для измерения использовали сво6однр« основание.
Таблица
Конфигурация и характеристики производных 2,3,4,5- тетрагидро-1,5-бензоксазепин-4-она
Q
(fY Vl H-CH-COOR
}СН2СН,-/Н)
(CHjjjCOOC. - 37
jCcHj CHj
-(СН)зСНз
Продолжение табл.2
6,505,65
(6,47)(5,59)
6,505,65
(6,20)(5,77)
6,73 8,01 (6,68) (7,56)
84 93)
7,56 5.1 (7,50) (5,
5,63 8,69 (5,62) (8,28)
450 450
433
434 322
(,7)
-200 (c-0,5)
Таблица 4
Конфигурация и характеристики производных 2,3,4,5- -тетрагидро-1,5-беиэоксаэепин-4-она
1 2 О Л- ЫНСНСОО
Jo сн2сн -(д)
НООС
43
1459613
44
Таблица 6
Влияние производных 2,3,4,5-тетрагидро-1,5-бензоксаэепин-4-она на гипертоническое действие ангиотензина 1 при оральном введении
1459613

| Трансформаторное долговременное запоминающее устройство | 1973 |
|
SU481937A2 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Кинематографический аппарат | 1923 |
|
SU1970A1 |
| Энергоприемник для повозок высокочастотного транспорта | 1944 |
|
SU72352A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Гребенчатая передача | 1916 |
|
SU1983A1 |
Авторы
Даты
1989-02-15—Публикация
1986-08-12—Подача