За последнее время в -химической науке и практике приобретают все большее значение методы анализа различных органических и неорганических веществ в неводных средах, позволяющие осуществлять химический контроль в производстве не только индивидуальных веществ, но и их смесей. До самого последнего времени в литературе описаны методы дифференцирова-нного титрования смесей солей и кислот, позволяющие анализировать указанные смеси из одиой навески анализируемого технического продукта.
Предлагаемый способ определения солей и кислот в Смеои потенциометрическим методом отличается тем, что анализируемую смесь. подкисляют избытком серной кислоты и титруют в среде бензола или метилэтилкетона раствором гидроокиси тетраэтиламмония (ГТЭА).
Уравнение реакции может быть представлено следующим образом:
Kt2An-|-HAni + H2SO4- Kt2S04 + 2HAn-bHAni + H2SO4 (избыток),
где: Kt2An-соль, содержащаяся в исходной анализируемой смеси;
HAni -кислота, содержащаяся в исходной анализируемой смеси;
НАп -кислота, выделившаяся в результате взаимодействия исходной соли с серной кислотой.
Предложенный способ является новым и представляет интерес для дифференцированного определения смесей органических кислот и их солей, так как в химических производствах кислоты и их соли часто сопутствуют друг другу.
Способ анализа отличается быстротой выполнения, достаточной чувствительностью и точностью (относительные ошибки определения не превышают 4%).
№ 147363 2Методика определения. 0,03-0,07 г анализируемой смеси помещают в стаканчик для титрования емкостью 100 мл, добавляют 1-2 мл метилового спирта и полученный раствор обрабатывают избыточным количеством серной кислоты. Полученную смесь разбавляют бензолом или метилэтилкето«ом до объема.25 мл и титруют 0,1 в. бензольно-метанольным (3:1) раствором гидроокиси тетраэтиламмония (ГТЭА). Титрование проводят нотенциометрическим методом со стеклянным и каломельным электродами на установке, состоящей из полумикробюретки емкостью 10 мл, градуированной через 0,02 мл, стаканчика для титрования, в который опущены электроды, потенциометра ЛП-5, магнитной мешалки и системы для осушки азота.
В процессе титрования в стаканчик с анализируемы. раствором пропускают ток сухого азота для предохранения титруемой смеси от влияния углекислоты воздуха. Титран добавляют по 0,1 мл т каждый раз измеряют величину потенциала. Титрование продолжают до тех пор, пока потенциал не достигнет максимума и будет оставаться относительно ПОСТОЯННЫМ ирл дальнейшем прибавлении титранта. По полученным данным, строят график, откладывая по оси абсцисс прибавленный объем раствора ГТЭА в миллилитрах, а по оси ординат- величину потенциала в милливольтах, получают кривую титрования смеои и находят по ней объем раствора ГТЭА, соответствующий эквивалентному моменту. Расчет производят по следующим формулам.
Содержание соли:
Э. { ,V, -М.Э
А //) 5 5.1(Г
а
ЗБ 1000
уммарное количество .кислоты:
Э, -N
.
1000
Количество кислоты, выделившейся из соли при взаимодействии ее с серной кислотой:
а, а.А.(З;
Содержание кислоты в анилизируемой смеси:
а.; -- Й1 - Яз - rt, - G -..- ,Г4)
где: о. - содержание соли в анализируемой смеси, в г; Й1 -суммарное количество кислоты (HAni-f-ПАп) (кислоты, находящейся в анализируемой смеси, и кислоты, выделившейся из соли в результате ее взаимодействия с серной кислотой, в г);
аа -количество кислоты ПАп, выделившееся «з соли при взаимодействии ее с серной кислотой, в г;
а - содержание кислоты НАп в анализируемой смеси, в з; и - количество серной кислоты, взятое для анализа, в г;
А -эквивалент определяемой соли;
д, -эквивалент определяемой кислоты (в частном случае сходный по аниону с солью);
Зв, -эквивалент сер-ной кислоты;
Yj .- объем раствора ГТЭА, пощедший на титрование общего количества кислоты (HAni 4-НАп + П2504), в мл;
1, хл /чV .
(УВ-УВ)(2)
VB - объем раствора ГТЭА, пошедший на титрование избытка серной кислоты, в мл;
NB -нормальность раствора ГТЭА.
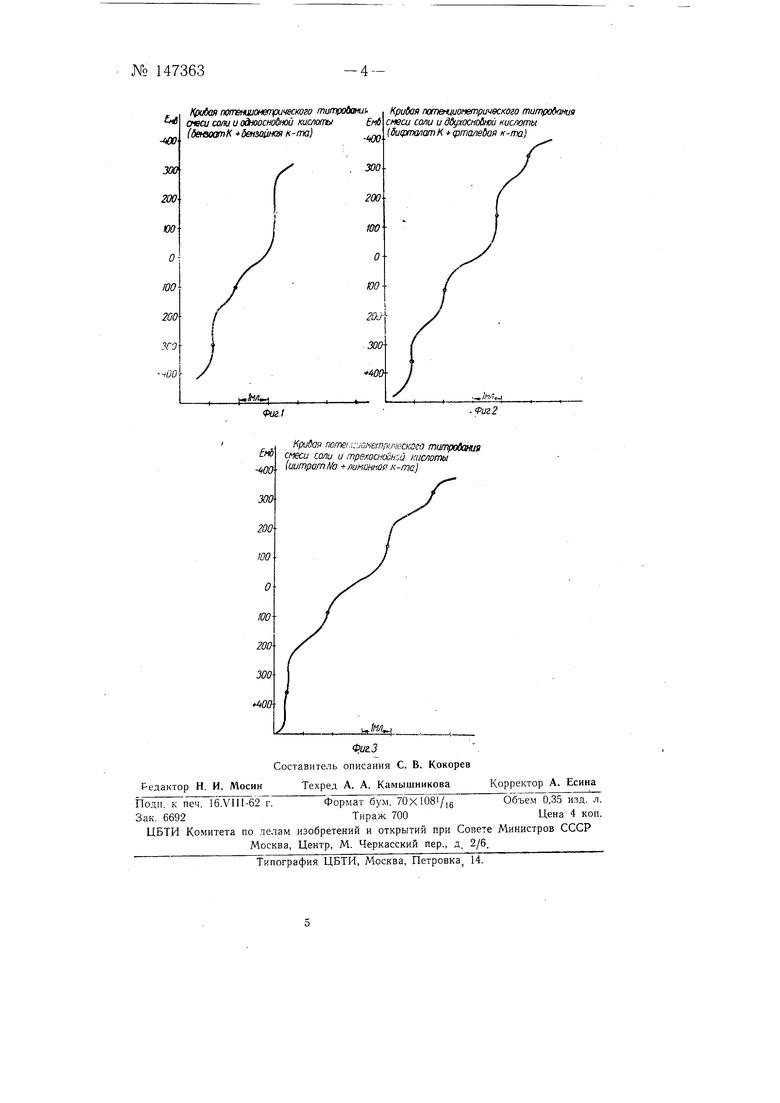
Характер кривых титрования нредставлен «а фиг. 1, 2 и 3.
На фиг. 1 представлена характерная кривая титрования для смесей солей и одноосновных кислот, первый и второй скачки титрования соответствуют первой и второй ступеням нейтрализации избытка серной кислоты, не вошедшей в реакцию, третий скачок соответствует, титроваяию суммарного количества кислоты (HAni + HAn), т. е. к слоты, содержащейся в анализируемой смеси, и мислоты, эквивалентной содержанию определяемой соли, из которой она образуется При взаимодействии соли с серной кислотой.
На фиг. 2 представлена характерная кривая титрования для смесей солей я двухосновных кислот, первый и третий скачки титрования соответствуют первой и второй ступеням нейтрализации избытка серной кислоты, не вошедшей в реакцию, а второй и четвертый скачки титрования соответствуют титрованию сум марного количества кислоты (НАп1 + НАп), т. е. кислоты, содержащейся s анализируемой смеси, и кислоты, эквивалентной содержанию определяемой соли, из которой она образуется при взаимодействии соли с серной
КИСЛОТОЙ.
На фиг. 3 представлена характерная кривая титрования для смесей солей и трехосновных кислот (цитрат натрия +лимонная кислота); первый скачок титрования соответствует первой стуиени нейтрализации избытка серной кислоты, не вошедшей в реакцию, второй и четвертый скачки титрования соответствуют первой и третьей ступеням нейтрализации суммарного количества лимонной кислоты, третий ачок титрования соответствует второй ступени нейтрализации избытка серной кислоты, не вошедшей в реакцию, и второй ступени нейтрализации суммарного количества лимонной кислоты, т. е. кислоты, содержащейся в анализируемой смеси, и кислоты, эквивалентной содержанию определяемой соли, из которой она образуется при взаимодействии соли с серной кислотой.
Указанным методом было оттитровало свыше 50 смесей, объектаjMH исследований были смеси солей и одно-, двух- и трехосновных кислот.
По заключению о промышленной полезности изобретения способ представляет интерес для химии удобрений, а также для химических заводов, выпускающих технические продукты.
Предмет изобретения
Способ определения |солей и кислот, находящихся в смеси, потенциометрическ1им методом, отличающийся тем, что анализируемую смесь подкисляют избытком серной кислоты и титруют в среде бензола или метилэтилкетона раствором гидроокиси тетраэтиламмония.
-3-NO 147363


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ количественного определения веществ, проявляющих кислотные свойства | 1975 |
|
SU586384A1 |
| Способ количественного определения азота в кремнийорганических соединениях | 1959 |
|
SU133260A1 |
| Способ количественного определения трехкомпонентной смеси муравьиной, уксусной и пропионовой кислот | 1973 |
|
SU483622A1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ МУРАВЬИНОЙ И УКСУСНОЙ КИСЛОТ в их СМЕСИ | 1973 |
|
SU390437A1 |
| Способ анализа ацетоксигрупп | 1960 |
|
SU137299A1 |
| Способ определения ароматических моно- и дисульфокислот | 1973 |
|
SU445906A1 |
| Способ количественного определения производных оксипуринов и их смесей | 1974 |
|
SU499529A1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФТОРА ВО ФТОРСИЛАНАХ | 1969 |
|
SU249748A1 |
| Способ определения @ -ацетилглутамина | 1985 |
|
SU1272231A1 |
| Способ получения силикатов металлов | 1961 |
|
SU143784A1 |


Авторы
Даты
1962-01-01—Публикация
1961-06-09—Подача