Предлагается усовершенствованный способ получения диалкиловых эфиров протопорфирина-IX общей формулы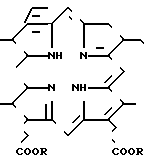 где R=CH3, C2H5; изо-С3Н7, которые могут найти применение в качестве исходных веществ при получении лекарственных препаратов, а также для синтеза катализаторов.
где R=CH3, C2H5; изо-С3Н7, которые могут найти применение в качестве исходных веществ при получении лекарственных препаратов, а также для синтеза катализаторов.
Целью изобретения является увеличение выхода целевых продуктов, упрощение процесса за счет нагревания тетраалкиловых эфиров гематопорфирина-IX в диметилформамиде с 2-3 эквивалентами бензоилхлорида в течение 15-20 мин при 120-125оС.
П р и м е р 1. Диметиловый эфир протопорфирина-IX(Ia).
Выдерживают раствор 0,5 г (0,76 ммоль) тетраметилового эфира гематопорфирина-IX, 10 мл диметилформамида, 0,35 мл (3,0 ммоль) бензоилхлорида 15 мин при 120оС, затем смесь охлаждают, приливают 7 мл воды, выпавший осадок отфильтровывают, сушат, хроматографируют на колонке с окисью алюминия (III степени, активности, элюент хлороформ), растворитель отгоняют в вакууме, остаток кристаллизуют из смеси хлористый метилен петролейный эфир и получают 0,403 г (89%) порфирина Ia.
Найдено, C 73,0; P 6,4; N 9,4.
C36H38N4O4.
Вычислено, С 73,2; Н 6,5; N 9,5.
УФ-спектр в хлороформе, λмакс ( ε . 10-3): 408,5 (163,0): 507,5 (13,8); 543,5 (11,5); 578 (6,8); 633 (5,5).
Спектр ПМР в CDCl3,δ 9,971; 9,967; 9,86; 9,84 (все с, 4Н, мезо-Н); 8,2 (д. д. 1Н, 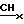 = CH2); 8,11 (д.д. 1Н,
= CH2); 8,11 (д.д. 1Н,  CH2); 6,29 Нa(д.д. 2Н, Iax 17,8; СН= СН2); 6,13 Нв (д.д. 2Н, Iвх 11,5, CH
CH2); 6,29 Нa(д.д. 2Н, Iax 17,8; СН= СН2); 6,13 Нв (д.д. 2Н, Iвх 11,5, CH 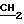 ); 4,31 (т. 4Н, СН2СН2СО); 3,22 (т. 4Н, СН2СН2СО); 3,64 (с. 6Н, ОСН3); 3,58; 3,57; 3,53; 3,52 (все с. 12Н,
); 4,31 (т. 4Н, СН2СН2СО); 3,22 (т. 4Н, СН2СН2СО); 3,64 (с. 6Н, ОСН3); 3,58; 3,57; 3,53; 3,52 (все с. 12Н, 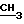 -кольца); 4,06 (с. 2Н, NH).
-кольца); 4,06 (с. 2Н, NH).
П р и м е р 2. Диэтиловый эфир протопорфирина-IX (Iб).
Выдерживают раствор 1 г (1,41 ммоль) тетраэтилового эфира гематопорфирина IX, 25 мл диметилформамида и 0,65 мл (5,6 ммоль) бензоилхлорида 15 мин при 120оС, затем смесь охлаждают, приливают 15 мл 35%-ного раствора ацетата натрия, выпавший осадок отфильтровывают, сушат и хроматографируют на колонке с окисью алюминия III степени активности (элюент хлороформ). Вещество кристаллизуют из хлороформа спирта и получают 665 мг (76,2%) порфирина (Iб).
Найдено, С 73,6: Н 6,88; N 9,13.
С38Н42N4O4.
Вычислено, С 73,76; Н 6,84; N 9,05.
УФ-спектр в хлороформе, λмакс ( ε · 10-3): 408,5 (162,4); 507,5 (14,0); 543,5 (11,7); 578 (6,9); 633 (5,6).
Спектр ПМР в CDCl3, δ 9,97; 9,95; 9,88; 9,83 (все с. 4Н, мезо-Н); 8,17 (д. д. 1Н, 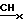 = CH2 8,13; (д.д. 1Н, СНх=СН2); 6,30 и 6,26 На (два д.д.2Н Iax 17,9; Iав 1,7; СН=СН2); 6,168 и 6,15 Нв (два д.д. 2Н, Ibx 11,5; Iва 1,7; СН= СН2); 4,33 (т. 4Н,
= CH2 8,13; (д.д. 1Н, СНх=СН2); 6,30 и 6,26 На (два д.д.2Н Iax 17,9; Iав 1,7; СН=СН2); 6,168 и 6,15 Нв (два д.д. 2Н, Ibx 11,5; Iва 1,7; СН= СН2); 4,33 (т. 4Н, 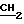 CH2CO); 3,22 (т. 4Н, CH
CH2CO); 3,22 (т. 4Н, CH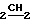 CO), 4,14 (к. 4Н,
CO), 4,14 (к. 4Н, 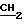 = CH3); 1,15 (т. 6Н, CH
= CH3); 1,15 (т. 6Н, CH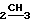 ); 3,57; 3,56; 3,54; 3,53 (все с. 12Н, СН3-кольца); 4,22 (с. 2Н, NH).
); 3,57; 3,56; 3,54; 3,53 (все с. 12Н, СН3-кольца); 4,22 (с. 2Н, NH).
П р и м е р 3. Диизопропиловый эфир протопорфирина-IX (Iв).
К раствору 0,8 г (1,04 ммоль) тетраизопропилового эфира гематопорфирина-IX в 15 мл диметилформамида добавляют 0,75 мл (6,45 ммоль) бензоилхлорида. Смесь выдерживают 15 мин при 120-125оС, охлаждают, добавляют 9 мл воды, выпавший осадок отфильтровывают, промывают водой. Сухой осадок растворяют в 50 мл хлористого метилена и пропускают через слой (2 см) окиси алюминия (III степени активности), растворитель отгоняют. Остаток кристаллизуют из смеси хлористый метилен гептан и получают 0,595 г (88%) порфирина Ib.
Найдено, С 74,2; Н 7,2; N 8,7.
С40Н46N4O4.
Вычислено, С 74,3; Н 7,2; N 8,7.
УФ-спектр в хлороформе, λмакс ( ε · -10-3): 409 (194); 507 (12,9); 543 (10,5); 579 (5,8); 633 (4,4). Спектр ПМР в CDCl3 δ: 10,04; 9,96; 9,92 (все с. 2Н, 1Н, 1Н, мезо-Н); 8,21 (д.д. 1Н, СНх=СН2); 8,19 (д.д. 1Н,  CH2), 5,6; 6,32 На (д. д. 2Н, Iах 17,8, Iaв 1,5, CH
CH2), 5,6; 6,32 На (д. д. 2Н, Iах 17,8, Iaв 1,5, CH 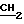 );6,31 На (д.д. 2Н, Iах 17,8; Iав 1,5, CH=CH2 6,15 Нв (д.д. 2Н, Iвх 11,5; Iав 1,5; CH
);6,31 На (д.д. 2Н, Iах 17,8; Iав 1,5, CH=CH2 6,15 Нв (д.д. 2Н, Iвх 11,5; Iав 1,5; CH 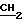 ; 6,14 Нв (д. д. 2Н, Iвх 11,5; Iав 1,5, СН=СН2); 5,06 (м. 2Н, ОСНМе2); 4,35 (т. 4Н, СН2СН2СО); 3,21 (т. 4Н, СН2СН2СО); 3,62; 3,61; 3,57; 3,57 (все с. 12Н, СН3 кольца); 1,11 (д. 12Н, ОСНМе2, I 6,3); 3,93 (с. 2Н, NH).
; 6,14 Нв (д. д. 2Н, Iвх 11,5; Iав 1,5, СН=СН2); 5,06 (м. 2Н, ОСНМе2); 4,35 (т. 4Н, СН2СН2СО); 3,21 (т. 4Н, СН2СН2СО); 3,62; 3,61; 3,57; 3,57 (все с. 12Н, СН3 кольца); 1,11 (д. 12Н, ОСНМе2, I 6,3); 3,93 (с. 2Н, NH).
Таким образом, данный способ позволяет упростить процесс получения диалкиловых эфиров протопорфирина-IX за счет значительного снижения объемов растворителей и исключения в некоторых случаях хроматографической очистки, повысить выход целевых продуктов до 89% а также обеспечивает возможность получения различных эфиров протопорфирина-IX.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТИОННЫЕ ДИМЕРНЫЕ АМФИФИЛЫ В КАЧЕСТВЕ АГЕНТОВ ТРАНСФЕКЦИИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2002 |
|
RU2233834C2 |
| Способ получения монометилового эфира протопорфирина 1х | 1985 |
|
SU1294807A1 |
| НОВЫЕ СУБСТРАТЫ КОНЦЕВОЙ ДЕЗОКСИНУКЛЕОТИДИЛТРАНСФЕРАЗЫ | 2003 |
|
RU2278869C2 |
| ПОВЕРХНОСТНО-АКТИВНЫЕ ВЕЩЕСТВА СО ВСТРОЕННЫМИ В УГЛЕВОДОРОДНУЮ ЦЕПЬ ОСТАТКАМИ ЦИКЛОПЕНТАНА | 2014 |
|
RU2589054C2 |
| ПРОИЗВОДНЫЕ 1,2,3,4-ТЕТРАГИДРОПИРИДО[4,3-b]ИНДОЛСОДЕРЖАЩИХ ФЕНОТИАЗИНОВ В КАЧЕСТВЕ ИНГИБИТОРОВ ХОЛИНЭСТЕРАЗ И БЛОКАТОРОВ СЕРОТОНИНОВЫХ РЕЦЕПТОРОВ 5-HT, СПОСОБЫ ПОЛУЧЕНИЯ ИХ ХЛОРГИДРАТОВ И ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 2013 |
|
RU2530881C1 |
| Способ получения гидроксамовых кислот, производных 2-арил-2,3-дигидрохиназолин-4(1Н)-онов | 2020 |
|
RU2744750C1 |
| Способ получения аминов клавулановой кислоты или их солей или сложных эфиров | 1976 |
|
SU639454A3 |
| Способ получения производных 1,3-пропилендифосфоновых кислот | 1985 |
|
SU1375141A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ N-3-ОКСОАЛКИЛТИОАМИДОВ | 1994 |
|
RU2068411C1 |
| Способ получения производных имидазола | 1989 |
|
SU1799383A3 |
Изобретение касается производных протопорфирина - IX, в частности его ди-C1c3 - алкиловых эфиров - полупродуктов для получения лекарственных веществ и катализаторов. Цель - повышение выхода целевых веществ и упрощение процесса. Последний ведут нагреванием соответствующих тетраалкиловых эфиров гемапорфирина-IX в диметилформамиде с 2 - 3-эквивалентным количеством бензоилхлорида при 120 - 125oС в течении 15 - 20 мин. Упрощение процесса достигается за счет снижения объемов растворителя и исключения в некоторых случаях хроматографической очистки при повышении выхода целевых веществ до 89% и возможности получения различных эфиров протопорфирина-IX.
Способ получения диалкиловых эфиров протопорфирина-IX общей формулы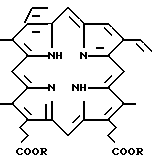
где R СН3, С2Н5, изо-С3Н7,
отличающийся тем, что, с целью упрощения процесса, увеличения выхода целевого продукта, тетраалкиловые эфиры гематопорфирина-IX общей формулы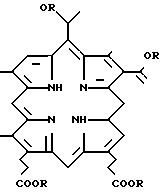
где R имеет указанные значения,
нагревают в диметилформамиде с 2 3 эквивалентами бензоилхлорида в течение 15 20 мин при 120 125oС.
| Аскаров К.А., Березин Б.Д., Евстигнеева Р.П | |||
| и др | |||
| Порфирины: структура, свойства, синтез, М.: Наука, 1985, с.333, 1979 | |||
| Linn I.A | |||
| Schreinev A.F | |||
| Inorganica chim | |||
| Acta, 1979, v.35, N 1, p | |||
| Ручной ткацкий станок | 1922 |
|
SU339A1 |
Авторы
Даты
1996-05-20—Публикация
1987-03-02—Подача