Изобретение относится к химии фосфорорганических соединений, а именно к усовершенствованному способу получения диарилокситетрахлорцик- лотрифосфаэенов общей формулы
P,N9Cl4(OAr)2,
где Аг фенил или замещенный фенил, которые могут быть использованы для получения полифосфаэенов и в качестве модифицирующих добавок для синтетических и природных полимеров.
Цель изобретения - повышение вы- целевых продуктов.
Поставленная цель достигается тем, что диарилоксифосфазены получают взаимодействием гексахлорцикло- трифосфазена (ГХФ) с фенолом и гидро- ксидом калия в двухфазной системе
органический растворитель - вода з присутствии катализатора межфазного переноса (КтМП) - дибензо 18-краун-6 или дициклогексил-18-краун-б, при молярном соотношении катализатора, гексахлорциклотрифосфазена и фенола, равном 0,03-0,05:1:3-5, объемном соотношении водной и органической фаз, равном 0,9-1,1:1 концентрации ГХФ в органической фазе 0,05- 0,15 моль/л, концентрации гидроксида калия в водной фазе 0,15-0,83 моль/л при 40-60°С в течение 3,0-4,0 ч с последующим отделением органического слоя и испарением растворителя.
Выбор указанных факторов определяется следующим: выход диарилокси- тетрахлорциклотрифосфазенов должен
вых солей или применение вместо гидроксида калия гидроксидов натрия или лития приводит также к снижению селективности процесса, что подтверждается примерами 20-23.
Изобретение иллюстрируется следующими примерами.
Пример 1.К раствору 1,74 г ГХФ в 50 мл бензола (концентрация ГХФ 0,1 моль/л) приливают раствор 1,2 г гидроксида калия, 1,9 г фенола и 0,09 г дибензо-18-краун-6 в 50 мл воды (соотношение водной и jj органической фаз 1:1, молярное соотношение КтМП:ГХФ:фенол 0,05:1:4, концентрация гидроксида калия 0,4 моль/л) и ведут реакцию при ин10
тенсивном перемешивании в течение составлять 90%, не должно наблюдать- 20 ч ПРИ 50 ± 2°с- Затем отделяют
ся потерь ГХФ вследствие гидролиза, а также появления продуктов с большими или меньшими степенями замещения атомов хлора в ГХФ в количестве 10%.
При проведении реакции в присутствии КтМП в количестве «i0,03 моль/л ГХФ при остальных условия, принятых постоянными повышается содержание продуктов с низшими степенями замещения (10%). Содержание 0,05 моль/моль ГХФ приводит к увеличению содержания продуктов с высшей степенью замещения (10%). Аналогичные эффекты производит соответственно уменьшение концентрации ГХФ в органической фазе (0,05 моль/л)
25
органический слой, отгоняют растворитель и получают 2,4 г (выход ,100%) смеси феноксихлорциклотрифосфа- зенов, состав которой, определенный на основании анализа ее ЯМР Р спектра по суммарной интегральной интенсивности линий, соответствующих
компонентов, следующий: бис (фенок30
35
и ее увеличение (0,15 моль/л), увеличение соотношения водной и органической фаз ( 1,1:1) и его уменьси) тетрахлорциклотрифосфазен 94,3%, трис (фенокси)-трихлорциклотрифосфа- зен 5,7%.
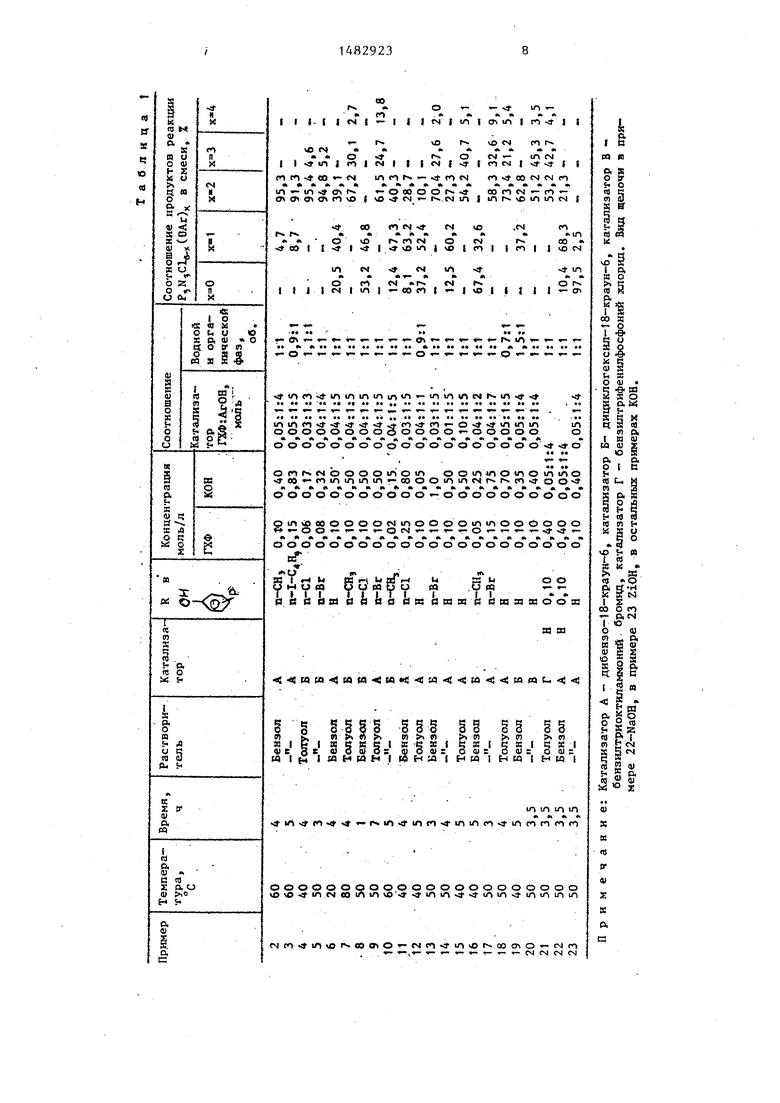
П р и м е ры 2-23. Примеры аналогичны примеру 1 по методике проведения и по последовательности операций. Конкретные условия проведения реакции и состав продуктов реакции, образующихся при взаимодействии ГХФ с различными фенолами в двухфазной системе приведены в табл. 1,
Данные элементного анализа для
шение(), уменьшёнйе моля1)но- 40 примеров 1-5, в которых достигается го соотношения фенола и ГХФ (-0:1) поставленная цель получения смесей и его увеличение (5:1), уменьшение арилоксихлорциклотрифосфазенов, со- времени реакции (3,0) часов и его. держащих свыше 90% диарилокситетра- увеличение (-4,0) часов. Проведение хлорциклотрифосфазена, приведены в
процесса при температуре меньше 40°С, таблг ,
В спектрах ЯМР Р спектральные
линии соединений, входящих в состав продуктов реакции, не перекрываются, что позволяет четко идентифицировать
определить, их содержание в смеси арилоксихлорциклотрифосфазенов по суммарной интегральной интенсивности линий, отвечающих определенным компонентам смеси. В зависимости от стеа также при концентрации гидроксида калия меньше 0,15 моль/л происходит увеличение содержания моноарилокси- проиэводных ГХФ.
Увеличение температуры реакции бо-SO отдельные продукты реакции и
лее чем 60 С или увеличение концентрации гидроксида калия в водной фазе (-0,83 моль/л) приводит к появлению потерь ГХФ вследствие гидролиза (10%), что подтверждается примера1 ми 6-19, приведенными в табл. 1.
Использование вместо краун-эфиров четвертичных аммониевых или фосфоние55
пени замещения атомов хлора в ГХФ
вид ЯМР3 Р спектров следующий: для моноарилоксизамещенных производных ГХФ - система - д - 20,0вых солей или применение вместо гидроксида калия гидроксидов натрия или лития приводит также к снижению селективности процесса, что подтверждается примерами 20-23.
Изобретение иллюстрируется следующими примерами.
Пример 1.К раствору 1,74 г ГХФ в 50 мл бензола (концентрация ГХФ 0,1 моль/л) приливают раствор 1,2 г гидроксида калия, 1,9 г фенола и 0,09 г дибензо-18-краун-6 в 50 мл воды (соотношение водной и органической фаз 1:1, молярное соотношение КтМП:ГХФ:фенол 0,05:1:4, концентрация гидроксида калия 0,4 моль/л) и ведут реакцию при ин
тенсивном перемешивании в течение ч ПРИ 50 ± 2°с- Затем отделяют
органический слой, отгоняют растворитель и получают 2,4 г (выход ,100%) смеси феноксихлорциклотрифосфа- зенов, состав которой, определенный на основании анализа ее ЯМР Р спектра по суммарной интегральной интенсивности линий, соответствующих
компонентов, следующий: бис (фенокопределить, их содержание в смеси арилоксихлорциклотрифосфазенов по суммарной интегральной интенсивности линий, отвечающих определенным компонентам смеси. В зависимости от сте5
пени замещения атомов хлора в ГХФ
вид ЯМР3 Р спектров следующий: для моноарилоксизамещенных производных ГХФ - система - д - 20,021,0 м.д., Ј„ 9,0-10,0 м.д,, j
Ae.
80-82 Гц, в зависимости от вида ари- локсизаместителя; для дизамещенных производных ГХФ - система - 24,0-24,6 м.д.,8в --.15,1-15,7 м.д., j 64-66 Гц, для триарилоксизаме- щенных производных ГХФ - синглет в области 18,1-18,8 м.д.
ИК-спектры синтезированных соеди-- нений идентичны и содержат полосы поглощения в области 500-600 см 1 (Р - С1), 910 - 960 (P-N) и 1350 (Р-К) характерные для исходного ГХФ, свидетельствующие о сохранении циклофосфазенового кольца, а также полосы поглощения, относящиеся к колебаниям ароматического коль- 20 ца при 1510 и 1610 (С-С) и 2800- 3100 (СН). В ИК-спектрах присутствуют также полосы, типичные для
сихлорциклотрифосфазенов, содержащие более 90% диарилокситетрахлорциклотрит фосфазена.
5
Формула изобретения
Способ получения диарилокситетра- хлорциклотрифосфазенов общей формулы
10 ), где Аг - фенил или замещенный фенил, взаимодействием гексахлорциклотрифосфазена с фенолом и гидроксидом калия в двухфазной системе органический растворитель 15 вода при 40-60°С в присутствии ката- лиэа лрра межфазного переноса, отличающийся тем, что, с целью повышения выхода целевого продукта, в качестве катализатора используют дибензо-18-краун-6 или ди- циклогексил-18-краун-6 и процесс ведут в течение 3,0-4, 0 ч при молярном соотношении катализатора, гексахлор- циклотрифосфазена и фенола, равном
колебаний связи РОАг в области
,1180-1240 . Кроме того, как спект-25 0,03-0,05:1:3-5, объемном соотноше- ральные, так и физико-химические ний водной и органической фаз, равном характеристики синтезированных арило - .0,9-1,1:1, концентрации гексахлор- ксихлорциклотрифосфазенов соответст- циклотрифосфаэена в органической вуют литературным данным.фазе 0,05-0,15 моль/л, концентрации
Таким образом, предлагаемый спо- 30 гидроксида калия в водной фазе 0,15- соб позволяет получать смеси арилок- 0,83 моль/л.
сихлорциклотрифосфазенов, содержащие более 90% диарилокситетрахлорциклотрит фосфазена.
Формула изобретения
Способ получения диарилокситетра- хлорциклотрифосфазенов общей формулы
), где Аг - фенил или замещенный фенил, взаимодействием гексахлорциклотрифосфазена с фенолом и гидроксидом калия в двухфазной системе органический растворитель 5 вода при 40-60°С в присутствии ката- лиэа лрра межфазного переноса, отличающийся тем, что, с целью повышения выхода целевого продукта, в качестве катализатора используют дибензо-18-краун-6 или ди- циклогексил-18-краун-6 и процесс ведут в течение 3,0-4, 0 ч при молярном соотношении катализатора, гексахлор- циклотрифосфазена и фенола, равном
5 0,03-0,05:1:3-5, объемном соотноше- ний водной и органической фаз, равном .0,9-1,1:1, концентрации гексахлор- циклотрифосфаэена в органической фазе 0,05-0,15 моль/л, концентрации
Ј- 00 ГО ЧО КЗ
OJ



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения гексаарилоксициклотрифосфазенов | 1990 |
|
SU1761759A1 |
| Способ получения гексакис-(2,2,2-трифторэтокси)циклотрифосфазена | 1990 |
|
SU1761758A1 |
| Способ получения моноарилоксипентахлорциклотрифосфазенов | 1984 |
|
SU1225845A1 |
| Способ получения ди- и триарилоксизамещенных производных гексахлорциклотрифосфазена | 1984 |
|
SU1225844A1 |
| ФОСФАЗЕНСОДЕРЖАЩИЙ ОЛИГОЭФИРАКРИЛАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2743697C1 |
| ФОСФАЗЕНСОДЕРЖАЩАЯ ЭПОКСИДНАЯ СМОЛА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2016 |
|
RU2639708C1 |
| Способ получения динитропроизводных дифениловых и трифениловых эфиров | 2017 |
|
RU2671581C1 |
| Способ получения алкил(фенилэтинил)селенидов | 1990 |
|
SU1728237A1 |
| Способ получения смеси моно-,бис-,трис- и тетракистрифторэтоксизамещенных производных гексахлорциклотрифосфазена | 1984 |
|
SU1245577A1 |
| Способ получения моноарилоксипентахлорциклотрифосфазенов | 1983 |
|
SU1113382A1 |
Изобретение относится к химии фосфорорганических соединений, в частности к получению диарилоксизамещенных производных гексахлортрифосфазена общей ф-лы P3N3CL4 (OAR)2, где AR - фенил или замещенный фенил, которые могут быть использованы для получения полифосфазенов, обладающих повышенной термостойкостью и пониженной горючестью и как модифицирующие добавки для синтетических и природных полимеров. Цель - увеличение выхода диарилокситетрахлортрифосфазенов и упрощение процесса их получения. Синтез ведут из гексахлорциклотрифосфазена, соответствующего фенола и КОН в двухфазной системе органический растворитель - вода в присутствии катализатора межфазного переноса дибензо -18-краун-6 или дициклогексил-18-краун-6, при молярном соотношении катализатора, гексахлорциклотрифосфазена и фенола =(0,03-0,05): 1: (3-5), объемном соотношении водной и органической фаз (0,9-1,1) : 1, концентрации гексахлорциклотрифосфазена в органической фазе 0,05-0,15 моль/л, концентрации КОН в водной фазе 0,13-0,83 моль/л при 40-60°С в течение 3,0-4,0 ч. Способ исключает использование сухих растворителей и стадию получения фенолята щелочного металла из фенола и металла. Выход целевого продукта более 90 против 82%. 2 табл.
Примечание: Катализатор А - дибензо-18-краун-6, катализатор Б- дициклогексил-18-краун-6, катализатор В бензилтриоктиламмоний бромид, катализатор Г - бензилтрифенилфосфоний хлорид. Вид щелочи в примере 22-NaOH, в примере 23 ZiOH, в остальных примерах КОН.
Таблица i
| Быков А.В., Володин А.А., Кутепов Д.Ф., Киреев В.В | |||
| Фенокси- хлорциклотрифосфазены | |||
| - Труды Московского химико-технологического института им | |||
| Д.И.Менделеева, 1975, вып | |||
| Пюпитр для работы на пишущих машинах | 1922 |
|
SU86A1 |
| Способ обделки поверхностей приборов отопления с целью увеличения теплоотдачи | 1919 |
|
SU135A1 |
| Способ получения моноарилоксипентахлорциклотрифосфазенов | 1984 |
|
SU1225845A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Способ получения ди- и триарилоксизамещенных производных гексахлорциклотрифосфазена | 1984 |
|
SU1225844A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1989-05-30—Публикация
1987-07-06—Подача