Изобретение относится к усовершенствованному способу получения производных дезокситионуклеотидов общей формулы I 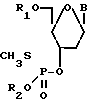 где В - остаток тимина, N4-бензоилцитозина, N6-бензоиладенина и N2-изобутирилгуанина;
где В - остаток тимина, N4-бензоилцитозина, N6-бензоиладенина и N2-изобутирилгуанина;
R1 - 4,4′ -диметоксититил;
R2 - Н или 2-цианэтил, и может быть испoльзовано в молекулярной биологии и генетической инженерии.
Цель изобретения - упрощение процесса за счет сокращения числа стадий и времени проведения при сохранении высоких выходов целевого продукта - достигается использованием в качестве реагента S-метилтиодихлорфосфата в присутствии 1,2,4-триазола.
П р и м е р 1. 5' -0-Диметокситритилтимидин-3' -0-(2-цианэтил-S- метилтио)фосфат.
К раствору диметокситритилтимидина (0,544 г, 1 ммоль) и 1,2,4- триазола (0,69 г, 10 ммоль) в 9 мл пиридина, охлажденного до 0оС, добавляют S-метилтиодихлорфосфат (0,2 мл, 2 ммоль), выдерживают при 0-5оС в течение 30 мин. Реакционную смесь обрабатывают этиленциангидрином (0,80 мл) и оставляют на 1 ч при комнатной температуре. Добавляют 1 мл 1М водного раствора бикарбоната триэтиламмония и через 10-15 мин экстрагируют хлороформом (10 мл). Экстракт промывают водой (5 мл 2), сушат безводным сульфатом натрия и упаривают в вакууме. Остаток растворяют в 20 мл трет-бутанола и подвергают лиофильной сушке. Выход 0,636 г (0,9 ммоль, 90% ).
Полученное вещество идентично по УФ-спектру и хроматографической подвижности заведомому образцу.
П р и м е р 2. 5' -0-Диметокситритил-N4-бензоил-2-дезоксицитидин- 3′ -0-(2-цианэтил-S-метилтио)фосфат.
Фосфорилирование 5' -0-диметокситритил-N4-бензоилцитидина (0,63 г, 1 ммоль) S-метилтиодихлорфосфатом и последующее цианэтилирование ведут аналогично. Выход (после лиофильной сушки из бензола) 0,716 г (90% ).
П р и м е р 3. 5' -0-Диметокситритил-N2-изобутирилдезоксигуанозин- 3′ -0-(2-цианэтил-S-метилтио)фосфат
Фосфорилирование 5' -0-диметокситритил-N2-изобутирилдезоксигуанозина (0,638 г, 1 ммоль) S-метилтидихлорфосфатом и цианэтилирование ведут аналогично. Выход 0,681 г (0,85 ммоль, 85% ).
П р и м е р 4. 5' -0-Диметокситритил-N6-бензоилдезоксиаденозин-3′ -0-(2-цианэтил-S-метилтио)фосфат.
Фосфорилирование 5' -0-диметокситритил-N6-бензоилдезоксиаденозина (0,656 г, 1 ммоль) S-метилтиодихлорфосфатом и цианэтилирование, как описано выше, дает 0,704 г (0,86 ммоль, 86% ) продукта (лиофильно высушен из бензола).
П р и м е р 5. 5' - 0-Диметокситритилтимидин-3′ -0-(S- метилтио)фосфат.
К раствору диметокситритилтимидина (0,544 г, 1 ммоль) и 1,2,4- триазола (0,69 г, 10 ммоль) в 9 мл пиридина, охлажденного до 0оС, добавляют S-метилтиодихлорфосфат (0,2 мл, 2 ммоль), выдерживают при 0-5оС в течение 30 мин. Добавляют 1 мл 1М водного раствора бикарбоната триэтиламмония и через 10-15 мин экстрагируют хлороформом (10 мл). Экстракт промывают водой (5 мл 2), сушат сульфатом натрия и упаривают в вакууме. Получают 0,692 г (95% , 0,95 ммоль) целевого соединения.
П р и м е р 6. 5' -0-Диметокситритил-N4-бензоил-2′ - дезоксицитидин-3′-0-(S-метилтио)фосфат.
Фосфорилирование 5′-0-диметокситритил-N4-бензоил-2′- дезоксицитидина (0,632 г, 1 ммоль) S-метилдихлортиофосфатом ведут аналогично. Выход 0,775 г (0,95 ммоль, 95% ).
П р и м е р 7. 5' -0-Диметокситритил-N2-изобутирил-2′- дезоксигуанозин-3-0-(S-метилтио)фосфат.
Фосфорилирование 5' -0-диметокситритил-N2-изобутирил-2 - дезоксигуанозина (0,638 г, 1 ммоль) S-метилтиодихлорфосфатом ведут аналогично. Выход 0,740 г (0,90 ммоль, 90% ).
П р и м е р 8. 5' -Диметокситритил-N6-бензоилдезоксиаденозин-3′- 0-(S-метилтио)фосфат.
Фосфорилирование 5′-0-диметокситритил-N6-бензоилдезоксиаденозина (0,656 г, 1 ммоль) S-метилтиодихлорфосфатом в условиях, приведенных в примере 5, дает 0,772 г (0,92 ммоль, 92% ) целевого продукта. Полученное вещество идентично по УФ-спектру и хроматографической подвижности при тонкослойной хроматографии в системе В известному образцу.
П р и м е р 9. Получение 5' -0-диметокситритилтимидин-3′-0-(2- цианэтил-S-метилтио)фосфата с использованием различных количеств триазола.
Фосфорилирование 5' -диметокситритилтимидина (0,544 г, 1 ммоль).
S-метилтиодихлорфосфатом (2 ммоль, 2 экв. ) в присутствии различных количеств триазола (0,2,4,10 экв. соответственно 0,2,4,10,15 ммоль) в 9 мл Ру (5оС, 20 мин) с последующим цианэтилированием (0,8 мл, 1 ч, 20оС аналогично примеру 1 с последующей хроматографической очисткой продукта дает соответственно 60,80,88,87 и 86% -ные выходы целевого вещества.
П р и м е р 10. Получение 5' -0-диметокситритил-N2-изобутирил-2′-дезоксигуанозин-3′-0-(2-цианэтил-S-мети тио)фосфата с различной продолжительностью фосфорилирования.
Фосфорилирование 5' -0-диметокситритил-N2-изобутирил-2′-дезоксигуанозина (0,638 г, 1 ммоль) S-метилтиодихлорфосфатом (2 ммоль, 2 экв. ) в присутствии 10 экв. триазола в 9 мл Ру при 5оС в течение 10,20,60 и 120 мин с последующим цианэтилированием (0,8 мл, 1 ч, 20оС) аналогично примеру 1 с последующей хроматографической очисткой продукта дает соответственно 80,83,80, 71% -ные выходы целевого вещества.
П р и м е р 11. Синтез 5' -0-диметокситритилтимидин-3′-0-(2- цианэтил-S-метилтио)фосфата с использованием различных количеств фосфорилирующего агента.
Фосфорилирование 5' -0-диметокситритилтимидина (0,544 г, 1 ммоль) различными количествами S-метилтиодиохлорфосфата (1, 1,5 и 3 экв. соответственно 1, 1,5 и 3 ммоль) в присутствии 10 экв. триазола (5оС, 20 мин) с последующей хроматографической очисткой продукта дает соответственно 79, 89 и 88% -ные выходы вещества.
Таким образом, данный способ позволяет упростить процесс за счет двукратного сокращения числа стадий и уменьшить его продолжительность (2-3 ч) в 2-5 раз при сохранении высокого выхода целевых продуктов. (56) Honda S. , Urakami K. , Koura K. , e. a. Synthesis of oligoribonucleotides by use of S, S-diphenyl-N- monomethoxytrityl ribonucleoside 3 -phosphorodithioates. - Tetrahedron 1984, v. 40, N 1, p. 153-163.
Авторское свидетельство СССР N 9269647, кл. С 07 Н 19/04, 1979.
Изобретение касается химии нуклеозидов, в частности получения производных дезокситионуклеотидов общей фрмулы 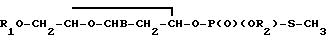 , где R1 - 4,4-диметокситритил, R2-H или N=C-(CH2)2; B - остаток тимина, N4 - бензоилцитозина, N6 - бензоиладенина, N2 - изобутирилгуанидина, которые могут быть использованы в молекулярной биологии и генетической инженерии. Цель - упрощение и интенсификация процесса. Синтез ведут из 5′ - диметокситритил-N-ацил-2-дезоксинуклеозидов и S-метилтиодихлорфосфата, взятого в 1,5 - 2-кратном молярном избытке, в среде пиридина при 0 - 5в присутствии 4 - 10-кратного избытка 1, 2, 4-триазола с дальнейшей обработкой (в случае необходимости) этиленциангидрином, нейтрализацией бикарбонатом триэтиламмония, экстракцией хлороформом, сушкой и отгонкой растворителя. Эти условия в сравнении с известным обеспечивают выход до 85 - 95% при сокращении в 2 раза числа стадий и в 2 - 5 раза продолжительности процесса (2 - 3 ч).
, где R1 - 4,4-диметокситритил, R2-H или N=C-(CH2)2; B - остаток тимина, N4 - бензоилцитозина, N6 - бензоиладенина, N2 - изобутирилгуанидина, которые могут быть использованы в молекулярной биологии и генетической инженерии. Цель - упрощение и интенсификация процесса. Синтез ведут из 5′ - диметокситритил-N-ацил-2-дезоксинуклеозидов и S-метилтиодихлорфосфата, взятого в 1,5 - 2-кратном молярном избытке, в среде пиридина при 0 - 5в присутствии 4 - 10-кратного избытка 1, 2, 4-триазола с дальнейшей обработкой (в случае необходимости) этиленциангидрином, нейтрализацией бикарбонатом триэтиламмония, экстракцией хлороформом, сушкой и отгонкой растворителя. Эти условия в сравнении с известным обеспечивают выход до 85 - 95% при сокращении в 2 раза числа стадий и в 2 - 5 раза продолжительности процесса (2 - 3 ч).
СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ДЕЗОКСИТИОНУКЛЕОТИДОВ общей формулы I
где B - остаток тимина, N4-бензоилцитозина, N6-бензоиладенина или N2-изобутирилгуанина;
R1 - 4,4-диметокситритил;
R2 - H или 2-цинэтил,
взаимодействием 5-О-диметокситритилнуклеозидов общей формулы II
(n-CH3OC6H4)2C(C6H5)-O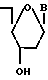
где B имеет указанные значения,
с фосфорилирующим агентом при 0 - 5oС в пиридине с последующей обработкой полученного продукта раствором этиленциангидрида в пиридине в течение 1 - 2 ч при комнатной температуре, отличающийся тем, что, с целью упрощения процесса и сокращения времени его проведения, в качестве фосфорилирующего агента используют S-метилтиодихлорфосфат формулы III
Cl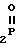 -SCH3
-SCH3
взятый в 1,5 - 2-кратном молярном избытке, и процесс осуществляют в присутствии 4 - 10-кратного избытка 1,2,4-триазола.
Авторы
Даты
1994-02-28—Публикация
1987-10-27—Подача