Изобретение относится к биоорганической химии, а именно к усовершенствованию способа получения п-хлорфениловых эфиров, N, 3'-0-дианцилдезоксинуклеотидов общей формулы 1 H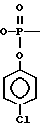 O
O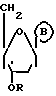 где B - защищенные по экзоциклическим аминогруппам гетероциклические основания - тимин, аденин, гуанин, цитозин;
где B - защищенные по экзоциклическим аминогруппам гетероциклические основания - тимин, аденин, гуанин, цитозин;
R - ацильный остаток.
п-Хлорфениловые эфиры защищенных дезоксимононуклеотидов используются для синтеза дезоксиолигонуклеотидов, являющихся биологически активными веществами.
Целью изобретения является повышение выхода целевого продукта, упрощение процесса и сокращение его длительности.
Поставленная цель достигается взаимодействием п-хлорфенола с предварительно активированным N, 3'-0-диацилдезок- синуклеотидом в растворителе с последующим выдерживанием реакционной смеси в течение 40-70 мин, при этом активацию исходного нуклеотида ведут смесью трифенилфосфина, 2, 2'-дитиодипиридина и 1-метилимидазола при их молярном соотношении 1 : 1 : (1,5-2) соответственно, а в качестве растворителя используют диметилформамид, содержащий эквивалентное п-хлорфенолу количество триэтиламина.
П р и м е р 1. Синтез п-хлорфенилового эфира N6-бензоил-3'-0-левулинилдезоксиаденозин-5'-фосфата.
В круглодонную колбу вместимостью 50 мл загружают 1 г (1,63 ммоля) пиридиновой соли N6-бензоил-3'-0-левулинилдезоксиаденозин-5'-фосфата и сушат в эксикаторе над P2O5 при 4 мм рт. ст. в течение 40 мин. К высушенному нуклеотидному материалу добавляют 7,48 мл диметилформамида и 0,75 мл (9,45 ммолей) 1-метилимидазола, закрывают колбу и энергично встряхивают до полного растворения нуклеотида. В полученный раствор добавляют 1,26 г (5,75 ммолей) 2, 2'-дитиодипиридина и 1,5 г (5,72 ммолей) трифенилфосфина, закрывают колбу и встряхивают полученную смесь в течение 10 мин при комнатной температуре.
К 4,19 (32,6 молей) п-хлорфенола, предварительно высушенного над P2O5 при 4 мм рт. ст. в колбе вместимостью 50 мл, добавляют 4,48 мл (32,6 ммолей) абсолютного триэтиламина и встряхивают до полного растворения п-хлорфенола. Затем растворенный в триэтиламине п-хлорфенол вливают в колбу с полученным 1-метил- имидазольным производным нуклеотида и выдерживают при перемешивании 60 мин при комнатной температуре.
К полученной реакционной смеси добавляют 8 мл дистиллированной воды и 6-9 мл пиридина, чтобы образовался гомогенный раствор. Затем избыток п-хлорфенола и полученного трифенилфосфиноксида экстрагируют серным эфиром (3 х 50 мл). Водный экстракт упаривают с пиридином (10 мл) на ротационном испарителе при 40оС, затем упаривают с толуолом (3 х 10 мл). К полученному остатку добавляют 50 мл хлороформа и наносят на колонку с сорбентом "Силасорб 600 (LC)" (объем колонки 200 мл). Проводят элюцию первого пика градиентом метанола в хлороформе: 0 -> 15 % (общий объем элюата 600 мл), а затем элюцию целевого продукта проводят градиентом метанола в хлороформе: 15 - 60 % (общий объем элюата 600 мл). Фракции, содержащие n-ClPhdpbzA(Lev), объединяют и упаривают растворитель на ротационном испарителе. Остаток растворяют в хлороформе и высаживают в серном эфире. Выпавший осадок отфильтровывают и сушат в вакуум-эксикаторе.
Выход n-ClPhdpbzA(Lev) 0,96 г (79 % ).
П р и м е р 2. Синтез n-хлорфенилового эфира N4-анизоил-3'-0-левулинилдезоксицитидин-5'-фосфата.
Синтез ведут аналогично описанному в примере 1 за исключением того, что в реакцию берут 0,99 г (1,63 ммоля) соли N4-анизоил-3'-0-левулинилдезоксицитидин-5-фосфа- та.
Выход n-ClPhdpanC(Lev) 0,94 г (77 % ).
П р и м е р 3. Синтез п-хлорфенилового эфира N2-изобутирил-3'-0-левулинилдезоксигуанозин-5'-фосфата.
Синтез ведут аналогично описанному в примере 1 за исключением того, что в реакцию берут 0,97 г (1,63 ммоля) пиридиновой соли N2-изобутирил-3'-0-левулинилдезоксигуанозин-5'-фосфата.
Выход n-ClPhdpibuG(Lev) 0,95 г (80 % ).
П р и м е р 4. Синтез п-хлорфенилового эфира 3'-0-левулинилдезокситимидин-5-фосфата.
Синтез ведут аналогично описанному в примере 1 за исключением того, что в реакцию берут 0,81 г (1,63 ммоля) пиридиновой соли 3'-0-левулинилдезокситимидин-5-фосфата.
Выход n-ClPhdpT(Lev) 0,82 г (80 % ).
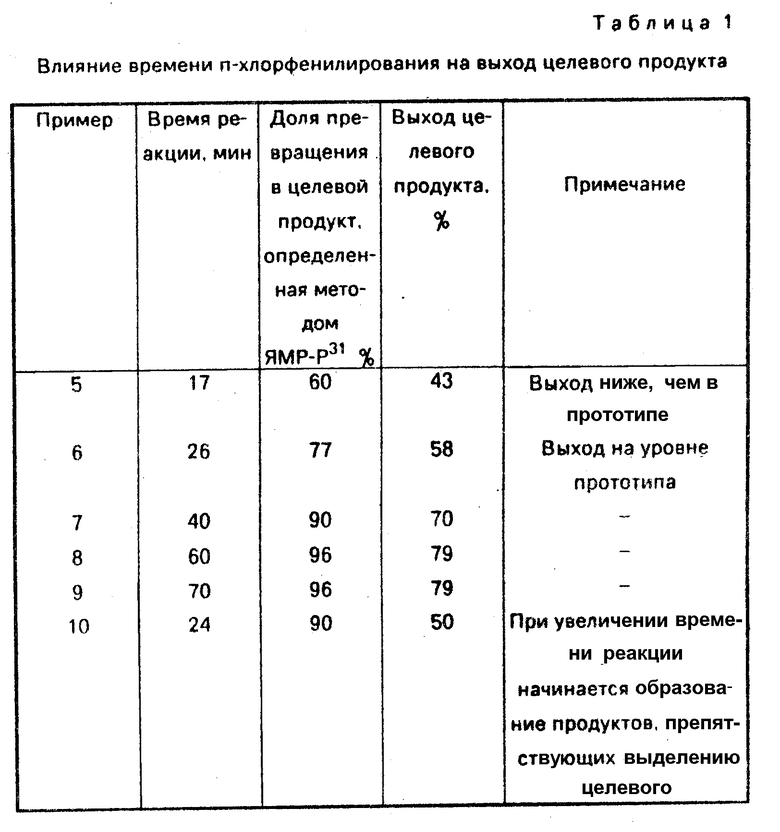
П р и м е р ы 5-10. Выбор времени реакции п-хлорфенилирования.
Синтез ведут аналогично описанному в примере 1, при этом время выдерживания реакционной смеси меняют от 17 мин до 24 ч. Результаты приведены в табл. 1.
П р и м е р ы 11-14. Выбор соотношения количества 1-метилимидазола к окислительно-восстановительной паре: трифенилфосфин 2, 2'-дитиодипиридин.
Синтез ведут аналогично описанному в примере 1, при этом меняют молярные соотношения реагентов активирующей смеси. Результаты приведены в табл. 2.
П р и м е р 15, обосновывающий необходимость использования в процессе триэтиламина.
Синтез ведут аналогично описанному в примере 1, но п-хлорфенол непосредственно добавляют в реакционную смесь. За образованием продукта следят методом ЯМР-Р31. Анализ показывает, что без добавления к п-хлорфенолу триэтиламина при выдерживании реакционной смеси 60 мин доля превращения исходного нуклеотида в целевой продукт незначительна.
Таким образом, изобретение позволяет увеличить выход целевого продукта до 80 % и сократить время проведения реакции до 1-1,2 ч. (56) Авторское свидетельство СССР N 813925, кл. C 07 H 21/00, 1980.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДЕЗОКСИНУКЛЕОЗИД-5'-ТРИФОСФАТОВ | 1994 |
|
RU2080325C1 |
| СИНТЕЗ ФОСФИТИЛИРОВАННЫХ СОЕДИНЕНИЙ С ИСПОЛЬЗОВАНИЕМ ЧЕТВЕРТИЧНОГО ГЕТЕРОЦИКЛИЧЕСКОГО АКТИВАТОРА | 2005 |
|
RU2440364C2 |
| 3'-ФОСФАТ, N, P-НЕЗАЩИЩЕННЫЕ ФОСФОТИОАТНЫЕ ОЛИГОДЕЗОКСНУКЛЕОТИДЫ В КАЧЕСТВЕ ИСХОДНЫХ СОЕДИНЕНИЙ ДЛЯ ПОЛУЧЕНИЯ ФОСФОТИОАТНЫХ, ОЛИГОНУКЛЕОТИДНЫХ РЕАГЕНТОВ ДЛЯ БИОТЕХНОЛОГИЧЕСКИХ ПРОЦЕССОВ, ФОСФОТИОАТНЫЕ ОЛИГОНУКЛЕОТИДНЫЕ ПРОИЗВОДНЫЕ, СОДЕРЖАЩИЕ 3'- И/ИЛИ 5'-СВЯЗАННЫЕ ХИМИЧЕСКИЕ ГРУППИРОВКИ В КАЧЕСТВЕ ФОСФОТИОАТНЫХ ОЛИГОНУКЛЕОТИДНЫХ РЕАГЕНТОВ ДЛЯ БИОТЕХНОЛОГИЧЕСКИХ ПРОЦЕССОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1994 |
|
RU2069214C1 |
| СИНТЕЗ ОЛИГОНУКЛЕОТИДОВ | 2006 |
|
RU2465280C2 |
| Тринуклеотидный кэпирующий реагент, способ его получения и применение | 2024 |
|
RU2829515C1 |
| СПОСОБ СИНТЕЗА ПРОИЗВОДНЫХ 9-АЛЛИЛКАМПТОТЕЦИНА | 2014 |
|
RU2658017C2 |
| Способ получения солей N-ацил-или N-арилдезоксинуклеозид-5 @ -фосфатов | 1989 |
|
SU1768610A1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНОЙ СИСТЕМЫ ДОСТАВКИ НУКЛЕОЗИДТРИФОСФАТОВ В КЛЕТКИ МЛЕКОПИТАЮЩИХ | 2013 |
|
RU2527681C1 |
| Способ получения ароматических эфиров хлоркарбоновой кислот | 1977 |
|
SU707908A1 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ЦИКЛОГЕКСАНА | 2002 |
|
RU2288221C2 |

Изобретение касается сахаров, в частности получения n-хлорфениловых эфиров N, 3′ -диацилдезоксинуклеотидов ф-лы (рисунок), где В - защищенные по экзоциклическим аминогруппам гетероциклические основания - аденин, гуанин, тимин, цитозин; R - ацильный остаток. Цель - повышение выхода целевого продукта, упрощение процесса и сокращение его длительности. Получение ведут реакцией n-хлорфенола с активированным смесью трифенилфосфина, 2, 2′ -дитиодипиридина и 1-метилмидазола при молярном соотношении 1: 1: (1,5 - 2) соответствующим N, 3′ -0-диацилдезоксинуклеотидом. Реакцию проводят в диметилформамиде, содержащем эквивалентное N-хлорфенолу количество триэтиламина, а реакционную смесь выдерживают 40 - 70 мин при комнатной температуре. Выход до 80% , время проведения реакции сокращается до 1 - 1,2 ч. 2 табл.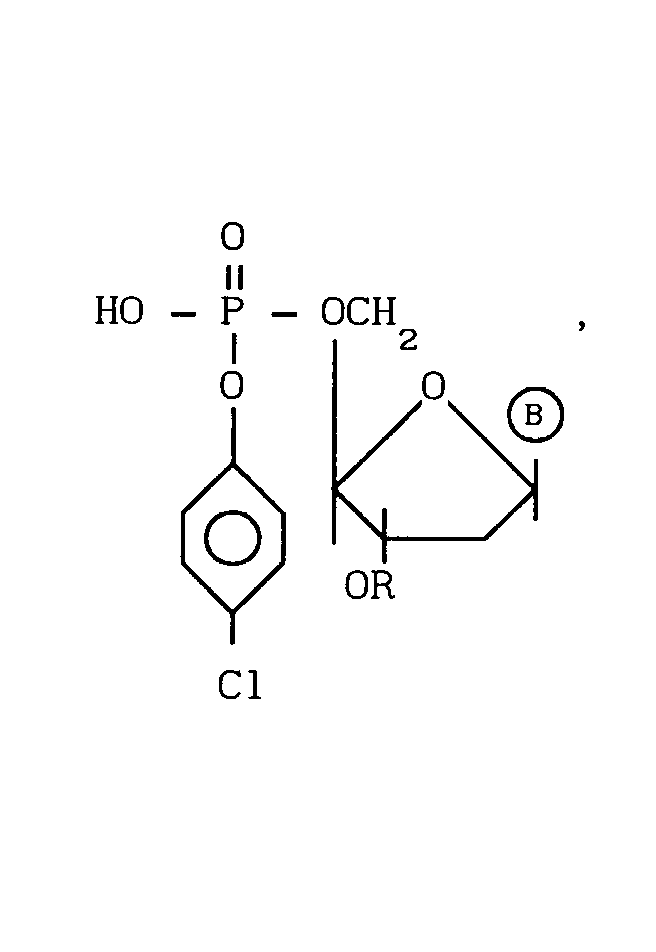
СПОСОБ ПОЛУЧЕНИЯ П-ХЛОРФЕНИЛОВЫХ ЭФИРОВ N, 3'-O-ДИАЦИЛДЕЗОКСИНУКЛЕОТИДОВ общей формулы
HO 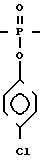
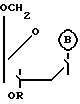 ,
,
где B - защищенные по экзоциклическим аминогруппам гетероциклические основания - аденин, гуанин, тиамин, цитозин;
R - ацильный остаток,
путем взаимодействия п-хлорфенола с предварительно активированным соответствующим N, 3'-O-диацилдезоксинуклеотидом в растворителе и выдерживания реакционной массы при комнатной температуре, отличающийся тем, что, с целью повышения выхода целевого продукта, упрощения процесса и сокращения его длительности, активацию исходного нуклеотида ведут смесью трифенилфосфина, 2,2'-дитиодипиридина и 1-метилимидазола при молярном соотношении реагентов активирующей смеси 1 : 1 : (1,5 - 2) соответственно, в качестве растворителя используют диметилформамид, содержащий эквивалентное п-хлорфенолу количество триэтиламина, а реакционную смесь выдерживают 40 - 70 мин.
Авторы
Даты
1994-01-30—Публикация
1988-09-16—Подача