Изобретение относится к производным пенициллина в виде их натриевых солей, обладающим свойствами антибиотика.
Известны производные пенициллина, более конкретно, производные ампициллина, у которых аминогруппа ацили- рована изокумарин-3-карбоновыми кислотами (авторское свидетельство НРБ № 34532, кл. С 07 D 499/46, опублик. 1983), которые проявляют активность против микроорганизмов Pseudomonas aeruginosa.
Целью изобретения является создание новых антибиотиков пенициллино- вого ряда с антимикробным действием по отношению к широкому кругу как грамположительных, так и грамотри- цательных микроорганизмов.
Цель достигается новыми производными пенициллина в виде их натриевых солей формулы
S
R-CO-fNH(:;HCO) (D
с с Н 5 ri г-опхтг.
4s
00
s|
о
COONa
где R - имеет формулы
РЗ
ИЛИ
каждый - метоксигруппа,
водород, каждый-водород,
метил или метоксикарбонил,
кислород или метилиминогруппа,
О или 1,
йствами антибиотика. ормулы (I) получают миногруппы пенама фор
S СНз KH-T-rjcHj
.
О
COOY
(II)
где n О или 1,
X - водород или триалкилсилильная группй,
Y - металл или аммониевая или триалкилсилильная группа, ацилиругощим агентом формулы
R - СО - Z (III) где R имеет указанные значения,
Z - галоген или группа -0-СО-Алкил.
Конденсацию ацильного производного общей формулы (III) с пенамовым производным формулы (II) осуществляют в безводной или водноорганической среде, в присутствии слабого органического «ли неорганического основания в качестве средства, связывающего хлороводород, и при температуре реакционной среды в пределах от -20 до + 20 С.
Для работы в водноорганической среде в качестве растворителей могут быть использованы ацетон, тетрагидро- фуран, диоксан, диметилформамид, ди- метилацетамид или диметилсульфоксид. Ацилирование в безводной среде осуществляют в несмешивающимся с водой органическом растворителе, таком как хлорированный углеводород, в частности хлороформ или метиленхлорид.
В качестве связывающего хлороводород средства используют слабое органическое и неорганическое основания.
10
15
4918714
такое как бикарбонат натрия, М,М-ди- метиланилин, триэтиламин или пиридин.
В тех случаях, когда ацилирование проводят в безводной среде, б-АДК (6-аминопенициллановую кислоту) или ее (/-аминопроизводное вводят в реакцию в форме М,0-бис-триалкилсилильных производных.
Силилирование осуществляют в безводном органическом растворителе. В качестве силилирующего агента используют триалкилхлорсилан, гексаме- тилдисилазан, N,0-бис-триметилсилил- ацетам1Щ, N,Ы-бис-триметилсилилкар5а- мид, а также и комбинация из гексаме- тилдисилазана и триметилхлорсилана.
Выделение конечных продуктов в виде их натриевых солей осуществляют после экстракции антибиотика из органического .растворителя раствором бикарбоната натрия и лиофилизации или посредством осаждения в органическом растворителе подходящим осадителем, ацетатом натрия или натриевой солью диэтилкапроновой кислоты.
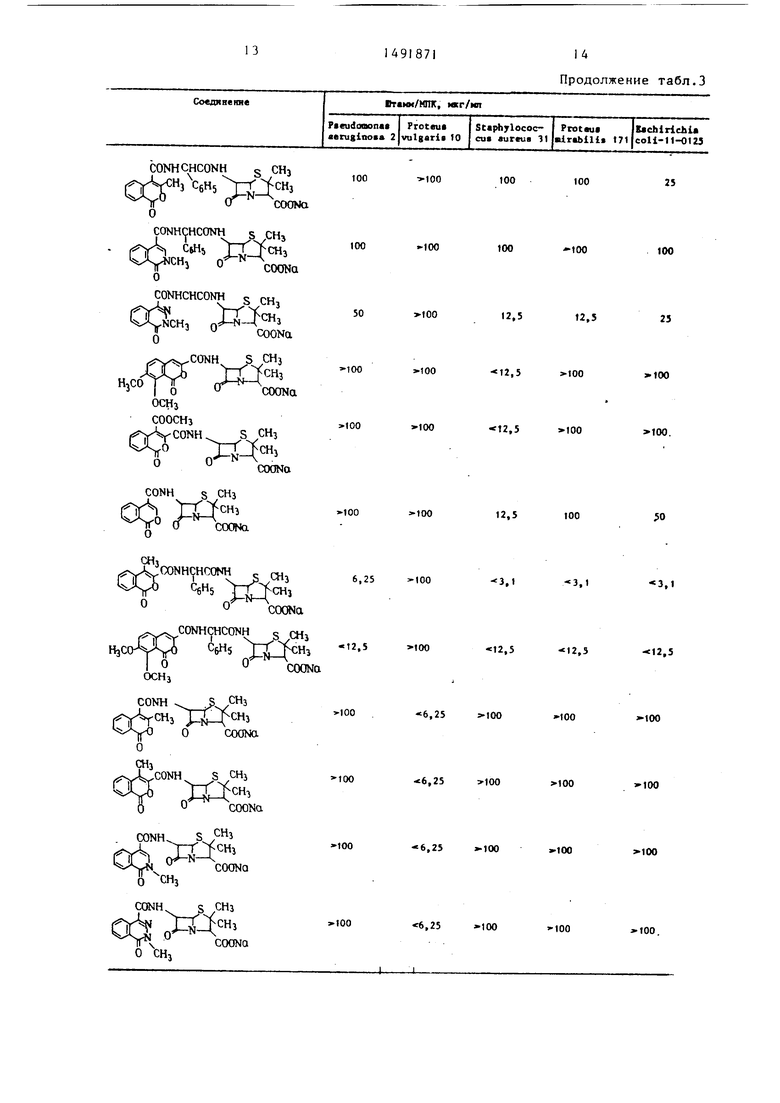
Проведенные испытания полученных соединений показьгоают, что они проявляют активность in vitro по отношению к патогенным микроорганизмам, таким как Staphylococcus aureus, Е. coll, PS. aeruginosa, P. vulgaris.
Пример. Натриевая соль 6-(4-метилизокумарин-3-карбоксами- до)-2,2-диметилпенам-З-карбоновой кислоты:
20
25
30
35
снз н
.CON
COONa
5
0
5
1 ммоль (216 мг) 6-АПК и 0,23 мл (1,1 ммоль) гексаметилдисилазана кипятят в 15,0 мл метиленхлорида до полного растворения. Реакционную смесь охлаждают до -5°С, добавляют 1 ммоль (0,14 мл) триэтиламина и после этого, порциями, твердый хлоран- гидрид, полученный из 1 ммоль (204 г) 4-метилизокумарин-З-карбоновой кислоты и 3,0 млгтионилхлорида. Охлаждение прекращают и реакционную смесь размещивают 1 ч при комнатной температуре. Растворитель отгоняют под вакуумом при 40 С. К остатку добавляют 10,0 мл этилацетата и смесь охлаждают до т5°С. Добавляют 2,0 мл воды и подкисляют раствор до рН 2
концентрированной соляной кислотой. Оба слоя разделяют и после сушки органического слоя над сульфатом натрия к нему добавляют эквивалентное количество насыщенного спиртового раствора ацетата натрия. Осадок соли натрия фильтруют и промывают ацетоном. Выход 290 мг (68%), т.пл. 178-181°С (с разл.).
ИК-спектр (нуджол), : 1600 (С00), 1650 (СО, амид), 1730 (СО, лактон) с инфлексом при 1780 (СО, (Ь-лактам), 3400 (NH).
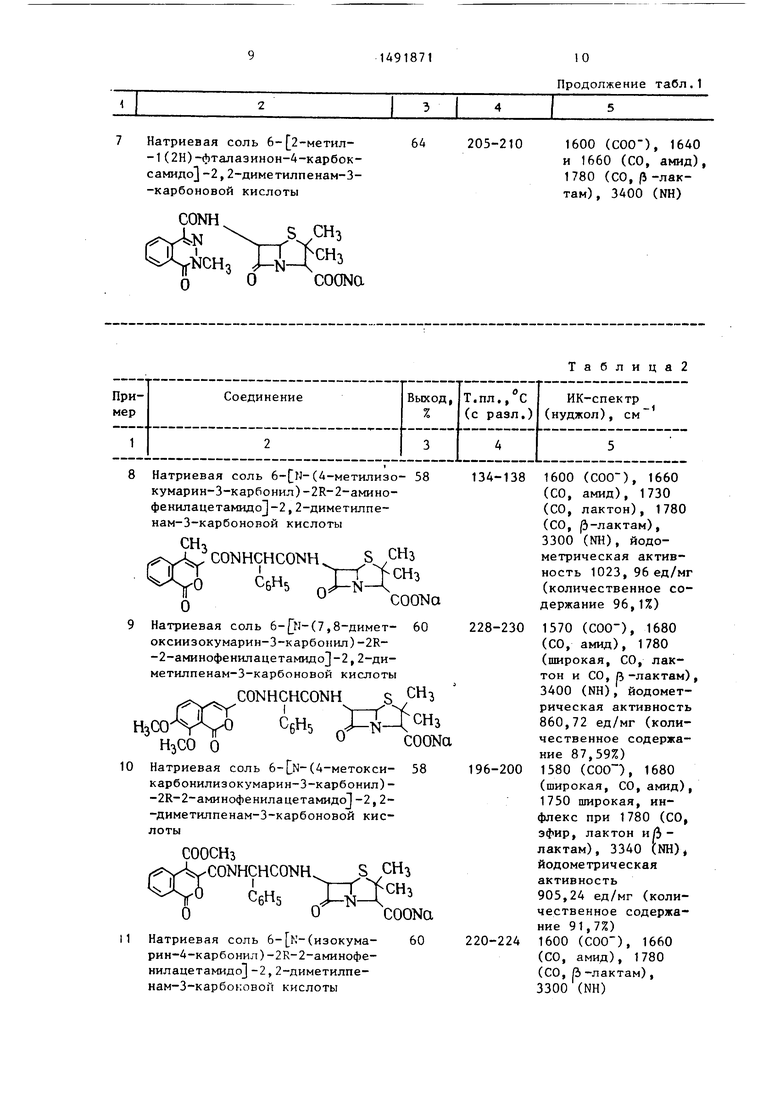
Примеры 2-7. Из 216 мг 6-АПК по методу, описанному в примере 1, синтезируют следующие целевые соединения формулы (I), приведенные в табл. 1.
Примеры 8-17. Из ампициллина (349 мг, 1 ммоль) по методу, описанному Б примере 1, синтезируют следующие соединения, приведенные в табл.2.
Данные по изучению свойств антибиотика натриевых солей производных пенициллина приведены в табл. 3.
Формула изобретения
1. Производные пенициллина в виде их натриевых солей общей формулы
S R-CO-fNHCHCO)H-r-f ЧСН
COONa
где R имеет формулы
Яз
или I I А -NCH
% ОбО
где R, и R - каждый- метоксигрупп.а,
R - водород, или R. и Rj каждый водород,
Rj - метил или метоксикарбо нил,
А - кислород или МеТИЛИМИ-
ногруппа, п О или 1, обладающие свойствами антибиотика.
0
5
0
5
5
О
g
Q
0
2.Натриевая соль 6-(4-метилизоку- марин-3-карбоксамидо)-2,2-диметилпе- нам-3-карбоновой кислоты.
3.Натриевая соль 6-(7,8-диметок- сиизокумарин-3-карбоксамидо)-2,2-диметилпенам-3-карбоновой кислоты.
4.Натриевая соль 6-(4-метоксикар- бонилизокумарин-3-карбоксамидо)-2,2- -диметилпенам-3-карбоновой кислоты.
5.Натриевая соль 6-(изокумарин- -4-карбоксамидо) -2., 2-диметилпенам- -3-карбоновой кислоты.
6.Натриевая соль 6-(3-метилизо- кумарин-4-карбоксамидо)-2,2-диметил- пенам-3-карбоновой кислоты.
7.Натриевая соль 6- 2-метил-1 (2Н)-изохинолинон-4-карбоксамидо 1- -2,2-диметилпенам-З-карбоновой кислоты.
8.Натриевая соль 6- 2-метил-1(2Н)-фталазинон-4-карбоксамидо - -2,2-диметилпенам-З-карбоновой кислоты.
9.Натриевая соль (4-мётил- изокумарин-3-карбонил)-2К-2-аминофе- нилацетамидо -2,2-диметилпенам-З-карбоновой кислоты.
10.Натриевая соль (7,8-ди- мeтoкcиизoкyмapин-3-кapбoнил)-2R-2- -аминофенилацетамидо -2, 2-диметилпе- нам-3-карбоновой кислоты.
11.Натриевая соль (4-меток- cикapбoнилизoкyмapин-3-кapбoнил)-2R- -2-аминофенилацетамидо -2,2-диметилпенам-З-карбоновой кислоты.
12.Натриевая соль (изокума- pин-4-кapбoнил)-2R-2-aминoфeнилaцeт- амидо1-2,2-диметилпенам-З-карбоновой кислоты.
13.Натриевая соль (3-метил- изoкyмapин-4-кapбoнил)-2R-2-aминoфe- нилацетамидо -2,2-диметилпенам-З-карбоновой кислоты.
14.Натриевая соль (2-метил- -1(2Н)-изохинолин-4-карбонил)-2R-2- -аминофенилацетамидо -2,2-диметилпенам-З-карбоновой кислоты.
15.Натриевая соль 6-(Н-(2-метил-1(2Н)-фталазинон-4-карбонил)-2R- -2-аминофенилацетамидо -2,2-диметилпенам-З-карбоновой кислоты.
Таблица 1




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения пенициллиновых производных или их солей | 1974 |
|
SU578888A3 |
| Способ получения амидов кислот или ихСОлЕй C щЕлОчНыМи МЕТАллАМи или ТРиАл-КилАМиНАМи | 1975 |
|
SU797579A3 |
| Цефалоспориновые соединения,проявляющие противомикробную активность | 1980 |
|
SU1130568A1 |
| Способ получения 7-замещенных 3-винилцефалоспоринов или их аддитивных солей с кислотами | 1983 |
|
SU1309911A3 |
| Производные 7 @ -метоксицефалоспорина или их натриевые соли,обладающие противомикробной активностью | 1981 |
|
SU1130569A1 |
| Способ получения ненасыщенных производных 7-ациламидо-3-цефем-4-карбоновой кислоты или их сложных эфиров или их солей с щелочными металлами | 1978 |
|
SU856388A3 |
| Способ получения цефалоспоринов или их солей и его вариант | 1980 |
|
SU1033004A3 |
| Способ получения производных цефалоспорина или их солей с щелочными металлами | 1981 |
|
SU1128838A3 |
| Способ получения ненасыщенных производных 7-ациламидо-3-цефем4-карбоновой кислоты или их солей | 1978 |
|
SU753361A3 |
| Способ получения ненасыщенных производных 7-ациламидо-3-цефем-4-карбоновой кислоты или их сложных эфиров или их солей с щелочными металлами | 1979 |
|
SU904524A3 |
Изобретение относится к гетероциклическим соединениям ,в частности, к производным пенициллина в виде их натриевых солей формулы @ , в которой R -радикал формулы @ или @ где R1 и R2, каждый - метоксигруппа и R3 - H или R1 иR2, каждый -H иR3- метил или метоксикарбонил: А-кислород или метилиминогруппа и N=0или 1, которые обладают свойствами антибиотика. Цель - выявление новых антибиотиков, которые проявляют активность по отношению к грамположительным и грамотрицательным микроорганизмам. Целевые соединения получают ацилированием аминогруппы пенама соответствубщим ацилирующим агентом. 14 з.п. ф-лы, 3 табл.
Натриевая соль 6-(7,8-димeтoк- cиизoкyмapин-3-кapбoкcaмидo- -2 ,2-диметилпенам-З-карбоновой кислоты
НзСЮ
СОМНS .З
Д
0 COONa
Натриевая соль 6-(4-метоксикар- бонил-3-карбоксамидо)-2,2-диметилпенам-З-карбоновой кислоты
.
,
о COONa
Натриевая соль 6-(изокума- рин-4-карбоксамидо)-2,2-диметилпенам-З-карбоновой кислоты
CONH
V.Sv -rjf снз
0 COONa
Натриевая соль 6-(3-метил-изо- кумарин-4-карбоксамидо)-2,2- -диметилпенам-3-карбоновой кислоты
S СНз VCYCH3
COONa
Натриевая соль 6- 2-метил- -1(2Н)-изохинолинон-4-карбок- самидо -2,2-диметилпенам-З- -карбоновой кислоты
212-214
1560 (СОО-), 1690 (СО, амид), 1770 (широкая, СО, лактон, СО, р-лактам), 3300 (NH)
1
9
195-199
1580 (СОО-), 1650 (СО, амид), 1700 (СО, эфир), 1760 пшрокая с инфлексом 1780 (СО, лактон, СО, р-лактам), 3400 (NH)
1590(СОО-),
1660(СО, амид),
1720(СО, лактон),
1780(СО,/5-лактам)
3400(NH)
220-222
1580 (С00), 1660 (широкая, СО, амид), 1750 (широкая, СО, лактон, СО, |3-лактам), 3400 (NH)
61 218-220 1600 (С00), 1660
(СО, амид), 1780 (СО, |3-лактам), 3400 (NH)
Натриевая соль 6- 2-метил- -1(2Н)-фталазинон-4-карбок- самидо -2,2-диметилпенам-З- -карбоновой кислоты
О
S СНз
Дснз cooNa
1
Натриевая соль (4-метилизо- 58 кумарин-3-карбонил)-2К-2-амино- фенилацетамидо -2,2-диметилпе- нам-3-карбоновой кислоты
CH-i,„1т
CONHCHCONH S СНз
бНйL-N-
Q COON
Натриевая соль (7,8-димет- 60 оксиизокумарин-3-карбоиил)-2R- -2-аминофенилацетамидоЗ-2,2-ди- метилпенам-3-карбоновой кислоты
CONHCHCONH
СбН5
О
-N
,сн
COON
58
НзСО
НзСО о
Натриевая соль 6-LN-(4-мeтoкcи- карбонилизокумарин-3-карбонил)- -2К-2-аминофенилацетамидо -2,2- -диметилпенам-3-карбоновой кислоты
СООСНз
CONHCHCONH S СНз
„
СбН5 .U-N-Л ОоCOONa
И Натриевая соль (изокума- рин-4-карбонил)-2К-2-аминофе- нилацетамидо -2,2-диметилпе- нам-3-карбоковой кислоты
Продолжение табл.1
64 205-210 1600 (COO), 1640
и 1660 (СО, амид), 1780 (СО, /i -лак- там), 3400 (NH)
Таблица2
58 134-138
т
з
нз
OONa
60 228-230
СИ,
сн
COONa
58
з
з
ONa
196-200
60
220-224
1600 (С00), 1660 (СО, амид), 1730 (СО, лактон), 1780 (СО, р-лактам), 3300 (Ш), йодо- метрическая активность 1023, 96 ед/мг (количественное содержание 96,1%)
1570 (СОО-), 1680 (СО, амид), 1780 (широкая, СО, лак- тон и СО, в-лактам), 3400 (NH), йодомет- рическая активность 860,72 ед/мг (количественное содержание 87,59%) 1580 (С00), 1680 (широкая, СО, амид), 1750 широкая, ин- флекс при 1780 (СО, эфир, лактон и А - лактам), 3340 (Ш), йодометрическая активность 905,24 ед/мг (количественное содержание 91,7%) 1600 (С00), 1660 (СО, амид), 1780 (СО, р-лактам), 3300 (NH)
CONHCHCONHS
ieH, coONa
Натриевая соль 6- К-(3-метил- изокумарин-4-карбонил)-2Е-2- -аминофенил-ацетамидо -2, 2-ди- метилпенам-3-карбонсгвой кислоты
COT JHСНСО Нv.,S
CHjVs
3 Q COQ-Na
3
Натриевая соль (2-метил- -1(2Н)-изохинолинон-4-карбо- нил)-2К-2-аминофенилацетами- до1-2,2-диметилпенам-З-карбо- новой кислоты
CONHCHCONH S СНз
С
. СбИ5
-кснз
,
оCOONa
Натриевая соль (2--меткп- -1(2Н)-фталаэинон-4-карбонил)- -2К-2-аминофенилацетамидо - -2,2-диметилпенам-З-карбоно- вой кислоты
.12,5
CONHCHCONH S СНэ
вН5 JJcHi
ОCOCfNQ
100
Продолжение табл.2
186-190
1590 (С00), 1670 (СО, амид), 1750 широкая с инфлексом при 1780 (СО, лак- тон, СО, (5-лактам) , 3400 (ЫН)
235-240
1590 (С00), 1660 (СО, амид), 1770 (СО, f -лактам), 3400 (NH)
218-222
1590 (СОО-), 1680 (широкая, СО, амид), 1780 (СО,р -лактам) 3400 (NH)
ТабляцаЗ
too
«12,5«12,5
42,5
-too
-3,1
6,26
25
CONHCHCONH S CHj 3 СбН5 СНз
(,
COONa
CONHCHCONH
CsHj
CHj 0
COONa
COONa
CONHCHCONH о PH vA.
„««
гс& ™ уД™4
,ooY „iOCHjСООСНз YCONH S
f
COONa
CONH S CHj
50
-100
100
100
о
оCOONa
CONHCHCONH
СбН5
О
X(
.СНз CHj
COCfNa
6,
CONHCHCONH S cHi
0 OCHj
I
C6H5
COONa
«12,
CONH CH
.
0 с
СНз CHj
COONa
0
Продолжение табл.3
100
100
100
25
-100
100
too
100
-ioo
12,5
12,5
23
100
12,5
100
too
-100
ft2,
too.
100
12,5
too
50
6,25 too
3,1
3,1
3,t
t2,5
,3
c12,5
«6,25э-tOO
too
too
Авторы
Даты
1989-07-07—Публикация
1985-04-19—Подача