СМ










| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения соединений цефалоспорина | 1988 |
|
SU1551249A3 |
| Способ получения производных 7- @ 2-/2-аминотиазолил/-2-оксииминоацетамидо @ -3-цефем-4-карбоновых кислот или их сложных эфиров или их солей с щелочными металлами | 1979 |
|
SU1098523A3 |
| Способ получения цефемовых соединений или их аддитивных солей с кислотами | 1988 |
|
SU1787158A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ЦЕФЕМА | 1989 |
|
RU2007408C1 |
| Способ получения производных тиазола или их аддитивных солей с кислотами | 1988 |
|
SU1753948A3 |
| Способ получения производного хинолона | 1990 |
|
SU1836367A3 |
| Способ получения производных тиазола или их аддитивных солей с кислотами | 1986 |
|
SU1597102A3 |
| Способ получения производных цефалоспорина или их аддитивных солей с галоидводородными кислотами | 1986 |
|
SU1375140A3 |
| СОЕДИНЕНИЯ ЦЕФЕМА И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1992 |
|
RU2081874C1 |
| Способ получения производных цефалоспорина в виде их аддитивных солей с галоидводородными кислотами | 1982 |
|
SU1331432A3 |
Изобретение относится к гетероциклическим соединениям, в частности к получению соединений цефалоспорина формулы I @ где R1 - аминогруппа
один из R2 и R3 - низший C1-C4-алкилтио, низший C1-C4-алкокси, низший C1-C4-алкил, аминогруппа или атом галогена, а другой из R2 и R3 - H или аминогруппа, которые обладают активностью против грамположительных и грамотрицательных бактерий, а также против микроорганизмов, продуциирующих β-лактамазу. Цель - разработка способа получения новых более активных соединений. Получение ведут реакцией соединений формул II и III @ (II) @ (III), где R4 - аминогруппа, возможно замещенная тритилом
R5 и R6 имеют значения, указанные для R2 и R3 и дополнительно низший ациламино, такой как формиламино, и в случае, когда R4 - защищенная тритилом аминогруппа и R5 и/или R6 являются низшими ациламиногруппами, удаляют аминозащищающую группу. 3 табл.
Изобретение относится к способу получения новых антибиотиков цефало- споринового ряда, в частности к способу получения соединений цефалоспо- рина формулы I
осоо R3
о
i
н
где R, - аминогруппа, один из R2 R - низший С,-С -алкилтио, низший алкокси, низший С -С -алкил, аминогруппа или атом галогена, а другой из R и R - атом водорода или аминогруппа, обладающих активностью против грамположительных и грамотрица- тельных бактерий, а также против микфильтрат выпаривают до сухого состояния при пониженном давлении В остаток добавляют простой эфир. Полученный в результате порошок собирают фильтрацией, растворяют в 50 мл воды и пропускают через колонну, упакованную неионной смолой для адсорбирования (которая производится фирмой
роорганизмов, продуцирующих В -пакта- 10 Митсубиши Кемикэл Индастриз Лтд под
мазу
Цель изобретения - получение новых соединений цефалоспоринового ряда, обладающих улучшенной антибактериальной активностью.
Пример (1)2,2 г дигидра- та (Z) -2-(2-тритиламинотиазол-4-ил) 2-Ј//3S (-2-оксопирролидин-З-ил)окси- имино уксусной кислоты растворяют в смеси 9,5 мл диметилацетамида и 20 14,5 мл метиленхлорида.
Смесь охлаждают до -20 С. По каплям в смесь при перемешивании при температуре от -15 до -20°С добавляют
торговым наименованием Диаион СХП-20П, в дальнейшем она именуется СХП-20П).
Фракции, содержащие целевой про- J5 дукт, собирают и выпаривают до сухого состояния при пониженном давлении, в результате чего получают 1,5 г -2-(2-аминотиазол-4- ил) (-2-оксопирролидин-З-ил) оксиимино | ацетамидоЯ -3- Ј(3-амино-5- метокси-1 пиридинио)метил -3-цефем- 4-карбоксилата
Т.пЛо 180-195°С (разложение). ЯМР(Вгр+СР3СООО),& : 2,0-2,7 (2Н,
синглет), 5,03 (1Н, триплет, Гц), 5,07 (1Н, дублет, Гц), 5,22 (1Н,
2,45 г оксихлорида фосфора. Смесь пе- 25мультиплет), 3,20 (1Н, дублет, 1
ремешивают при -5°С в течение 10 мин, 18 Гц), 3,2-3,6 (2Н, мультиплет),
а затем охлаждают до -35° С (получен-3,63 (1Н, дублет, Гц), 3,88 (ЗН, ный в результате раствор в дальнейшем именуется как раствор А).
С другой стороны 1,92 г дигидрата 50дублет, Гц), 5,37 (1Н, дублет,
йодгидрата 7 ft -амино-3-П(3-амино-5-I 14 Гц), 5,77 (1Н, дублет, Гц)
метокси-1-пир идинио метил -З-цефем-4-7,00 (1Н, синглет), 7,10 (1Н, широкарбоксилата суспендируют в 19 млкий синглет)„
этанола и в суспензию при перемешива- Примеры 2-3 Соответствующие
нии добавляют 12 мл воды„ Смесь ох- 35исходные соединения обрабатывают по
лаждают до -20°С и в нее по каплямтой же схеме, что была описана в
добавляют 8,8 мл триэтиламина Смесьпримере 1 (О в результате чего поперемешивают при -20°С до тех пор, по-лучают следующие соединения, ка она не становится прозрачным раст- (2-1) 7ft- i/Z/ -2-(2-тритиламиновором, а затем охлаждают до -35°С0 В 40тиазол-4-ил)-2-Ј//35(-2-оксопирролинего добавляют полученный раствор А дин-3-ил)оксиимино ацетамидоЯ-3-(2и смесь энергично перемешивают. Смесьметилтио-1-пиридинио)метил -3-цефем- перемешивают при температуре в области от -15 до -20°С в течение 10 мин, а затем в нее по каплям добавляют 45 20 мл 6Н раствора серной кислоты0 Выпавшие в осадок кристаллы собирают, промывают водой и сушат, в результате чего получают 2,7 г 7ft- Г/Z/ -2(24-карбоксилат.
тритиламинотиазол-4-ил)-2 //3S (-2- оксопирролидин-3-ил)оксиимино ацет- амидоЯ -3- Ј(3-амино-5-метокси-1-пири- динио)метил -3-цефем-4-карбоксилата0
50
: 1775 1675 ЯМР (DMCO-d6),S :2,1-2,5 (2Н, муль; типлет), 3,12 (ЗН, синглет), 2,7 - 3,4 (4Н, мультиплет), 4,60 (1Н, триплет, Гц), 5,00 (1Н, дублет, 1 5 Гц), 5,4-5,9 (ЗН, мультиплет), 6,60 (1Н, синглет), 7,2 (15Н) 7,6 - 8,0 (1Н, мультиплет), 8,1-8,4 (1Н, мультиплет), 8,6 - 8,9 (2Н, мульт К : 1775 1675 ЯМР (DMCO-d6),S :2,1-2,5 (2Н, муль типлет), 3,12 (ЗН, синглет), 2,7 - 3,4 (4Н, мультиплет), 4,60 (1Н, триплет, Гц), 5,00 (1Н, дублет, 1 5 Гц), 5,4-5,9 (ЗН, мультиплет), 6,60 (1Н, синглет), 7,2 (15Н) 7,6 - 8,0 (1Н, мультиплет), 8,1-8,4 (1Н, мультиплет), 8,6 - 8,9 (2Н, муль(2) Полученный продукт растворяют типлет), 9,3-9,6 (1Н, мультиплет). в 20 мл 88%-ной муравьиной кислоты и ,
(3-1) 7р-{/г/-2-(2-тритиламино- тиазол-4-ил)-2- //3S(-2-оксопирролидин-З-ил )оксиимижГ ацетамидо1 -3- (3перемешивают при комнатной температуре в течение 20 мин. Нерастворимые материалы отделяют фильтрацией, а
фильтрат выпаривают до сухого состояния при пониженном давлении В остаток добавляют простой эфир. Полученный в результате порошок собирают фильтрацией, растворяют в 50 мл воды и пропускают через колонну, упакованную неионной смолой для адсорбирования (которая производится фирмой
0
торговым наименованием Диаион СХП-20П, в дальнейшем она именуется СХП-20П).
Фракции, содержащие целевой про- 5 дукт, собирают и выпаривают до сухого состояния при пониженном давлении, в результате чего получают 1,5 г -2-(2-аминотиазол-4- ил) (-2-оксопирролидин-З-ил) оксиимино | ацетамидоЯ -3- Ј(3-амино-5- метокси-1 пиридинио)метил -3-цефем- 4-карбоксилата
Т.пЛо 180-195°С (разложение). ЯМР(Вгр+СР3СООО),& : 2,0-2,7 (2Н,
мультиплет), 3,20 (1Н, дублет, 1
синглет), 5,03 (1Н, триплет, Гц), 5,07 (1Н, дублет, Гц), 5,22 (1Н,
3,63 (1Н, дублет, Гц), 3,88 (ЗН,
метилтио-1-пири
4-карбоксилат.
метилтио-1-пиридинио)метил -3-цефем-
: 1775 1675 ЯМР (DMCO-d6),S :2,1-2,5 (2Н, муль; типлет), 3,12 (ЗН, синглет), 2,7 - 3,4 (4Н, мультиплет), 4,60 (1Н, триплет, Гц), 5,00 (1Н, дублет, 1 5 Гц), 5,4-5,9 (ЗН, мультиплет), 6,60 (1Н, синглет), 7,2 (15Н) 7,6 - 8,0 (1Н, мультиплет), 8,1-8,4 (1Н, мультиплет), 8,6 - 8,9 (2Н, мультиплет), 9,3-9,6 (1Н, мультиплет). ,
амино- 1-тшридинио)метил З-цефем-4- карбоксилат.
Т.пл. 180-19ЬЭС (разложение).
. НЧИОА1
ИК, 10
20
макс (см 1 ): 1780, 1695.
ЯМР (DMCO-dg), : 2,1-2,4 (2Н, муль- типлет), 2,9-3,3 (4Н, мультиплет), 4,8-5,3 (ЗН, мультиплет), 5,05 (1Н, дублет, Гц), 5,5-5,7 (1Н, мультиплет), 6,59 (1Н, синглет), 7,16 (15Н, синглет), 7,45-7,60 (1Н, мультиплет), 7,75-7,8 (1Н, мультчплет), 7,9-8,2 (2Н, мультиплет)о
Соответствующие исходные соединения обрабатывают при помощи той же процедуры, что была описана в примере 1 , в результате чего получают следующие соединения.
(2-2) 7/}- 7Z/-2- (2-аминотиазол-4- ил) (2-оксопирролидин-З-ил) оксиимино ацетамидо -3- (2-метилтио- 1-пиридинио)метил -3-цефем-4-карбо- ксилат.
ИК,3МДЈ(см-): 1780, 1690.
HMP(),R : 2,0-6,7 (2Н, мультиплет), 2,76 (ЗН, синглет), 3,1-3,6 (4Н, мультиплет), 4,96 (1Н, триплет, Гц), 5,13 (1Н, дублет, Гц), 30 5,18 (1Н, дублет, Гц), 5,65 (Ш, дублет, 1 15 Гц), 5,75 (IH, дублет, Гц), 6,83 (1Н, синглет), 7,4 - 7,8 (2Н, мультиплет), 8,0-8,3 (1Н, мультиплет), 8,53 (Ш, дублет, I 35 7 Гц).
(3-2) 7f -{/ Z/-2-(2-аминотиазол-4- ил) (-2-оксопирролидин-3-ил)ок- сиимино ацетамидоТ -3-(З-амино-1-пиП р и м е р 24. Смесь 260 мг |(2)-2- (2-пминотиазол-4-ил)2- V/3S
(-2-ОКСОПИррОЛИДИН-З-Ил) О KCHH rHHOJ
с ацетамидо-3-(3-формиламино-5-меток си-1-пиридинио)метил -З-цефем-4- карбоксилата и 6 мл 5%-ной хлористо водородной кислоты перемешивают при 40°С в течение 45 мин. Смесь охлаждают и рН обеспечивают на уровне 4,8 при помощи анионообменной смолы (которая производится (Ьирмой Ром и Хасс Ко., США., под торговым наимено ванием Амберлит ИРА-93, а в даль- 15 она сокращенно обозначается ИРА-93). Смолу отделяют фильтрацией и фильтрат пропускают через колонну упакованную материалом СХП-20П. Колонну промывают водой и элюируют 30%-ным водным раствором метанола. Фракции, содержащие целевой продукт собирают и выпаривают до сухого сос тояния при пониженном давлении. В о таток добавляют ацетон. Полученный в результате порошок собирают филь-
25
трацией, в результате чего получают 102 мг 7R-(л)-2-(2-аминотиазол-4- ил)-2- L//3S(-2-оксопирролидин-З-ил) оксиминоЗ ацетамидоJ-3- Ј(3-амино-5- метокси- 1-пиридинио) метшЛ-3-цефем- 4-карбоксилата.
Т.пл. 180-195°С (разложение).
ЯМР (D O+CF3COOD), 8 : 2,0-2,7 (2Н м); 3,20 (1Н, д, Hz), 3,2-3,6 (2Н, м), 3,63 (1Н, д, Hz),.3,88 (ЗН, с), 5,03 (1Н, т, Hz), 5,07 (1Н, д, Hz), 5,22 (1Н, д, 5 Hz), 5,37 (IH, д, 1 14 Hz), 5,77
(1Н, шир.с), 7,80 (2Н, шир.с).
45
ридинжГ)метигГ}-3-цефем-4-карбоксилат,, 40 (jHj д Hz), 7,00 (1Н, с), 7,10
ИК, (): 1770, 1690, 1660.
ЯМР(В20-СО О+СР5С02В), : 2,2-2,7 (2Н, мультиплет), 3,2-3,5 (2Н, мультиплет), 3,21 (1Н, дублет, Гц), 3,67 (1Н, дублет, Гц), 4,95 (1Н, триплет, Гц), 5,11 (1Н, дублет, I 15 Гц), 5,21 (1Н, дублет, Гц), 5,55 (1Н, дублет, Гц), 5,82 (Ш, дублет, 5 Гц) 6,95 (1Н, синглет) 7,5-7,6 (2Н, мультиплет), 7, 9-8,2 (2Н, мультиплет).
50
Получение исходных соединений.
Смесь перемешивают при 80 С в течение 30 мин. Смесь выпаривают до сухого состояния при пониженном давлении, а в остаток добавляют ацетон Полученный в результате порошок со- 55 бирают фильтрацией и этот порошок растворяют в 15 мл метанола. В раствор добавляют 10 мл 25%-ного раствор хлористого водорода в метаноле. Смес перемешивают при комнатной темпераПримеры 4-23j Соответствующие исходные соединения,обрабатывают по той же схеме, что была описана в .примере 1, в результате чего получают соединения, приведенные в табл.1.
10
20
-
5424176
П р и м е р 24. Смесь 260 мг |(2)-2- (2-пминотиазол-4-ил)2- V/3S
(-2-ОКСОПИррОЛИДИН-З-Ил) О KCHH rHHOJ
с ацетамидо-3-(3-формиламино-5-меток- си-1-пиридинио)метил -З-цефем-4- карбоксилата и 6 мл 5%-ной хлористоводородной кислоты перемешивают при 40°С в течение 45 мин. Смесь охлаждают и рН обеспечивают на уровне 4,8 при помощи анионообменной смолы (которая производится (Ьирмой Ром и Хасс Ко., США., под торговым наименованием Амберлит ИРА-93, а в даль- 15 она сокращенно обозначается ИРА-93). Смолу отделяют фильтрацией и фильтрат пропускают через колонну, упакованную материалом СХП-20П. Колонну промывают водой и элюируют 30%-ным водным раствором метанола. Фракции, содержащие целевой продукт, собирают и выпаривают до сухого состояния при пониженном давлении. В остаток добавляют ацетон. Полученный в результате порошок собирают филь-
25
трацией, в результате чего получают 102 мг 7R-(л)-2-(2-аминотиазол-4- ил)-2- L//3S(-2-оксопирролидин-З-ил) оксиминоЗ ацетамидоJ-3- Ј(3-амино-5- метокси- 1-пиридинио) метшЛ-3-цефем- 4-карбоксилата.
Т.пл. 180-195°С (разложение).
ЯМР (D O+CF3COOD), 8 : 2,0-2,7 (2Н, м); 3,20 (1Н, д, Hz), 3,2-3,6 (2Н, м), 3,63 (1Н, д, Hz),.3,88 (ЗН, с), 5,03 (1Н, т, Hz), 5,07 (1Н, д, Hz), 5,22 (1Н, д, 5 Hz), 5,37 (IH, д, 1 14 Hz), 5,77
(jHj д Hz), 7,00 (1Н, с), 7,10
(1Н, шир.с), 7,80 (2Н, шир.с).
(jHj д Hz), 7,00 (1Н, с),
Получение исходных соединений.
Смесь перемешивают при 80 С в течение 30 мин. Смесь выпаривают до сухого состояния при пониженном давлении, а в остаток добавляют ацетон. Полученный в результате порошок со- бирают фильтрацией и этот порошок растворяют в 15 мл метанола. В раствор добавляют 10 мл 25%-ного раствора хлористого водорода в метаноле. Смесь перемешивают при комнатной температуре в течение 30 мин, а затем выпаривают до сухого состояния при пониженном давлении. Остаток растворяют в 10 мл воды, рН раствора обеспечи- вают на уровне 3,0 при помощи 10%-но го водного раствора гидрата окиси натрия при охлаждении.В смесь добавляют 4,0 г йодида натрия и смесь перемешивают. Осажденные кристаллы собирают Лильтрацией, промыв ают водой и сушат, в результате чего получают 2,8 г дигидрата йодгидрата но-3-Ј(3-амино-5-метокси-1-пириди- нио) метил -3-цефем-4-карбоксилата.
Т.пл. 174-179 С (разложение).
Приводимое соединение получают при помощи обработки соответствующего соединения по той же схеме,, что была описана.
Йодгидрат 7А-амино-3- {(2-метил- тио-1-пиридинио)метил |-3-цефем-4- карбоксилата.
ИК,°(): 3400, 3300, 1780,
1 NVC(KCV
ЯМР (DgO+CF CO D),) : 2,80 (ЗН, синглет), 3,48 (2Н, синглет); 5,16 (1Н, дублет, Гц), 5,29 (1Н, дублет, Гц), 5,45 (1Н, дублет, 1 16 Гц), 5,63 (1Н, дублет, Гц), 7,57 (1Н, дублет, дублет, дублет, . ,6,1 Гц), 7,78 (1Н, дублет, 1 8 Гц), 8,19 (1Н, дублет, дублет, дублет, ,7,1 Гц), 8,54(Ш, двойной дублет, ,1 Гц).
Т.пл. 160-180°С (разложение).
3400 330° 320°
1790, 1630.
ЯМР (D40+CF}C01D), 0 : 3,40 (1Н, дублет, Гц), 3,73 (Ш, дублет,
5
0
5
0 5
0 5 0
5
), 5,20 (1Н, дублет, Гц), 5,68 (1Н, дублет, Гц), 5,2-5,4 (2Н, мультиплет), 7,5-7,7 (2Н, мультиплет), 7,9-8,2 (2Н, мультиплет).
Соединения формулы I обладают сильной противомикробной активностью против грамположительных и грамотри- цательных батерий, включающих самые разнообразные микроорганизмы, принадлежащие семействам Staphylococcus, Escherichia, Salmonella, Klebsiella, Proteus, Citrobacter, Enterobacter и Serratia. Соединения формулы I обладают также сильной противомикробной активностью против бактерий, принадлежащих семействам Pseudomonas, Shigella и Enterococcus.
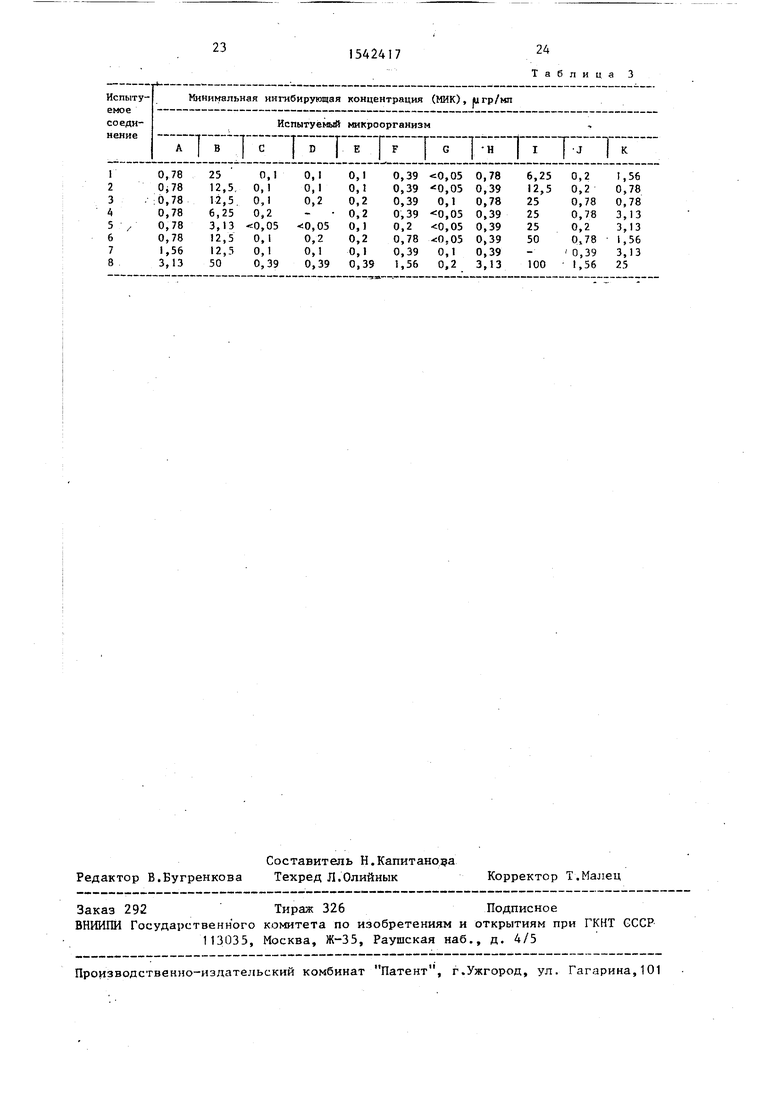
Например, при исследовании минимальной ингибирующей концентрации (МИК) испытуемого соединения с использованием метода разбавления стандартных агаровых пластинок (которьй основан на стандартном методе Японского общества по Хемотерапии), с использованием агара Мюллера-Хинтона в качестве среды АМХ, фирма Ниссуи), противомикробная активность 7В-(Z)- 2-(2-аминотиазол-4-ил)(-2-ок- сопирролидин-3-ил)оксиимино %ацетами- до1 -3- (З-амино-5-метокси-1 -пириди- нио)метшГ)-3-цефем-4-карбоксилата, против Staphylococcus aureus 252R, Proteus morganii 6501, Proteus ret- tgeri 6259 и Enterobacter cloacae TV-680 была не менее, чем примерно в 4 раза выше по сравнению с противомикробной активностью (Z)-2- (2-аминотиазол-4-ил)(2-оксо- пирролидин-3-ил)оксиимино ацетамидоС- 3- Г( 1-пиридинио)метил -З-цефем-4- карбоксилата, которьй был предложен в Европейском Патенте № 101265. Противомикробная активность вышеупомянутого соединения, являющегося предметом изобретения, против Staphylococcus aureus Terajima, Escherichia coli NIHJ JC-2, Salmonella ty- phimurium, Proteus vulgaris IID-874, Proteus inconstans 6764, Citrobacter freunolii TL-12 и Serratia marces- cens 7006 была также примерно в 2 раза выше, чем противомикробная активность соединения из Европейского .Патента. Кроме того, когда 50%-ную минимальную ингибирующую концентрацию против клинически изолированных штаммов анализировали при помощи
У15
той же процедуры,что была упомянута выше, противомикробная активность (Z)-2- (2-уаминотиазол-4-ил)-2- //35(-2-оксопирролидин-3- ил)оксиими- жГ ацетамидо -3-Ј(3-акино-5-метокси- 1-пиридинио)метил -З-цефем-4-карбок- силата, являющегося предметом настоящего изобретения, против Staphylo- coccus aureus (бактерии, стойкие про- тив метициллина, 19 штаммов), Citro- bacter freundii (20 штаммов), Ente- robacter sp. (20 штаммов), Serratia marcescens (20 штаммов) была примерно в 2-4 раза выше по сравнению с противомикробной активностью вышеупомянутого соединения из Европейского Патента.
Кроме того, соединения формулы I характеризуются тем, что они облада- ют сильными защитными эффектами против инфекционных заболеваний, вызванных различными бактериями, которые включают Staphylococcus aureus и Pseudomonas aeruginosa. Соединения формулы I характеризуются также сильной противомикробной активностью в живом организме вследствие их высокой абсорбируемости или большей продолжительности эффектов в живой ткани. Например, каждое испытуемое соединение применяют внутримышечным способом мышам, которые были предварительно заражены внутрибрюшинным способом бактериями в достаточной степени, чтобы все необработанные мыши погибли в течение 24 ч, а затем его 50%-ную эффективную дозу (ЕДга) оценивали через 7 дней после заражения методом проб на основе коэффи- циента выживания мыши. В этих экспериментах защитные эффекты Ј(Z)-2- (2-минотиазол 4-ил)(-2-оксо- пирролидин-3-ил)оксиимино | ацетамидоС - 3-Г(амино-5-метокси-1-пиридинио)ме- тил -3-це6ем-4-карбоксилата, являющегося предметом настоящего изобретения против Staphylococcus aureus. Смита (дифАузионного типа), Staphylococcus aureus 712 и Pseudomonas aerugin. Т-408 были соответственно в примере 6,2 и 3,5 раза выше по сравнению с защитными эффектами вышеупомянутого соединения, предложенного в Европейском Патенте К 101 265.
Кроме того, соединения (1) обладают высокой стабильностью против микроорганизмов, продуцирующих ft-лак- тамазу, например, против ft-лактамаз,
17Ю
продуцированных организмами Escheri- chia coli МЛ-1410 РГН-823 или Prote- us vulgaris ГН 76/С-1. Соединения формулы I обладают также низкой токсичностью.
Результаты сравнительных испытаний
Антибактериальная активность in vitro.
Минимальную ингибирующую концентрацию (МИК) нижеперечисленных испытуемых соединений определяли стандартным методом на пластине в растворе агара.
В табл. 2 приведены испытуемые соединения формулы Iх
Из приведенных результатов видно, что соединения по изобретению много активнее, чем соединения по Европейскому патенту.
а)Активность против грамположи- тельных бактерий:
Соединения настоящего изобретения (испытуемые соединения 1-6) в 4 раза сильнее, чем соединение 8 по Европейскому патенту в части активности против микроорганизма А, а соединения 2-7 в 4 раза или более сильнее в части активности против микроорганизма В.
б)Активность против грамотрица- тельных бактерий:
Соединения по изобретению (испытуемые соединения 1-7 в два раза или более сильнее, чем соединение 8 (Европейский патент) в части активности против микроорганизмов С-Н, и практически в 4 раза и более сильнее, чем соединение 8 в части активности против микроорганизма Н.
в)Активность против микроорганизмов, продуцирующих -лактамазу:
Соединения по изобретению (.испытуемые соединения 1-7) в два раза и более сильнее, чем известное соединение 8 в части активности против микроорганизмов 1-К и почти в восемь раз и более сильнее соединение 8 против микроорганизма К.
Соединения по изобретению в испытуемых дозах признаков токсичности не проявляют и их можно отнести к категории малотоксичных.
Формула изобретения
Способ получения соединений цефа- лоспорина общей Формулы
и
ЧтГ™
о
о
соо
RJ
R
аминогруппа; з
один из К и R - низший
С,-С4С -С4 алкалкилтио, низший окси, низший С -С4 алкил, ю аминогруппа или атом,галогена, а другой из R и R - водород или аминогруппа, личающийся тем, что ционно-способное производное 15 иминоуксусной кислоты общей фор
-тгс-соон
R J II
S N20
О
N25
н
Свойства производных цефалоспорина формулы
H TtC°NH-UfcH2
R3
О
(о8Ь
и N Н
соо
Т.пл. 178-185 С (разложение) ЯМР (D40), 0 :
2,0-2,7 (2Н, м), 2,51 (ЗН, с), 2,9-3,6 (4Н, м), 4,95 (Ш, т, I-7HZ), 5,13 (1Н, д, ), 5,18 (Ш, д, T 15Hz), 5,52 (1Н, д, ), 5,73 (Ш, .g, ), 6,81 (Ш, с), 7,2-7,6 (2Н, м), 7,90 (IH, м) ЯМР (ПгО), $ :
2,1-2,9 (2Н, м), 2,64 (ЗН, с), 3,0-3,9 (4Н, м), 5,03 (Ш, т, I-7HZ), 5,25 (Ш, д, ), 5,28 (Ш, д, ), 5,60 (1Н,
1542417 где
12
Ч
аминогруппа, возможно защищенная тритилом,
подвергают конденсации с 7-аминоцефалоспорином общей формулы
&Т-С ХгН
COO R6
Rc и
Reнизший .де один из ±vs
алкилтио, низший С,-С4.-алк- окси, низший С -С -алкил, а аминогруппа, низший ацил- амино, такой, как формилами- но, или галоген, а другой из R5 и Rg - водород, амино или низшая ациламиногруппа, такая, как формиламино, и в случае, когда R4 защищенная тритилом аминогруппа, и R5 и/или R6 являются (является) низшими ациламино- группами, удаляют аминоза- щищающую группу.
Таблица 1
fc
соо
д, I-15HZ), 5,82 (1Н, ц, ), 6,90 (Ш, с), 7,7-8,0 (1Н, м), 8,1-8,4 (Ш, м), 8,5-8,7 (1Н, м), 8,82 (Ш, с)
Рч 3-ЖгТ.пл. 180-190°С (разложение) R3 4-CH3ЯМР (ВгО),& : 2,0-2,7 (2Н, мультиплет) 2,29 (ЗН, синглет), 2,9- 3,7 (4Н, мультиплет), 4,97 (1Н, триплет, Гц), 4,9-5,5 (2Н, мультиплет, Гц), 4,9-5,5 (2Н, мультиплет), 5,19 (1Н, дублет, Гц), 5,75 (1Н, дублет, Гц), 6,83 (1Н, синглет), 7,43 (1Н, дублет, Гц), 7,92 (1Н, дублет, Гц), 8,60 (IH, синглет)
R 3-NIi4Т.пл. 180-190°С R- 5-SCH5(разложение)
ЯМР (ВгО-СГ5СОг В), &: 2,1-2,7 (2Н, мультиплет), 2,56 (ЗН, синглет), 3,35 (1Н, дублет, Гц), 3,3-3,7 (2Н, мультиплет), 3,75 (Ш, дублет, Гц), 5,13 (Ш, триплет, Гц), 5,20 (1Н, дублет, Гц), 5,32 (1Н, дублет, Гц), 5,62 (Ш, дублет, Гц), 5,88 (1Н, дублет, Гц), 7,16 - (Ш, синглет), 7,45 (1Н, синглет), 7,96 (2Н, широкий синглет)
,Т.пл. 177-185°С (разложение) ЯМР (D20-CF3CO D), & : 2,1-2,9
(2Н, мультиплет), 3,38 (1Н, дублет, Гц), 3,4-3,7 (2Н, мультиплет), 3,80 (1Н, дублет, Гц), 5,16 (1Н, триплет, Гц), 5,25 (1Н, дублет, Гц), 5,36 (1Н, дублет, Гц), 5,70 (1Н, дублет, Гц), 5,92 (1Н, дублет, Гц), 7,20 (1Н, синглет), 7,90 (1Н, дублет, Гц), 8,2-8,4 (2Н, мультиплет)
,Т.пл. 185-200° С (разложение) R3 4-SCH3ЯМР (DaO+CD,CN),Ј : 2,3-2,8 (2Н,
мультиплет), 2,95 (ЗН, синглет). 3,4-3,8 (2Н, мультиплет), 3,35 (1Н, дублет, Гц), 3,83 (Ш, дублет, Гц), 5,18 (1Н, дублет, Гц), 5,22 (1Н, триплет, Гц), 5,25 (Ш, дублет, 1 15 Гц), 5,45 (1Н, дублет, Гц), 6,02 (Ш, дублет, Гц), 6,95 . (1Н, синглет), 7,68 (1Н, дублет, Гц), 8,28 (1Н, синглег), 8,28 ОН, дублет, 1 5 Гц)
Т
10R2 2-CHVТ.пл. 170-178°С R,5-NH.(разложение)
ЯМР (ВгО),& : 2,0-2,85 (2Н, муль- типлет), 2,61 (ЗН, синглет), 3,03.7(4Н, мультигшет), 5,03 (1Н, триплет, Гц), 5,15 (1Н, дублет, Гц), 5,25 (Ш, дублет, Гц), 5,45 (1Н, дублет, Гц), 5,84 (1Н, дублет, Гц), 6,93 (1Н, синглет), ,7 (2Н, мультиплет),
11R2 3-NH,Продукт постепенно начинает разла- R 5-NH2гаться при 175°С
HMP(DZ0+CD3CN)& : 2,1-2,6(2H, мультиплет), 3,02 (1Н, дублет, Гц), 3,47 (1Н, дублет, Гц), 3,1-3,5 (2Н, мультиплет), 4,81 (Ш, дублет, Гц), 4,88 (Ш, триплет, 1 7 Гц), 5,09 (Ш, дублет, Гц), 5,12 (Ш, дублет, Гц), 5,67 (Ш, дублет, Гц), 6,81 (Ш, синглет), 6,67 (Ш, триплет, 1 2 Гц), 7,40 (2Н, дублет, Гц)
12Ег 3-Мг,Т.пл. 160-170° С F.,5-C1(разложение)
ИК,ХмВцКС (см-1 ): 1770, 1690, 1610
ЯМР (ПгО+СВ,СМ),Ј : 2,10-2,60 (2Н, мультиплет), 3,20-3,50 (2Н, мультиплет), 3,08-3,75 (2Н, мультиплет), 4,90 (Ш, триплет, Гц), 4,80- 5,50 (2Н, мультиплет), 5,13 (1Н, дублет, Гц), 5,72 (1Н, дублет, Гц), 6,86 (1Н, синглет), 7,52-7,61 (Ш, мультиплет), 8,18-8,25 (2Ы, мультиплет)
13Ra 3-F,Т.пл. 175-190°С F Н(разложение)
ЯМР (DZ0),S: 2,0-2,6 (2Н, мультиплет), 3,2-3,8 (4Н, мультиплет), 4,93 (1Н, триплет, Гц), 5,17 (1Н, дублет, Гц), 5,28 (1Н, дублет, Гц), 5,57 (Ш, дублет, Гц), 5,73 (Ш, дублет, Гц), 6,89 (1Н, синглет), 7,8-9,0 (4Н, мультиплет)
14R 4--SCI13,ИК,(см- ): 1780
R3 RЯМР (D20) 81 : 2,0-2,7 (2Н, мупьтиплет), 2,49 (ЗН, синглет), 3,0-3,8 (4Н, мультиплет), 4,89 (1Н, триплет, 1 7 Гц), 5,00 (1Н, дублрг, Гц), 5,08 (1Н, дублет,Т -5 I ч),
ПНИ
5,43 (1Н, дублет,1 15 Гц), 5,64 (IH, дублет,Т 5 Гц), 6,88 (1Н, синглет), 7,47 (2Н, дублет, 1 7 Гц), 8,22 (2F, дублет, 7 Гц)
, ЯМР (Г 40),& : 2,0-2,8 (2F, мульти- РЗ Нплет), 2,60 (ЗН, синглет), 3,1-3,6
(2Н, мулътиплет), 3,15 (IF, дублет, 1 17 Гц), 3,62 (1Н, дублет, 17 Гц), 4,92 (1Н, триплет, 7 Гц), 5,21 (1Н, дублет, 5 Гц), 5,27 (1Н, дублет, Гц), 5,43 (1Н, дублет, 1 15 Гц), 5,76 (1Н, дублет, 5 Гц), 6,84 (1Н, синглет), 7,73 (2Н, дублет, 6 Гц), 8,60 (2Н, дублет, Гц).
16Rt 2-CHv ямр (ого),Б : 2,1-2,7 (2Н, мульти- R3 Нплет), 2,73 (ЗН, синглет), 3,1-3,6
(4Н, мультиплет), 4,90 (1Н, триплет, Гц), 5,11 ОН, дублет, 5 Гц), 5,17 (1Н, дублет, Гц), 5,42 (1Н, дублет, Гц), 5,69 ОН, дублет, Гц), 6,78 (1Н, синглет), 7,5-7,8 (2Н, мультиплет), 8,0-8,3 (IF, мультиплет) 8,52 (1Н, широкий дублет, Гц).
17R2 3-СН2, ЯМР (БгО)Д : 2,0-2,6 (2Н, мультй- R3 Нплет), 2,45 (ЗН, синглет), 3,0-3,7
(4Н, мулътиплет), 4,90 (1Н, триплет, Гц), 5,13 (1Н, дублет, Гц), 5,42 (1Н, дублет, Гц), 5,70 (1Н, дублет, Гц), 6,80 (1Н, синглет), 7,6-7,9 (1Н, мультиплет), 8,0-8,3 (IF, мультиплет), 8,4-8,7 (2Н, мультиплет).
18R4 3-СНгСН3 ЯМР (), 8 : 1,27 (ЗН, триплет, R. Гц), 2,1-2,6 (2Н, мультиплет),
2,83 (2Н, квартет, 7 Гц), 3,1- (4Н, мультиплет), 4,95 (1Н, триплет, Гц), 4,9-5,6 (2Н, мультиплет), 5,18 (1Н, дублет, Гц), 5,73 (Н, дублет, Гц), 6,82 (1Н, синглет), 7,79 (1Н, двойной дублет, ,5 Гц), 8,22 (1HJ дуб- лет, Гц), 8,59 (1Н, дублет, Гц), 8,63 (1Н, синглет).
19R,j 4-СНгСН3, ЯМР (D20)Ј:J,28 (ЗН, триплет, RJ Гц), 2,1-2,6 (2Н, мультиплет), 2,88 (2Н, квартет, Гц), 3,1-3,6 (4Н, мулътиплет), 4,95
(1Н, триплет, Гц), 4,9-5,6 (2Н, мультиплет), и 5,18 (1Н, дублет, Гц), 5,72 (1Н, дублет, Гц), 6,80 ОН, синглет), 7,70 (2F, дублет, ,5 Гц), 8,59 (2Н, дублет, Гц).
ZE:
20 Кг 2-8СН2СН3, R3 11
21
Н„ -4-NH- R3 H
22RЈ 3-С1
R3 H
23 Кг 3-ОСН},
R Н
ИК, )
MQ.CC ): 1780 690, 1610
ЯНР, (D20) S1 : 1,40 (ЗН, триплет, Гц), 2,1-2,6 (2Н, мулътиплет), 3,0-3,5 (6Н, мультиплет), 4,92 (1Н, дублет, Гц), 5,08 (1Н, дублет, Гц), 5,13 (1Н, триплет, 5 Ги), 5,54 (1Н, дублет, Гц), 5,70 (1Н, дублет,. Гц), 6,80 (1Н, синглет), 7,35-7,6 (1Н, мультиплет), 7,69 (1Н, дублет, Гц), 7,95- 8,2 (1Н, мультиплет), 8,50 (1Н, дублет, Гц) . ИК К ): 1 7 75, 1 690 1 610
ЯМР (DaO+CF3C02D) , 81 : 2,1-2,6 (2Н,мультиплет), 3,2-3,7 (4Н, мультиплет), 4,95 (IH, триплет, Гц), 5,0-5,6 (2Н, мультиплет), 5,15 ОН, дублет, Гц), 5,70 (1Н, дублет, Гц), 6,96 (1Н, синглет), 7,7-7,9 (2Н, мультиплет), 8,3-8,6 (2Н, мультиплет)
иМУ°Л(): 1775, 1690, 1610
WOIKC
ЯМР (), 8 : 2,0-2,6 (2Н, мультиплет), 3,1-3,5 (4Н, мультиплет), 4,95 (1Н, триплет, Гц), 5,14 ОН, дублет, Гц), 5,74 (1Н, дублет, Гц), 6,83 (1Н, син- лет), 7,8-8,1 (1Н, -мультиплет), 8:3-8,9 (IF, мультиплет), 8,7-8,9 (1Н, мультиплет), 9,04 (1Н, дублет, Гц )
ИК, ( 1775, J685, 1605
ЯМР (ВгО) S1 : 2,2-3,0 (2Н, мультиплет), 3,1-4,1 (4Н, мультиплет), 4,16 (ЗН, синглет), 5,17 (1Н, триплет, Гц), 5,40 (1Н, триплет, Гц), 5,42 (1Н, дублет, Гц), 5,70 (1Н, дублет, Гц), 5,95 (1Н, дублет, Гц), 7,01 (IH, синглет), 7,8-8,3 (2Н, Мультиплет), 8,5-8,7 (ЗН, мультиплет),8, (1Н, мультиплет).
Примечание: Соединение формулы I имеет (Z)-конфигурацию. (S) означает, что атом углерода имеет (З)-конфигу- рацию.
1542417
20 Продолжен ; - табл.1
MQ.CC
У°Л
WOIKC
Таблица 2 Испытуемые соединения формулы 1
N-jr-C-CONH
НТ
Испытуемые микроорганизмы:
Грамположительные бактерии
A: Staphylococcus aureus 209 Р
В: Enterococcus faecalis (S. f
Грамотрицательные бактерии.
С: Escherichia coli NIHI IC-2
D: Salmonella typhimurium
E: Proteus vulgaris IID-874
F: Proteus inconstans 6764
G: Serratia marcescens 7006
H: Pseudomonas aeruginosa 4098
Микроорганизм, продуцирующий л
I: Staphylococcus aureus 252 R
J: Proteus vulgaris GN 76/C-l
K: Proteus morganii 6501
Сф-сн 1 Яз
23
1542417
24 Таблица 3
Авторы
Даты
1990-02-07—Публикация
1987-06-15—Подача