Изобретение относится к новому химическому соединению 3-метил-6-[1-этил-2-a-(5-нитрофурфурилиден)]-гидразиноурацилу формулы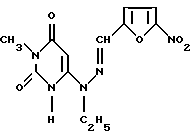
которое может найти применение в медицине.
Цель изобретения поиск в ряду производных 5-нитрофурфурола нового соединения, обладающего более высокой и избирательной антимикробной активностью и малой токсичностью.
П р и м е р 1. Синтез описываемого соединения.
Растворяют 1,84 г (0,01 моль) 3-метил-6-(1-этил)-гидразиноурацила в 25 мл этанола при нагревании и добавляют в течение 5 мин при перемешивании раствор 1,4 г (0,01 моль) 5-нитрофурфурола в 10 мл этанола. Через несколько минут начинает образовываться светло-коричневый осадок. Реакционную смесь кипятят 1 ч, затем перемешивают при комнатной температуре еще 2 ч. Осадок отфильтровывают, промывают небольшим количеством холодного спирта, затем эфиром. Выход 2,4 г (80%). После перекристаллизации из диметилформамида - желтые блестящие кристаллы; т.пл. 269 270oC (разложение).
Найдено, C 46,72; H 4,46.
C12H13N5O5.
Вычислено, C 46,91; H 4,26.
Масс-спектр: M+ 307 (71,4)
ПМР-спектр (CDCl3, δ, м. д.): 1,29 т (3Н, N-СH3); 3,33 c. (3H, N-CH3); 3,88 к. (2Н, -СН2-); 5,22 c. (1H, H5 пиримидинового цикла); 6,98 и 7,42 д.д. (2Н фуранового цикла); 7,58 с. (1Н, СН=); 8,9 с. (1Н, N-H).
П р и м е р 2. Биологическая активность описываемого соединения.
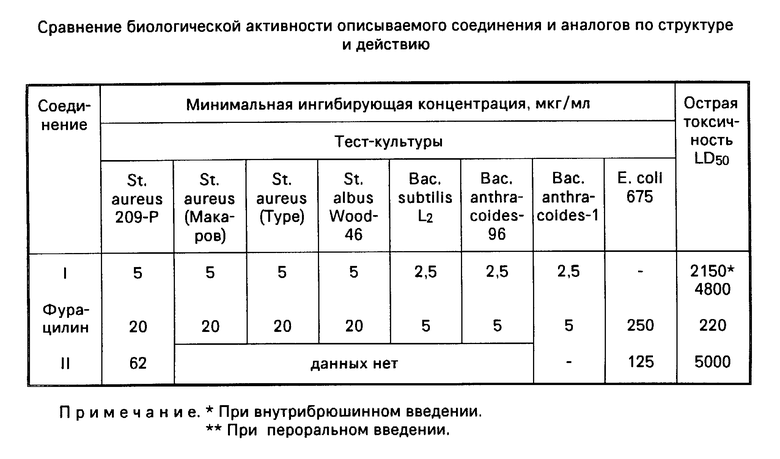
Для определения антимикробного действия соединениe I растворяют в диметилсульфоксиде, получая концентрацию основного раствора 6400 мкг/мл. Дополнительные растворы готовят в десятикратном разведении. Мерные количества основного или дополнительного растворов тщательно перемешивают с 20 мл стерильного расплавленного и охлажденного до 50oC питательного агара (ПА), затем выливают в стерильные чашки Петри. В питательном агаре создают концентрацию исследуемого вещества 320, 160, 80, 40, 20, 10, 5 и 2,5 мкг/мл. Чашки делят на сектора, которые засевают 100-миллионной взвесью суточных тест-культур. Контролем служат посевы тех же культур на ПА: 1) без исследуемого вещества, 2) с добавлением растворителя, 3) с добавлением раствора фурацилина в той же концентрации, что и исследуемое вещество. Все посевы инкубируют в течение суток при 37oC. Результаты сравнения биологической активности соединения I с фурацилином и со структурным аналогом бензиламидом N-(5-нитрофурфурилиден)-антраниловой кислоты (соединение II) приведены в таблице.
Острую токсичность соединения I определяют на белых мышах обоего пола массой 18 23 г по 36 животных в каждой серии экспериментов. LD50 при пероральном введении 4800 мг/кг, при внутрибрюшинном 2150 мг/кг.
Как видно из данных таблицы, описываемое соединение при низкой токсичности обладает более избирательным антимикробным действием, чем структурный аналог и превосходит по активности фурацилин в 2 4 раза.
Изобретение относится к гетероциклическим соединениям, в частности 3-метил-6-[1-этил-2-a-(5-нитрофурфурилиден)-гидразиноурацилу, который может найти применение в медицине. Цель - выявление соединений, обладающих более высокой и избирательной антимикробной активностью и малой токсичностью. Получение ведут реакцией 3-метил-6-(1-этил)-гидразиноурацила с 5-нитрофурфурола в среде этанола. Выход 80%, т.пл. 269 - 270oC; брутто-фор-ла С12N13N5O5; LD50 при пероральном введении 4800 мг/кг, при внутрибрюшинном 2150 мг/кг. Новое соединение превосходит по активности фурацилин в 2 - 4 раза. 1 табл.
3-Метил-6-[1-этил-2-a-(5-нитрофурфурилиден)]-гидразиноурацил формулы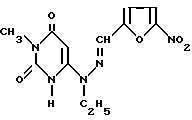
обладающий действием против стафилококков и бацилл.
| Машковский М.Д | |||
| Лекарственные средства | |||
| М.: Медицина, 1985, т | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| АВТОМАТ ДЛЯ ПУСКА В ХОД ПОРШНЕВОЙ МАШИНЫ | 1920 |
|
SU299A1 |
| Бензиламид 5-нитрофурфурилиденантраниловой кислоты, проявляющий антимикробную активность | 1982 |
|
SU1107537A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1996-10-27—Публикация
1988-07-29—Подача