Изобретение относится к химическому анализу и может быть использовано для определения железа в промышленных водах, содержащих примеси металлов, и чистых реактивах, в которых железо находится в качестве примеси
Цель изобретения - расширение интервала определяемых концентраций при повышении селективности и точности определения
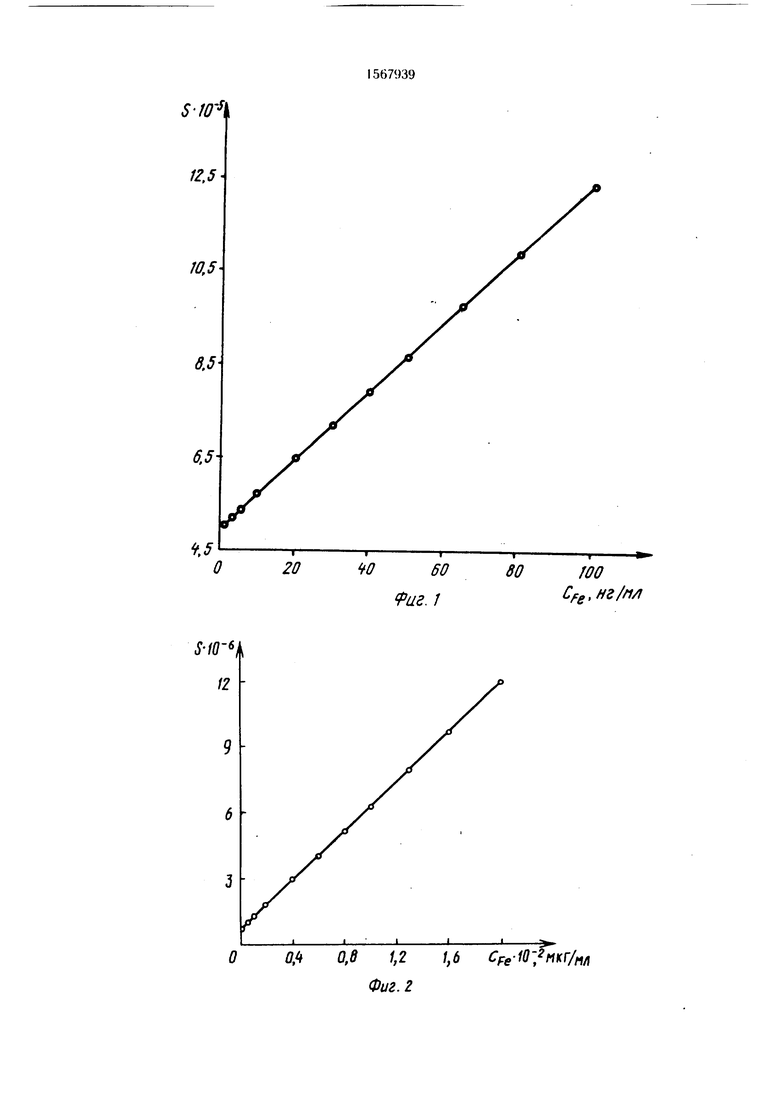
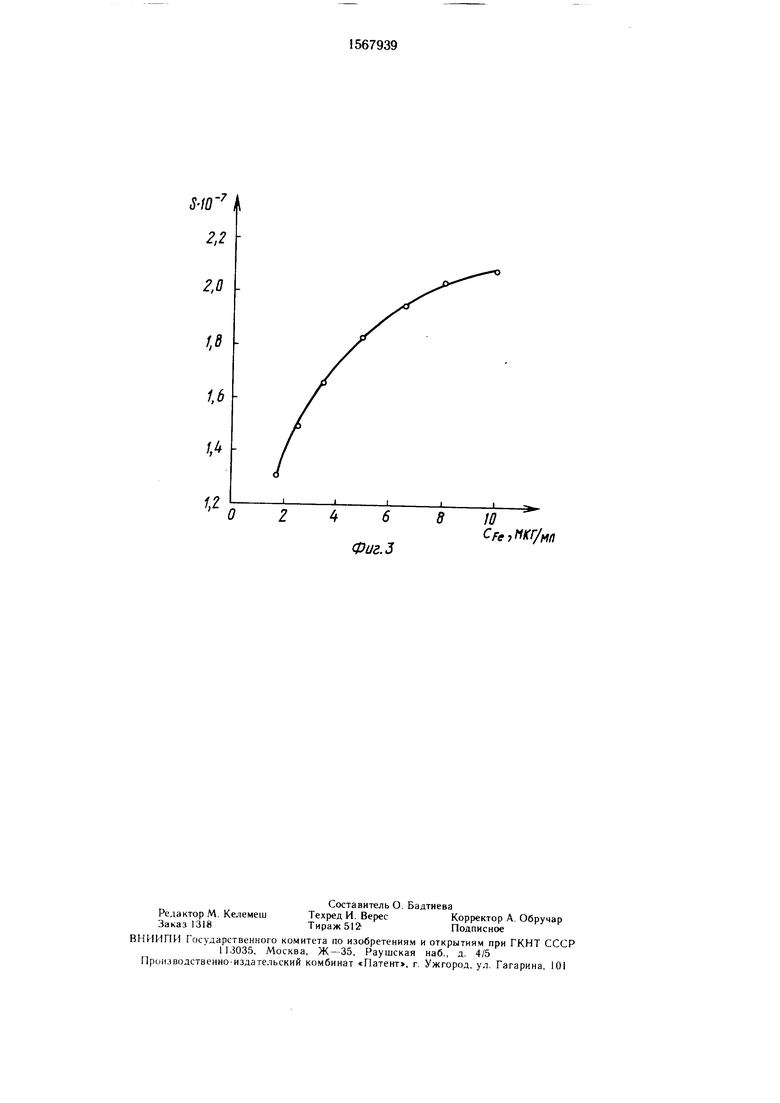
На фиг. 1 изображен рабочий калибровочный график для определения железа в пределах его содержаний 2,5-100 нг в 1 мл раствора, на фиг. 2 - то же, в пределах его содержаний 100-1700нгв 1 мл раствора; на фиг. 3 - то же, в пределах его содержаний 1700-10000 нг в 1 мл раствора.
Допустимые содержания примесей в анализируемом растворе, не мешающие опре делению железа, приведены в табл. 1.
СП
0
со со со
В табл. 2 приведены максимальные значения относигольпых ошибок определения железа для различных его концентрационных интервалов.
Таблица 2
Питер нал содержаний железа, кг/мл
2,0 1,6 1,4 1,2 0,9 0,7 О 8 1,2
Концентрации нитрата 9-циано- 10-метил акридиння, перекиси водорода, о-фенантроли- иа и рН ацетатного буфера выбраны оптимальными для хемилю.минесценции, т. е. для получения наибольшей разности между выходом света в смеси, содержащей железо и бет него, что обуславливает чувствительность и точность определения железа. Выбор оптимальных концентраций реагентов: (3,0 8,0)-10 моль/л - для нитрата 9-аиано- 10-мегнлакридиния; 1,3-1,7 моль/ /л -- для перекиси водорода; (4 - 6) 1C) 4 моль/лдля о-фенантролина и
оптнмчдыюго рН (5.0-5,3) ацетатного буфера, сделан на основании результатов эксперимента. Установлено, что независимо от соотношения содержаний других компонентов оптимальные концентрации нитрата 9-цнано-10-метилакридиния, перекиси волоро да. о-фенантролина и оптимального рН ацетатного буфера соответствуют указанным.
Количества реагентов, а также значения рН ацетатного буфера, отличающиеся ог оптимальных, дают более низкое значение разности светосумм за 60 с. что отрицательно отражается на чувствительности и точности определений, так как уменьшает значение аналитического сигнала.
Выбор оптимальной концентрации ацетатного буфера сделан на основании того, что концентрация ацетатного буфера 0,17 моль/л позволяет обеспечить необходимую буфер ную емкость. При концентрациях ацетатного буфера меньших, чем 0,17 моль/л, вследствие низкой буферной емкости, рН конечной смеси не соответствует рН буфера; количества ацетатного буфера, превышающие 0,17 моль/л, заметно тушат свечение. Замена ацетатного буфера на универсальный фталатный или фосфатный приводит к уменьшению разности светосумм в присутствии железа и без него. Так. при при- мененни фосфатного буфера разность свече
ния уменьшалась приблизительно в 3 раза, 1то приводит к снижению чувствительности и точности.
В оптимальных условиях значение свето- суммы за (Ю с достигает максимального значения при содержании железа 10 мкг/мл, затем уменьшается при дальнейшем увеличении содержания железа.
Линейная зависимость светосуммы от содержания железа наблюдается в интервале его содержаний от 2,5 нг/мл до 1,7 мкг/мл. Предел обнаружения рассчитан по 3 т-крите.- пию и составляет 2,5 иг железа в 1 мл раствора.
Пример. Анализируемый раствор, содержащий железо в пределах от 2,5 до 100 нг/мл, смешивают с нитратом 9-циано- - 10-метилакридиния и вносят в кювету хе- мнлюминесцентного фотометра. Затем в кю- в(му прибавляют смесь перекиси водорода, ацетатного буфера с рН 5,0 и о-фенантро0 липа. Концентрации реагентов в расчете на конечный объем смеси должны составлять: для нитрата 9-циано-10-метилакрндиния - 3,0-10 моль/л, для перекиси водорода - 1,3 моль/л, для о фенантролина 4,0- 10 моль/л и для ацетатного буфера с рН 5,0 0,17 моль/л.
С помощью хемилюминесцентного фотометра измеряют сумму выделившегося света за 60 с и ее значение в дальнейшем ис- Q пользуют для определения концентрации железа с помощью калибровочного графика (фи|. 1). Относительная ошибка определения не превышает 1,7%.
Использование предлагаемого способа ;., дает возможность определения железа в широком концентрационном интервале от 2,5 нг/мл до 10 мкг/мл и обеспечивает высокую точность и селективность определения
5
40
Формула изобретения
Способ определения железа, включающий взаимодействие железа с органическим соединением в присутствии перекиси водорода и регистрацию хемилюминесиенгного свечения образующейся смеси, по светосум- ме которого определяют количество железа, отличающийся тем, что, с целью расширения интервала определяемых концентраций при увеличении селективности и точности о пределения в анализируемый раствор, содержащий 2,5 нг/мл -- 10 мкг/мл железа вводят (3,0- 8,0) моль/л нитрата 9- -циано 10-метилакридиния, добавляют смесь, состоящую из 1,3-1,7 моль/л перекиси водорода, (4,0- -6,0) 10 4 моль/л о-фенантролипа и 0,17 моль/л ацетатного буфера с рП 5,0 -5,3, и регистрируют в течение не менее 60 с светосумму хемилюминесцентного свечения
г гпф vu/J ui-Ol-3J3 9/ Z / 90 0 0
t I|--J-i-ry-T

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ проведения иммуноферментного анализа | 1989 |
|
SU1654750A1 |
| Способ определения железа в растворе | 1989 |
|
SU1727058A1 |
| Способ определения аскорбиновой кислоты | 1985 |
|
SU1352361A1 |
| Способ хемилюминесцентного опре-дЕлЕНия СВиНцА | 1978 |
|
SU812719A1 |
| СПОСОБ ДИАГНОСТИКИ ИНФИЦИРОВАННОГО ПАНКРЕОНЕКРОЗА | 2006 |
|
RU2319150C1 |
| Способ количественного определения катионных поверхностно-активных веществ | 1990 |
|
SU1755134A1 |
| Способ кинетического определения вольфрама | 1978 |
|
SU691751A1 |
| СПОСОБ КИНЕТИЧЕСКОГО ОПРЕДЕЛЕНИЯ КОБАЛЬТА | 1998 |
|
RU2132554C1 |
| Способ определения железа | 1989 |
|
SU1732224A1 |
| СПОСОБ ДИАГНОСТИКИ ДИАБЕТИЧЕСКОЙ РЕТИНОПАТИИ | 2005 |
|
RU2304786C2 |
Изобретение относится к химическому анализу и может быть использовано для определения железа в промышленных водах, содержащих примеси металлов, и чистых реактивах, в которых железо находится в качестве примеси. Целью изобретения является расширение интервала определяемых концентраций при повышении селективности и точности определения. Анализируемый раствор, содержащий железо, смешивают с нитратом 9-циано-10-метилакридиния. Добавляют смесь перекиси водорода, о-фенантролина и ацетатного буфера с PH 5,0-5,3, взятых в оптимальных соотношениях, и при получении светящейся смеси измеряют сумму хемилюмиесцентного свечения за 60 с. 2 табл., 3 ил.
I/U/2H 9J 001
л
9-W f
S b
S Zl
JH-S
6Cf)Z9S I
4 6 Фиг.З
8
JO
CFeiHKr/МП
| Долманова И | |||
| Ф , Рычкова В | |||
| И | |||
| и Пешкова В | |||
| М | |||
| Определение микроколичесгв железа с использованием каталитической реакции окисления n-фенетидина периодатом калия | |||
| - ЖАХ, т | |||
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Прибор для видения предметов на расстоянии при помощи электричества | 1924 |
|
SU1763A1 |
| Калиниченко И Е и Грищенко И М Активирование солей железа диэтилентриами- ном при окислении люминола перекисью водорода | |||
| - Украинский химический журнал т | |||
| Коридорная многокамерная вагонеточная углевыжигательная печь | 1921 |
|
SU36A1 |
| ШАХТНАЯ ТОПКА ДЛЯ МНОГОЗОЛЬНОГО ТОРФА | 1922 |
|
SU610A1 |
Авторы
Даты
1990-05-30—Публикация
1988-07-26—Подача