Изобретение относится к органической химии, в частности к новым химическим соединениям общей формулы I
где а) R Cl; б) R Br; в) 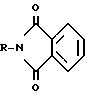
Предлагаемые соединения могут найти применение в качестве полупродуктов для синтеза γ-(2,4-ди-трет-амилфенокси)пропиламид-1-оксинафтойной -2-кислоты формулы II
используемой в качестве голубой защищаемой компоненты в цветной фотографии.
Цель изобретения изыскание новых полупродуктов, которые позволяют получить голубую защищаемую компоненту II с более высоким выходом и более простым способом.
Получение γ-(2,4-ди-трет-амилфенокси)пропилхлорида (Ia).
Пример 1. Раствор изопропилата натрия, приготовленный из 11,5 г (0,5 моль) натрия и 200 мл изопропанола, смешивают с 117 г (0,5 моль) 2,4-ди - трет-амилфенола. Полученный таким путем фенолят прибавляют по каплям к нагретому до кипения и энергично перемешиваемому раствору 113 г (1 моль) 1,3-дихлорпропана в 50 мл изопропанола. Смесь кипятят 2 3 ч, затем охлаждают и отфильтровывают выпавший в осадок хлористый натрий (25 27 г). Избыток спирта и дихлорпропана отгоняют в вакууме водоструйного насоса, а остаток фракционируют в глубоком вакууме, собирая следующие фракции.
2,4-Ди-трет-амилфенол, т. кип. 138 140oC/4 5 мм рт. ст. Возврат 28 30 г, который может быть повторно использован для получения целевого соединения.
g-(2,4-Ди-трет-амилфенокси)пропилхлорид, т. кип. 160 163oC/4 5 мм рт. ст. Выход 92 96 г ( 80 84% в расчете на вступивший в реакцию фенол).
Найдено, C 73,2; H 10,0; Cl 11,3.
C19H31OCl
Вычислено, C 73,4; H 10,0; Cl 11,4.
ПМР спектр (в CCl4, стандарт ГМДС, 60 мГц): фенольный фрагмент: 7,05 (1H, c, 3-H), 6,65 (1H, d, 5-H), 6,90 (1H, d, 6-H) м.д. I 8 Гц; трет-амильный фрагмент: 1,25 (3H, c, CH3), 1,15 (3H, c, CH3), 1,68 (2H, кв, -CH2-), 0,59 (3H, т, CH3) м.д. пропиленовая цепочка: 3,28 (2H, т, -CH2Cl), 3,50 (2H, т, -OCH2), 2,25 1,89 (2H, м, -CH2-) м.д.
Пример 2. Получают аналогично при тех же загрузках исходных веществ, но вместо изопропанола используют этиловый, пропиловый или бутиловый спирт. Выход составляют 89,7 93,7 г (78 82%).
Пример 3. Получают по аналогии с вышеописанным, используя в качестве растворителя метанол. Выходы продукта реакции заметно снижаются и составляют 75 80 г (65 70%).
Пример 4. Раствор щелочи, приготовленный растворением при нагревании 8,2 г (0,2 моль) 98% -ного едкого натра или 13,2 г (0,2 моль) 85%-ного едкого кали в 200 мл одного из спиртов (CH3OH, C2H5OH, н- или изо- C3H7OH), смешивают с 46,8 г (0,2 моль) 2,4-ди-трет-амилфенола и кипятят в течение 1 ч. После охлаждения его прибавляют по каплям к кипящему и интенсивно перемешиваемому раствору 68 г (0,6 моль) 1,3-дихлорпропана в 40 - 50 мл соответствующего спирта. Смесь кипятят в течение 6 8 ч и выделяют продукт реакции, как описано в примере 1. Выходы составляют 57,5 63 г (50 - 55%).
Пример 5. 4,1 г (0,1 моль) 98%-ного NaOH кипятят в 80 мл н-бутанола и 10 мл толуола в колбе с насадкой Дина-Старка до тех пор, пока не выделится 1,8 мл воды. Затем полученный раствор смешивают с 23,4 г (0,1 моль) 2,4-ди-трет-амилфенола, кипятят 1,5 ч и после охлаждения прибавляют по каплям к кипящему и перемешиваемому раствору 34 г (0,3 моль) 1,3-дихлорпропана в 40 мл н-бутанола. Смесь кипятят 8 ч и выделяют продукт реакции, как в примере 1. Выход 18,6 г (60%).
Пример 6. К раствору 234 г (1 моль) 2,4-ди-трет-амилфенола в 0,5 л толуола, нагретому до 100 110oC (в масляной бане), прибавляют при энергичном перемешивании 50%-ный раствор едкого натра или едкого кали, приготовленный из 41 г (1 моль) 98%-ного NaOH в 40 мл воды или из 65 г (1 моль) 85%-ного КОН в 56 мл воды. Затем температуру в бане поднимают до 135 - 140oC и отгоняют воду с помощью насадки Дина-Старка (55 и 65 мл соответственно). При этом наблюдается выпадение в осадок фенолята. Для полного его растворения к толуольному раствору после охлаждения прибавляют 150 мл одного из спиртов этанола, н- или изопропанола. Полученный таким путем 2,4-ди-трет-амилфенолят натрия (калия) вводят в реакцию с 226 г (2 моль) 1,3-дихлорпропана в условиях, описанных в примере 1. Выход 200 210 г (65 - 68% в расчете на взятый в реакцию фенол или 80 82% с учетом его возврата).
Получение g-(2,4-ди-трет-амилфенокси)пропилбромид (Iб).
Пример 7. Получают по примеру 1 из 46,8 г (0,2 моль) 2,4-ди-трет-амилфенола, 4,6 г (0,2 моль) натрия и 80,8 г (0,4 моль) 1,3-дибромпропана в 100 мл изопропанола. Выход составляет 56 68 г (80 - 82%), т. кип. 148 150/5 мм. рт. ст.
Найдено, C 64,1; H 9,1; Br 22,3.
C19H31OBr
Вычислено, C 64,2; H 8,8; Br 22,5.
ПМР-спектр (в CCl4, стандарт ГМДС, 60 мГц): фенольный фрагмент: 7,08 (1H, c, 3-H), 6,63 (1H, д, 5-H), 6,92 (1H, д, 6-H) м.д. I 8 Гц; трет-амильный фрагмент: 1,26 (3H, c, CH3), 1,16 (3H, c, CH3), 1,64 (2H, кв, -CH2-), 0,58 (3H, т, CH3) м.д. пропиленовая цепочка: 3,48 (2H, т, -CH2Br), 3,98 (2H, т, -OCH2), 2,27 1,91 (2H, м, -CH2-) м.д.
Пример 8. Получают аналогично при тех же загрузках исходных соединений с использованием этилового, пропилового или бутилового спирта. Выходы колеблются в пределах 52,5 56 г (75 80%).
Пример 9. Получают аналогично описанному в примере 4 при тех же загрузках 2,4-ди-трет-амилфенола, КОН (или NaOH), соответствующего спирта и 121 г (0,6 моль) 1,3-дибромпропана. Выходы продукта реакции не превышают 33 35 г (48 50%).
Пример 10. Получают, как описано в примере 6, используя вместо 1,3-дихлорпропана 404 г (2 моль) 1,3-дибромпропана. Выход 223 231 г (63 - 65% в расчете на взятый в реакцию фенол и 78 80% с учетом его возврата).
Получение N-g-(2,4-ди-трет-амилфенокси)пропилфталимида (Iв).
Пример 11. Смесь 155,3 г (0,5 моль) g-(2,4-ди-трет-амилфенокси)пропилхлорида (Iа) и 139 г (0,75 моль) фталимида калия нагревают при кипении и перемешивают в 0,8 л диметиформамида (температура масляной бани 160 170oC) в течение 6 ч. Затем отгоняют почти досуха растворитель в вакууме водоструйного насоса, остаток охлаждают и смешивают с 150 200 мл холодной воды. Маслообразный продукт отделяют, растворяют в 0,5 л хлороформа и сушат хлористым кальцием. После отгонки растворителя получают 189,5 192,5 г (90 91,5% ) густого масла, которое при охлаждении примерно до 5oC кристаллизуется, т. пл. 20 22oC.
Найдено C 76,8; H 8,2; N 3,2.
C27H35NO3
Вычислено, C 76,9; H 8,4; H 3,3.
В ИК-спектре этого соединения (в вазелиновом масле) имеются интенсивные полосы поглощения в области 1710, 1715, 1770 см-1, соответствующие валентным колебаниям C O-группы.
Пример 12. Получают по аналогии с вышеописанным из 177,5 г (0,5 моль) g-(2,4-ди-трет-амилфенокси)пропилбромида (Iб) и 139 г (0,75 моль) фталимида калия. Выход 191,5 193,6 г (91 92%).
Пример 13. Получают по аналогии с примером 12 при тех же загрузках исходных веществ, увеличив время проведения реакции до 8 ч. Выход продукта 193,6 195,6 (92 93%).
Пример 14. Получают, как описано в примере 12, взяв эквивалентное количество фталимида калия. Выход фталимида (Iв) снижается до 175 г (83%).
Перед синтезом компоненты II фталимид Iв превращают в g-(2,4-ди-трет-амилфенокси)пропиламин.
Пример 15. Смесь 42,1 г (0,1 моль) N-g-(2,4-ди-трет-амилфенокси)пропилфталамиди (Iв) и 11 мл (0,21 моль) 98%-ного гидразингидрата в 300 мл этанола нагревают при кипении в течение 1,5 2 ч. Выпавший белоснежный творожистый осадок фталилгидразида отфильтровывают и промывают примерно 50 мл этанола. Из фильтрата отгоняют растворитель, а остаток перегоняют в вакууме, собирая фракцию, кипящую при 142 145oC/3 мм рт. ст. Выход 23,3 24,7 г (80 85%).
Получение g-(2,4-ди-трет-амилфенокси)пропиламида 1-оксинафтойной-2-кислоты (компонента II).
Пример 16. Смесь 30,0 г (0,103 моль) g-(2,4-ди-трет-амилфенокси)пропиламида и 26,4 г (0,1 моль) нафтосалола сплавляют в течение 1,5 ч при 160 165oC (в масляной бане). Затем отгоняют в вакууме водоструйного насоса выделившийся фенол (около 7,8 8 г), а остаток выливают в 100 мл охлажденного примерно до 10oC и перемешиваемого изопропанола. Выпадает светло-розовый осадок, количество которого заметно увеличивается при стоянии. Через 5 ч осадок отфильтровывают, хорошо отжимают и промывают охлажденным изопропанолом. Выход 40 41,5 г (87 - 90%). После перекристаллизации из н-гексана т. пл. 91 92oC (белоснежные призмы).
Таким образом, полученные новые соединения Iа Iв позволяют получить голубую защищаемую компоненту II с более высоким выходом (50 60% в расчете на исходный 2,4-ди-трет-амилфенол вместо 25 27% по известному способу) при исключении процесса гидрирования под давлением водорода на пирофорном катализаторе.
| название | год | авторы | номер документа |
|---|---|---|---|
| α ПРОИЗВОДНЫЕ δ -[2,4-ДИ-(ТРЕТ-АМИЛ)ФЕНОКСИ]БУТАНА В КАЧЕСТВЕ ПОЛУПРОДУКТОВ ДЛЯ ПОЛУЧЕНИЯ ГОЛУБЫХ ЗАЩИЩЕННЫХ КОМПОНЕНТОВ ДЛЯ ЦВЕТНОЙ ФОТОГРАФИИ | 1984 |
|
SU1205508A1 |
| Трет-бутилзамещённые трифенодиоксазины, обладающие люминесцентными свойствами, и способ их получения | 2019 |
|
RU2708625C1 |
| 13-Е-(2,4-ДИОКСО-1,2,3,4-ТЕТРАГИДРОПИРИМИДИН-5-ИЛ) ЭВДЕСМАНОЛИДЫ, ОБЛАДАЮЩИЕ ПРОТИВОЯЗВЕННОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2536870C1 |
| Способ получения м-(2,4-ди-(трет-амилфенокси)-ацетиламинобензойной кислоты | 1989 |
|
SU1694575A1 |
| Способ получения 2-хлор-5-[ @ -(2 @ ,4 @ -ди-трет-амилфенокси)-бутироиламино]-анилида @ -хлорпивалоилуксусной кислоты | 1988 |
|
SU1574591A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО БЕНЗО[b][1,4]ДИАЗЕПИН-2,4-ДИОНА | 2010 |
|
RU2553676C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3-{2-/4-(6-ФТОРБЕНЗО [D] ИЗОКСАЗОЛ-3-ИЛ)ПИПЕРИДИН-1-ИЛ /ЭТИЛ}-2-МЕТИЛ-6,7,8,9-ТЕТРАГИДРО-4H-ПИРИДО /1,2-А/ ПИРИМИДИН-4-ОНА И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ЕГО ПОЛУЧЕНИЯ | 1995 |
|
RU2123004C1 |
| ПРОИЗВОДНЫЕ ПИРИДОКСИНА С НЕЛИНЕЙНЫМИ ОПТИЧЕСКИМИ СВОЙСТВАМИ | 2012 |
|
RU2501801C1 |
| 2,4-Диарил-6-алкил-1,3,5-триазины и способ их получения | 2023 |
|
RU2812149C1 |
| ПРОИЗВОДНЫЕ КАРБАЗОЛОНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2119914C1 |
Изобретение касается тризамещенных бензолов, в частности соединений общей ф-лы 2,4-трет-C5H11-C6H3-O-(CH2)3-R, где R равно a) Cl, б) Br или в) фталимидная группа, - полупродуктов для синтеза голубой защищаемой компоненты - g - (2,4-ди-трет-амилфенокси)пропиламид-1-оксинафтойной-2-кислоты для цветной фотографии. Цель - создание более эффективных полупродуктов для указанного назначения. Синтез ведут конденсацией 2,4-ди-трет-амилфенола с 1,3-дихлор- или 1,3-дибромпропаном в присутствии щелочных агентов при 80 - 120oC в спиртовой или спиртотолуольной среде. Выход, %; брутто-ф-ла: а) 84; C19H31ClO; б) 82; Cl9H31OBr. Затем при нагревании соединения а или б с фталимидом калия в диметилформамиде при 160 - 170oC получают соединение в с выходом 93% и брутто - ф-лой C27H35NO3. При использовании соединений а-в в синтезе компоненты для цветной фотографии получают больший выход целевого продукта (50 - 55% против 25 - 27%) с исключением гидрирования под давлением с пирофорным катализатором.
α--Производные γ-(2,4-ди-трет-амилфенокси)-пропана общей формулы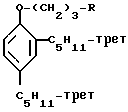
где а) R Cl;
б)R Br;
в) 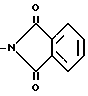
в качестве полупродуктов для получения γ-(2,4-ди-трет-амилфенокси)-пропиламид-1-оксинафтойной-2-кислоты.
| СПОСОБ ПОЛУЧЕНИЯ КОНСЕРВОВ "СЕЛЬДЬ В ВИННОМ СОУСЕ" | 2011 |
|
RU2474293C1 |
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Автоматическое или полуавтоматическое телефонное устройство | 1925 |
|
SU1949A1 |
Авторы
Даты
1997-02-27—Публикация
1987-12-23—Подача