Изобретение относится к способу получения замещенных №-бензоил-К - тиенилмочевины, которые могут быть использованы в сельском хозяйстве для борьбы с насекомыми-вредителями.
Целью изобретения является разработка способа получения новых замещенных Н-бензоил- -тиенилмочевины, которые обладают более высокой активностью, чем известный пестицид дифлюдензурон-г
N- |(4-хлорфенил)аминоЗкарбонил}-: 2,6- дифторбензамид.
Пример 1. Получение М-2,6-ди- фторбензоил-N 5-(4-хлорфенил)-4-ме- тил-2-тиенил J-мочевины.
К раствору хлоргидрата 2-амино-4- метил-5-(5-хлорфенил)-тйофена (0,45 г 1,73 ммоль) в 4 мл диметилформамида и 4 мл хлористого метилена добавляют 2,6-дифторбензоилизоцианат (0,32 г,
ы
1s73 ммоль), затем триэтиламин (0,23 г 0,3 мл, 2,25 ммоль). Смесь перемешивают в течение ночи пои комнатной температуре, после чего добавляют воду и удаляют растворитель. Остаток отфильтровывают и твердый остаток промывают 50%-ной смесью гексан/хлористый метилен, чтобы получить на-званный Bj iiiie продукт реакции (табл„ 1, соедине- ние 1) .
П р и м е р 2. Получение N-2s6-flH- фторбензоил-N 5-(4 трифторметокси- фенил)-4-метил-2-тиенил -мочевины„
К раствору трифторуксуснокислой соли 2-амино-4-метил-5-(4-трифторме токсифенил)-тиофена (1S88 ммоль) в 30 мл хлористого метилена добавляют при охлаждении триэтиламин
взросльх насекомых (в общем случае в течение 6 дней). Изучали ЭД э т.е дозу, при которой погибает 50% насекомых (например; гибель личинок, гибель куколок, неполное созревание взрослого насекомого).
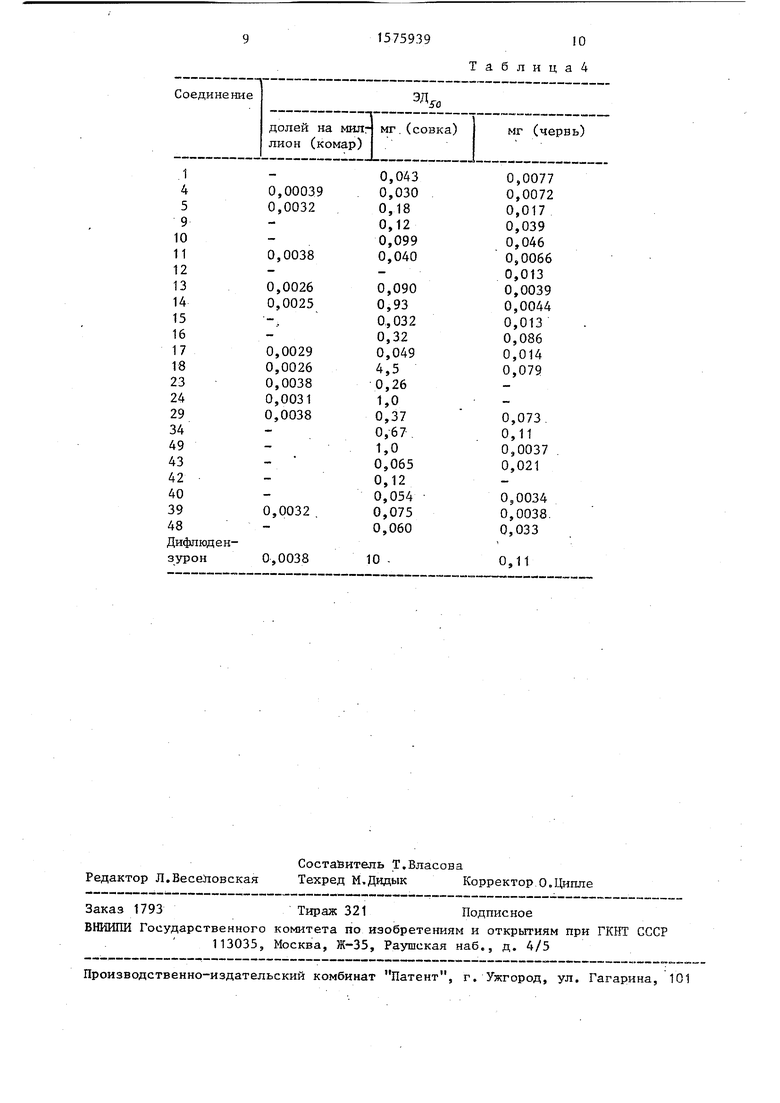
РезультатЕ 1 для нескольких выбранных насекомых приведены в табл.4.
Пример 6 Личинки совки Heliothis virescens в третьей возрастной стадии обрабатывали местным способом в области дорсального брюшка с использованием 1 и л соединения при испытываемой концентрации„ Затем личинки помещали на искусственную диету в отдельные ячейки пластиковой сеткиа содержащейся в накрытом контейнере (личинки помещают в отдельны

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных фенилмочевины | 1987 |
|
SU1491333A3 |
| Способ получения ароматических соединений | 1985 |
|
SU1402252A3 |
| N-АЦИЛИРОВАННОЕ СОЕДИНЕНИЕ АРИЛПИРРОЛА, СПОСОБ БОРЬБЫ С НАСЕКОМЫМИ, СПОСОБ ПОЛУЧЕНИЯ N-АЦИЛИРОВАННЫХ СОЕДИНЕНИЙ АРИЛПИРРОЛА | 1991 |
|
RU2099326C1 |
| Способ борьбы с вредными насекомыми и клещами | 1988 |
|
SU1681721A3 |
| Способ получения производных дифторциклопропана | 1986 |
|
SU1500152A3 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕНЕТИЧЕСКИ МОДИФИЦИРОВАННОГО БАКУЛОВИРУСА, ШТАММ ВИРУСА ЯДЕРНОГО ПОЛИЭДРОЗА, СПОСОБ БОРЬБЫ С НАСЕКОМЫМИ, ИНСЕКТИЦИДНАЯ КОМПОЗИЦИЯ | 1991 |
|
RU2099420C1 |
| Способ получения азотсодержащих гетероциклических соединений | 1986 |
|
SU1456010A3 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИРРОЛА | 1993 |
|
RU2109012C1 |
| (24R)-3 @ -Бром-24-метил-5 @ -холеста-7,22-диен-6-он, обладающий инсектицидной активностью | 1986 |
|
SU1351072A1 |
| Средство для борьбы с насекомыми | 1976 |
|
SU609454A3 |
Изобретение касается сероорганических веществ, в частности способа получения замещенных N-бензоил-NЪ-тиенилмочевины L-C(O)NH-C(A)-NH-M, где A=0*98 или S*98
L=-C=CX1-CH=CH-CX3=CX2
каждый из X1, X2 и X3 (независимо)-H или галоген
M-группа формулы -C=CH+CR1=CR2-S, каждый из R1 и R2 (независимо)-H, галоген, C1-C8-алкил (может быть замещен галогеном) или группа -(CH2)N-C6H3YZ
R3-H, галоген или -C(O)OR
R-H или C1C2-алкил
N=0 или 1
Y-H или галоген
Z-галоген или замещенные галогеном C1-C8-алкил или C1-C8-алкокси, которые могут быть использованы в сельском хозяйстве для борьбы с насекомыми-вредителями. Цель - создание новых более активных соединений указанного класса. Синтез ведут реакцией бензоилизоцианата или изоциоцианата формулы L-C(O)-N=C=A, где L и A указаны выше, с аминотиофеном формулы H2N-M, где M указано выше. Новые соединения вызывают гибель личинок или замедление роста, или кутикулярные отклонения у комаров, совок и походных червей на свекле в дозе ЭД50=0,00039-0,0038 долей на 1 млн (для комаров) или 0,03-4,5 мг/насекомое (для совок), или 0,0034-0,11 мг/ насекомое (для червей) против соответственно 0,0038 долей на 1 млн или 10 мг/насекомое, или 0,11 мг/ насекомое для дифлюдензурона. 4 табл.
(33,75 ммоль), затем 25 6-дифторбе 3оил 20 ячейки для предотвращения каннибализизоцианат (1,88 ммоль)„ Смесь обрабатывают, как в примере 1, и получают названное выше соединение (табл.1., соединение 39).
ПримерЗ. Следуя методикам примера 1, каждое из целевых соединений 2-22, 34-38, 40-43 и 48-49 (табл. 1) и 23-29 (табл. 2) получают из соответствующего тиофена и бензоил- изоцианата или интермедиатов изотио- цианата.
П р и м е р 4. 3-Амино-5(4-хлср- , фенил)-тиофен подвергают взаимодействию с 2,6-дифторбензоилизоцианатом и 2-хлорбезоилизоцианатомг следуя методике примера 1, чтобы получить соответственно
Ы-2,6-дифторбензоил-Ы - 5-(4-хлор фенил)-3-тиенил -мочевину (табл„ 3, соединение 30) и М:-2-хлорбензоил-М 5-(4-хлорфенил)-3-тиенил мочевину (табл.3, соедине ние 31),
Аналогично получают целевые соединения, представленные в табл, 3S из соответствующего тиофена и бензоил™ изоцианата или интермедиатов изотио- цианата.
ПримерЗ. 50 мкм соединения при испытываемой концентрации перемешивали в 50 мл водопроводной воды Е пластиковых высоких стаканах (3 стакана для каждой концентрации). Затем десять личинок комара Aedes aegypti в четвертой возрастной стадии помешали в каждый стакан. В качестве источника корма добавляли несколько капель суспензии порошка печени. Стаканы накрывали и личинкам давали возможность развиваться при 28 С до появления
35
55
ма) и выдерживали при 27°С в течение срока от второй линьки до пятой возрастной стадии (в общем случае 8 дней). Изучали , т,.е. дозуэ при которой погибает 50% насекомых (напримерs гибель личинок, замедление ростаs кутикулярные отклонения).
Результаты для выбранных соединений приведены в табл, 4.
Пример 7, Личинки походных червей на четвертой возрастной стадии (менее чем через 24 ч после линьки) обрабатывали местным способом в области дорсального брюшка в дозе 1ил соединения при испытываемой концентрации о Затем личинки помещали в накрытый контейнер на искусственную диету и выдерживали при 27°С от двух линек до окукливания (в общем случае 10 дней) о Проводили исследование ЭД т„е, дозы5 при которой погибает 50% насекомых (например, гибель личинок, замедление роста кутикулярные отклонения) .
Результаты для выбранных соедине™ ний приведены в табл, 4.
Как показывают результаты5 новые соединения формулы I обладают более высокой активностью,; чем известный пестицид., противs по крайней мере9 одного из трех известных насекомых, Формула изобретения
Способ получения замещенных N-бен тиенилмочевины общей формулы
Вз ,Ri
Xj0
А
О С-ИН-C- NH
А -&-
X.,
ячейки для предотвращения каннибализ5
5
ма) и выдерживали при 27°С в течение срока от второй линьки до пятой возрастной стадии (в общем случае 8 дней). Изучали , т,.е. дозуэ при которой погибает 50% насекомых (напримерs гибель личинок, замедление ростаs кутикулярные отклонения).
Результаты для выбранных соединений приведены в табл, 4.
Пример 7, Личинки походных червей на четвертой возрастной стадии (менее чем через 24 ч после линьки) обрабатывали местным способом в области дорсального брюшка в дозе 1ил соединения при испытываемой концентрации о Затем личинки помещали в накрытый контейнер на искусственную диету и выдерживали при 27°С от двух линек до окукливания (в общем случае 10 дней) о Проводили исследование ЭД т„е, дозы5 при которой погибает 50% насекомых (например, гибель личинок, замедление роста кутикулярные отклонения) .
Результаты для выбранных соедине™ ний приведены в табл, 4.
Как показывают результаты5 новые соединения формулы I обладают более высокой активностью,; чем известный пестицид., противs по крайней мере9 одного из трех известных насекомых, Формула изобретения
Способ получения замещенных N-бен тиенилмочевины общей формулы
Вз ,Ri
Xj0
А
О С-ИН-C- NH
А -&-
X.,
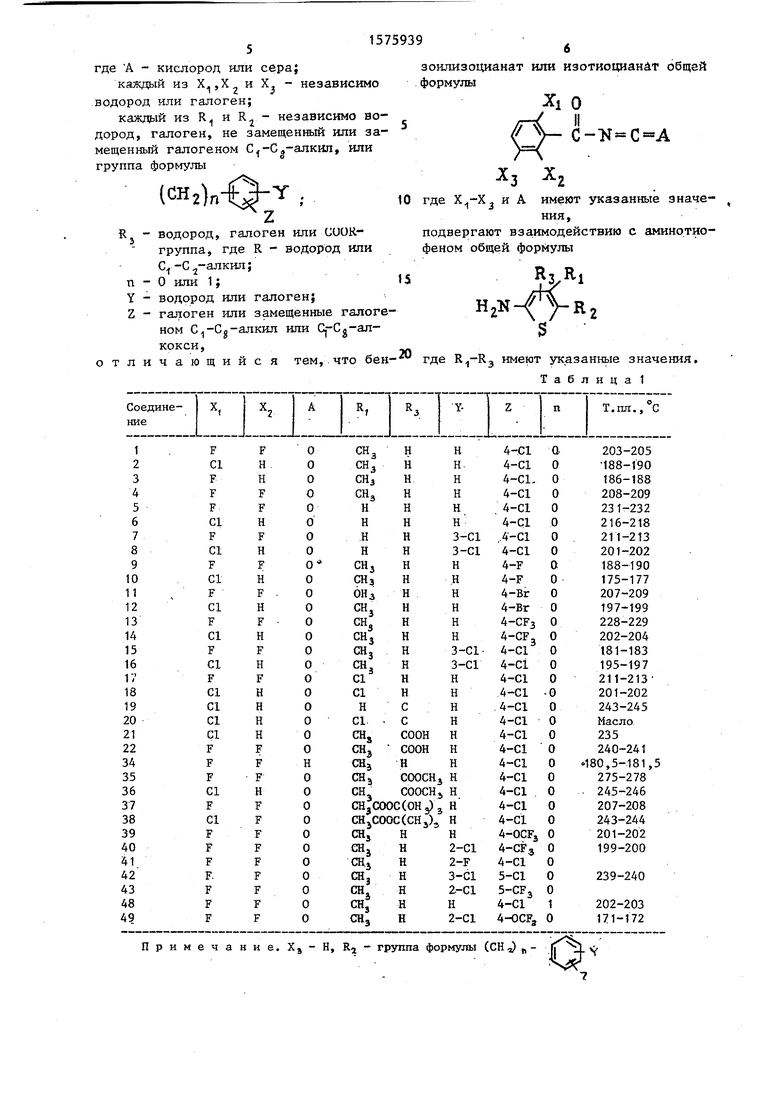
где А - кислород или сера;
каждый из X. ,Х и X. - независимо водород или галоген;
каждый из R1 и R2 - независимо водород, галоген, не замещенный или замещенный галогеном С --С ,,-алкил, или
1 о
группа формулы
(сн2)„
R. - водород, галоген или CUOR- группа, где R - водород или С1 -С2-алкил;
Примечание. XS-H, R - группа формулы (СН „ зоилизоцианат или изотиоцианат общей формулы
10 где Х.,-Х3 и А имеют указанные эначе- t
ния,
подвергают взаимодействию с аминотио- феном общей формулы
25
О
26
ClН
О
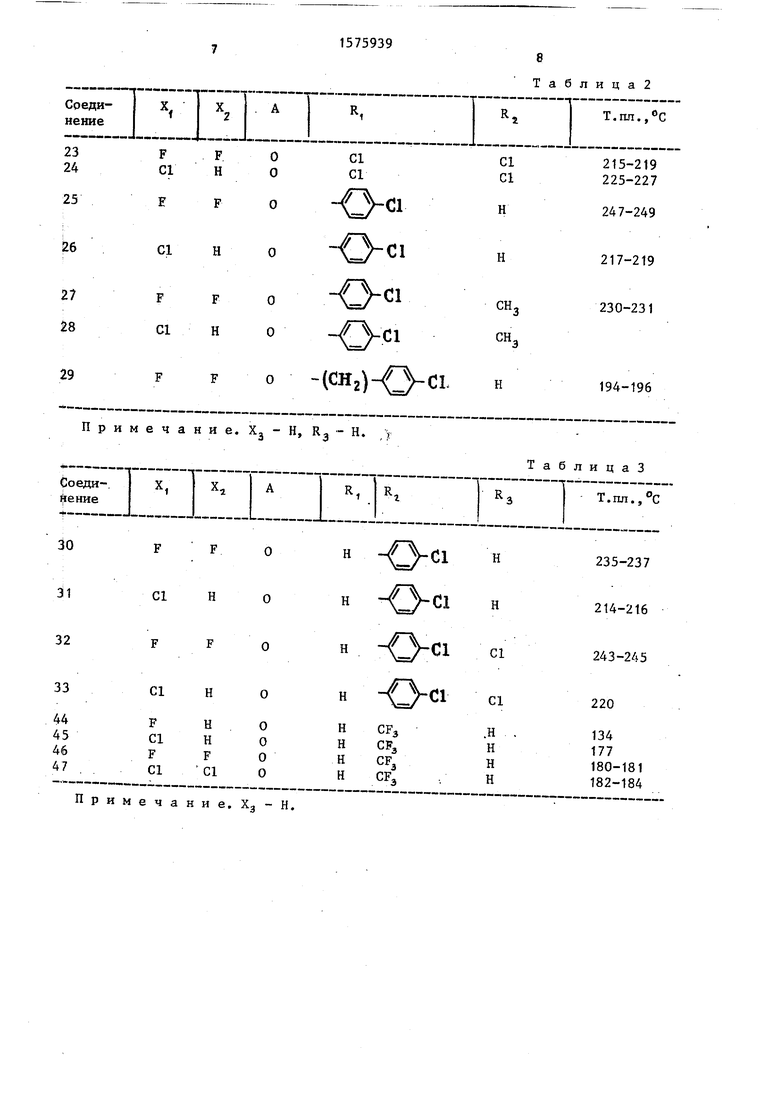
Примечание. Ха-Н.
Таблица2
Cl
Н
247-249
С1
н
217-219
157593910
Таблица4
| Бюпер К | |||
| и Пирсон Д | |||
| Органические синтезы | |||
| Мир, 1973, ч | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ передачи радиотелеграфных сигналов | 1922 |
|
SU394A1 |
| V | |||
Авторы
Даты
1990-06-30—Публикация
1988-07-19—Подача