нейтральными системами растворите-- лей.
Обработку биомассы проводят трех- кратно, каждый раз не менее 4,5 ч, используя 25-50-кратные объемы растворителей. При Сокращении числа стадий экстракции (табл. 1), продолжительности каждой стадии и объема экстрагента не достигается полное извлечение целевого продукта. Увеличение объема смеси растворителей вызывает переход в экстракт больших количеств трудноотделимых примесей, в особенности мембранных фосфолипи- дов. Активному извлечению последних способствует также повышение содержания хлороформа в экстрагенте, качество конечного продукта в этом случае снижается, Увеличение доли метанола или/и соляной кислоты в смеси растворителей приводит к: во-первых, к неполному извлечению лиии- да А, во-вторых, к загрязнению экстракта нелипидными примесями. При использовании кислоты с концентрацией выше 1,8% липид А заметно деградирует, а кислота с концентрацией менее 0,9% не обеспечивает количественного гидролиза липополисахарида, вследствие чего выход целевого продукта падает.
Количество липида А в экстрактах в процессе его извлечения из клеток Salmonella minnesota R-595 и Shigella flexneri 2A по отношению к максимально извлекаемому количеству (по результатам 9 процессов выделения) представлено в табл 1 .
Для удаления водорастворимых веществ из экстракта к нему добавляют хлороформ и воду до достижения равных (+5%) объемов всех трех растворителей в смеси. В результате образуется двухфазная система, где липид А практически полностью находится в нижней фазе, а гидрофильные примеси - в верхней. При увеличении количества хлороформа в смеси растворителей не обеспечивается максимальное освобождение от примесей. Увеличение доли воды или/и метанола влечет потерю части целевого продукта с верхней фазой и снижает его выход.
На стадии основной очистки липида А применяют колоночную хроматографию с обращением фаз на сфероне ОД 1000. В данной конкретной опера5
0
5
5
0
0
5
ции сферой имеет существенные преимущества по сравнению с сефадексом LH-20, предложенным ранее для очистки липида А (т), вследствие значительно большей его селективности и технологичности.
Вещества вносят в колонку в аце- тонитриле. Этим же раствором вымывают полярные примеси, а для удаления менее полярных примесей используют смесь ацетонитрил - изопропанол (4-5):1. Увеличение дозы изопропано- ла в смеси растворителей приводит к частичному элюированию липида А вместе с примесями и снижению его выхода; при уменьшении содержания изо- пропанола полное удаление примесей не достигается. Окончательную очистку целевого продукта осуществляют путем его перекристаллизации из аце- тонитрила, после чего продукт сушат в вакууме. Выход липида А при получении его из S. minnesota R-595 составляет 5-6 мг/г сухих клеток, а из Sh. flexneri 2А-1-2 мг/г сухих клеток содержание основного вещества в обоих случаях не менее 95%.
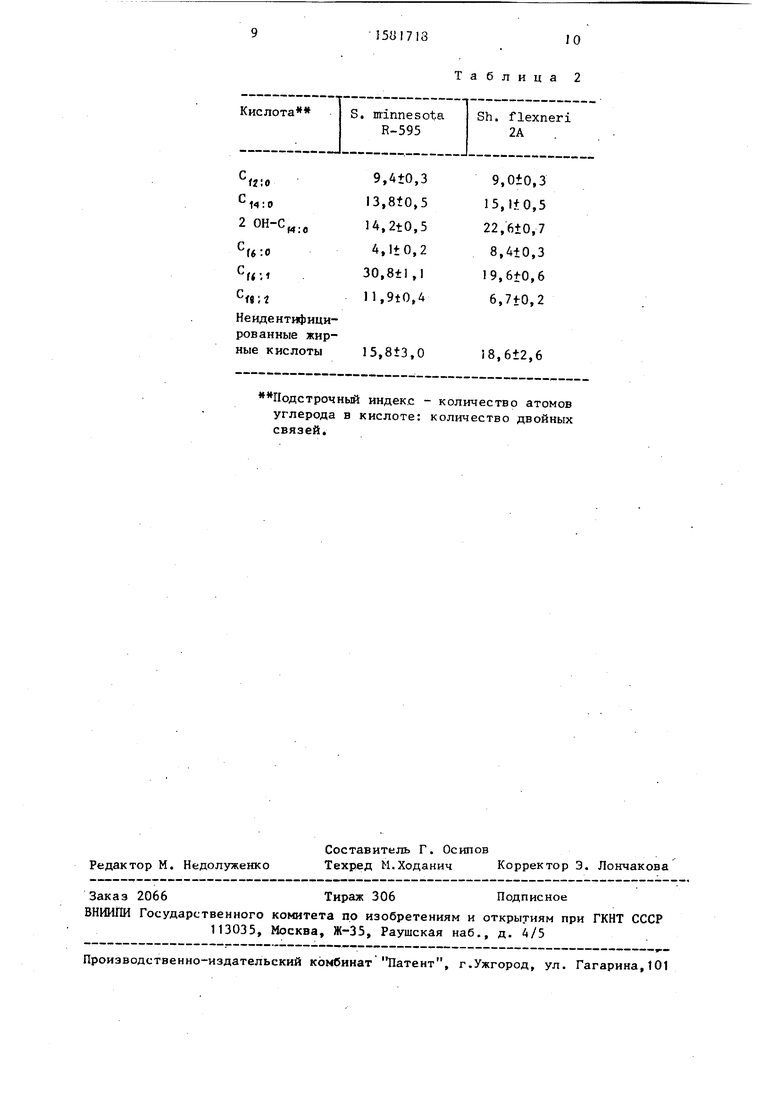
Структура и состав полученных препаратов доказана методами ТСХ, ВЭЖХ, ГЖХ5 Ж- и ПМР спектрами. Состав жирных кислот приведен в табл. 2.
Способ иллюстрируется следующими примерами.
Пример 1. Суспензию 25 г лиофильно высушенных клеток S. minnesota R-595 в 625 мл (25-кратный объем) раствора хлороформ - метанол - 1,8%-ная соляная кислота (10:21:7), перемешивают 4,5 ч ифильт- руют через пористый стеклянный фильтр. Цикл операций повторяют с отфильтрованными клетками еще 2 раза. Полученные фильтраты объединяют, добавляют 540 мл хлороформа и 690 мл воды (до объемного соотношения растворителей в смеси 1034:1036:1035), смесь встряхивают 5 раз и центрифугируют при 10000 g в течение 7 мин. Нижнюю фазу отделяют и упаривают досуха (здесь и далее растворители отгоняют на роторном испарителе при 30ГС и 20 мм рт.ст,). Остаток растворяют в 30 мл ацетонитрила и рас т- вор вносят в колонку, заполненную 200 г сферона ОД 1000. Колонку последовательно промывают 2500 мо ацетонитрила, 2000 мл смеси ацетонитрил - ичопропанол (5:1). Элюент, по51
лученный при промывании 1500 мл чистого изопропанола, упаривают досуха, остаток перекристаллизовывают из 15 мл ацетонитрила, сушат в вакууме (здесь и далее сушку проводят при 25-30 С при 0,2 мм рт. ст.) и получают 129 мг липида А (5,16 мг/г сухих клеток) в виде бисфосфата с содержанием основного вещества 96,4%. i
Пример 2. Суспензию 11 г лиофильно высушенных клеток S. min- nesota R-595 в 550 мл (50-кратный объем) раствора хлороформ -метанол -. О, 9%-ная соляная кислота (10:17:12) перемегаивают 5 ч и фильтруют через пористый фильтр. Цикл операций повторяют с отфильтрованными клетками еще 2 раза. Полученные фильтраты объединяют, добавляют 300 мл хлороформа и 210 мл воды, смесь встряхивают 5 раз и центрифугируют при 10000 g в течение 7 мин. Нижнюю фазу отделяют и упаривают досуха. Остаток растворяют в 20 мл ацетонитрила и раствор вносят в колонку заполненную 100 г сферона ОД 1000. Колонку последовательно промывают 1500 мл ацетонитрила, 1000 мл смеси ацетонит- рил-изопропанол (4:1). Элюент, полу- ченный при промывании 1000 мл чистого изопропанола, упаривают досуха, остаток перекристаллизовывают из 18 мл ацетонитрила, сушат в вакууме и получают 66,4 мг липида А (6,04 мг/г . сухих клеток) в виде бисфосфата с содержанием основного вещества 97,97,,
Пример 3. Суспензию 13 г лиофильно высушенных клеток S. min- nesota R-595 в 400 мл (31-кратный объем) раствора хлороформ - метанол - 1,5%-ная соляная кислота (10: :20:8) перемешивают 5 ч и фильтруют через пористый стеклянный фильтр. Цикл операций повторяют с отфильтрованными клетками еще 2 раза. Полученные фильтраты объединяют, добавляют 320 мл хлороформа и 380 мл воды, смесь встряхивают 5 раз и центрифугируют при 10000 g в течение 7 мин. Нижнюю фазу отделяют и упаривают досуха. Остаток растворяют в 20 мл ацетонитрила и раствор вносят в колонку, заполненную 120 г сферона ОД 1000 о Колонку последовательно промывают 1800 мл ацетонитрила и 1200 мл смеси ацетонитрил - изопропанол 4:1 . Элюент, полученный при промывании
0
- 0 5
0
5
0
5
0
5
186
1200 мл чистого ичопроианола, упаривают досуха, остаток перекристал- лизоьывают из 25 мл ацетонитрипл, сушат в вакууме и получают 77,9 мг липида А (5,99 мг/г сухих клеток) в виде бисфосфата с содержанием основного вещества 98,2%. i
Пример 4. Суспензию 15 г лиофильно высушенных клеток Shigella flexneri 2A в 375 мл (25-кратный избыток) раствора хлороформ - метд- -нол - ,8%-ная соляная кислота (10: :21:7) перемешивают 4,5 ч и сЬильтру- ют через стеклянный пористый фильтр. Цикл операций повторяют с отфильтрованными клетками еще 2 раза. Полученные фильтраты объединяют, добавляют 325 мл хлороформа и 415 мл воды. Смесь встряхивают 5 раз и центрифугируют при 10000 g в течение 7 мин. Нижнюю фазу отделяют и упаривают досуха. Остаток растворяют в 10 мл ацетонитрила и раствор вносят в колонку, заполненную 100 г сферона ОД 1000. Колонку последовательно промывают 1800 мл ацетонитрила и 1200 мл смеси ацетонитрила - изопропанол (5:1). Элюент, полученный про промывании 1200 мл чистого изопропанола, упаривают досуха, остаток перекристаллизовывают из 5,0мл ацетонитрила, сугаат в вакууме и получают 15,1 мг (1,01 мг/г сухих клеток) липида А в виде биофосфата с содержанием основного вещества 95,1%.
Пример 5. Суспензию 30 г лиофильно высушенных клеток Sh. flexneri 2А в 500 мл (50-кратный избыток) раствора хлороформ - метанол - О,9%-ная соляная кислота, взятых в объемном соотношении 10:17:2, перемегаивают 5 ч и фильтруют через стеклянный пористый фильтр. Цикл операций повторяют с отфильтрованными клетками еще 2 раза. Полученные фильтры объединяют, добавляют 270 мл хлороформа и 1 90 мл воды. Смесь встря- хявают 5 раз , центрифугируют при .10000 g в течение 7 мин. Нижнюю фазу отделяют и упаривают досуха. Остаток растворяют в 10 мл ацетонитрила и раствор вносят в колонку, заполненную 100 г сферона ОД 1000. Колонку последовательно промывают 1800 мл ацетонитрила и 1200 мл смеси ацетонитрил - изопропанол (4:1). Элюент, полученный при промывании 1200 мл чистого изопропанола, упаривают досуха, остаток перекристаплизовьша- wr из 5S0 мл ацетонитрила и получают 1991 мг липида А (1,91 мг/r сухих клеток) в виде бисфосфата с содержанием основного вещества 96,6%.
Пример 6. Суспензию И г лиофильно высушенных клеток Sh. flex neri 2A в 340 мл (31-кратный избыток) раствора хлороформ - метанол - 1,5%-ная соляная кислота (10;20:8) Перемешивают 5 ч и фильтруют через Пористый фильтр. Цикл операций повторяют с отфильтрованными клетками еще 2 раза Полученные фильтраты
Объединяют, добавляют 270 мл хлороформа и 320 мл воды. Смесь встряхивают 5 раз и центрифугируют при 10000 g в течение 7 мин. Нижнюю Фазу отделяют, упаривают досуха о Остаток раств.оряют в 10 мл адетонитрила и вносят в колонку, заполненную 100 г Сферона ОД 1000, Колонку последовательно промывают 1700 мл ацетонитри jia и 1200 мл смеси ацетонитрил:изо- Пропанол (4:1). Элюент, полученный При промывании 1200 мл чистого изо- Пропанола, упаривают досуха, остато перекристаллизовывают из 5,0 мл ацетонитрила и получают 21„8 мг липида А. (1,98 мг/г сухих клеток) в виде бисфосфата с содержанием основного
Вещества 97„1%,
Формула и з о б р е т е н и
3. Способ получения липида А из грам-отрицательных бактерий, включа-
Q 5
0
0
5
ющий лиофильную сугаку бактериальных клеток, гидролиз липополисахарида соляной кислотой, освобождение сырого продукта от водорастворимых примесей путем экстракции в двухфазной системе, образованной смесью хлороформа, метанола и воды, а также обра- щеннофазную хроматографию, отличающийся тем, что, с целью упрощения технологического процесса и повышения выхода целевого продукта, клетки экстрагируют три раза по 4,5 ч 25-50-кратными объемами смеси хлоро- форм-метанол-0,9-1,8%-ная соляная кислота, взятых в обт емном соотношении 10:(17-21):(), объединенный экстракт разбавляют хлороформом и водой до установления в смеси равных объемов растворителей, нижнюю фазу образовавшейся двухфазной системы упаривают досуха, остаток хромато- графируют на колонке со сфероном ОД-1000, колонку промывают ацетонит- рилом и смесью ацетонитрила и изопро- панола, взятых в объемном соотношении (4-5):1, после чего изопропано- лом вымывают липид А , который перекристаллизовывают из ацетонитрила .
2. Способ по п. 1, о т л и ч а ю щ.и и с я тем, что клетки грам- о трицательных бактерий используют в fe- или S-форме,



Изобретение относится к биотехнологии, в частности к способам получения биологически активных веществ из бактерий. Цель изобретения - упрощение технологического процесса и повышение выхода липида А при получении его из грам-отрицательных бактерий. С этой целью лиофильно высушенные бактериальные клети экстрагируют не менее трех раз по 4,5 ч 25-50-кратными объемами смеси хлороформ - метанол - 0,9-1,8-ная соляная кислота, взятых в объемном соотношении 10:(17-21):(7-12), объединенный экстракт разбавляют хлороформом и водой до установления в смеси равных объемов растворителей, нижнюю фазу образовавшейся двухфазной системы упаривают досуха, остаток хроматографируют на колонке со сфероном ОД-1000, колонку предварительно промывают ацетонитрилом и смесью ацетонитрила и изопропанола, взятых в объемном соотношении (4-5):1, после чего изопропанолом вымывают липид А, который перекристаллизовывают из ацетонитрила. При осуществлении способа из 1 г сухих клеток S.MINNESOTA R-595 получают 5-6 мг липида А, а из SH.FLEXNERI 2А - 1 - 2 мг липида А с содержанием основного вещества не менее 95%. Способ может быть осуществлен практически в любом масштабе и не требует сложной аппаратуры. 1 з.п. ф-лы, 2 табл.
65-70 25-28
2-5
Менее 1 Следы Не обнаружено
Таблица 1
70-75
28-33
5-9
1-2 Следы Не обнаружено
Подстрочный индекс - количество атомов углерода в кислоте: количество двойных связей.
Таблица 2
| Qureshi N., Takayama К., Ribi E | |||
| -I | |||
| Biol | |||
| Chern, 1982, v | |||
| Аппарат для нагревания окружающей его воды | 1920 |
|
SU257A1 |
| Столярный рабочий стол | 1928 |
|
SU11808A1 |
Авторы
Даты
1990-07-30—Публикация
1988-08-08—Подача