Изобретение относится к области аналитической химии и может найти применение в сельском хозяйстве.
Известен способ количественного определения тифенсульфуронметила (3-[3-(4-метокси-6-метил-1,3,5-триазин-2-ил)уреидосульфонил]тиофен-2-карбоновой кислоты метиловый эфир) (Хармони -торговое название гербицида) в зерне, соломе и зеленой массе зерновых колосовых культур и кукурузы, семенах и соломке льна-долгунца [1] заключающийся в том, что навеску измельченного зерна гомогенизируют в присутствии этилацетата и децимолярного раствора бикарбоната натрия, выдерживают в течение часа, подкисляют 10%-ной соляной кислотой до pH 3,0, вновь добавляют этилацетат, перемешивают и дают отстояться. Экстракт декантируют, фильтруют. Экстракцию повторяют еще дважды, встряхивая каждый раз 15 мин и объединяя объемы в делительной воронке. К объединенному экстракту прибавляют децимолярный раствор бикарбоната натрия, воронку встряхивают в течение 2 мин, после разделения фаз нижний слой сливают в стеклянный стакан, эту операцию повторяют еще дважды, используя новые объемы бикарбоната натрия. Водные экстракты объединяются, а этилацетатные фракции отбрасываются. Бикарбонатную фракцию подкисляют 10%-ной соляной кислотой до pH 3,5, подкисленный экстракт переносят в делительную воронку и реэкстрагируют хлороформом. После разделения фаз нижний хлороформовый слой сливают через слой безводного сернокислого натрия в концентратор. Экстракцию хлороформом повторяют дважды и объединенные хлороформовые экстракты упаривают досуха на ротационном испарителе при температуре 35oC. Сухой остаток растворяют в 5 10 мл подвижной фазы и хроматографируют.
Условия хроматографирования. Жидкостный хроматограф "Уотерс-510" с фотокондуктивным детектором "Трактор-365". Колонка стальная длиной 300 мм, внутренний диаметр 3 мм. Неподвижная фаза -μ-Порасил, Уотерс. Скорость потока подвижной фазы 0,5 мл/мин. Время удержания хармони 12 мин. Подвижная фаза циклогексан 750 мл, изопропанол 125 мл, метанол 125 мл, 10%-ный водный раствор уксусной кислоты 1 мл.
Метрология метода. Точность определения 89,6±7,0% Предел обнаружения 10 мкг/кг.
Недостатками способа являются невозможность определения тифенсульфурон-метила в почве и его длительность (10 ч).
Технической задачей является способ количественного определения тифенсульфурон-метила, позволяющий определять тифенсульфурон-метил в почве и сокращающий время определения.
Эта задача решается способом, заключающимся в том, что экстрагируют навеску почвы в воздушно-сухом состоянии смесью метанола, воды и гидрофосфата калия, экстракт фильтруют через фильтр, процесс экстракции повторяют еще раз, экстракты объединяют, из эликвоты удаляют метанол, водный остаток подкисляют концентрированной ортофосфорной кислотой до pH 3,5, затем реэкстрагируют хлороформом и реэкстракцию повторяют еще дважды, объединенные хлороформовые экстракты упаривают досуха, сухой остаток растворяют в экстрагенте, подкисляют концентрированной ортофосфорной кислотой и хроматографируют.
Метрология метода. Точность определения 80,5±7,4% Предел обнаружения 1 мкг/кг.
Условия хроматографирования. Насос высокого давления 114 М ("Бекман", США) с ультрафиолетовым детектором Spectroflow 757 ("Кратос", США). Колонка с обращенной фазой С-18 размером 250х4,6 мм (фирма "Бекман"), диаметр частиц неподвижной фазы 5 мкм. Объем петли инжектора 100 мкл, скорость подвижной фазы 0,7 мл/мин. Время удержания тифенсульфурон-метила ≈ 15 мин. Длина волны детектора 254 нм. Подвижная фаза содержит 22 части метанола, 77 частей воды, 1 часть одномолярного гидрофосфата калия. Концентрированной ортофосфорной кислотой доводят pH фазы до 7,0 (расход кислоты ≈ 200 мкл на 1 л фазы), контролируя процесс с помощью иономера.
Практически способ осуществляют следующим образом. Навеску почвы в воздушно-сухом состоянии (20 г) помещают в колбу вместимостью 250 мл и добавляют 40 мл экстрагента: 12 мл метанола, 24 мл воды, 4 мл одномолярного гидрофосфата калия. Суспензию встряхивают 1 ч на качалке. Экстракт фильтруют через фильтр "синяя лента" в чистую колбу. Процедуру экстрагирования повторяют еще раз. Оба экстракта объединяют. Из 40 мл аликвоты водно-метанольного экстракта испаряют метанол на вакуумном роторном испарителе при 70oC. Водный остаток количественно переносят в делительную воронку на 100 мл и доводят его до pH 3,5 концентрированной ортофосфорной кислотой (расход кислоты ≈ 1 мл), контролируя процесс с помощью иономера. Затем в воронку добавляют 30 мл хлороформа, встряхивают 1 мин, дают фазам разделиться в течение 5 мин и нижний хлороформовый слой сливают в концентратор. Операцию повторяют еще дважды. Объединенный хлороформовый экстракт затем упаривают досуха на вакуумном роторном испарителе при 35oC. Сухой остаток растворяют в 1 мл экстрагента. Образец подкисляют концентрированной ортофосфорной кислотой (расход кислоты 1 капля) и хроматографируют.
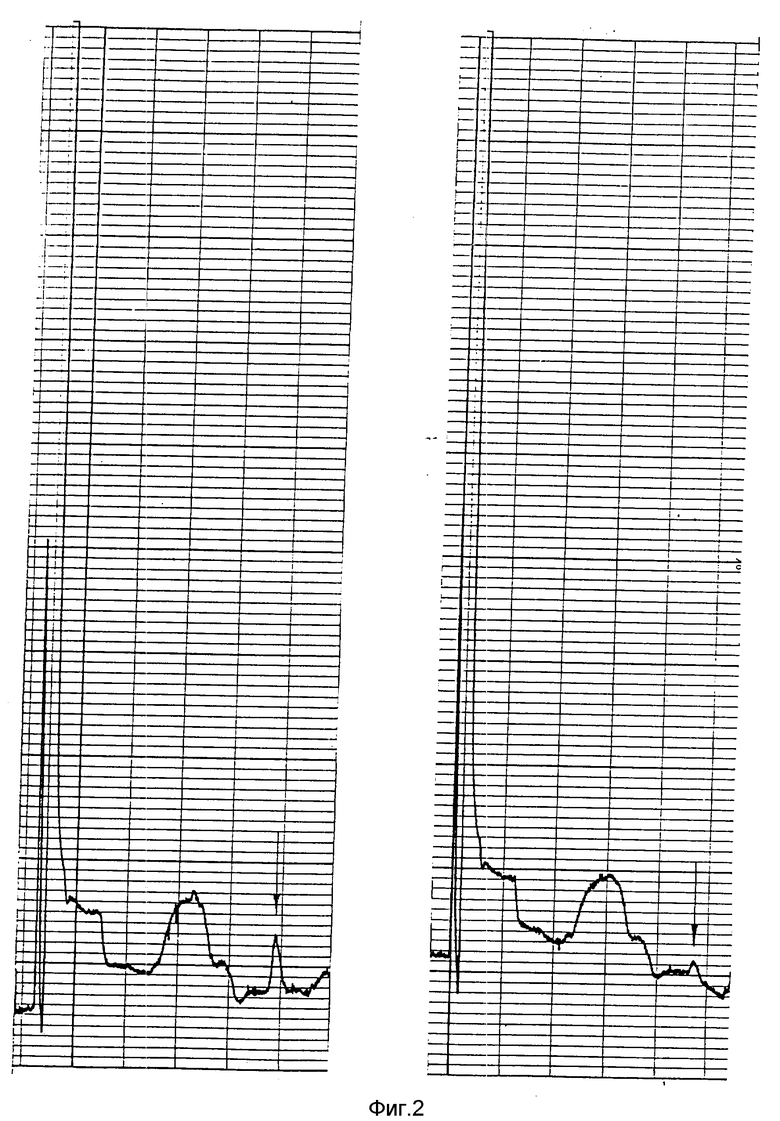
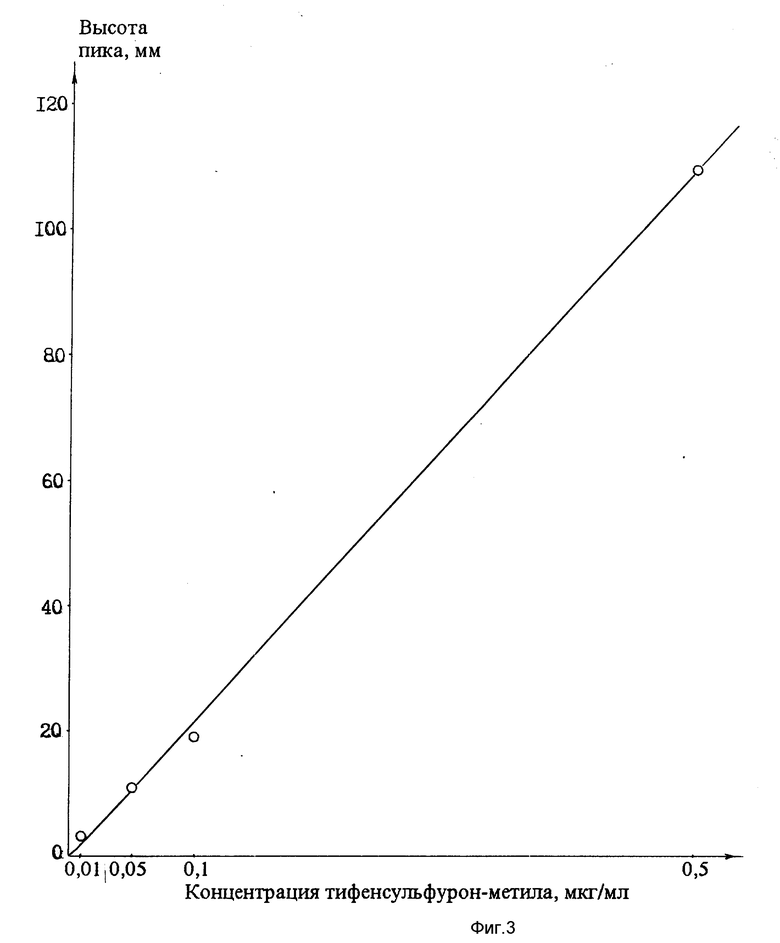
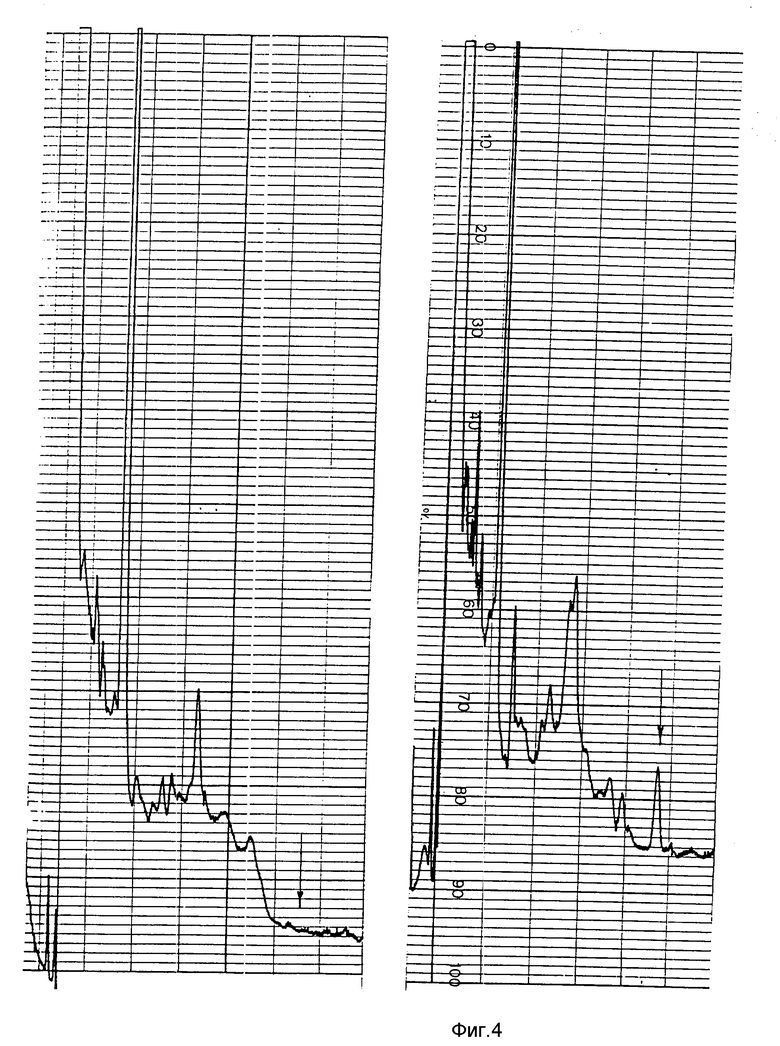
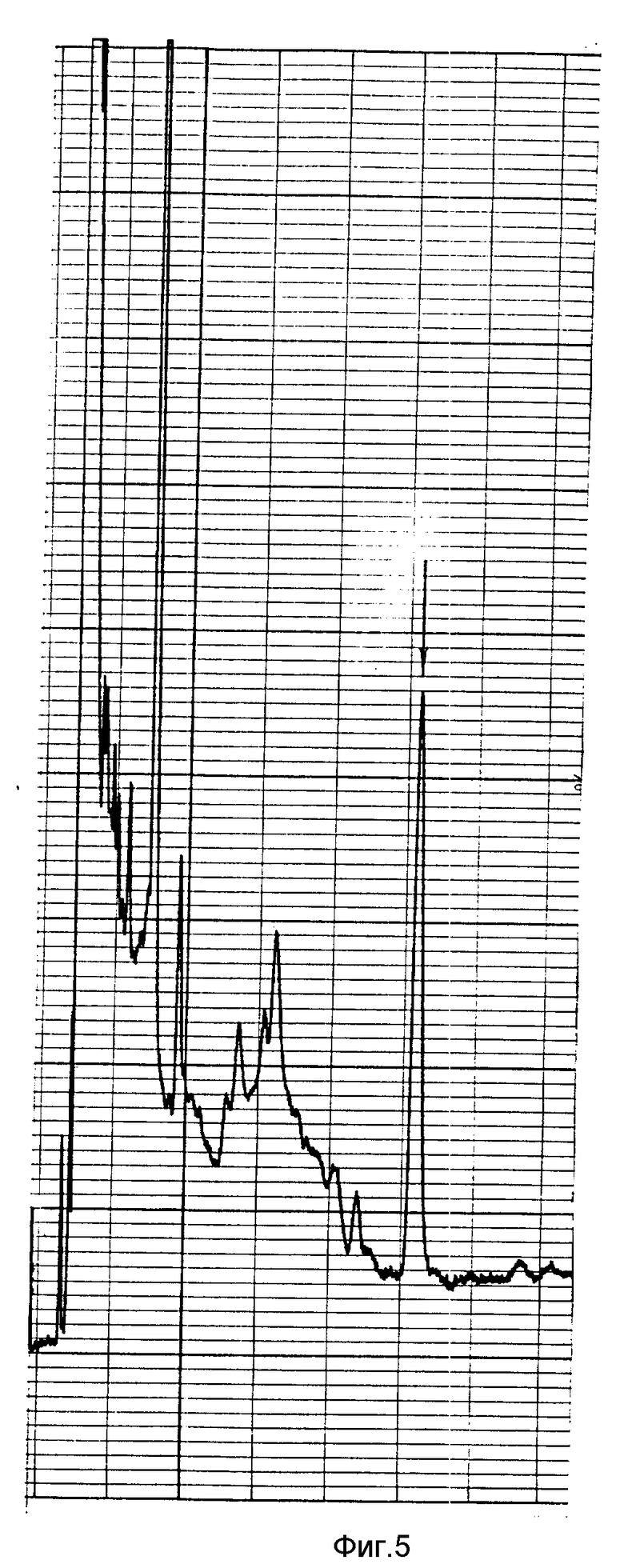
Для приготовления стандартных растворов берут 0,0050 г тифенсульфурон-метила и растворяют в 100 мл ацетонитрила. Получают концентрацию 50 мкг/мл. Затем определенные количества матричного раствора растворяют в 10 мл экстрагента (3 мл метанола, 6 мл воды, 1 мл одномолярного гидрофосфата калия) и получают стандартные растворы с концентрациями: 0,5; 0,1; 0,05; 0,01 мкг/мл. Перед использованием стандартов их подкисляют концентрированной ортофосфорной кислотой (≈ 200 мкл) до pH 3,0. При хроматографировании стандартов получают значения высот пиков (фиг.1 2). По этим данным строят градуировочный график (фиг. 3). Почву, не обработанную гербицидом, используют для определения процента выхода препарата при экстракции. Для этого в навески почвы добавляют 0,1 и 0,5 мкг тифенсульфурон-метила (5 повторностей) (фиг.4 5). По этим данным рассчитывают точность определения. Для контроля анализируют чистую почву (фиг.4). На фиг.6 7 представлены хроматограммы экстрактов из почвы, обработанной хармони за 7, 60 и 85 суток до пробоотбора (доза внесения гербицида 20 г/га). Тифенсульфурон-метил обнаружен только в первом образце почвы (фиг.6) в концентрации 0,01 мг/кг.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2011 |
|
RU2453848C1 |
| Способ получения производных 5/или 6/-ацилированных бензимидазолкарбоновых-2-кислот или их солей | 1979 |
|
SU888819A3 |
| Способ получения 5-(замещенный фенил)-оксазолидинонов или их серусодержащих аналогов | 1977 |
|
SU888821A3 |
| СОЕДИНЕНИЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2305096C2 |
| Способ получения производныхкарбазола или их опти-ческих изомеров,или их солей | 1973 |
|
SU509220A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЭСТРАТРИОЛА | 1971 |
|
SU308571A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПРОПЕНОВОЙ КИСЛОТЫ И ИХ СТЕРЕОИЗОМЕРОВ | 1988 |
|
RU2014320C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ O-(2,3-ДИГИДРО-2,2-ДИМЕТИЛ-7-БЕНЗОФУРАНИЛ)-N-МЕТИЛКАРБАМАТА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2004 |
|
RU2269780C1 |
| ПРОИЗВОДНЫЕ ПИПЕРИДИНА, ИХ СОЛИ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ПРОМЕЖУТОЧНЫЕ ВЕЩЕСТВА | 1995 |
|
RU2143425C1 |
| Способ получения производных азепина или их солей | 1971 |
|
SU507237A3 |
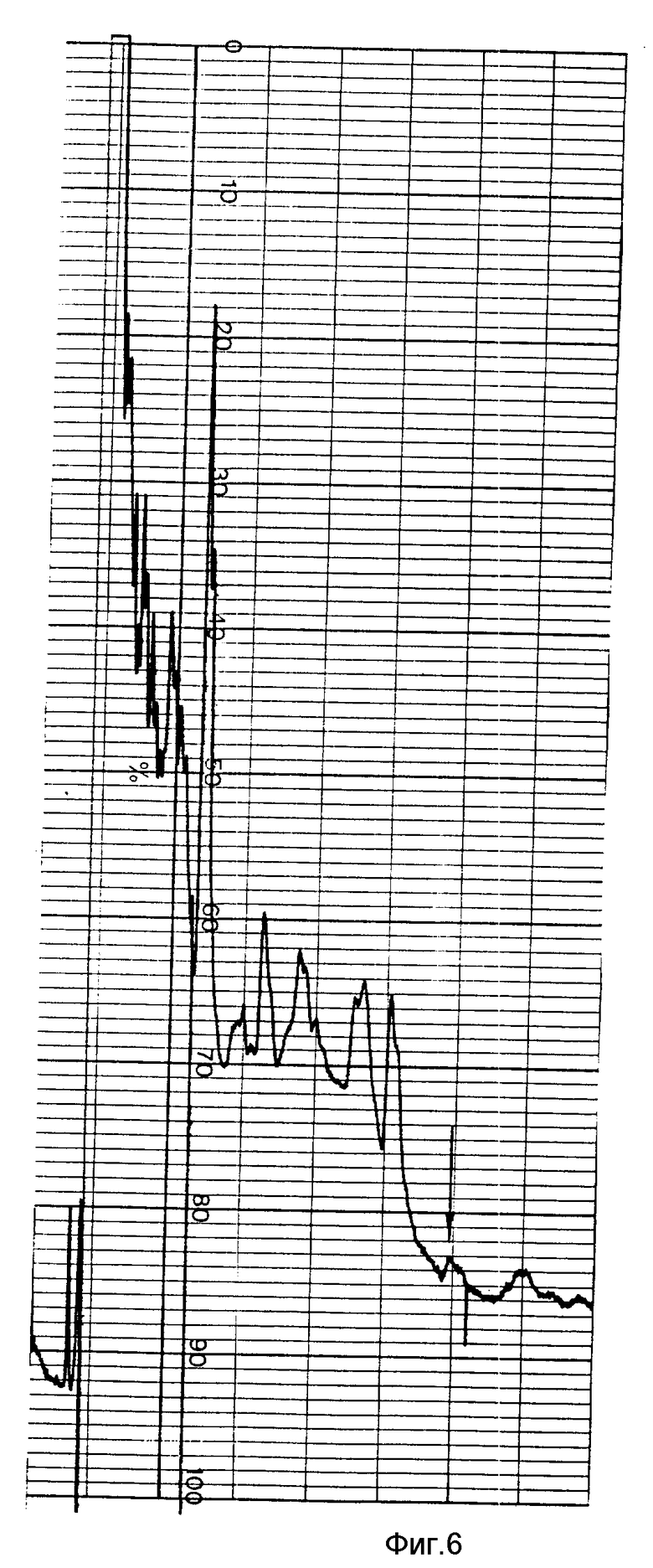
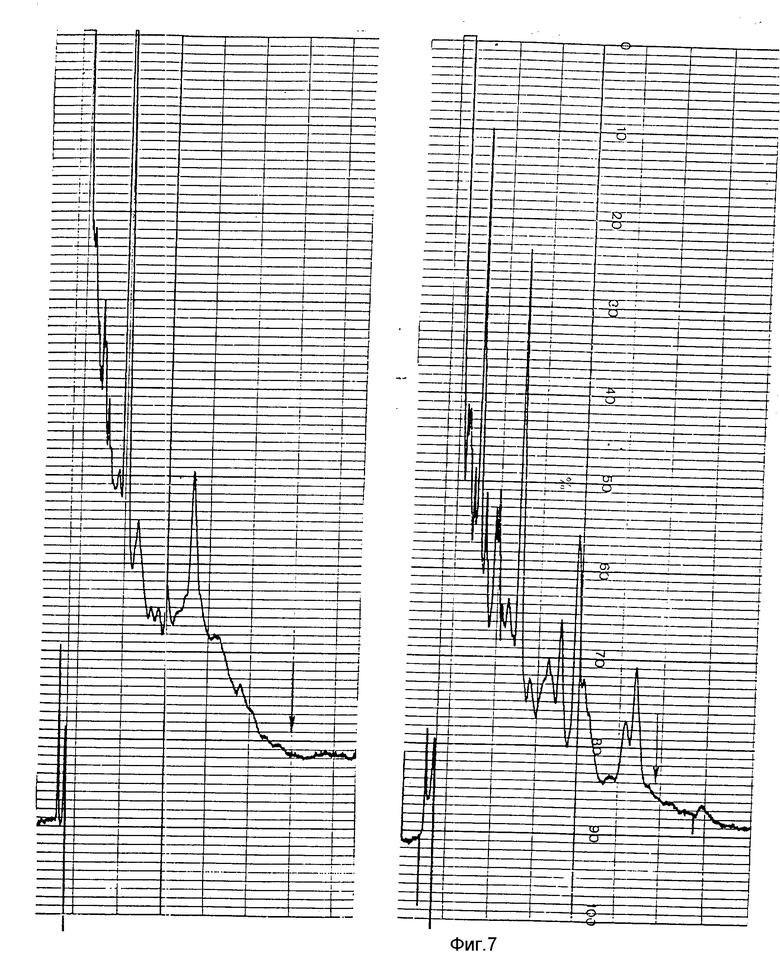
Способ количественного определения тефенсульфурол-метила (3-[3-(4-метокси-6-метил-1,3,5-триазин-2-ил)уреидосульфонин] тиофен-2- карбоновой кислоты метиловый эфир) в почве включает экстракцию пробы смесью метанола, воды и гидрофосфата калия, удаление метанола, подкисление водного остатка концентрированной ортофосфорной кислотой, обработку хлороформом и упаривание хлороформных экстрактов досуха. Сухой остаток растворяют в смеси метанола, воды и гидрофосфата калия, подкисляют концентрированной ортофосфорной кислотой и хроматографируют. Способ позволяет количественно определять тифенсульфурон-метил в почве. 7 ил.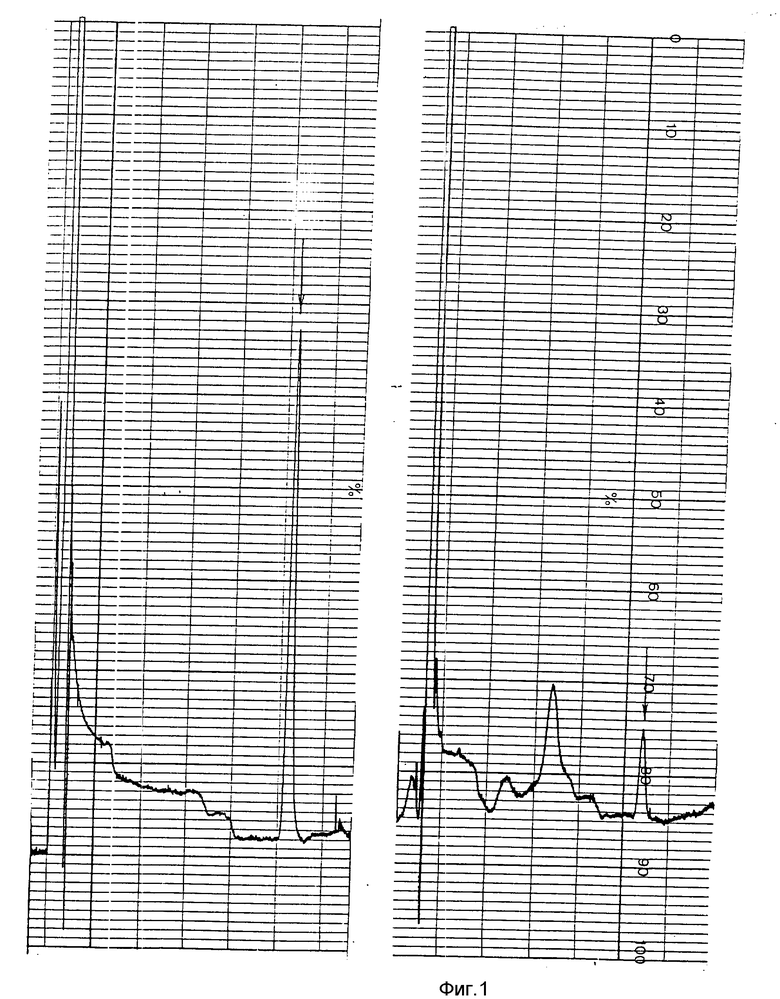
Способ количественного определения тифенсульфурон-метила (3-[3-(4-метокси-6-метил-1,3,5-триазин-2-ил)уреидосульфонил] тиофен-2-карбоновой кислоты метиловый эфир) в почве, включающий экстракцию пробы смесью метанола, воды и гидрофосфата калия, из экстракта удаляют метанол, водный остаток подкисляют концентрированной ортофосфорной кислотой, обрабатывают хлороформом, хлороформные экстракты упаривают досуха, сухой остаток растворяют в смеси метанола, воды и гидрофосфата калия, подкисляют концентрированной ортофосфорной кислотой и хроматографируют.
Авторы
Даты
1998-01-20—Публикация
1996-06-19—Подача