и ее изменение непрерывно или дискретно по ходу растворения образца, а количество растворенного оксида определяют по формуле
4Р - В (а - а« + „
РА,
-Ч1Р
Г) - (а.)
-VP т J
де В
100 А га
о
(D (2)
Ј - экспериментальная константа, определяющая влияние футеровки тигля;
атомные массы кислорода, металла, образующего исследуемый оксид, и раскислителя соответственно;
Р, q Q
Е Т К,
стехиометрические коэффициен ты оксида (hOffl) и продукта реакции раскисления (RpCn); масса расплава, г: показание ККЭ, мВ; температура, К; константа равновесия реакции раскисления;
а, а - первоначальная и текущая активности кислорода соответственно.
Принципиальное отличие предлагав- Иого способа от известного заключается в том, что изучение кинетики взаи- модействия производится не путем сравнения исходной массы (или размера) образца с массой (или размером) после эксперимента, которые зависят не только от количества растворившегося окси да, но и от количества наморозившегося металла, глубины пропитки оксида металлом, количества выкрасившегося оксида, а по активности кислорода в металле, которая определяется только количеством растворившегося оксида. Таким образом, производится непосред ртвенное измерение только той части образца, которая провзаимодействова- ла с расплавом стали или чугуна. А так как датчик окисленности позволяет определить активность кислорода с высокой точностью ( 5%), то существенно повышается точность эксперимента. Кроме того, по ходу эксперимента активность можно измерять любое, нужное количество раз или проводить непрерывный замер, что увеличивает надежность результатов.
В качестве материала тигля используют оксид металла, обладающего большим сродством к кислороду, чем рас- кислитель, и поэтому влияние тигля незначительно и определяется в холостом эксперименте и дает постоянную поправку.
При соприкосновении расплава с окисленностью, определяемой по реакции раскисления
q 0 (RPOJ,
Р V
(3)
и оксидом, равновесное значение активности кислорода с которым задается реакцией диссоциации
(BQJ nCx m 0, (4) одновременно происходят оба эти процесса диссоциации и раскисления, так как активность кислорода, определяемая реакцией (Ц), больше, чем активность кислорода, определяемая реакцией (3).
При этом количество раскислителя в расплаве уменьшается, а содержание кислорода увеличивается. Изменения концентраций элементов в металле описываются системой уравнений:
где , х , 0 - концентрация в
металле раскислителя , металла, образующего оксид, кислород соответственно;
их начальные концентрации соответственно;
Г,, DO., со,
ад, ,
Сх,
изменение концентраций элементов
за счет реакции раскисления и диссоциации соответственно.
Пример. Изучение кинетики растворения оксидов с металлом.
Опыты проводят в печи сопротивления в нейтральной атмосфере при I60(fc Состав металла следующий, %: С 0,01; Si, Mn, Сг отсутствуют, Р 0,005; S 0,007; А1 0,06; Fe остальное.
В качестве образца используют цилиндр плавленного кварца (Si02) диаметром м, массой 30-Ю-3 кг. Выбор образца обусловлен тем, что большинство отечественных огнеупоров, используемых для кладки ковша, имеют высокое содержание кремнезема в своем составе. Масса металла составляет 0,3 кг. Так как количество растворившегося оксида определяется окис- ленностью металле, задаваемой содержанием алюминия, то максимально возможное количество оксида кремния, способное раствориться в металле, не может превысить 0,35 Ю-3 кг. Такое количество вещества невозможно правильно определить ни взвешиванием, ни измерением линейных размеров в силу того, что на образец намерзает металл; могут попасть кусочки шлака; может произойти разрушение образца и т.д., т.е„ ошибка может значительно превысить измеряемую величину. В то же самое время активность кислорода в стали в процессе эксперимента значительно меняется (от 0,002 до 0,01%), что легко определяется датчиком окис- ленности.
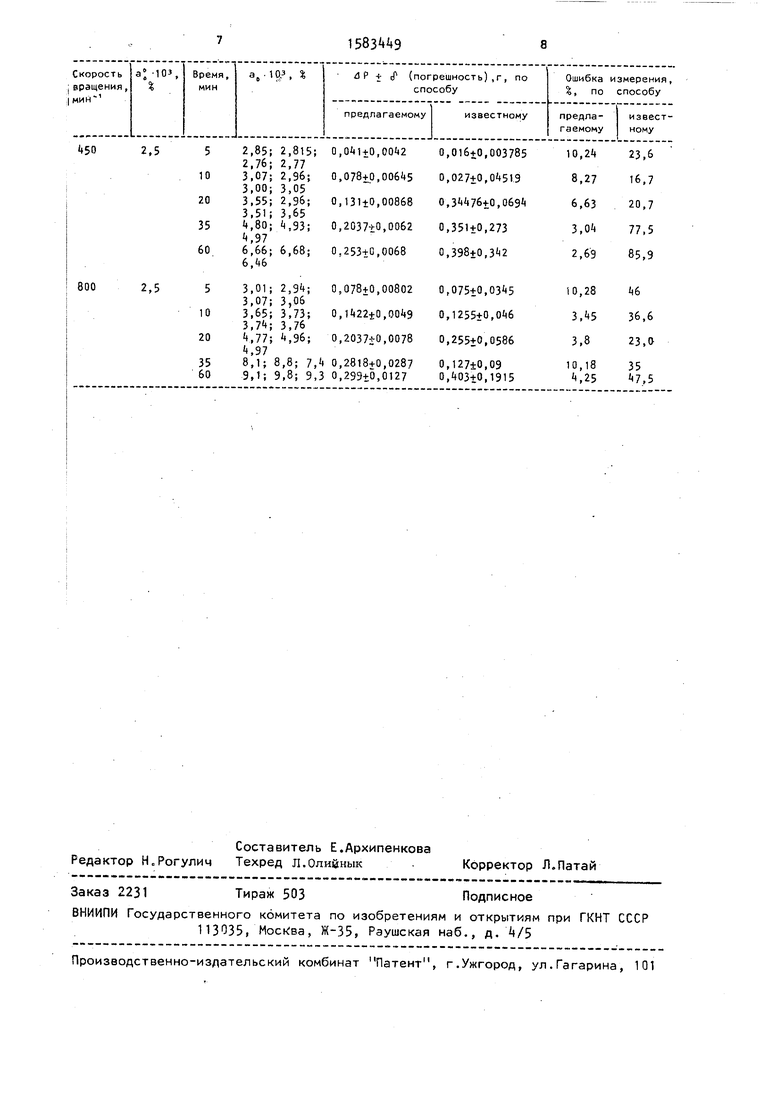
Изменение активности кислорода в процессе эксперимента и количество растворившегося оксида при различных скоростях вращения образца представлено в таблице.
В расчетах KR 5,6-10 11 , m 2, n 1, p 2,q 3, Ax 28, AR 27, Ай 16, $ 0.
Из данных таблицы видно, что с увеличением скорости вращения взаимодействие происходит более интенсивно, кроме того, даже при незначительных изменениях количества прореагировавших веществ реакция легко фиксируется
Использование предлагаемого способа обеспечивает существенное повышение точности эксперимента, возможность определения скорости взаимодействия, даже если массы реагирующих веществ очень малы.
I 5 Формула изобретения
Способ определения массы твердых оксидов, провзаимодействовавших с расплавом металла, включающий приведение исследуемого образца оксида в контакт с жидким металлом, содержащим раскислитель, выдержку и последующее определение массы прореагировавшего оксида, отличающийся тем, что, с целью повышения точности определения массы оксида, дополнительно при помощи кислородно-концентрационного элемента измеряют активность кислорода в расплаве металла до взаимодействия его с оксидом, а также ее величину после выдержки образца в жидком металле, при этом количество иР провзаимодействуощего оксида определяют по формуле
йР - В ав - а . +
РА,
-г/р . Ч-Ч/Р, „ - (а,) +Ј;
С
т-Ао + пАх
Q;
5
0
5
где А., Ах и А. 5
0
n, m, p и q
Q а.
атомные массы кислорода металла, образующего исследуемый оксид, и рас- кислителя в составе металла соответственно;
стехиометрические коэффициенты оксида (х„0го) и продукта реакции (RP0«y); масса расплава, г; активность кислорода после расплавления и выдержки расплава соответственно, %;
экспериментальный поправочный коэффициент , определяющий влияние футеровки тигля, определяется на основании холостого эксперимента.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВНЕПЕЧНОЙ ОБРАБОТКИ СТАЛИ | 1992 |
|
RU2031138C1 |
| Активный раскислитель жидких и тугоплавких горячих и холодных шлаков | 2022 |
|
RU2786789C1 |
| Способ производства стали для подшипников качения | 1981 |
|
SU956573A1 |
| СПОСОБ ВЫПЛАВКИ СТАЛЕЙ В ПЕЧАХ С КИСЛОЙ ФУТЕРОВКОЙ | 2024 |
|
RU2833976C1 |
| СПОСОБ ПРОИЗВОДСТВА БЕЗУГЛЕРОДИСТЫХ ЛИТЕЙНЫХ ЖАРОПРОЧНЫХ СПЛАВОВ НА ОСНОВЕ НИКЕЛЯ | 2014 |
|
RU2563403C1 |
| Способ раскисления стали | 1990 |
|
SU1731827A1 |
| Способ получения конструкционной низколегированной стали | 1984 |
|
SU1296597A1 |
| Способ раскисления металлов | 1979 |
|
SU852941A1 |
| Способ обработки стали | 1986 |
|
SU1371980A1 |
| СПОСОБ ПРОИЗВОДСТВА ЛИТЕЙНЫХ ЖАРОПРОЧНЫХ НИКЕЛЕВЫХ СПЛАВОВ ДЛЯ ПОЛУЧЕНИЯ ОТЛИВОК С НАПРАВЛЕННОЙ И МОНОКРИСТАЛЛИЧЕСКОЙ СТРУКТУРОЙ | 1993 |
|
RU2035521C1 |
Изобретение относится к черной металлургии, в частности к определению химического взаимодействия оксид-металлический расплав. Цель изобретения - повышение точности определения массы оксида. Кинетику химического взаимодействия определяют по изменению активности кислорода. Фиксируют первоначальную активность кислорода в металле при помощи кислородного концентрационного элемента (ККЭ) и ее изменение непрерывно или дискретно по ходу растворения образца. Количество растворенного оксида определяют по формулеΔР=B[A* 0-*A 0+QA 6X R A R][(A 0° -Q/P)-(A 0 -Q/P)]+ξ, где B=[(MA 0+NA X)Q]/100A 0M
A 0,A X, A R- атомные массы кислорода, металла, образующего исследуемый оксид, и раскислителя соответственно: N, M, P, Q - стехиометрические коэффициенты оксида (X N O M) и продукта реакции раскисления (R P O Q)
Q - масса стали
E - показания ККЭ (мВ)
T - температура
K, K R - константа равновесия реакции раскисления
A 0, A 0 - первоначальная и текущая активности кислорода соответственно
ξ - экспериментальный поправочный коэффициент. Данная методика позволяет разрабатывать технологию раскисления стали длп различных агрегатов с учетом влияния огнеупорной футеровки. 2 табл.

| Авторское свидетельство СССР № , кл | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| Ленинских Б.М | |||
| Диффузия элементов в жидких металлах группы железа | |||
| - М.: Наука, 19У | |||
| ( СПОСОБ ОПРЕДЕЛЕНИЯ МАССЫ ТВЕРДЫХ ОКСИДОВ, ПРОВЗАИМОДЕЙСТВОВАВШИХ С РАСПЛАВОМ МЕТАЛЛА | |||
Авторы
Даты
1990-08-07—Публикация
1988-03-31—Подача