Йзобретение относится к аналитической химии и имеет огромное значение для клинической химии, биохимии, фармацевтической химии и химии пищевых продуктов.
Цель изобретения - повышение чувствительности определения.
. Изобретение предусматривает использование в качестве субстрата липазы соединение общей формулы
00
и ti HjC-Y-C-A-C-X
HC-Y-R
I
H C-Z-KI
где A - алкильная или алкиленовая группа с 2-12 атомами углерода;
о g
Ot) SI
ы
R и
R - одинаковые или разные, каждый означает алкильную группу с 6-18 атомами углерода, один из остатков R и R также атом водорода;
X - резоруфин, 6-метилрезоруфин, I,6-диметилрезоруфин, 8 этил- резоруфин, 8-бромрезоруфин; Y и Z - каждый независимо друг от друга означают -S- или
-О-, Z также -СН- , и оптическое определение по окраске количества освобожденного аромати- ческого гидроксильного или тиолово- го соединения непосредственно, или после сочетания с подходящим хромогеном.
Для R и R предпочитают алкильные группы в противоположность ацильным группам, так как они не чувствительны к гидролизу.
Примерами для R и/или R, являются остатки метила, этила, пропила, бутила, пентила, гексила, гептила, октила, нонила, деДила, ундецила, до децила, тетрадецила, гексадецила и октадецила как алкильные группы, а также соответствующие ацильные труп- пы, как грзшпы ацетила, пропионила, бутирила, валерила, капронила, кап- рила, капринила, лаурила, миристила, пальмитила и стеарила, олеила, крото- нила, линолила, фенила, бензила или октилфенила.
Далее предлагаемый субстрат липазы содержит остаток дикарбоновой кислоты СООН-А-СООН, в которой А имеет предпочтительно 3-7 С-атомов. Кислотами, образующими А, являются малоновая, янтарная, глутаровая, адипиновая, пимелиновая, пробковая азелаиновая, себациновая, нонандикар- боновая, декандикарбоновая к ундекан дикарбоновая кислоты. Предпочитают кислоты от глутаровой кислоты до азелаиновой кислоты, которые соответствуют А с 3-7 С-атомами.
X может быть ароматическим окси- или тиолсоединением, которое представ ляет хромофор или может быть переведено в красящее вещество лишь после- довате.пьной реакцией. Типичными при-. мерами являются фенол, тиофенол, нафтол, тионафтол и их производные,а также хромогенные соединения, как остаток резоруфина, 6-метилрезоруфин, | 4,б-дикетилрезоруфин, 1,6-диметилре-
Q
15
jQ
25 Q 35
5
зоруфин и 8-зтилрезоруфин, и 8-бромрезоруфин, хлорфенолового красного, индоксила или тиофлуоресцеина.
Предпочитают хромофоры, которые имеют небольшую полярность и являются жирорастворимь ми. Однако при этом должна быть.гарантирована еще водо- растворимость.
Жирорастворению названных хромофоров способствует подходящее замещение с алкильными группами, Так, для остатка резоруфина оказались группы метила, диметила и этила, а та1сже замещение с бромом.
Соединения по изобретению являются новыми. Они имеют асимметрический центр и поэтому оптически активны. В качестве субстрата липазы можно применять как образующиеся при, обычных методах получения рацематы, так и оптические изомеры.
Субстраты липаэы по изобретению можно получать известными методами.
Способ предусматривает использование в составе аналита реактива, предпочтительно содержащего, мг/мл: субст- рат 0,05-10, дезоксихолат 2-50, коли- паза 0,001-0,01, мочевина 1-100, NaCl 0,1-10, буфер 1-50, устанавливающие рН от 6 до 10,5 соответственно в пересчете на годный к употреблению раствор.
Приведенные примеры иллюстрируют как получение субстратов, так и способы определения липазы с их использованием
Пример 1. а) Сложный моноэфир 1,2-0-дигексил-рац-глицеро-З- глутаровой кислоты.
В раствор 3,3 г (11,5 ммоль) 1,2- О-дигексил-глицерина в 30 мл хлороформа добавляют последовательно 2,5 МП пиридина, на кончике шпателя 4-диметш1аминопиридин и 2,6 г (23 ммоль) ангидрида глутаровой гис- лоты. Смесь нагревают IО ч при флегме и после охлаждения разбавляют 200 мл хлороформа. Фазу хлороформа взбалтывают с J н. соляной кислотой и сушат. После отфильтровывания высушивающего вещества растворитель удаляют и остаток очищают на колонне с силикагелем (элюент: уксусный эфир - петролейный эфир 1:1).
ДС: Rf 0,45 (уксусный эфир - петролейный эфир 1:2 + % ледяной уксусной кислоты).
Сложный резоруфиновый эфир 1,2-0- дигексил-рац-глицеро-3-глутаровой кислоты.
Ь) 1,4 г (3,7 ммоль)раствора по способу 1а растворяют в 20 мл хлороформа и при охлаждении льдом закапывают 2 мл (23,3 ммоль) хлористого оксалила. Ледяную ванну удаляют и перемешивают раствор 12 ч при комнатной температуре. Затем сливают растворитель, остаток поглощают в толуоле и снова выпаривают. Полученное таким путем масло применяют без дальнейшей очистки.
с) О,8 г (3,7 ммоль) резоруфина суспендируют в 40 мл диметилформами- да при добавке 1,1 мл пиридина и на кончике шпателя 4-диметиламинопир дина. Туда закапывают раствор по способу 1Ь в 20 мл диметилформамида. После одно - и двухсуточного перемешивания при комнатной температуре фильтруют и сливают растворитель. Остаток поглощают в уксусном эфире, отфильтровывают нерастворимые компоненты и взбалтывают фильтрат с 1 н. соляной кислотой, затем с водой. После сушки органической фазы и отгонки растворителя получают маслянистый остаток, который очищают хроматографией на колонне с силикаге- лем (элюент: уксусный эфир - петро- лейный эфир 1:1)
ДС: Rf 0,70 (уксусный эфир - гексан 1:1).
Пример 2. а). Сложный моноэфир 1,2-0-диоктил-рац-глицеро-З- глутаровой кислоты.
Получение аналогично примеру 1а из 13 г (41 ммоль) 1,2 0-диоктил-гли церина, 150 мл хлороформа, 10 мл пиридина и 6,8 г (59,5 ммоль) ангидрида глутаровой кислоты. Выход 6,5 г (37%).
ДС: Rf 0,31 (уксусный эфир - пе ролейный эфир 1:1).
Сложный резоруфиновый эфир 1,2-0- диоктил-рац-глицеро-3-глутаровой кислоты.
b). Получение аналогично примеру Ib из 2 г (4,5 ммоль) по примеру 2а. с). 0,96 г (4,5 ммоль) резоруфина растворяют в 50 мл хлороформа при добавке 0,75 мл (5 ммоль) 1,8-диаза- бицикло-(5,4,0)-ундец-7-ена и 0,1 г 4-диметиламинопиридина. Туда закапывают раствор по примеру 2Ь в 20 мл хлороформа. После одно- и двухднев04167
- 10
ного перемешивания при комнатной температуре фильтруют и удаляют растворитель. Переработка аналогична примеру 1с.
ДС: Rf 0,66 (уксусньп эфир гексан 1:1).
Примерз, а). Сложный моноэфир 1,2-0-диоктил-рац-глицеро-З-пи- мелиновой кислоты.
Получение аналогично примеру 1а из 3,2 г (10 ммоль) 1,2-0-диоктил- глицерина и 2,1 г (15 ммоль) ангидрида пимелиновой кислоты.
ДС: Rf 0,61 (уксусный эфир - петролейный эфир 1:1).
IR (см-):(пленка):1740; 1710.
Сложный резоруфиновый эфир 1,2-0- диоктил-рац-глицеро-3-пимелиновой
кислоты.
Ъ). Получение аналогично примеру 1Ь из 2,2 г (4,7 ммоль) За.
с). Получение аналогично примеру 2с из 1 г (4,7 ммоль) резоруфина, 25 0,7 мл 1,8-диазабицикло-(5,4.0)-ун- дец-7-ена и ЗЬ.
ДС: Rf 0,78 (уксусный эфир - гексан 1:2).
Пример4. а). Сложньй моноэфир 1,2-0-диоктил-рац-глицеро-З-азе- лаиновой кислоты.
15
20
30
0
5
Получение аналогично примеру 1а из 6,3 г (20 ммоль) 1,2-0-диоктил- глицерина, 80 мл хлороформа, 5 мл пиридина и 5,2 г (30 ммоль) ангидрида азелаиновой кислоты.
Сложный резоруфиновый эфир 1,2-0- диоктил-рац-глицеро-3-азелаиновой
кислоты.
Ь). Получение аналогично примеру Ь из 3,2 г (6,5 ммоль) 4а и 3 мл хлористого оксалила.
с). Получение аналогично примеру 2с из 1,4 г (6,5 ммоль) резоруфина, 65 мл хлороформа, 1,1 мл 1,8- диазабицикло-(5,4,0)-ундец-7-ена и 4Ь.
ДС: Rf 0,86 (уксусный эфир - гексан 1:2).
IR (см- ): (пленка) 1762; 1736.
Пример5. а). Сложный моноэфир 1,2-0-дидецил-рац-глицеро-З- глутаровой кислоты.
Получение аналогично примеру 1 а из 3,7 г (10 ммоль) 1,2-0-дидецил- глицерина, 40 мл хлороформа, 2,5 мл пиридина и 1,8 г (15,8 ммоль) ангидрида глутаровой кислоты.
0
5
ДС: Rf 0,77 (уксусньш эфир - гексан 1:2),
Сложный резоруфиновый эфир 1,2-0 дидецил-рац-глицеро-3-глутаровой кислоты,
b). Получение аналогично примеру 1Ьиз 2,5 г (Зммоль) 5а, 50 мл хлорформа и 2,2 мл хлористого оксалила.
с). Попучение аналогично приме- ру 2с из 1,1 г (5 ммоль) резоруфи- на, 1 мл 1,8-диазабицикло-(5,4,0)- ундец-7-ена и 5Ь.
ДС: Rf 0,70 (уксусный эфир - гексан 1:1).
П р и м е р б. а). Сложный моноэфир 1,2-0 диундецил-рац-глицеро З- глутаровой кислоты.
Получение аналогично примеру 1а. из 2 г Г 5 ммоль ) 1,2-0-диундецш1- глицерина, 25 мл хлороформа, 1,4 мл пиридина и 0,9 г (7,5 ммоль) ангидрида глутаровой кислоты.
ДС: Rf 0,55 (уксусный эфир - петролейный эфир 1:2).
IR (см ):(пленка) 1740; 1710.
Сложный резоруфиновый эфир 1,2-0 диундецил-рац-глицеро-3-глутаровой кислоты.
Ь). Получение аналогично приме- pyjb из 2 г (3,9 ммоль) 6а 5 мл хлороформа и 1,8 хлористого оксалил
с). Получение аналогично примеру 2с из 0,83 г (3,9 ммоль) резору- фина, 0,61 мл 1,8-диазабицикло-(5,4 0)-ундец-7-ена и 6Ъ.
ДС: Rf 0,47 (RP 18, этанол - ацетон 2:1).
П р и м е р 7. а). Сложный моноэфир ,2-0 -дилаурШ1-рац-глицеро-3- глутаровой кислоты.
Получение аналогично примеру 1 а из 10,7 г (25 ммоль) 1,2-0-дилаурил- глицерина, 70 мл хлороформа, 5,5 пиридина и 3,3 г (29 ммоль) ангидрида глутаровой кислоты.
ДС: Rf 0,33 (уксусный эфир - перолейный эфир 1:1).
IR()(пленка): 1741; 1708.
Сложный резоруфиновый эфир 1,2-0- дилаурил-рац-глидеро-З-глутаровой кислоты
Ь)„ Получение аналогично примеру 1Ь из 5,5 г (10 1чмоль) 7а, 50 мл хлороформа и 4,3мл хлористого оксалил
сТ Иолучение аналогично примеру 2с из 2,2 г (10 ммоль) резоруфина, 100 мл хлороформа и 1,5 ил 1,8-диaз бициклo-(5 94,0)-ундец-7-ена и 7Ь.
8
ДС: Rf 0,78 (уксусный эфир/петр лейный эфир 1:1).
IR (см-О(пленка): 1765; 1720.
П р и м е р 8. а). Сложный моноэфир 1,2-0-дилаурШ1-рац-глицеро-3- пимелиновой кислоты.
Получение аналогично примеру 1а и 8,6 г (20 ммоль) 1,2-0-дилаурил-гли- церина, 50 мл хлороформа, 15 мл пиридина и 4,3 г (30 ммоль) ангидрида пимелиновой кислоты.
ДС: Rf 0,5 (уксусный эфир - петролейный эфир 1:2).
IR ()(пленка): 1740; 1710. Сложный резоруфиновый эфир 1,2-0дилаурил-рац-глицеро-З-пимелиновойкислоты.
Ь). Получение аналогично примеру Ib из 1,66 г (3 ммоль) 8а и 1,3 мл хлористого оксалила.
с). Получение аналогично примеру 2с из 0,65 г (3 ммоль) резоруфина, 30 мл хлороформа, 0,5 мл 1,8-диаза- бицикло-(5,4,0)-ундец-7-ена и &Ь.
ДС: Rf 0,75 (уксусный эфир - Iгексан 1:1).
IR (см- )(пленка): 1768; 1739.
П р им 8 р 9. а). Сложный моноэфир 1,2-0-дитетрадецш1-рац-глицеро- 3-глутаровой кислоты.
Получение аналогично примеру 1а из 14,6 г (30 .ммоль) 1,2-0-дитетра- децил-глицерина, 150 мл хлороформа, 8,2 мл пиридина и 5,1 г (45 ммоль) ангидрида глутаровой кислоты.
ДС: Rf 0,42 (уксусный эфир - петролейный эфир 1:2).
IR ()(КВг): 1740;. 1710.
Сложный резоруфиновый эфир 1,2-0- дитетрадецил-рац-глицеро-3-глутарово кислоты.
Ь). Получение аналогично примеру 1Ь из 3 г (5 ммоль) 9а и 2,2 мл хлористого оксалила.
с). Получение аналогично примеру 2с из 1,06 г (5 ммоль) резоруфина, 50 мл хлороформа, 0,75 мл 1,8-диаза- Iбицикло-(5,4,0)-ундец-7-ена и 9Ь. ДС: Rf 0,34 (RP18, ацетонитрил дихлорметан 1:1).
IR (см ИкВг): 1763, 1735.
П р и м е р 10. а). Сложный моноэфир 1 ,2-0-дитетрадецнл-рац-глицеро3-пимелиновой кислоты .
Получение аналогично примеру 9а из 6,4 г (45 ммоль) ангидрида пимелиновой кислоты.
ДС: Rf 0,45 (уксусный эфир - петролейный эфир 1:2).
IR ()(пленка): 1740; 1708.
Сложный резоруфиновый эфир 1,2-0- дитетрадецил-рац-глицеро-З-пимелино- вой кислоты.
Ь). Получение аналогично примеру 1Ь из 3,1 г (5 ммоль) 10а и 2,2 мл хлористого оксалила.
с). Получение аналогично примеру 2с из 1,06 г (5 ммоль) резоруфи- на, 50 мл хлороформа и 0,78 мл 1,8- диазабицикло-(5,4,0)-ундец-7-ена
и lOb,
ДС: Rf 0,71 (уксусный эфир - петролейный эфир 1:2)
IR (см-)(пленка): 1755; 1734.
Пример 11. а). Сложный моноэфир 1,2-0-дигексадецил-8п-глицероглутаровой кислоты.
Получение аналогично примеру 1а из 2,7 г (5 ммоль) 1,2-0-дигек- садецил-Зп-глицерина, 50 мл хлорофома, 3 мл пиридина и 1,5 г (13 ммоль ангидрида глутаровой кислоты.
ДС: Rf 0,65 (уксусный эфир - петролейный эфир 151)
IR (см- )(КВг) :.1740; 1710.
Сложный резоруфиновый эфир 1,2-0 дигексадецил-8п-глицеро-3-глутарово
кислоты.
Ь). Получение аналогично примеру 1Ь из 2,2 г (3,3 ммоль) Па и 1 мл хлористого оксалила.
с). Получение аналогично примеру 1с из 0,71 г (3,3 ммоль) резору- фина, 20 мл диметилформамида, 0,5 мл пиридина и ПЬ.
ДС: Rf 0,72 (уксусньш эфир - петролейный эфир 1:2).
Пример 12. а). Сложный моноэфир 1,2-0-дибензил-рац-глицеро-З- глутаровой кислоты
Получение аналогично примеру 1а из 3 г (11 ммоль) 1,2-0-дибензш1- глицерина, 30 мл хлороформа, 2,5 мл пиридина и 1,8 г (16 ммоль) ангидрида глутаровой кислоты.
ДС: Rf 0,39 (уксусный эфир - петролейный эфир 1:Г+ 1% ледяной уксусной кислоты).t
Сложный резоруфиновый эфир 1,2-0- дибензил-рац-глицеро-3-глутаровой
кислоты.
Ь). Получение аналогично примеру 1Ь из 2,9 г (7,5 ммоль 12а), 30 мп хлороформа и 3,3 мл хлористого оксалила.
5
0
5
с) . Получение аналогично примеру , 2с из 1,6 г (7,5 ммоль) резоруфииа, 75 МП хлороформа, 1,2 мл 1,8 диазаби- цикло-(5,4,0)-ундец-7-ена и 12Ь.
ДС: Rf 0,48 (уксусньш эфир - гексан 1:1).
Пример 13. а). Сложный моноэфир 1-0-октадещш-2-0-бензил-5п- глицеро-3-глутаровой кислоты.
Получение аналогично примеру 1а из 2,2 г (15 ммоль 1-0-октадецил-2- О-бензил-Зп-глицерина, 50 мл хлороформа, 3 МП пиридина и 1,5 г (13 ммоль) ангидрида глутаровой кислоты.
IR ()(пленка): 1730; 1700.
Сложный резоруфиновый эфир 1-0- октадецил-2-0-бензил-8п-глицеро-3глутаровой кислоты.
Ь). Получение аналогично примеру 1Ь из 1,7 г (3,1 ммоль) 1 За и 1,3 мл хлористого оксалила.
с). Получение аналогично примеру 1с из 0,8 г (37 ммоль) резоруфина, 20 мл диметилформамида, 0,7 мл пиридина и 1ЗЬ.
ДС: Rf 0,68 (уксусный эфир - петролейньш эЛир 1:1).
IR ()(КВг): 1768; 1739.
П р и м е р 14.а). Сложньш моно- . эфир 1,2-диоктаноил-5п-глицеро-3-глу- таровой кислоты.
Получение аналогично примеру 1а из 6,8 г (20 ммоль) 1,2-диоктаноил- , Sn-глицерина, 100 мл хлороформа, 12,5 мл пиридина и 5,8 г (50 ммоль) ан1:идрида глутаровой кислоты.
ДС: Rf 0,49 (уксусный эфир - петролейный эфир 1:1).
Сложный резоруфиновый эфир 1,2- диоктанош1-8п-глицеро-3-глутаровой кислоты.
Ь). Получение аналогично примеру 1Ь из 2,2 г (5 ммоль) 14а и 2,2 мл д5 хлористого оксалила.
с). Получение аналогично примеру 1с из 1,05 г (5 ммоль) резоруфина, 30 мл диметилформамида, 0,75 мл пиридина и 14Ь.
ДС: Rf 0,86 (RP18, ацетонитрил - дихлорметан 1:2).
Пример 15. а). Сложный моноэфир 1,2-диолеил-рац-глицеро-З-глута- ровой кислоты.
Получение аналогично примеру 1а из 3,1 г (5.ммоль) диолеина, 40 мл хлороформа, 3 мл пиридина и 1,5 г (13 ммоль) ангидрида глутаровой кис- лоты.
0
40
50
55
11
ДС: Rf 0,32 (уксусный эфир - п ролейный эфир 1:1).
IR () (пленка): 1740; 1706. Диолеин можно получать в чистой форме из технического диолеина хроматографией на колонне с силикаге- лем при использовании уксусного эфира - петролейного эфира 1:3 в качестве растворителя.
Сложный резоруфиновый эфир 1,2- диолеил-рац-глицеро-3-глутаровой кислоты.
Ь). Получение аналогично примеру 1Ь из 3,5 г (4,8 ммоль) 15а и 1,3 м хлористого оксалила.
с). Получение аналогично примеру 1с иэ 0,9 г (4,2 ммоль) резоруфина, 20 мл диметилформамида, 1 мл пиридина 15Ь.
ДС: Rf 0,78 (уксусный эфир - петролейньй эфир 1:1).
Пример 16. Сложный нафтило- вый эфир 1,2-0-дитетрадецил-рац- глицеропимелиновой кислоты.
Получение осзпцествляют аналогично примеру 1 Ob и с из 0,72 г (5 ммоль) 1-нафтола. Очистка Flash- хроматографией на силикагеле с растворителем уксусным эфиром - гекса- ном 1I3.
ДС: Rf 0,89 (уксусный эфир - петролейный эфир 1:5).
Пример 17. Сложный реэсруфи- новый эфир 1,2-диолеш1-рац-глидеро- 3-глутаровой кислоты.
10,3 г (14,2 ммоль) сложного мо- нозфира 1,2-диолеил-З-глицеро-глу- таровой кислоты по примеру 15а, 3,2 г (15 ммоль) резоруфина, 6,2 г (30 ммоль) дициклогексилкарбодиими- да и на кончике шпателя 4-диметил- аминопиридин перемешивают в 75 мл диметилформамида 2-3 дня при комнатной температуре. Затем разбавляют уксусным эфиром и осадок отфильтровывают. Фазу уксусного эфира взбалтывают с 1 н. соляной кислотой и сушат над сульфатом натрия. После отгонки растворителя остается маслянис тый остаток, который очищают хроматографией на колонне с силикагелем (растворитель:уксусный эфир - петролейный эфир 1:1).
Таким образом получают соответст- вующее производное хлорфенолового красного.
ДС: Rf 0,69 (RP18; изопропанол метанол 1:2).
)
041
0
15
20
25
30
,,
Q j л
5
6712
Пример 18. Получение сложного моноэфира 1,2-0-диоктил-З-пимелино- вой кислоты.
Стадия I:. синтез сложного бензило- вого моноэфира пимелиновой кислоты.
Стадия 2: аналогично примеру 1Ь из 2,5 г (10 ммоль) сложного бензи- лового эфира пимелиновой кислоты; полученное масло закапывают в раствор 3,2 г (10 ммоль) 1,2-0-диoктшl- глицepинa, 7 мл пиридина; обработка аналогично приме. 1с.
Стадия 3: указанный продукт растворяют в 20 мл тетрагидрофурана и после добавки 0,4 г палладия - активированного угля гидрируют. Сырой продукт очищают на колонне с силикагелем; растворитель уксусный эфир - петролейньй эфир 1:1.
ДС: Rf 0,61 (уксусный эфир - петролейный эфир 1:1)
IR ( ) (пленка): 1740; 1710.
Пример 19. Синтез сложного моноэфира 1,2-диолеил-глицеро-3-глутаровой кислоты.
а). Сложный трихлорзтиловьш эфир 1,2-0-изопропилиден-глидеро-З-глута- ровой кислоты.
Стадия 1: 5,55 г (42 ммоль) изопро- пилиденглидерина и 12 г (45,3 ммоль) 2,2,2-трихлорэтш1-гидро-глутарата растворяют в простом диметиловом эфире этиленгликоля и смев1ивают с 10,5 г (51 ммоль)дидиклогексилкар- бодиимида, после двухдневного перемешивания фильтруют и подвергают перегонке; т.кип, ; (0,1 торр), бесцветное масло.
ДС: Rf 0,82 (адетон - хлороформ 1:1).
Стадия 2: полученное масло растворяют в П мл простого эфира, смешивают с 3 мл метанола и 3 мл 3 н. соляной кислоты и перемешивают 12 ч при комнатной температуре; органическую фазу встряхивают с нacьш eнным раствором бикарбоната натрия, затем с насыщенным раствором хлористого натрия и сзппат; после удаления растворителя остается маслянистый остаток.
ДС: Rf 0,23 (уксусный эфир - петролейный эфир 1:1).
Ь). Сложный трихлорэтиловый эфир 1,2-диолеш1-глидеро-3-глутаровой кислоты.
Стадия 3: 6,1 г (18 ммоль) полученного продукта и 7,84 г (38 ммоль) олеиновой кислоты растворяют в
100 мл простого диметилового эфира ч этиленгликоля и закапывают раствор 10,5 г (37 ммоль)дициклогексилкар- бодиимида в 50 мл простого диметилового эфира этиленгликоля; после 12-часового перемешивания при комнатной температуре фильтруют и последовательно встряхивают с 3 н. соляной кислотой с раствором бикарбоната натрия, затем с водой. После сушки и концентрирования органической фазы остаток хроматсграфируют на силика- геле.
Стадия 4: слохньш моноэфир 1,2- диолеш1-глицеро-3-глутаровой кислоты отщепление защитной группы трихлор- этила осуществляют известным методом. .
П р и м е р 20. а). Сложный моноэфир I,2-0-дидецил-рац-глицеро-З- пимелиновой кислоты.
Получение аналогично примеру 1а из 5,6 г (15 ммоль) 1,2-0-дидецил- глицерина, 100 мл хлороформа, 3,2 мл .пиридина и 4,0 г (28 ммоль) ангидрида пимелиновой кислоты.
ДС: Rf 0,36 (уксусный эфир - гексан 1:1).
IR (см-)(пленка): 1735; 1710.
Сложный резоруфиновый эфир 1,2-0- дидецил-рац-глидеро-3-пимелиновой кислоты.
Ь). Получение аналогично примеру 1Ь из 3 т (5,8 ммоль) 20а, 50 мл хлороформа и 2,2 мл хлористого оксалила
с). Получение аналогично примеру 2с из 1,1 г (5 ммоль) резоруфи- на, 1 мл (6,4 ммоль) 1,8-диазаби- цикло-(5,4,0)-ундец-7-ена и 20Ь.
ДС; Rf 0,71 (уксусный эфир - гексан 1:1).
IR (см - )(пленка): 1755; 1720.
П р и м е р 21. а). Сложный моно- эфир 1,2-0-дилаурил-рац-глицеро-З- азелаиновой кислоты.
;
.
10
15
-
604167
Получение аналогично примеру 1 а из 6,7 г (15,6 ммоль) 1,2-0-дилаурил- глицерина, 100 мл хлороформа, 3,2 мл пиридина и 4,0 г (23 ммоль) ангкдри- i да азелаиновой кислоты.
ДС: Rf 0,22 (уксусный эфир - гексан 1:1)
IR ()(пленка): 1738; 1710.
Сложный резоруфиновый эфир 1,2-0- дилаурил-рац-глицеро-3-азелаиновой кислотыо
Ь). Получение аналогично примеру 1Ь из 1,5 г (2,5 ммоль) 21а 30 мл . хлороформа и 1,5 мл хлористого оксалила.
с). Получение аналогично примеру 2с из 0,55 г (2,5 ммоль) резоруфи- на, 25 мл хлороформа, 0,5 мл 20 (3,2 ммоль) 1,8-диaзaбициклo-(5,4,0)- yндeц-7-eнa и 21Ь.
ДС: Rf 0,78 (уксусный эфир - гексан 1:1).
IR () (пленка):, 1762; 1740.
П р и м е р 22. 60 мл дистиллированной воды растворяют при перемешивании 1. ,2 г дезоксихолата натрия и 0,15 мл колипазы (от свиньи). При сильном перемешивании впрыскивают туда по возможности тонкой струей 70 мг субстрата липазы сложного ре- зоруфинового эфира 1,2-0 -диоктил- рац-глицеро-3-азелаиновой кислоты (пример 4) в 1,7 мл п-пропанола при давлении. Раствор, который в 200 мл дистиллированной воды содержит в растворенном виде 1,5 г мочевины, 1 г дезоксихолата натрия, 200 мг хлористого натрия, 800 мг TRIS и 107 мг TRIS - НС1 буфера, хорошо смешивают с полученной Bbmie эмульсией.
2,5 мл изготовленного таким путем раствора смешивают с 100 мл пробы (сыворотка). Реакцию проводят при 578 мм рт.ст. с показаниями на фотометре.
При известной по стандарту активности липазы вычисляют активность липазы пробы следующим образом:
25
30
35
40
45












| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных резоруфина | 1986 |
|
SU1621811A3 |
| Способ получения тризамещенных аминов или их фармакологически-приемлемых солей в виде рацемата или оптически активных изомеров | 1989 |
|
SU1731044A3 |
| ФОСФОЛИПИДНЫЕ ПРОИЗВОДНЫЕ НУКЛЕОЗИДОВ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1991 |
|
RU2104282C1 |
| Способ получения сульфонамидов алкилфенилкарбоновых кислот | 1981 |
|
SU1088664A3 |
| Способ получения 12-эпидигоксина или его производных | 1976 |
|
SU668612A3 |
| Способ получения N-замещенных производных азиридин-2-карбоновой кислоты или натриевой соли кислоты | 1985 |
|
SU1431676A3 |
| Способ получения производных резазурина или резоруфина в виде таутомеров | 1986 |
|
SU1574173A3 |
| Способ получения аммонийалкиловых эфиров фосфорной кислоты (его варианты) | 1981 |
|
SU1241994A3 |
| Способ получения производных феноксиалкилкарбоновой кислоты,их солей,сложных эфиров и амидов | 1979 |
|
SU1052157A3 |
| Способ получения производных оксимов пировиноградной кислоты или ее амидов | 1981 |
|
SU1279526A3 |
Изобретение относится к аналитической химии. Цель изобретения - повышение чувствительности. Способ определения липазы посредством воздействия на субстрат липазы с образованием хромогена предусматривает использование субстрата общей формулы X-CO-A-CO-Y-CH2-CH(Y-R)-CH2-Z-R1, где A - алкильная или алкиленовая группа с 2 - 12 C-атомами, R и R1, которые могут быть одинаковыми или разными, каждый обозначают алкильную группу с 6 - 18 C-атомами, один из остатков R и R1 также обозначает атом водорода. X - резоруфин, 6-метилрезоруфин, 4,6-диметилрезоруфин, 1,6-диметилрезоруфин, 8-этилрезоруфин и 8-бромрезоруфин и каждый Y и Z, независимо друг от друга обозначают -S- или -О-, Z также обозначает -CH2-. Количество освобожденного ароматического гидроксильного или тиолового соединения непосредственно или после сочетания с подходящим хромогеном оптически определяют по получившейся окраске. 3 табл.
активность
активность
Д Е/мин.
(пробы
активписмл/ V-U .-,,
,i Z§SB§2l2- iE ° b 2.
л .«г«
Д Е/мин
Вычисление активности липазы пробы возможно также по следующей формуле:
активность
(пробы)
(ед./1)
lOOO - V-n1kr ««V
Д Е/мин.
U
л .«г«
Д Е/мин
(стандарт)
где V
ges
5
- общий подъем испытывае- мой исходной смеси, см ;
I
гЗ.
V пробы- объем пробы, см ,
- коэффициент экстинкции
хромогена при 578 нм; d - толщина слоя кюветы,см;
АЕ/мин изменение экстинкции за 1 мин при 578 им.
При названных условиях реакции коэффициент экстинкции составляет 60,65 см.мкмоль
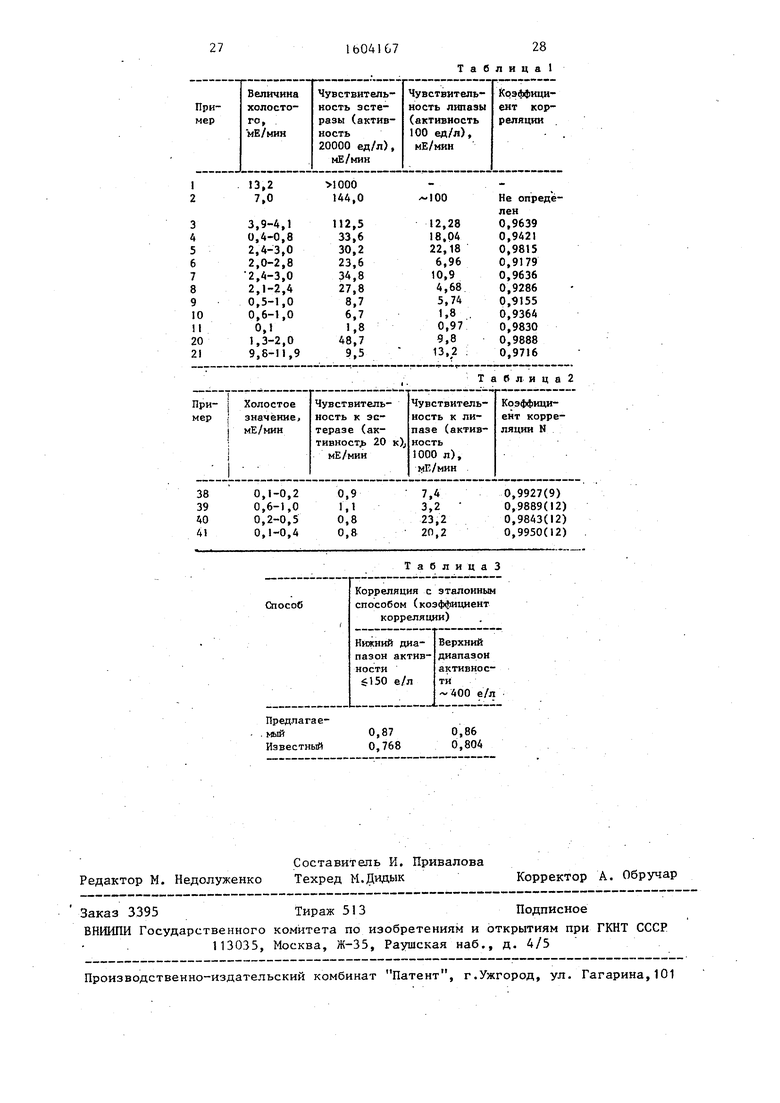
Пример 23. Для различных субстратов липазы определены изменения величины холостого опыта, чувствительность эстеразы и липазы и корреляция к нефелометрическому тесту с помутнением.
Изменение величины холостого опыта определено с реактивом по примеру 1 и различными субстратами липазы Вместо пробы добавляли 100 мл воды и наблюдали по фотометру изменение зкстинкции при 578 (мЕ/мин).
Дпя определения чувствительности эстеразы добавляли вместо пробы 100 мл карбоксилэстеразы (ЕС 3.1.1.1 около 20000 ед/л Берингер Маннхайм ГмбХ, номер определения 10 46 98) и наблюдали, как описано вьше, изменние экстинкциио
Для определения чувствительности липазы вместо пробы добавляли 100 мл липазы (ЕС 3.1.1.3, около 100 ед/л., Берингер Маннхайм ГмбХ, номер определения .41 45 90) и наблюдали, как описано вьше, изменение экстинкции,
Для определения корреляции к фелометрическому тесту с помутнением проводили с возрастающими количествами липазы (0-1000 ед/л) тест с помутнением (Берингер Маннхайм ГмбХ, номер определения 26 23 58), сравнивали с цветным тестом по примеру 22 и определяли коэффициент корреляции,.
Результаты показаны в табл.1.
При мер 24. 8,5 г дезоксихола та натрия, 0,05 г колипазы, 20 г ман нита, 0,05 г хлористого кальция , Оэ82 г хлористого натрия, 2,7 г TRIS и 0,4 г TRIS-HC1 растворяют в 200 мл дистиллированной воды. При перемешивании впрыскивают раствор, который содержит в растворенной форме 0,35 г сложного нафтолового эфира 1,2-0 ДИтетрадецш1-рац-глицеро-3- пимелиновой кислоты в 7 мл пропано- ла. Полученную таким путем эмульсию замораживают при -40°С и подвергают лиофилизации.
70 г полученного лиофилизата растворяют в 2 мл дистиллированной воды
0
5
0
5
0
5
0
5
и смешивают с 100 мл TR-раствора красного паранитроанилина (красный паранитроанилин-4-хлор-З-метилбен- золдиазоний-нафталин-1,5-дисульфо- нат) (231 мг в 10 мл дистиллированной воды).
После добавки 100 мл сыворотки наблюдают за реакцией при 405 нм по фотометру с
Определение концентрации липазы проводят по калибровочной кривой аналогично примеру 22.
Пример 25. В раствор 3,04 г тауродезоксихолата, 2,7 г поливоска 4000, 7 мг хлористого кальция, 0,2 мг колипазы (от свиньи) в 120 дистиллированной воды впрыскивают при перемешивании 150 мг субстрата липазы сложного резоруфинового эфира 1,2-0- дидецил-рац-глицеро-3-глутаровой кислоты в 3,5 мл п-пропанола.
К полученной таким путем эмульсии добавляют следую ций раствор и хорошо смешивают
10 г тауродезоксихолата, 6,4 г поливоска, 50 г маннита, 14 г мочевины, 800 мг хлористого натрия и 15 г ТР.ИС растворяют в 300 мл дистиллированной воды. При помощи раствора ной кислоты устанавливают рН 7,5 о После этого раствор дополняют до 400 мл дистиллированной водой.
2,5 мл полученной таким путем реакционной смеси смешивают с 100 мл сыворотки. Реакцию наблюдают при 578 нм по фотометру.
Оценку проводят, как в примере 22.
П р и м е р 26. В раствор 3,04 г тауродезоксихолата, 2,7 г поливоска 4000, 7 мг хлористого кальция, 0,2 мг колипазы (от свиньи) в 120 мл дистиллированной воды впрыскивают при перемешивании 150 мг субстрата липазы сложного резоруфинового эфира 1,2-0-дидецил-рац-глицеро-З-глу- таровой кислоты в 3,5 мл п-пропанола.
К полученной таким путем эмуль- сии добавляют и хорошо перемешивают следующий раствор.
10 г тауродезоксихолата, 6,4 поливоска, 50 г маннита, 14 г мочевины, 800 мг хлористого натрия, 28 г буфер- ного раствора CHES в 300 мл дистиллированной воды. При помощи раствора соляной кислоты устанавливают рН 8,5. После этого дополняют раствор до 400 мл дистиллированной водой.
1716041
2,5 мл полученной таким путем реакционной смеси смешивают с 100 мл сыворотки. Реакцию наблюдают при 578 им по фотометру.
Оценку производят, как указано в примере 22.
П р и м е р 27, В раствор из 4,0 г тауродезоксихолата Na, 0,06 г хлористого кальция, 0,2 мг колипазы (от Q свиньи), 5,0 г маннита и 2,0 г поливоска 4000 в 100 мл дистиллированной воды впрыскивают при перемешивании 150 мл сложного нафтолового эфира 1,2-0-дитетрадецш1-рац-глицеро-3-пи- 5 мелиновой кислоты, который растворен в 4 мл п-пропанола. При хорошем охлаждении полученную таким путем эмульсию обрабатывают несколько минут ультразвуком 20
Второй раствор содержит в 100 мл 2,4 г тауродезоксихолата Na, 2,0 г TRIS, 12,0 г маннита, 3,5 г мочевины и 0,5 г хлористого натрия. При помо- пщ соляной кислоты устанавливают рН 25 8,3.
Третий раствор содержит 1 г красного паранитроаналина TR (красный па- ранитроаналин TR 4-хлор-метил-бензол-, диазоний-нафталин-1,5-дисульфонат) в ЗО 40 мл дистиллированной зоды в растворенной форме,
5 ч. раствора 1 и 6 ч. раствора 2 смешивают с I ч. раствора 3. Полученным раствором пропитывают пригодную для получения тест-полоски всасывающую бумагу, например, сорта, VS532 фирмы Шляйхер унд Шулл и о сто- рожно сушат в камерной сушилке с цир- куляцией воздуха при температуре от 30 до 654.
До дальнейшего применения рекомендуется хранение в присутствии средства дегидратации.
35
Для испытания на липазу сыворотк
небольшое количество (несколько капель) ее наносят на полоску.
На основании кривой окрашивания в желтый цвет по времени можно еде- лать вывод об активности липазы исследуемой пробы,
П р и м е р 28. а). Сложный моноэфир 1,2-0-дилаурил-рац-глицеро-З- тетрадекандикислоты.
Получение аналогично примеру 1а из 8,6 г (20 ммоль) 1,2-0-дилаурил-. глицерина, 100 мл хлороформа, 4 мл пиридина, 0,4 г диметиламинопириди
Q 5 0
5
О
5
5
на, 9,6 г (40 ммоль) ангидрида двухосновной тетрадекановой кислоты.
ДС: R 0,45 (уксусный эфир - петролейный эфир 1:5).
Сложный (6-метилрезоруфиновый) эфир 1,2-0-дилаурип-рац-глицеро-З- тетрадекановой дикислоты.
Ь). Получение аналогично примеру 1Ь из 3,35 г (5 ммоль) 28а и 2,2 мл хлористого оксалила.
с). Получение аналогично примеру 2с из 1,2 г (5 ммоль) 4-метш1резору- фина, 20 мл хлороформа, 0,75 мл 1,8- диазабицикло-(5,4,0)-ундец-7-ена, 0,1 г диметиламинопиридина и 28Ь. ДС: R 0,63 (уксусный эфир - гексал 1:4).
d). Получают эмульсию, как указано в примере 22„ Однако вместо названного субстрата липазы применяют раствор 70 мг субстрата липазы сложного (6-метилрезоруфинового) эфира 1,2-0-дилаурил-рац-глицеро-З-тетра- декановой дикислоты, растворенного в 1,7 мл п-пропанола.
При этом получены следукщие тест- специфические параметры (ср. пример 23 и табл.1): величина холостого опыта 0,2 мЕ/мин; активность эстеразы 0,7 мЕ/мин; чyвcтвитeльнofeть липазы 23,6 мЕ/мин на 100 ед/л; коэффициент корреляции 0,09509.
П р и м е р 29. Сложный (6-метил- резоруфиновый) эфир 1,2-0-дш1аурил- рац-глицеро-3-глутаровой кислоты,
а). Получение аналогично примерам 7d,-c 2,3 г (10 ммоль). 4-метш1резо - руфина.
ДС: R, 0,68 (уксусный эфир - гексан 1:2).
Ь). Б 60 мл дистиллированной воды растворяют при перемешивании 0,9 г тауродезоксихолата натрия и 0,3 г кол1тазы (от свиньи). При хорошем перемешивании впрыскивают туда раствор сложного (6-метилрезоруфинового) эфира 1,2-0-дилаурил-рац-гл1щеро-3-глу- таровой кислоты, 70 мг в 1,7 мл п- пропанола. Затем добавляют.раствор (200 мл), которьй содержит в 200 мл 0,5 г мочевины, 1 г тауродезоксихолата натрия, 200 мл хлористого натрия и 2,9 г TRIS и устанавливают его величину рН до 7,5. После хорошего перемешивания 2,5 мл полученного таким путем раствора смешивают с 100 мл пробы (сыворотка). Реакцию наблюдают при 578 нм рт.ст. по фото19оценку,
16 как указаметру, производят
но в примере 22,
Тестоспецифические параметры (ср. пример 23 и табл.1): величина холостого опыта П,4 мЕ/мин; чувствительность липазы 28 мЕ/мин на 100 мЕ/мин; коэффициент корреляции 0,988.
Пример 30. 4-Метилрезоруфин. Получают из 7,5 г 2-метш1-4-нитро- зорезорцина, 4,2 г резорцина, 3,6 г пиролюзита, 4,3 МП серной кислоты, 75 мл метанола, 4 г цинкового порошка и 18 мл 25%-ного аммиака.
ДС: R, 0,70 (этанол - ацетон 2:1).
UY/YIS (0,1 М буферный раствор фосфата калия, рН 8,5),(о,кс 579 нм.
2-Метил-нитрозорезорцин получают по немецкому патенту 23 11 574, AI.
Пример 31. Сложньй (4-метил- умбиллифериловьй) эфир 1,2-0-дш1ау- p IЛ-paц-глицepo-3-глyтapoвoй кислоты,
а). 2,75 г (5 ммоль) 7а и 1 г (5 ммоль) 4-метилумбеллиферона раст- воряюТ в 30 мл тетрагидрофурана и затем добавляют 2 г (10 ммоль) ди- циклогексилкарбодиимида и 0,15 г диметиламино-пиридина. После 24-часо- вого перемешивания при комнатной температуре фильтруют и сгущают. Сырой продукт очип ают Flash-хроматографией .
ДС: R 0,40 (уксусньй эфир - петролейный эфир 1:3).
Ь). Эмульсию получают, как указано в примере 22, но вместо использованного там субстрата липазы применяют 35 мг сложного (4-метилумбеллиферило- вого) эфира 1,2-дш1аурил-рац-глицеро 3-глутаровой кислоты, растворенного в 1,7 мл п-пропанола о
Реакцию наблюдают по флуорометру при 25°С, а именно при длине волны возбуждения 364 нм, ширине щели 5 нм и длине волны излучения 448 нм и ширине щели 10 нмс
Тест-специфические параметры (ср пример 23 и табл.1): величина холостого опыта 0,4 мЕ/мин; чувствительность липазы 28 мЕ/мин на 100 единиц/л; коэффициент корреляции 0,9942
П р и м е р 32. Сложньй (р-нитро- тиофениловый) эфир 1,2-0-дилaVpил-paц- глицepo-3-rлyтapoвoй кислоты.
Получение 32 -Ь аналогично примерам 7а-Ъ.
5 О
5
0
20
с). Получение аналогично 1 с из 1,4 г (10 ммоль) р-нитротиофенола, 100 мл диметилформамида, 2,4 мл пиридина, 0,2 г диметиламинопиридина и 32Ь.
ДС: R 0,76 (уксусный эфир - гексан 1:4).
d) . В 27 МП дистиллированной воды растворяют при хорошем перемешивании следующие соединения: 4,83 мг. деоксихолата натрия; 28,00 мг CHES-2- (циклогексиламино)-этан-сульфокисло- та, 17,50 г мочевины, 2,13 мг хлористого натрия, 0,16 мг колипазы свиньи, 0,33 мг хлористого кальция, 152,00мг тауродезоксихолата натрия,
рН раствора 8,3. В этот раствор при хорошем перемешивании впрыскивают раствор сложного (р-нитротиофени- лового) эфира 1,2-0-дилаурил-рац-гли- церо-3-глутаровой кислоты. Затем раствор обрабатывали при охлаждении 2 мин ультразвуком (средней интенсивности) .
В 1 МП полученного таким путем эмульсионного раствора добавляли 50 мл пробы (содержащей липазу человеческой сыворотки) и смешивали. Реакцию наблюдали при 405 нм рт.ст. по фотометру и проводили вычисление, как указано в примере 22.
Тестоспецифические параметры: величина холостого опыта 0,3 мЕ/мин; чувствительность липазы 12,2 мЕ/мин на 100 ед/л; коэффициент корреляции 0,998.
П р и м е р 33. а). Сложньй моноэфир 1-О-(2-метокси-октадецил)-2-0- метйл-рац-глицеро-3-глутаровой кислоты.
Получение аналогично примеру 1а из 3 г (7,7 ммоль) 1-0-(2-метокси-окта- децил)-2-0-метил-глицерина, 25 мл хлороформа, 1,8 мл пиридина, 0,1 г диметиламинопиридина и 1,75 (15 ммоль) ангидрида глутаровой кислоты. Выход 1,5 г (39%).
ДС: R, 0,68 (RP18, ацетон - этанол 1:2).
Сложньй (6-метилрезоруфиновьй) эфир 1-0-(2-метокси-октадецш1)-2-оме- тил-рац-глицеро-3-глутаровой кислоты.
Ь). Получение аналогично примеру 1Ь из 1,5 г (3 ммоль) ЗЗа и 1,5 мл хлористого оксалила.
с). Получение аналогично примеру 2с из 0,68 г (3 ммоль) 4-метилр г
1
зоруфина, 0,45 мл 1 ,8-диазабицикло(5,4,0)-ундец-7-ена и ЗЗЬ .
ДС: R 0,86 (уксусный эфир), d), Тест-эмульсию получают, как указано в примере 22, однако в качес ве субстрата липазы используют сложный (6-метил-резоруфиновый J эфир 1(2-метокси-октадецил)-2-0-метил-рац глицеро 3-глутаровой кислоты.
Спределение концентрации липазы производят через калибровочную прямую из двух стандартов различной концентрации липазы, при которой изменение экстинкции за 1 мин наносят относительно изменения экстинкции.
Величина холостого опыта 8,4 мЕ/ми чувствительность эстеразы 25,3 мЕ/ми чувстбительность липазы 19,0 мЕ/мин на 100 ед/л; коэффициент корреляции 0,9483.
П р и м е р 34. а). Сложный моноэфир 1,2-0-дилаурил-рац-глицеро-З- янтарной кислоты.
Получение аналогично примеру 1а из 8,56 г (20 ммоль) I,2-0-дилаурШ1- глицерина, 4 г (40 ммоль) ангидрида янтарной кислоты, 60 мп хлороформа, 4,6 мл пиридина и 0,24 г диметилами- нопиридина. Продукт кристаллизуют из гексана. Т.пл. 41-43°С.
ДС: R, 0,26 (уксусный эфир - гексан 1:4).
Сложный резоруфиновый эфир 1,2-0-
дилаурил-рац-глицеро-3-янтарной кислоты.
Ь). Получение аналогично примеру 17 из 2,65 г (5 ммоль) 34а, 1,06 г (5 ммоль) резоруфина, 6,18 г (30 ммол дициклогексилкарбодиимида, 0,1 г ди- метиламинопиридина и 50 мл диметил- формамида
ДС: R 0,47 (уксусный эфир - петролейный эфир 1:3).
с). Получают эмульсию как указано в примере 22, однако в качестбе субстрата липазы в этом случае применяют 70 мг сложного резоруфинового эфира 1,2-0-дш1аурил-рац-глицеро-3- янтарной кислоты, растворенного в 1,7 мл п-пропанола.
При этом следующие тест- специфические параметры (ср,пример 23 и табл.1): величина холостого опыта 3,8-4,0 мЕ/мин; чувствительность эс- теразы не определена; чувствительность липазы 8,7 мЕ/мин на 100 ед/л; коэффициент корреляции 0,8793.
6722
П р и м е р 35. а). Сложный моноэфир 2-0-лаурил-октадекандиол (1,2)глутаровой кислоты.,
Получение аналогично примеру 1а из 4,6 г (10 ммоль) 2-0-лаурил-окта- декандиола (1,2), 29 мл хлороформа, 2,3 мл пиридина, 0,12 г диметлламино пиридина, 2,3 г (20 ммоль) ангидрида глутаровой кислоты.
ДС: R 0,54 (петролейный эфир - уксусный эфир 4:1)
Сложный (f-метилрезоруфиновый) эфир 2-0-лаурил-октадекандиол (1,2)глутаровой кислоты.
Ь). Получение аналогично примеру 1Ь.из 1,15 г (2 мноль) 35а и 0,88 мл хлористого рксалила.
с). Получение аналогично примеру 2с из 0,45 мл (2 ммоль) 4-метилрезо- руфина, 20 мл хлороформа, 0,3 мл 1,8-диазабицикло-(5,4,0)-ундец-7- ена, 40 мг диметиламинопиридина и 35Ь„
ДС: R, 0,37 (петролейный эфир - уксусный эфир 5:1).
d). Получают эмульсию, как указано в примере 22, однако в качестве субстрата липазы используют 70 мг сложного (б-метил-резоруфинового) эфира 2-0-лаурШ1-октадекандиол-1,2- 1-глутаровой кислоты растворенного .в 1,7 мл п-пропанолао
В соответствии с примером 23, табл.1 получают следующие тест-специфические параметры: величина холостого опыта 0,3-1,0 мЕ/мин; чувствительность эстеразы 1,0 мЕ/мин; чувствительность липазы 25,5 мЕ/минк хна 100 ед/ло, коэффициент корреляции 0,996с
П р и м е р 36„ а). Сложный моноэфир 1,2-0-дилаурил-рац-З-тиоглицеро- 3-глутаровой кислоты.
Получение аналогично примеру 1а из 2,5 г (4,8 ммоль)1,2-0-дилаурил- рац-З-тиоглицерина 14 мл хлороформа 1 МП. пиридина и 1,1 г (9,6 ммоль) ангидрида глутаровой кислоты.
ДС: RI 0,5 (гексан - тетрагидро- фуран 1:4).
Сложный (6-метилрезоруфиновый) эфир 1,2-0-дилаурш1-рац-3-тиоглице- ро-3-5-глутаровой кислоты.
Ь). Получение аналогично примеру 1Ь из 0s 74 г (1,3 ммоль) Зба и 0,6 мл хлористого оксалила.
с). Получение аналогично примеру 2с из 0,3 г (1,3 ммоль) 4-метилрезо23
руфина, 13 мл хлороформа, 0,2 мл
1,8-диазобицикло-(5,4,0)-ундец-7-ена
27 мг диметиламинопиридина и ЗбЬ.
ДС: R 0,38 (петролейный эфир
уксусньш эфир 17:3).
Использованньй в качестве исходного вещества 1,2-0-дилаурил-рац-З- тиоглицерин получают известным способом следующим образом.
Превращение 1,2-0-дилаурилглицерина с хлорангидридом толуолсульфо- кислоты до дилаурил-глицеро-3-толуол сульфоната, затем реакция с тиомочев ной до соответствующей соли изотиоур ния, последующий гидролиз с соляной кислотой с
ДС: R 0,52 (петролейный эфир - уксусный эфир 49:1).
d). Получают эмульсию, как указано в примере 22. Однако вместо примененного там субстрата липазы используют раствор 70 мг сложного (б-метил резоруфинового) эфира 1,2-0-дш1аурил рац-3-тиоглицеро-3-5-глутаровой кислоты в 1,7 мл п-пропанола
Тестоспецифические параметры: величина холостого опыта 0,2 - 0,9 мЕ/мин; чувствительность эстара- зы 1,3 мЕ/мин; чувствительность ли- паз.ы 4,1 мЕ/мин на 100 ед/л., коэффициент корреляции 0,857.
П р и м е р 37. а). Сложный моноэфир 1,2-8-дилаурил-рац-1,2-дитио- глицеро-3-глутаровой кислоты.
Получение аналогично примеру 1а из 3 г (6,5 ммоль) 1,2-8-дилаурил- 1,2-дитиоглицерина, 30 мл пиридина и 1,5 г (13 ммоль) ангидрида глу- таровой кислоты.
ДС: Rf 0,43 (петролейный эфир - уксусный эфир 1:1).
ДС: Rf 0,37 (уксусный эфир - петролейный эфир 1:4).
Сложный (6-метилрезоруфиновьш) эфир 1,2-8-дилаурил-рац-1,2-дитио- глицеро-3-глутаровой кислоты.
Ь). Ползгчение аналогично примеру 1Ь из 1,2 г (2 ммоль) 37а и 1 мл хлористого оксалила.
с). Получение аналогично примеру 2с из 0,46 г (2 ммоль) 4-метилрезо- руфина, 20 мл хлороформа, 0,3 мл 1, диазабицикло-(5,4,0)-ундец-7-ена и 37Ь.
Примененный в качестве исходного вещества 1,2-8-дилаурил-рац-1,2-ди- тиоглицерин получают следующим образом.
24
В раствор 9 г (160 ммоль)гидроокиси калия в 250 мл этанола закапывают
0
5
10).
при комнатной температуре 10 г (80 ммоль) 2,3-димеркаптопропано- ла в 100 мл этанола. После одночасового перемешивания закапывают раствор 40 г (160 ммоль) додецилбромида в 100 мл этанола. Для дополнения реакции перемещивают еще два дня, затем фильтруют и фильтрат смешивают со льдом. После подкисления 2 н. соляной кислотой трижды экстрагируют простым эфиром, органическую фазу сушат и сгущают. Остаток очищают на колонне с силикагелем (растворитель: уксусный эфир - петролейный эфир 1: ДС: Rf 0,54 (уксусный эфир - петролейный эфир 1:10).
d). Получают эмульсию , как указано в примере 22. Вместо использованного там субстрата липазы применяют в этом случае сложный (6-метилрезоруфиновый) эфир 1,2-5-дш1аурил-рац-1,2-дитио- 5 глицеро-3-5-глутаровой кислоты, 70 мг, растворенные в 1,7 мл п-пропанола.
Холостой опыт 3 мЕ/мин; чувствительность эстеразы 3,4 мЕ/мин; чувствительность липазы 24 мЕ/мин; коэффициент корреляции 0,9943.
П р и м е р 38. 4,6-Диметилрезору- финовый эфир 1j 2-0-дилаурил-рац-гли- церо-3-глутаровой кислоты.
Указанное соединение получают аналогично примерам 7а-с, используя в качестве исходного материала 2,4 г (Ю ммоль) 4,6-диметилрезофурина. Тонкослойная хроматография: Rf 0,63 (смесь уксусноэтилового эфира и гексана в соотношении 1:2).
30
35
40
5
0
5
П р и м е р 39. 8-Бром-резоруфи- новый эфир 1,2-0-дилаурил-рац-глице- ро-3-глутаровой кислоты.
Указанное соединение получают аналогично примерам 7а-с, используя в качестве исходного материала 2,7 г (5 ммоль) 2-бромрезофурина.
Тонкослойная хроматография: Rf 0,6 (смесь уксусноэтилового эфира и гексана в соотношении 1:2)
П р и м е р 40. 8-Этш1резоруфино- вый эфир 1,2-0-дилаурил-рац-глицеро- 3-глутаровой кислоты.
Указанное соединение получают аналогично примерам 7а-с, используя в качестве исходного материала 1,2 г (5 ммоль) 2-этилрезоруфина.
10
20
25
Тонкослойная хроматография: Rf 0,51 (смесь уксуснаэтилового эфира и петролейного эфира в соотнррении .1:3)
П р и м е р 41. 1-,6-Диметилреэору- финовый эфир 1,2-0-дилаурил-рац.-гли- церо-3-глутаровой кислоты.
Указанное соединение получают аналогично примерам 7а-с, используя в качестве исходного материала 1,2 (5 ммоль) 1,6 диметилрезоруфина.
Тонкослойная хроматография: Rf 0,73 (смесь уксусноэтилового и петролейного эфиров в соотношении 1:2),
П р и м е р 42. 4,6-Диметилрезору- jj фин.
Указанное соединение получают таким же образом, как Это описано в примере 30, используя в качестве исходных материалов 60 г 2-метил- 4-нитрсзорезорцина, 43,5 г 2-метил- резорцина, 34 г двуокиси марганца, 40 мл серной кислоты, 400 мл 25%-но- го раствора аммиака и 40 г цинковой пыли.
УФ/VIS . (О, 1 М калийфосфатный буфер с рН 8,5)(сс 585 нм.
П р им е р 43. 2-Бромрезоруфин.
Указанное соединение получают таким же образом, как это описано в примере 30, используя в качестве исходных материалов 19 г 4-бромрезор- цина, И г 4-нитрозорезорцина, 9,7 г двуокиси марганца, 11,5 мл серной КИСЛОТЫ, 115 мл 25%-ного раствора аммиака и 1,5 г цинковой пыли.
УФ/VIS (0,1 М калийнофосфатный буфер с рН 8,5),акс 576 нм.
П р и м е р 44. 2-Этилрезоруфин.
Указанное соединение ползгчают таким же образом, как это описано в примере 30, используя в качестве исходных материалов 5 г 4-ЗТИЛ-6-НИТ- розорезорцина, 3,3 г резорцина, 3 г двуокиси марганца, 3,4 мл серной кислоты, 50 мл 25%-ного раствора аммиака и 4 г цинковой пьши.
УФ/VIS (О,. М калийфосфатный буфер с рН 8,5); Л„о(Кс 573 нм.
П р и м е р 45. 1,6-Диметилрезору- фин.
Ука,занное соединение получают таким же образом, как это описано в . примере 30, используя в качестве исходных материалов 7,2 г 3,5-диокси- толуола, 7,7 г нитрозорезорцина, 4,9 г двуокиси марганца, 6,8 мл сер30
35
40
45
50
55
10
20
25
jj
30
ной кислоты, 60 мл 25%-ного раствора серной кислоты и 6 г цинковой пыли.
УФ/VIS (О,1 М калийфосфатный буфер с рН 8,5) ц.р 574 нм. Цветной тест на липазы (Р 2711.
Результаты определения активности липазы с замещенными резоруфино- вымк производными по примерам 38-41 представлены в табл.2.
Сравнение корреляции способа по изобретению и известного по Курсо- ка показано в табл.3.
I
Формула изобретения
Способ определения липазы, пре- дусматривающий взаимодействие знали- , та с субстратом липазы, приводящее к образованию хромогена, с последующим определением результата оптическим методом, отличающийся тем, что, с целью повышения чувстви- -тельности, в качестве субстрата используют грзшпу вег еств общей формулы
00
н 1}
HjC-y- C-A-C-X
где
35
40
45
50
HC-Y-R
I
HjC-z-Ki
R и R X 5
- алкИльная или алкилено- вая группы с 2-12 атомами углерода; одинаковые или различные, каждый обозначает алкильную группу с 6-18 атомами углерода, причем один из R и R обозначает водород;
резоруфин, б-метилрезору финовый остаток, 4,6-ди- метилрезоруфин, 1,6-ди- метилрезоруфин, 8-этидре : зоруфин и 8-бромрезору фин;
Уи Z - каждый независимо друг от друга означают -Sили -0-;
Z -CHji-,
а оптическим методом определяют количество высвобожденного гидроксиль- ного или тиолового соединегая непосредственно изда после сочетания с соответствующим хромогеном.
Корреляция с эталонным Способспособом (коэффициент
корреляции)
ТаблицаЗ
| .Henning F | |||
| Proelss and Billy W | |||
| Wright Lipoxygenic Micromethod for Specific Determination of Lipase Activity in Serum | |||
| and Duodenal Fluid | |||
| Clinical Chemistry v | |||
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| Передвижной дровокольный станок | 1913 |
|
SU522A1 |
| Shigeru Kurooka, et al | |||
| A | |||
| Novel and Simple Colorimetric Assay for Human Serum Lipase | |||
| J | |||
| Biochem., v | |||
| Горный компас | 0 |
|
SU81A1 |
| Способ получения продуктов уплотнения фенолов с альдегидами | 1920 |
|
SU361A1 |
Авторы
Даты
1990-10-30—Публикация
1986-04-30—Подача