где Rj - Н, ОН или ацилоксигруппа X - хлор или фтор, Cj-С1|-алки или Cj-C -алкоксигруппа; А I дигитоксозильный радикал формулы где Rg Н, ацил, где R и R имеют указанные значения;Нц - водород, гидрируют с помощью гидрида металла в инертном растворителе при 15-50°С и полученное со динение формулы I или выделяют, или в случае, когда Н, Rg и RJ - водород, алкилируют для получения 22-алкилпроизводных формулы IP предпочтительно соответствующим алкилгалогенидом в присутствии гидрид натрия, или ацилируют для получения 12-ацилпроизводных форму,лы I предпочтительно соответствующи ангидридом кислоты в присутствии органического основания. Пример 1. 12 Эпидигоксино 10 г 12-дегидродигоксина, раство ренного в 700 мл тетрагидрофурана (безводного) после добавления 23 г литийтрц-трет-бутоксиалюминий гидри да перемешивают в течение 20 ч при комнатной температуре. После добавл ния 180 мл 20%-ной водной уксусной кислоты и 550 МП воды обрабатывают :хлороформом, хлороформные фазы дваж ды промьшадот 5%-ным раствором бикарбоната натрия и водой. После сушки сульфатом натрия упаривают в вакууме Полученный сырец, смесь 12-эпидигок сина и дигоксина разделяют путем мультипликативного распределения в смеси четыреххлористый углерод - эф уксусной кислоты - метанол - вода, 3:3s2s4. Из упаренной органической фазы получают после кристаллизации из смеси хлороформ - метанол - эфир 5,6 г 12 эпидигоксина, т .пл, 211- 215С.
О
Л&. хч,
Сн f
-о-Х г
ок 24 заключающийся в циклизации соответствуюа.их стероидных эфиров 1. Использование известного метода восстановления кетогруппы комплексными гидридами металлов позволяет получать новые соединения формулы I 2 Цель изобретения - получение новых соединений, расширяющих класс биологически активных карденолидных ГЛИКОЗИДОБ. Цель достигается описываемым способом j заключающимся в том, что соединение формулы II Пример 2. 12-Эпи- -метилдиГОКсии10 г 12-дигидро-j5-метилдигоксина, растворенного в 700 мл безводного тетрагидрофурава после добавления 23 г литийтри-трет-бутоксиалюминий гидрида oбpaбaтывaJoт. так же, как в примере 1, Сырец подвергают мультипликативному распределению в смеси четыреххлористый углерод -- эфир уксусной кислоты - метанол - вода, 4:2:3:3, Упаренные органические фазы после кристаллизации из смеси хлороформ - метанол эфир позволяют получить 5,4 г 12-эпи- 5 -метилдигоксина, т.пл. 221-225 С. Пример 3„ 12-Зпи-/J-метилдигоксин. 2 г 12-эпидигоксина растворяют в 15 Г4Л диметилформамида и обрабатыва от 15 мл толуола, 2,46 г гидроокиси стронция и 1,54 г окиси алюминия {фирмы Мерк, по Брокману), 4,62 г диметилсульфата, растворенного в 25 мл толуола, был добавлены при комнатной температуре при пере1 1е11шваниие Затем смесь перемешивают, в течение 4 ч при комнатной температуре, разбавляют 100 мл хлороформа, отсасывают над силикагелем, проьывают хлороформом, обрабатывают 24 мл пиридина и упаривают в вакууме до получения густого остатка. Этот остаток перено сят в 60 мл хлороформа и три раза промывают по 10 мл воды. Объединенные промывные воды еще раз обрабатывают 10 тп хлороформа и объединенные хлороформные фазы сушат сульфатом натрия и упаривают в вакууме. Полученный сухой остаток разделяют путем мульти пликативного распределения в смеша ной фазе четыреххлори стый углерод уксусный эфир - метанол - вода, 4:2:3:3, Изорганической фазы посл упаривания з вакууме и кристаллиза ции из смеси хлороформ - метанол эфир получают 1,1 г 12--эпи-;3-мети дигоксина, т.пл 220 224°С, Пример 4, 12-Эпи-о ;-метил гоксин. 5 г 12--дегидро-(ji-метилдигоксин растворенного в безводном тетратид фуране (350 мл) после добавления 11,5 г литийтри-трет-бутоксиалюмин гидрида обрабатывают, как описано в примере 1, Для разделения примен смесь фаз четыреххлористый углерод уксусный эфир метанол - вода, 4:2:3:3. Упаренные органические фа подвергают кристаллизации из смеси хлороформ метанол эфир и получ 2.1г 12-эпи ci-метилдигоксин , т.пл. 163-167С. Пример 5. о(.-Ацетил-1 2-эпи дигоксин. 8,9 г диметилацетамида и 12,6 г Х1:иметилсуль)ата перемешивают в тече ние 2 ч при 80°С, затем охлаждают и обрабатывают 100 мл хлороформа и 8.2г безводного ацетата натрия и о тавляют перемешиваться до утра при комнатной температуре. Затем добавляют 2 г 12-эпидигоксина, перемешивают 3 ч при комнатной температуре Органическую фазу после добавления 100 мл хлороформа промывают 5%-ным раствором бикарбоната натрия и водо Полученный сырец разделяют на колон ке, наполненной целлюлозой, пропитанной формамидом, используя смесь циклогексан : уксусный эфир, 1:1. Единые хроматографические фракции подвергают кристаллизации из смеси хлороформ - метанол - эфир и получают 580 мг вС ацетил-12 эпидигоксина, т.пл. 20б-211°С. При м ер 6. 0- UJeтил-12-эпи дигoкcин . 1,2 г 12-эпидигоксина, растворен ного в 12 глл диметилформалМида, обра батывают 240 мг триэтилендиа.мина и 240 мг уксусного ангидрида и оставляют на 24 ч при комнатной тектерат ре. После разбавления 180 мл воды отфильтровывают осадок, сушат и фра ционируют на колонке, наполненной целлюлозой, обработанной формамидом с применением смеси циклогексан - уксусный эфир, 1:1. Единые хроматог рафические фракции подвергают кристаллизации из смеси метанол - вода, 1:1 и получают 520 мг -ацетил-12-эпидигоксинаг т.пл. 278-281°С. Пример 7. 12-Ацетил-12-эпи дигоксин, 2 г 12-эпидигоксин-а, растворенного в 10 t.in пиридина, обрабатывают 920 мг уксусного ангидрида и нагре126вают в течение 5 ч при 40°С, Затем разбавляют водой, обрабатывают хлороформом, хлороформную фазу промывайт 2 н. серной кислотой, раствором соды и водой, упаривают в вакууме и сырец растворяют в 200 мл метанола, посла чего обрабатывают 1,9 г бикарбоната калия и 100 мг карбоната калия в 100 мл воды и нагревают в течение 5 ч при 40°С. После разбавления водой и обработки хлороформом хлороформную фазу упаривают и полученный остаток разделяют на колонке, наполненной целлюлозой, пропитанной фopмaJ идoм, с применением смеси ксилол -- метилэтилкетон, 3:2. Единые хроматографические фракции подвергают кристаллизации из смеси хлороформ - метанол - эфир и получают 410 мг 12-ацетил-12-эпидигоксин, т,пл, ISS-ieS C. Пример 8, С 22-метил-12 эпидигоксин, 1,5 г 12-эпидигоксина, растворенного в 15 рлл диметилсульфоксида, обрабатывают 1,05 мл метилйодида При комнатной температуре, перемешивая, добавляют по порциям в течение 10 мин 210 мг гидрида натрия ( суспензия в масле) Реакционную смесь затем перемешивают еще 10 мин, разбавляют 10 14Л хлороформа, фильтруют через окись алюминия, промывают смесью хлороформ - метанол, itl и фильтрат упаривают в вакууме. Сырец разделяют на колонке, наполненной целлюлозой, пропитанной форма.шдом, с применением смеси ксилол - метилэтилкетон, 2:1. Единые хроматографические фракции подвергают кристаллизации из смеси хлорофорг/. - метанол - эфир - петролейный эфир и получают 360 мг С-22-метил-12-эпидигоксина,т.пл. 166- 70С. Пример 9. С-22-ЭТИЛ-12-зпидигоксин. 2,4 г 12-эпидкгокс1- на, растворенного в 24 мл дл.метилсульфоксида, обрабатывают 1,7 мл этилйодида и 336 мг гидрида натрия (50%-ная суспензия в масле) таким же образом, как в примере 8, Сырец разделяют на колонке, наполненной целлюлозой, пропитанной формамидом, с применением смеси ксилол - метилэтилкетон, 2:1. Единые хроматографические фракции подвергают кристаллизации из смеси хлороформ - -метанол - Эфир и получают 620 мг С-22-этил-12-эпидигоксина, т.пл. 183- 188°С. Пример 10. С-22-н-бутил-12-эпидигоксин, 1,6 г 12 эпидигоксина, растворенного в 16 мл диметилсульфоксида, обабатывают 1,36 W1 п-бутилйодида и 192 мг гидрида натрия (50%-ная суспензия в масле) таким же образом, какописано в при.мере 8„Единые хроматограф1-1ческне фракции подвергают крисаллизации из смеси хлороформ мета-
НОЛ - эфир - петролейный эфир и получают 580 мг С-22-п 5утил-12--ЗПИЯИГОКсина, , . 5б-160С ,
П р и мер 11, С-2.2-этиЛ 12 эпи-ot -метилдигоксин,.
1 г 12-эпи-с- -ме-илдигоксина, ра-створенного Е 10 м.-; диметилсульфок--сида, обрабатывают 0/7 мл этилйодила и 136 Г гиддрИлЕа нэлонп (50о-ная сус-пензия 3 масле), как описано Б примере 8. Сырец разделяют на колонке, наполненной целлюлозой, пропитанной формамидом, с применением омеси циклогексан -- уксусный эйир 2:1, Единые хроматографические фракции подвергают кристаллизации из смеси хлороформ - метанол - sqn-ip и получают 320 мг С--22-этил--1 2 эпи-У. -метилдигокскна, т.пЛа 151-155 С,
При м а р 12. С--22-метиЛ 12-г, -эпи метилдигоксин.,
1,6 г 12--ЭПИ- 0-метилдигокоина , растЕзоренного в 6 мл диметилоульфок-сида, обрабатывают 0,56 MJ; метилйо-дида и .168 мг гидрида натрия (бО%--иал суопензия в мггсле) , как оиисано в примере 8„ Сырец разделяют на колонке наполненной целлюлозой, пропитанной фopмar тадoм с применением омеси пиклогексануксусный эфир, 2t1. Единые хроматографичеокие фраки,11и подверга-от кристаллизации из смеои хлороформ метанол - эфир -- пе тролейный эфир и получают 480 мг С 22-метил 12-эпи-3 -метилдигоксина,, т „ил, 161-16 5° С,
Пример 13„ С--22-ЭТИЛ-12-эпи- j3 Метилди1оксин а
г 12-э1ги-/ -метилдигокоина , растворенного в 24 мл диметилсульфок., 7
сида, обрабатьява-от
и 336 мг гидрида натрия (50%-ная суспензия в масле), как описано в примере 8 о Сырец разделяют на колонке,наполненной целлюлозой, иропитанной формамидом с применением смеси |{сиЛОЛ - метилэтилкетон; 3;1, Единые хроматографические фракции подверга-ют кристаллизации из смеои хлороформ - метанол -- эфир и получают 680 мг С--22-ЭТИЛ--12-ЭПИ- /3 -метилди-гоксина., т,пла 264--269°cJ
П р и м е р 14, С-22-изопроиил-12-эпи- -метилди ГОК СИЕ „
1,6 г 12--эпи- /3 -метилдигоксш-га
растворенного в 16 мл диметилформ-.алида,обрабат1лвают 1,2 мл изопропилйодида .и 192 мг гидрида натрия (50%ная суспензия в масле), как оиисано в примере 8 Сырец разделяют на колонке, наполненной целлолозой, проиитанной формаг.тидом, с применением смеси циклогексан - уксусный эфир, 2:1, Единые хроматографические фракции подвергают кристаллизации из смеси хлороформ - метанол - эфир - петролейный эфир и полуЧЕЯ1Т 320 мг С-22™ -изопропил-12-эпи- fl -метилцигоксина , т,гш, .
При м е р. 1,5. С 22-алл5-:л-12-ЭПИ J3 -метилдигокснн
1,6 г ,У -метилдигоксина, растворенного в 16 мл диметилформами ;.а, обрабатывают 2,й мл аллил бромида и 168 мг гидр1- да натрия ( суспензия в масле), как описано в примере 8. С.ыреи, разделяют на колонке, наио;;неиной целлюлозой, пропитанной (;)ог:;мамидог-,, с применением омеои цик.пот-ексан - уксусный эфир, 2:1, Единые хроматографические фракции подвергают кристаллизации из смеои -хлороформ метанол -эфир - петролейный эфир и получают 360 мг С-22 аллил 12 Эпи-уЗ -метилдигоксина, т.пл, 146 - ,
При м ер 16. 12-Эпи- уЗ -этилдиГОКС1И-1,
5 :г 1 2-дигидро-- -этилдигоксина ; растворенного в 350 мл беззодного тетрагидрофурана, после добавления 11,5 г литийтри-трет-бутоксиалюминий
1И.дрида обраб 1тывают так же, как описанО в примере 1, Сырец разделяют на колонке, наполненной целлюлозой, Гроиитанной формамидорд, о применением смеои циклогекоан - уксусный эфир,
2;1 Единые хроматографические фракции подвергают кристаллизации из смеси хлороформ - эфир и получают 2,2 г 12-эии- и -этилдигоксин.а, т,пл. 156- ,
П р ; мер 17, 12-Эпи- о/ , J3 -ди
метилдигоксин.
2,5 г 12-дигидро- л, -диметилдигоксипа, растворенного в 175 глл без- зо-цного тетрагидрофурана, после добазлеЕ;ия 6 г литийтри-трет-бутоксиалюминий гидрида обрабатывают, как описано в примере 1. Сырец разделяют ла колонке, наполненной целлюлозой, пропитанной формамидом, с применением смеси Циклогексан - уксусный эфир,
2:1, Единые хроматографические фракции подвергают кристаллизации из смеси хлороформ - эфир и получают J , 3 г 12-эпи- c-i ,/3 -диметилдигокоина, тл;л, 225-228-С,
П Р и м ер 18. 12- Ацетил 12-эпи -ji -метнлдигоксип.
8 г 12-эпи- & -1х,етилдигоксина, растворенного в 15 мл пиридина, после добаЕленип 1,4 г уксусного ангидрида
оставляют на 5 ч при комнатной температуре. Затем разбавляют водой, обрабатр-лвают хлорофор1лом, промывают водо-й, с пиатчнад сульфатом натрия и выпаривают в вакууме. Сырец разделяют иа колонке, наполненной целлюлозой,
пропитанной формамидом, с применением cMect циклогексан - уксусный эфир, 2:1. Единые хроматографические фрг1кцни подвергают кристаллизап.ии из смеси хлороформ - эфир - петролейный эфир и получают 450 мг 12 -ацетил--12-зпи-/3 -метилдигоксина, т,пл. 224-226 0.
П р и м ер 19, С-22 Изопропил-12 -эпидигонйии.:,
1,б г 12-эпидитоксина; растворенного в 16 МП диметилсульфоксида. обрабатывают 1,2 мл изопропилйодида и 192 мгтидрида натрия (50%-ная суспензия в масле), как описано в примере 8. Сырец разделяют в колонк наполненной целлюлозой, пропитанной формамидом, с применением смеси кси лол - метилэтилкетон, 2:1, Единые хроматографические фракции подверга ют кристаллизации из смеси хлорофор метанол - эфир и получают 350 мг С 22-изопропил-12-эпидигоксина, т.пл. 166 170С. Пример 0, С-22-н-бутил-12 -эпи- jS -метилдигоксин. 2 г 12-эпи-;3 -метилдигоксина, растворенного в 20 мл диметилформами да, обрабатывают 1,7 мл н-бутилйоди да и 240 мг гидрида натрия (50%-ная суспензия в масле) , как описаьо в примере 8. Сырец разделяют на колон ке, наполненной целлюлозой, пропитан ной формамидогл, с применением смеси циклогексан - уксусный эфир, 3:1, Еди ные хроматографические фракции подвергают кристаллизации из смеси хлороформ - метанол - эфир и получают 550 г С-2-2-н-бутил-12-эпи- /i-метилдигоксина, т.пл, 143-147с. Пример 21. С-22-АЛЛИЛ-12 эпидигоксин . 2 г 12 эпидигоксина, растворенного в 20 мл диметилформамида, обрабатывают 3,5 мл аллилбромида и 140 м гидрида натрия (50%-ная суспензия в масле), как описано в примере 8. Сырец разделяют на колонке, наполне 1но целлюлозой, пропитанной формамидом, с применением смеси ксилол - метилэтилкетон, 2:1. Единые хроматографические фракции подвергают кристаллизации из смеси хлороформ - метанол - эфир и получают 450 мг С-22-аллил-12-эпидигоксина, т.пл. 158-1бЗ°С. Пример 22, ff-ffi -диацетил-12-эпидигоксин, 3 г 12-эпидигоксина, растворенного в 30 мл диметилформамида, после добавления 600 мг триэтилендиамина и 420 мг уксусного ангидрида оставляют на 24 ч при комнатной температуре, затем добавляют еще 0,4 мл уксусного ангидрида и оставляют еще на 24 ч. После разбавления 60 мл отсасывают осадок, сушат и разделяют на колонке, наполненной целлю лозой, пропитанной фор.мамидом, с при менением смеси циклогексан - уксусны эфир, 2:1, Единые хроматограа;)ические фракции подвергают кристаллизации из смеси хлороформ - эфир - петролейный эфир и получают 590 мг ,Sb -диацети -12-эпидигоксинаf т.пл. 2О 6-210 с. Пример 23 12-Пропионил-12 -эпидигоксин, 3 г 12-эпидигоксинаf растворенного в 15 NUI пиридина, после добавления 1,75 г пропионового ангидрида оставляют на 24 ч при комнатной температуре Затем обрабатывают смесь, как описано в примере 7 Сырец разделяют на колонке, нагюлненной целлюлозой, пропитанной а:ормаМИДОМ, с применением смеси циклогексан - уксусный эфир, 1;1. Единые хроматографические фракции подвергают кристаллизации из смеси хлороформ - метанол - эфир и получают 390 мг 12-пропионил-12-эпиднгоксина, т.пл, 136- , Пример 24. 12-Пропионил-12-эпи- fl -метилдигокс Н, 2,5 г 12-эпи- 3 -метилдигоксина, растворенного в 25 мл пиргдина, после добавления 12,5 кш пропионового ангидрида оставляют на 24 ч при ко.мнатной температуре. Затем смесь обрабатывалот, как описано в примере 7„ Chjpeij, разделяют на гсолоЬКе, .чапсл 1енной ггеллюлозой, пропитанной формамидо;/, с применением смеси циклогексан - уксусный эфир, 2:1. Единые кроматографИческие фракции подверга от кристаллизации из смеси хлороформ - эфир - петролейный эфир и ,от 330 г 12-проп онил--12-эпи- -.метилдигоксина, т.пл, 141 - 145С. П р и м е р 25. С- 1 2--ЭПИДИГОКСИН . 1,4 г 12-эпидигоксина, растворенного в 14 мл димет :лформам 1П 5 , сбрабатывают 620 З-брсмпролиг-га и 84 мг гидрида атрия (50.-иая суспензия в масле), как описано з примере 3. Сырец разделяют на кслонко, наполненной целлюлозой, П1ропнтаь:ной формамидом, с применение. смеси циклогексан - хксусг ый эфир, 2:3, Елиные хроматограсически фра ;:цни подвергают коистал;:изации из смеси хлорофор. - метанол - ::фир и получают 350 -пропаогнл-1 2-эпид1-ь7Окс.ина ,- т . 153°С/ П р и м е р 26. С-22-прспа -12-ЭПК-/3 -метилдигоксин , 1,5 г 12-эп1имет1 лдигоксина, растворен iioro в 12 мл дпметил Ьормамида, обрабатывают 1,07 г 3-бромпропина и 144 мг гидрида натрия ( суспензия в масле), как описано в приере 8. Сырец разделяют на колонке, наполненной целлюлозой, прогп танной формамидом, с применением смеси цикогексан - уксусный эф1{р, 2: 1 . Единые хроматографичаские фракции подвергают кристаллизации из смеси хло оформ - эфир - петролейный эфир и олучагот 400 мг С-22-пропаргил-12 эпи- f -метилдигоксина, 187°С, Фопмула изобоетения 1, Способ получения 12--зпидигок ина или его производных общей форулы I этил или агдетильный остаток; - водород, ацетильная15 группа, пропионильный остаток;о т л и ч соединение Ч,- I водород, алкильная группа с 1-4 атомами углерода, аллильный остаток пропаргильный остаток, ющийся тем, что бщей формулы II
R J и Rg имеют указанные значения, R( - водород, гидрируют с помощью
гидрида металла в инертном . растворителе при 15-50°С и полученное соединение формулы- 1 или вьщеляют, или в случае, когда
R(, R, Rj - водород, алкилируют ацйлируют.
2, Способ по П.1, о т л и ч а ющ и и с я тем, что для получения 22-алкилпроизводных формулы I алкилирование проводят соответствующим
алкилгалогенидом в присутствии гидрида натрия.
3. Способ поп,1, отличающийся тем, что для получения
12-ацилпроизводных формулы I ацилирование проводят с помощью соответствующего ангидрида кислоты в присутствии органического основания. Источники информации, принятые во
внимание при экспертизе
1.Патент СССР № 357725, кл. С 07 J 19/00, 31..
2.Бюлер К а, Пирсон Д. Органические синтезы. М,, 1973, Ч.1, .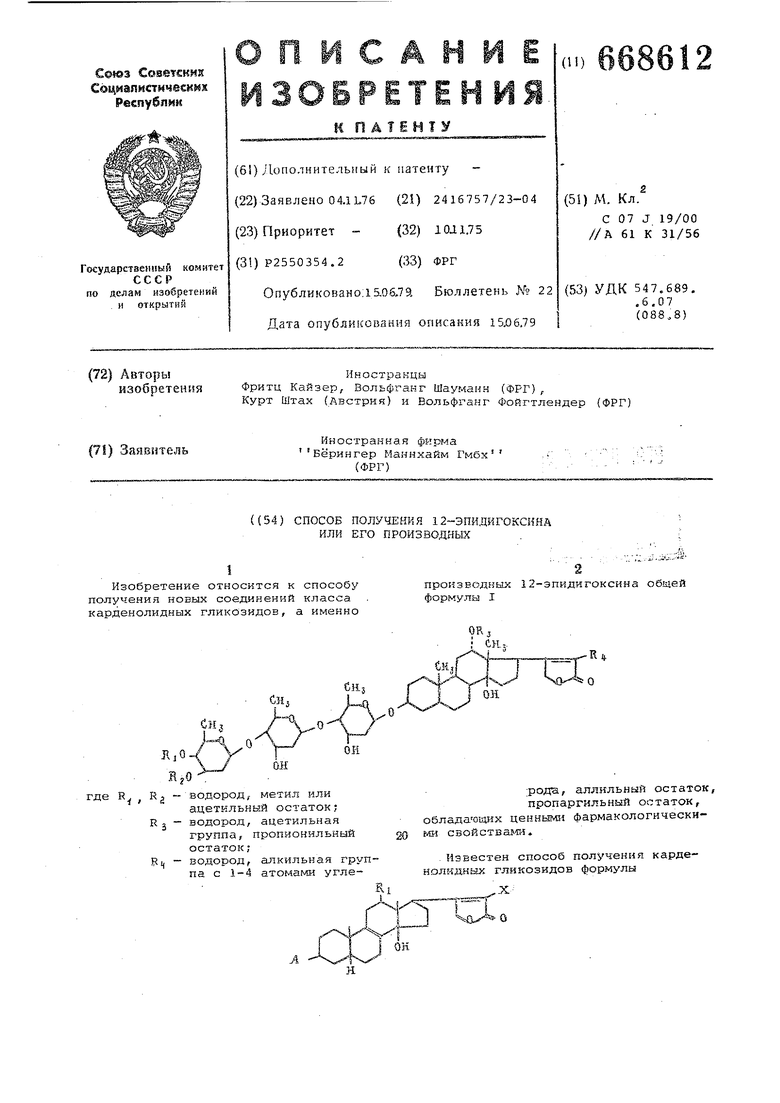





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных фенилацетонитрила или гидратов, или дигидратов их оксалатов, или цитратов | 1985 |
|
SU1508956A3 |
| Способ получения производных азиридина | 1977 |
|
SU673167A3 |
| Способ получения производных аминопропанола или их солей | 1977 |
|
SU1041033A3 |
| Способ получения производных 1-ацил-2-цианоазиридинов или их солей | 1978 |
|
SU1077565A3 |
| Способ получения производных индазола | 1977 |
|
SU680643A3 |
| Способ получения индоксильных или тиоиндоксильных сложных эфиров аминокислот или пептидов | 1981 |
|
SU1156595A3 |
| Способ получения -3- (3,4-диоксифенил) -2-метилаланинпептидов | 1976 |
|
SU656505A3 |
| Способ получения производных пиперидинопропила или их фармацевтически приемлемых солей | 1980 |
|
SU1021342A3 |
| Способ получения производных аминопропанола или их солей | 1980 |
|
SU1243622A3 |
| Способ получения производных аминопропанола или их фармацевтически приемлемых гидрогалогенидов | 1981 |
|
SU1277889A3 |


Авторы
Даты
1979-06-15—Публикация
1976-11-04—Подача