4
а:






| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения тиазоло [4,5-с] хинолина или его кислотно-аддитивных солей | 1986 |
|
SU1544190A3 |
| Способ получения производных 12Н-дибензо( @ , @ )(1,3,6)диоксазоцина в виде их кислотно-аддитивных солей | 1988 |
|
SU1641190A3 |
| Способ получения производных аминоалканоилдибензо ( @ , @ ) (1,3,6) диоксазоцина или их фармацевтически приемлемых аддитивных солей с кислотами | 1987 |
|
SU1575938A3 |
| ПРОИЗВОДНЫЕ 2-МЕРКАПТОБЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЕ СЕЛЕКТИВНОЙ АНКСИОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ | 1994 |
|
RU2061686C1 |
| 2-ФЕНИЛ-2-МЕТИЛАМИНОЭТОКСИ-1,7,7-ТРИМЕТИЛБИЦИКЛО[2,2,1]ГЕПТАН, ЕГО ОПТИЧЕСКИ АКТИВНЫЕ ИЗОМЕРЫ И ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ ДЛЯ ФАРМАЦЕВТИЧЕСКИХ КОМПОЗИЦИЙ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1997 |
|
RU2199523C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНКСИОЛИТИЧЕСКИМ ДЕЙСТВИЕМ, НА ОСНОВЕ ГИДРИРОВАННЫХ ПИРИДО(4,3-b)ИНДОЛОВ (ВАРИАНТЫ), ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2007 |
|
RU2338533C1 |
| Способ получения производных иминотиазолидина или их гидрохлоридов | 1986 |
|
SU1549480A3 |
| Способ получения производных иминотиазолидина или их гидрохлоридов | 1986 |
|
SU1375132A3 |
| СПОСОБ ЛЕЧЕНИЯ СОСТОЯНИЯ СТРАХА ИЛИ ЛЕЧЕНИЯ И/ИЛИ ПРЕДУПРЕЖДЕНИЯ СОСТОЯНИЯ ПАНИКИ, ОЧИЩЕННЫЙ БЕЛОК, СПОСОБНЫЙ СВЯЗЫВАТЬ ГАБАПЕНТИН, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ УСПОКОИТЕЛЬНЫМ, ПРОТИВОПАНИЧЕСКИМ И ПРОТИВОСУДОРОЖНЫМ ДЕЙСТВИЕМ | 1995 |
|
RU2168982C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИДЕПРЕССАНТНЫМ, АНКСИОЛИТИЧЕСКИМ, НЕЙРОПРОТЕКТОРНЫМ И ИММУНОСТИМУЛИРУЮЩИМ ДЕЙСТВИЕМ | 2010 |
|
RU2429834C1 |
Изобретение касается холинтиоэфиров, в частности получения соединений общей ф-лы: @ , где R1=C1-C3-алкил, C2-C5-алкенил (или алкинил)
X1 и X2 (равны или различны) - H, галоген, при условии, что если R1 - этил, то по меньшей мере один из R1, X2 и X2≠H, или их фармацевтически пригодных солей присоединения кислот, обладающих анксиолитическим действием, что может быть использовано в медицине. Цель - создание новых более активных веществ указанного класса. Синтез ведут введением группы R1 в соответствующий тиол с помощью R1 - X, где X - удаляемая группа, с последующим выделением целевого продукта или переводом его в нужную соль. Новые вещества в сравнении с известным хлордиазоэпоксидом значительно активнее, например, 3-амино-4-этилтио-7-хлорхолин гидрохлорид в 20 раз активнее при дозе 10 мг/кг и токсичности 465 мг/кг (для ЛД50), при меньшем в 5 раз седативном эффекте. 6 табл.
Изобретение относится к способу получения новых простых хинолинтио- эфиров ИЛИ к их фармацевтически пригодным солям присоединения кислот, обладающим ценными терапевтическими cвoйcтвa и.
Цель изобретения - синтез новых соединений в ряду хинолинтиоэфиров.
до своей активности превосходящих структурный аналог с той же активностью.
Пример. 17,62 г (0,1 моль) З-амино-4-хинолинтиола растворяют в 50 мл 2М раствора гидроксида натрия, после чего при температуре ниже 40°С добавляют 21,29 г (0,15 моль)
ы
е.тилиодида. Реакционную смесь пере- -шивают час при . Продукт экстагируют хлороформом, осветляют активным углем и концентрируют. Полу- чают 18,6 г З-амино-4-метилтиохиноли- на. BbikoA 94,6%. Т.пл. 9б-98°С (из метанола).
19 г (0,1 моль) указанного осно вания растворяют i 150 мл этилацета- -JQ та, после чего добавляют солянокислый этанол. Получают 21 г З-амино-4- . метилтиохинолин гидрохлорида. Выход 95%, Т.пл. 228-229°С (разложение).
И р и м е р ы 2-11. По аналогии с f5 примером 1 получают следующие, пере- численные в табл.1, соединения.
Пример 12. 21,06 г (0,1 моль) 3-амино-7-хлор-4-хинолинтиола раст- 20 Воряют в 100 мл 2М раствора гидрокси- да натрия. После добавки 23,30 г (0,125 моль) этилового эЛира.бензол- сульфокислоты реакционную смесь кипятят с обратным холодильником в те- 25 чение 2 ч.
Образовавшийся продукт экстрагируют хлороформом. Хлороформньш раствор осветляют активным углем,высушивают и подкисляют солянокислым СПИр- 3Q
том. Получают 24,0 г З-амино-4-этил- тио-7-хлорхинолин гидрохлорида. Выход 852.. После кристаллизации из метанола продукт плавится при 212 - 216°С (разложение). Продукт иденти- 35 чен полученному в примере 5 соединению.
П р и м е р 13. 22,67 г (0,1 моль) З-амино-4-метилтиохинолин гидрохлорида или 19,02 г (0,1 моль) соот- дО ветствующего основания растворяют в 125 мл пиридина, после чего при 10-15°С добавляют 10,7 г (0,105 моль) уксусного ангидрида. Когда желтая окраска раствора исчезнет, реакцион- 45 ную смесь вьтивают в 1000 мл воды. Выделившиеся белые кристаллы отфильтровывают. Получают 20,9 г-.З-шдётил- амино-4-метилтиохинолийа. Выход 90%. Т.пл. 137-138°С (из этилацетата).Q
П р и м е р ы 14-19. По аналогии с примером 13 получают указанные в табл.2, соединения.
П р и м е р 20. 21,06 г (0,1 моль) 3-амино-7-хлор-4-хинолинтиола растворяют в 100 мл 2 М раствора гидрок- сида натрия, после чего добавляют 19,27 г (0,125 моль) диэтилсульфата. Реакционную смесь кипятят с обратным
холодильником в течение 2ч, затем охлаждают до комнатной температуры и экстрагируют дихлорэтаном. Дихлор- этановый раствор высушивают, осветляют и выпаривают. Получают 20,2 г 3-амино-4-этилтио-7-хлорхинолина. Выход 85%. После кристаллизации из метанола продукт плавится при 105-106°С.
11,9 г (0,05 моль) указанного основания обрабатывают 150 мл этилаце- тата. После добавки солянокислого этанола отфильтровывают выделившиеся кристаллы. Получают 13,0 г 3-амино- 4-этилтио77-хлорхинолин гидрохлорида Выход 95%. Т.пл. 212-216 0. Продукт идентичен полученному в примере 5 соединению.
Пример21.По аналогии с примером 20 получают 3-амино-7-хлор-4- метилтиохинолин гидрохлорид. Выход 80%. Т.пл. 235-237°С.
П р и м е р 22. Описанным в примере 1 способом .получают следующие сое- нения: 3-амино-4-этилтио-6-хлорхино- лин гидрохлорид (выход 85%, Т.пл. 250-252°е); 3-амино-4-этш1тио-6,7- диметоксихинолин гидрохлорид (выход 80%, Т.пл. 210-212 С).
Фармакологический спектр действия предлагаемых в изобретении новых соединений общей форкулы I доказывается, руководствуясь тест-испытаниями типичного представителя. В качестве тест-соединения использ.уется 3-амино- 4-этилтио-7-хлорхинолин гидрохлорид (далее называется соединение А).
Острая токсичность. Определяется на СРУ-крысах с весом тела 100-160 г Используют по 10 крыс на каждую подопытную группу. Соединение А вводится в объеме 10 мл/кг орально. Животных перед началом опыта в течение 16 ч не кормят. Каждую дозу вводят группе крыс, состоящей из 50% самцов и 50% самок животных. .Регистрируют происшедшую в течение 48. ч гибель. ЛД 5(j -значения определяют с, помошью метода Litchfield и Wilcoxon; Щ,о 465 мг/кг перорально.
Определение корреляций между анк- сиолитическим и седативным действием. Измерение анксиолитического действия теет-соединения основано на том принципе, что наблюдают проявляемую в конфликтной ситуации активность тест- роединения. Осуществляется награди- тельная реакция, после чего эту наступившую реакцию оттесняют благодаря
наказанию. Анксиолитическое действие измеряется на основании определения, вызванного за счет тест-соединения увеличения реакции наказания. В качестве меры седативного действия служит вызванное тест-соединением уменьшение реакции ненаказания.
Подопытных крыс лишают корма в течение 96 ч; в течение этого периода времени, однако, животные получают питьевую воду для выживания. В течение четырехдневного периода отсутствия корма животные выпивают около
7 мл воды, причем прием воды крысами, 55 РОЛЬНЫМ значением (безнаказуемое зна- которые получают сухой корм,возрас- чение).
После 96-часового периода лишения корма животных переправляют на час в устройство. Очень голодные крысы 20 спустя длительный период
тает до 35 мл/дн. Это означает, что если питьевая труба электрически связана с образующей дно клетки решеткой и животным, которое пытается пить, систематически подвергают удару электрическим TOKQM, то крысу, которая не может принимать корм без питья, максимально заставляют устранять препятствие на пути. Указанньй тест представляет собой очень чувствительный метод определения анксио- литического действия.
Самцов СРУ-крыс (вес тела 230 голоданияв первый час съедают 5-6 г кормовых гранул. Поглощение воды очень голод- ными крысами измеряется в первый час периода кормления, в ненаказуемой 25 группе крыс прием воды составляет . 6-7 мл. При воздействии наказания прием воды снижается до величины ниже 3 мл.
Тест-соединение вводится перенте250 г) постоянно держат на стандарт- 30 рально в дозе 0,5 мл/100 г веса тела.
ных кормовых гранулах; животные получают водопроводную воду для выживания. Животных в виде групп, состоящих из 10 крыс каждая, держат в течение 2 нед при стандартных условиях окружающей среды (при 22-24°С) вплоть до начала испытания. Содержащихся отдельно в клетках крыс лишают корма в течение 96 ч, с начала испытания животные получают водопроводную воду для выживания.
После испытаний отбирают тех животных, у которых в период голодания уменьшение веса тела составляет не более, чем 80 г.
Уменьшение веса тела используемых в вышеуказанном тесте 550 CFY самцов крыс составляет в среднем 66 г.
Другая точка зрения в.выборе животных в том, что животные после периода 50 мг/кг.
голодания.визуально обладают хорошим физическим состоянием и должны показывать нормальную активность. Из-за неудовлетворительного физического состояния нужно исключать менее чем 10% животных.
Для испытания используют коробку (39x27x12 см), которая изготовлена из прозрачного плексигласа и снабже
на решетчатым дном (для кормо вых гранул) и трубой для питьевой воды. Решетчатое дно, труба для питьевой воды и электрический стимулятор (brass 48) электрически связаны с цепью тока, в интервалы времени 20 с осуществляются длительностью 10 с электрические удары током. Параметры тока (100 В, 25 Ом, 7,5 с, 5 Гц) эмпирически выбираются так, что электрические удары током в случае очень голодных крыс уменьшают принятие воды на одну треть по сравнению с контПосле 96-часового периода лишения корма животных переправляют на час в устройство. Очень голодные крысы спустя длительный период
голодания в первый час съедают 5-6 г кормовых гранул. Поглощение воды очень голод- ными крысами измеряется в первый час периода кормления, в ненаказуемой группе крыс прием воды составляет 6-7 мл. При воздействии наказания прием воды снижается до величины ние 3 мл.
Тест-соединение вводится перенте5
0
5
Из-за длительного периода лишения корма мы воздерживались от орального введения биологически активного вещества.
Для статического анализа служит Student t -тест. Анксиолитическое действие определяется на наказываемых, а седативная активность - на ненаказываемых животных.
Корреляция между анксиолитичес- кими и седативными действиями хлор- диазоэпоксида (действие на ненаказуемое и наказуемое поведение в конфликтном тесте) представлена в табл.3.
Хлордиазоэпоксид.оказывает характеристическое анксиолитическое действие в дозе 0,1 мг/кг подкожно,причем седативная доза составляет
Так как хлордиазоэпоксид оказывает свое действие как воздействующий на бензодиазепиновые рецепторы аго- нист, анксиолитическое действие это- биологически активного вещества антагонизируется за счет обозначаемых как R 0-15-1788 селективных антагонистов бензодиазепиновых рецепторов.
Антагонизирование анксиолити.ческо действия хлордиазоэпоксида благодаря
RO15-1788 в конфликтном тесте представлено в табл.4,
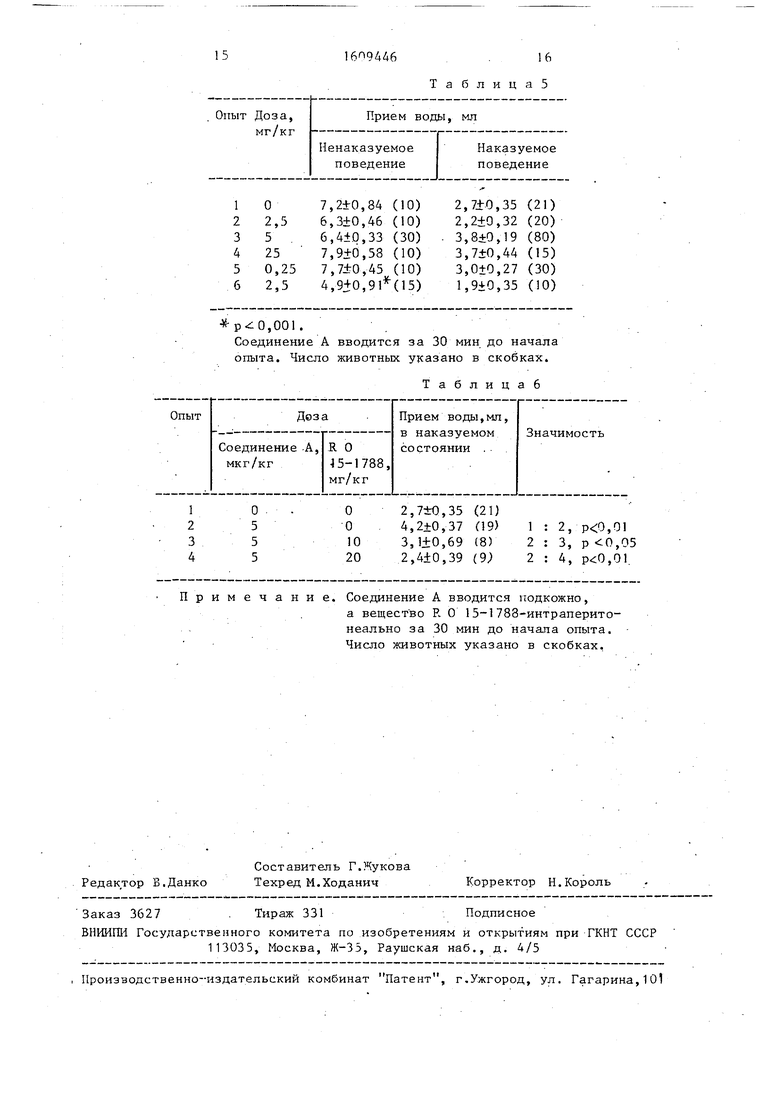
Анксиолитическая активность соединения А на ненаказуемое и наказуемое /товедение в конфликтном тесте дана в табл.5.В этом тесте соединение А показывает примерно в 20 раз усиленное анксиолитичеекое действие, чем хлор- диазоэпоксид.
Антагонизирование анксиолитической активности соединения А за счет антагонистов R 0-15-1788 в KOHduiHTHOM тесте показано в табл.6. I
Найдено, что соотношение седатив- ных и анксиолитических доз для хлордиазоэпоксида составляет 10:0,1 - 100 (см. табл.3), причем в случае соединения А это соотношение составляет 2,5:0,005 500 (см. табл.5. Определение связывания соединения А с бензодиазепиновыми рецепторами. Ин витро связывание соединения А, по сравнению с хлордиазоэпокси- дом, определяется на препаратах мозговых мембран крыс. Кору головного мозга самцов СРУ гомогенизируют в 0,32 М сахарозе при применении снабженного тефлоновой ступкой стеклянного гомогенизатора. Ядро (Nukleus) уплотняют (сжигают) в течение 15 мин при lOOOg. Надосадочную жидкость центрифугируют при 40000g в течение 15 мин. Осадок, после центрифугирова- йия гомогенизируют в 5 мМ трис-цит- ратном буфере (,1) с помощью Политрона Р 10 и лизируют при О С в течение 15 мин. Смесь центрифугируют при 40000g в течение 15 мин, осадок после центрифугирования обрабатывают в 50 мМ трис-цитратном буфере (рН 7,1) и оставляют на ночь при -20 С. После размораживания и центрифугирования (при 40000g, -в течение 15 мин) осадок после центрифугирования промывают трижды 50 мМ трис-цитратным буфером (рН 7,1). Таким образом, полученный осадок после центрифугирования обрабатывают в объемном соотношении 1:30 указанным буфером.
Н-Диазепам (удельЛиганд: 2 нМ ная активность 86 Ci (мнллимоль), Ин кубация: при 0-4 С, в течение часа, в 50 м1- трис-цитратном буфере (рН 7,1). Конечный объем 0,25 мл.
5
0
5
0
5
0
5
0
5
Последняя концентрация белка примерно 0,5 мг/мл.
Связывание прерывают путем разбавления холодным буфером, и смесь быстро фильтруют через Фильтровальную бумагу GF/B Ватман. Для вытеснения биологически активное вещество используется в 6 различных концентрациях, причем осуществляют по 3 параллели. Опыты повторяют дважды. Соединение А растворяется в концентрированной уксусной кислоте и в дистиллированной воде и далее раствор разбавляется инкубационным буфером.Раствор .холостой пробы происходит указанным образом, но без биологически активного вещества.
Хлордиазоэпоксид и соединение А вытесняют Н-Диазепам из рецепторов зависяш м от концентраций образом. ICjQ-значения для обоих биологически активных веществ попадают в одинаковый концентрационный интервал. Принимая во.внимание то, что холостая проба в концентрациях ниже 10 моль не вытесняет маркированный изотопом Диаяепам, можно исключить оказываемое на соединение А действие уксусной кислоты.
Действие соединения А на электрогенные и вызываемые лекарственными средствами судороги. Соединение А не предотвращает вызванную при оральной дозе вплоть до 200 мг/кг пентамета- |золом, стрихнином и пикротоксином судорогу и показывает на крысах против вызванной электрошоком судороги только очень слабое защитное действие.
Инъекцированная в количестве 120 мг/кг подкожно доза пентаметазо- ла на передних и задних конечностях крыс вызывает судорогоо бразные вывихи, и погибают 100% животных. В случае, если животным до- инъецирова- ния 120 мг/кг подкожной дозы пента- метазола вводят в дозе 10 мг/кг диа- зепам или фенобарбитал натрия, то судороги облегчаются, животные остаются жить и не умирает ни одна таким, образом предварительно обработанных крыс. В противоположность этому,осуществленная с помощью 200 мг/кг соединения А предварительная обработка не облегчает силы вызванных за счет пентаметазола судорог, и ни одна кры- ,са не переживает опыт.
-Соединение А в дозе 200 мг/кг не оказывает никакого влияния на антиконвульсивное действие диазенама (10 мг/кг).
Вызванные стрихнином (2,5 мг/кг подкожно) смертельные судороги ан- тагонизируются отчасти благодаря дозе 50 мг/кг фенобарбитала натрия и дозе 0 hfr/кг диазепама (размер гибели составляет 40% в сравнении с 80%), в противоноложность этому сое динение А также в дозе 200 мг/кг оказывается полностью неактивным.
Вызванные пикротоксином (10 мг/к подкожно) смертельные судороги легко антагонизируются дозой фенобарби- тала натрия 50 мг/кг (размер гибели 80%). В противоположность этому, у предварительно обработанных диазепа- мом или соединением А крыс действие судорог остается неизменным.
На вызванные электрошоком смертелные судороги легко влияют благодаря дозе 200 мг/кг соединения А (70% животных умирают), причем осуществляемая с помощью дозы 30-50 мг/кг Фено- барбитала натрия предварительная обработка полностью защищает крыс от электрогенных судорог, а диазепам спасает жизнь 80% животных.
Из указанного следует, что сог- ласно испытаниям на животных соединение А - сильное и селективное анк- сиолитическое биологически активное вещество. Анксиолитическое действие вероятно связано с бензодиазепино- выми рецепторами. В процессе клинического применения, однако, соеци- нение А в противоположность бензодиа- зепинам практически лишено седатив- ных и антиконвульсивных действий.
Предметом изобретения являются фармацевтические препараты, которые в качестве биологически активного вещества содержит, по меньшей мере,сое динение общей формулы I или его Лар- мадевтически пригодную соль присоединения кислоты и пригодные инертные твердые или жидкие фармацевтические носители.
Биологически активное вещество можно приготовлять в пригодной для орального (например, таблетки,покрытые оболочкой таблетки, драже, мягкие и твердые желатиновые капсулы, растворы, эмульсич или суспензии), па- рентерального (например, инъецируемые растворы) или ректального (например, свечи) введения форме.
in
5 ,0
25
30 -зе дО
.,
0
Предлагаемые согласно изобретению фармацевтические препараты можно приготовлять по известным способам путем смешения биологически активного вещества с пригодными инертными, твердыми или жидкими, органическими или неорганическими, фармацевтическими носителями.
При приготовлении таблеток, покрытых оболочкой таблеток, драже и твердых желатиновых капсул в качестве носителей (основ) можно применять,например, лактозу, кукурузный крахмал,картофельный крахмал, тальк, карбонат магния, стеарат магния, карбонат кальция, стеариновую кислоту и ее соли и т.д. Мягкие желатиновые капсулы могут содержать в качестве носителей, например, растительные масла, жиры, воски или многоатомные спирты пригодной консистенции. При приготовлении растворов и сиропов в качестве носителей могут найти применение, например, вода, многоатомные спирты,поли- этиленгликоль,сахароза или глюкоза. Инъецируемые растворы могут содержать в качестве носителей, например, воду, спирты, многоатомные спирты, глицерин или растительные масла. При приготовлении свечей в качестве носителей можно использовать, например,масла, воски, жиры и многоатомные спирты пригодной консистенции.
Предлагаемые в изобретении фармацевтические препараты могут содержать обычные вспомогательные вещества (наприйер, смачиватели, дисперга- торы, консерванты, эмульгаторы,красители, подслащиваюшие вещества, ароматизирующие вещества, соли для изменения осмотического давления, буферы и т.д.) и/или другие фармацевтические активные вещества.
Соединения общей формулы I могут предпочтительно вводиться в виде таблеток или капсул орально. Таблетки и капсулы с содержанием биологически активного вещества 2,5-50 м-г оказались предпочтительными. Суточная доза соединений общей формулы I может изменяться в широких пределах и зависит от многих факторов (например, активность биологически активного вещества, состояние и возраст пациентов, тяжесть заболевания и т.д.). Суточная оральная доза составляет в i общем примерно 1-300 мг, причем суточная парентеральная доза в общем
п
находится в пределах примерно 0,5 - 150 мг. Указанные интервалы только информативного характера, (Ьактичес- кая доза может быть также .вьЕие или ниже указанных пределов и всегда определяется врачом.
Формулаиз б. ретения Способ получения хинолинтиоэфиров общей формулы :
16004/46 2
ет этил, то по меньшей мере один из радикало в R, Хд и Х отличен от водорода, или их фармацевтически пригодных солей присоединения кислот, отличающийся тем, что З-амино-4- хинолинтиол общей формулы,
10
где R - С -С -алкил, С,-С5.-алкён Ил, С С -алкинил;
и Х2
могут быть одинаковыми или разными и обозначают водород или галоген при условии, что если R означа3-Амино-А-(н-пропилтио)хино- лин НС1
З-Амино-4-бензилтиохинолин-HCl
3-Амино-7-хлор-4-метилтиохино- ЛИН-НС1
3-Амино-4-этилтио-7-хл6рхинолин НС1
3-Амино-7-хлор-4-изопропилтио- хинолин НС 3-Амино-7-хлор-4-(н-пропилтио) хинолин НС 3-Амино-4-аллилтио-7-хлорхинолин/f HCl
3-А ино-7-хлор-4-пропаргилтио- хинолин НС
3-Амино-4-бенз илтио-7-хлорхино- лин НС
3-Амино-7-хлор-4-(4-хлор-бензил- т ио) хрнолин HCl
где Х и Х имеют указанные значения, подвергают взаимодействию с соединением общей формулы
RI - X, где R имеет указанные значения;
X означает удаляемую группу, с выделением целевого продукта или с переводом полученных продуктов в их фармацевтически пригодные соли.
Таблица 1
168-170
214-215
235-237 214-216
232-233
(разложение)
209-210 t (разложение)
210-212
222-223
15 (разложение)
,05;
,001.
Хлордиазоэпоксид вводится за ЗЪ мин до начала опыта подкожно. Число животных указано в скобках.
, . Таблица
римечание. Хлордиазоэпоксид вводится
подкожно, а вещество R О 15-1788 - интраперито- неально за 30 дн до начала опыта (число животных указано в скобках)..
Таблица2
ТаблицаЗ
,001.
Соединение А вводится за 30 мин до начала опыта. Число животных указано в скобках.
Таблицаб
Примечание. Соединение А вводится подкожно,
. а вещество R О 15-1788-интраперито- неально за 30 мин до начала опыта. Число животных указано в скобках.
ТаблицаЗ
| Вейганд-Хильгетаг | |||
| Методы эксперимента в органической химии | |||
| М | |||
| : Химия, 1968, с | |||
| Аппарат для предохранения паровых котлов, экономайзеров, кипятильников и т.п. приборов от разъедания воздухом, растворенным в питательной воде | 1918 |
|
SU585A1 |
| . | |||
Авторы
Даты
1990-11-23—Публикация
1988-04-22—Подача