Изобретение относится к способу получения новых соединений - к способу получения индентиазола формулы
N Нз
(.
т
(I)
где X и Y - одинаковые или различные и каждый обозначает водород, галоид, низший кил;
п - целое число от О до 4;
R - водород, низший С,-С -алкил; 2. низший Cf-Cj-алкил или морфолиногруппа;R - водород или ацетил.
С/1
или Rj и Rj вместе с ЫССН) образуют группу пиррола при условии, что при X Y R, RJ Н R не может быть алкилом, или при X - Y - га лоид , R2 - морфолин, Rj Н R, не может быть водород, или при X - FI, Y - 6-С1 или 7-F, Rg - Н, R,2 - мор:фолин R не может быть алкилом, кли при X Y RJ - Н, Rg - морфолин RJ не может быть алкилом, которые могут найти применение в качестве
;противоязвенных препаратов.
Цель изобретения - изыскание новы I соединений указанной формулы,обладаю |щих более высоким противоязвенным :действием.
Пример 1. К 40. МП этанола добавляют 3,5 г 2-бром-5-Фтор-1-ин- данона и 3,1 г Ы-(З-морфолинопропйл) тиомочевины, полученную смесь кипятят 10 мин и перемешивают 24 ч .при комнатной температуре-с осаждением кристаллов, которые собирают фильт- рованием. Отфильтрованные кристаллы промывают этанолом, сушат, переносят в 40 мл 5%-ного водного раствора NaOH, экстрагируют этилацетатом,про- мывают водой, сушат, перегоняют при пониженном давлении, после чего пере :кристаллизовывают из смеси этилаце- ;т ат-изопропиловый эфир с получением IB результате 3,9 г 2-(3-морйолино- ; пропил)амино-б-фтор-8Н-индено l , :тиазола. Полученное соединение имеет температуру плавления 113-115°С и да :ет следующий результат анализа:
Найдено,%: С 61,00; Н 6,04; Н 12,47.
Вычислено,%: С 61,24; Н 6,04; N 12,60.
П р и м е р 2. В .50 m 0,1 н. расвора НС1 растворяют 3 г 2-(3-мрр оли- нопропил) амино-6-азтор-8Н-индено l , 2- ё тиазола, оставляют на 3 дня при комнатной температуре, спабо подшела- чивают 5%-ным водным раствором КОН, экстрагируют хлороформом, промывают водой, растворитель отгоняют при пониженном давлении, остаток выделяют и очищают колоночной хроматографией на силикагеле с применением для вымывания смеси, состоящей из хлороформа, метанола и водного аммиака в соотношении 10; 1 :0,1 , с получением в результате таутомера (1 г) следующей формулы:
N
N-(CH2VNQO
с
Ю
f5
20 25 0
5
5
Полученное соединение обладает также следующими показателями.
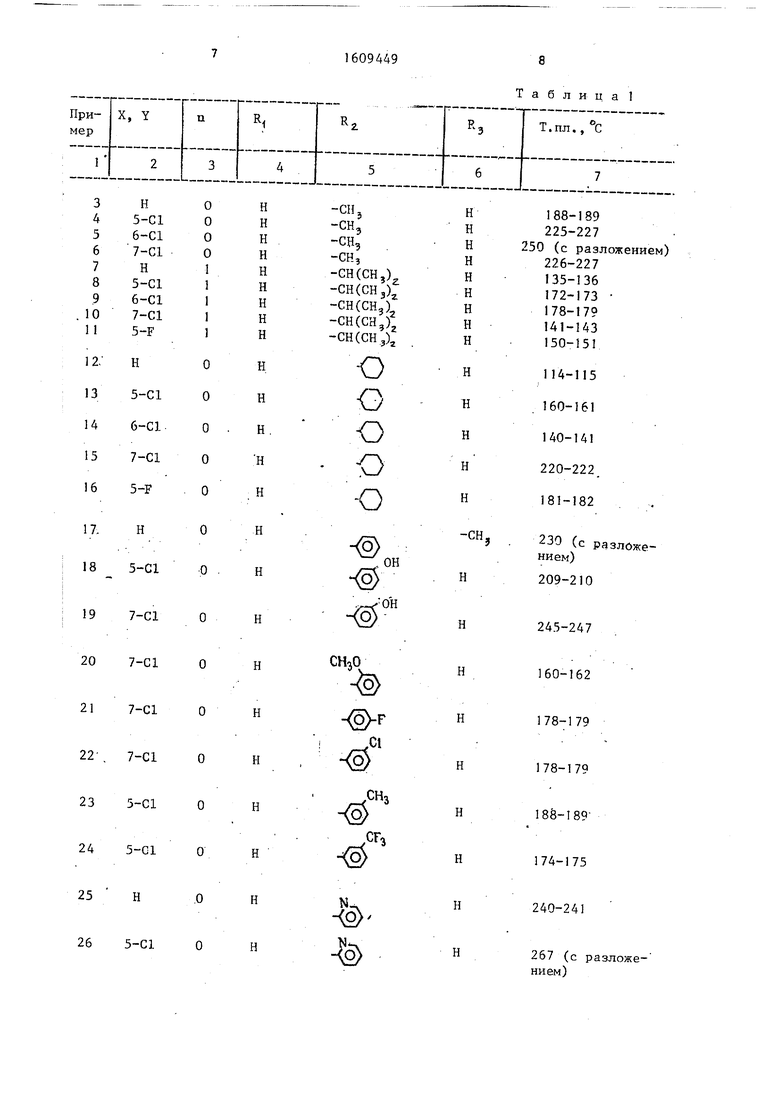
ИК-спектр (КВг) , см- :3270; 1600; 1485; 1250; 1115; 1065; 860; 755. ЯМР-спектр (DMCO-d) , млн- : 1,59 (к,2Н), 2,24 (т, 4Н), 2,28 (т,2Н); 2,83 и 3,5 (дв. д, 2Н),3,13 (т, ЗН), 3,54 (т, 4Н),4,15 (дв, д, Ш), 6,98 (дв. д, 1Н), 7,03 (тр.д, 1Н), 7,35 (дв, д, Ш). П р и м е р ы 3-122. Соединения получены по-методике примера 1 (формула 1а) .
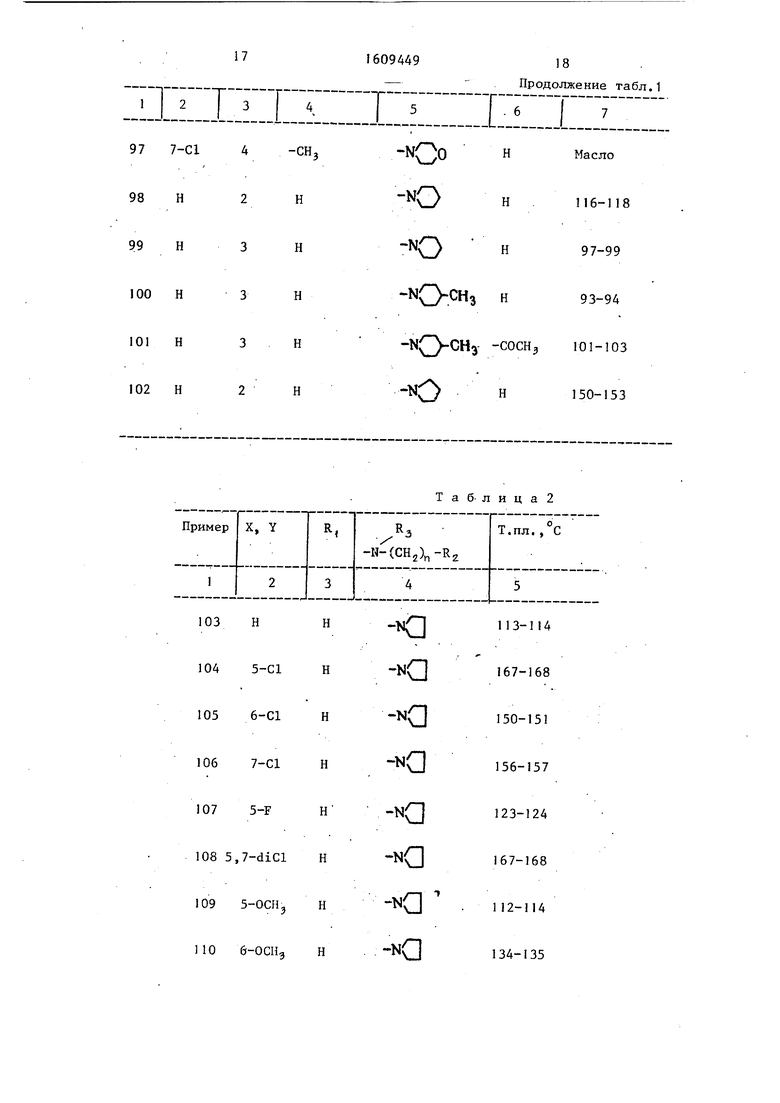
Значения заместителей соединений и их температуры плавления приведены в табЛо1 и 2.
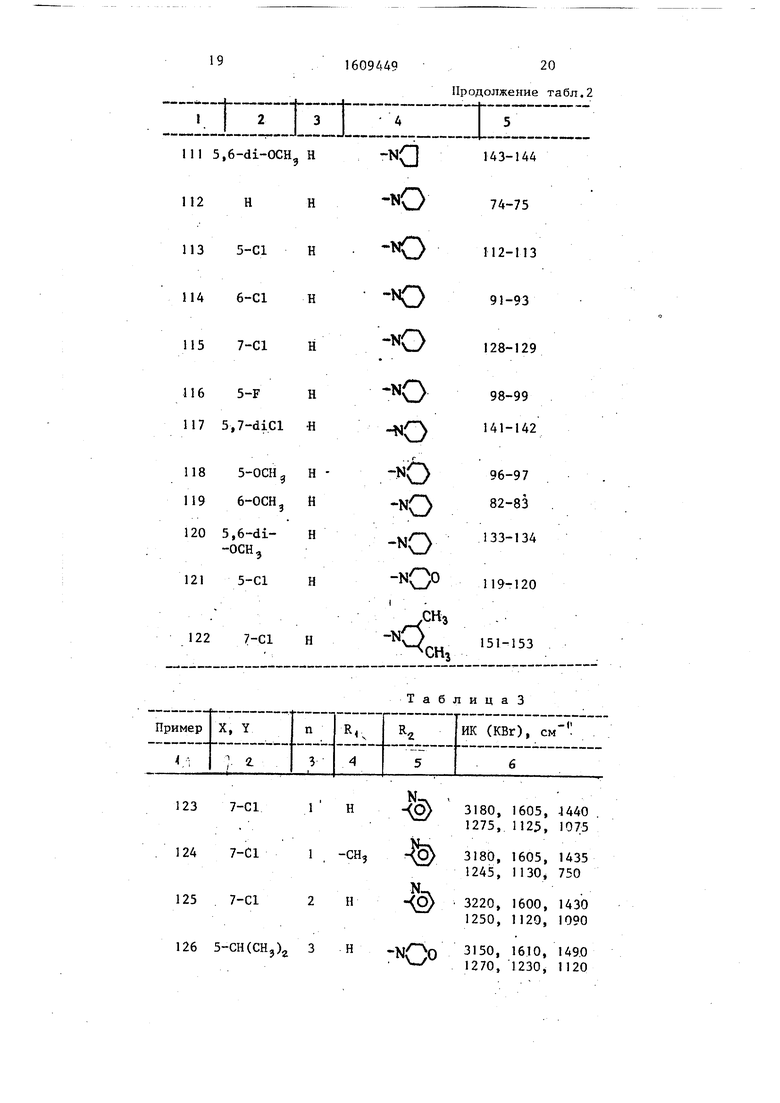
П р -и м е р ы 123-129. Соединения синтезированы по методике приме- ра 2 (формула Ib).
Значения заместителей в соединениях и результаты инфракрасной спектрографии приведены в табл.3. X Фармакологические испытания.
В испытаниях использованы крысы линии Вистар весом примерно 200 г (самцы), образующие группы в 9-10 животных и не получивших ни воды, ни пищи за 24 ч до испытаний. Каждое испытуемое соединение вводилось в количестве 50 мг/кг, а используемое -для сравнения лекарство Нойер производство Дайичи Фармацетикл Ко., ЛтД, активный компонент - центраксат в количестве 300 мг/кг. Каждое испытуемое соединение вводилось перорально каждой крысе первой группы, а сравниваемое лекарство вводилось каждой крысе второй группы за 1 ч до перорального введения каждой крысе 1 мл чистого этанола. Спустя 1 ч каждую крысу умерщвляют путем обескровливания, их желудки фиксируют 30 мнн в 10 мл 70%-ного этанола. Третьей группе крыс . дают 0,5%-ный раствор трагаканта. Невооруженньш глазом определяют длину язв, после чего у испытуемых hpynn крыс выявляют соответствующую степень ингибирования по сравнению с третьей группой.
Как испытуемые соединения, так и сравниваемое соединение применяют в испытаниях в виде суспензии или раствора в 5%-ном солевом растворе трагаканта.
В табл.4 приведены значения степени ингибирования изъязвления,полученные в результате применения каждого из испытуемых соединений и сравниваемого соединения по сравнению со значениями, полученными при использовании контрольного раствора.







Изобретение относится к гетероциклическим соединениям, в частности к получению идентиазола ф-лы @ , где X и Y - одинаковые или различные и каждый - H, галоид, низший C1 - C3 - алкил
N - 0-4
R1 - H, низший C1 - C5 - алкил
R2 - низший C1 - C3 - алкил или морфолиногруппа
R3 - H или ацетил, или R2 и R3 вместе с N(CH2) образуют группу пиррола, при условии, что при X=Y=R1-R3-H, R2 не может быть алкилом, или при X=Y - галоид, R2 - морфолин, R3 - H, R1 - не может быть H, или при X - H, Y-6-CL или 7F, R3-H, R2 - морфолин, R1 не может быть алкилом, или при X=Y-R3=H, R2 - морфолин, R1 не может быть алкилом, которые могут найти применение в качестве противоязвенных препаратов. Цель изобретения - разработка способа получения более активных соединений. Получение ведут реакцией соответствующего бромзамещенного инданона с замещенным производным тиомочевины при 20-120°С в течение 1-24 ч. 4 табл.
Степень ингибированияизъязвления
Острая токсичность.
В испытаниях используют самцов крыс линии Вистар весом примерно 150 г, объединенные в группы по пять зверьков. После растворения или сус- пендирования каждого испытуемого соединения в солевом физиологическом растворе (водном) суспензию вводят каждой испытуемой крысе перорально или внутрибрюшинно. Обработанные таким образом крысы наблюдают в течение 8 дн с целью выявления летальной дозы (ЛДдд) и в результате устанавливают, что JTflgo ДЛЯ каждого испытуемого соединения по меньшей мере равна 1000 мг/кг при пероральном введении и по меньшей мере 300 мг/кг при внутрибрюшинном введении.
Из результатов приведенных испытаний на острую токсичность установлено, что соединения Лормул (1а) и (ТЪ и их соли с кислотами езопасны и обладают хорошим противоязв енным действием при отсутствии побочных эффектов. Соответственно, при их и споль- зовании для медикаментозного лечения, профилактики и предотвращения рецидивов изъязвления эти соединения могут считаться достаточно эффективными как лекарства.
Формула изобретения
Способ получения индентиазола формулы
Показатель изъязвления для 3-й гр. - Показатель изъязвления дпя 1-й и 2-й гр.
1
Показатель изъязвления для 3-й { контрольной) группы
X
N RJ
20
v-(CHiVR7
(I)
5
R. Ч
0
5
0
5
где X и Y - одинаковые или различные и каждый обозначает водород, галоид, низший С -С -алкил;
п - целое число от О до 4; водород, низший алкил;
низший С-С -алкил или морфолиногруппа; R - водород или ацетил, или R и R вместе с Ы(СН) образуют группу пиррола npti условии, что при X Y R, Rj - Н R-z. не может быть алкилом или при X Y - галоид, R - морфолин, R - Н Р не может быть водород, или при X - И, Y - 6-С1 или 7F, R, - Н, R - морфолин R не может быть алкилом, или при X Y , морболин Rj не может быть аЛКилом, отличающийся тем, что соединение формулы II подвергают взаимодействию с соединением формулы III
ОQ
Вг NH2-C-N(R3V(CH2)n-R2
50
III
при 20-120°С п течение 1-24 ч.
1609449
Продолжение табл.1
13
:ш1;п;1 : ::2
16094А914
Продолжение табл.1
Г
17
n:izr -г
1 I 2 I 3 97 7-Cl 4 -CH,
98 H
H
99 H
100 H
101 H
H
102 H
2 H
1075-F
1085,7-diCl
1095-OCHj
1106-OCH,
18 Продолжение табл.1
6 I 7
H
H
Масло
116-118
-NO H -NO-СНз H
97-99
93-94
101-103
-О H
150-153
Таб-лица2
.
123-124
167-168
112-114
134-135
126 5-СН(СНз)2 3 Н
v
O
v
3150, 1610, 149.0 1270, 1230, 1120
21
1609449
22 Продолжение табл.3
| Applied pharinacol for bnglish transl | |||
| Планшайба для точной расточки лекал и выработок | 1922 |
|
SU1976A1 |
Авторы
Даты
1990-11-23—Публикация
1987-09-15—Подача