Изобретение относится к сельскохозяйственной биотехнологии и может быть использовано в животноводстве для кормления животных.
Целью изобретения является повышение продуктивности.
Цель достигается тем, что получают препарат, способный изменять соотношение уксусной и пропионовой кислот в желудочном соке рубца жвачных животных в интервале (1,5-4,0): 1. При этом в качестве биологически активного ингредиента в препарате используют штамм Proplontbacterlum sp. HNCMB № 00287 или штамм Veilonella sp. HNCMB N 00288, или штамм Bifidobacterium sp. HNCMB №00289. Штаммы Propionlbacterium sp., Veilonella sp., Bifidobacterium sp. выделены из рубца жвачных животных, селектированы по способности к биосинтезу летучих жирных кисСд
лот и депонированы в Национальной коллекции микроорганизмов при Венгерском государственном институте здравоохранения под номером 00287 и/или 00288 и/или 00289.5
Для увеличения выхода мяса жвачных животных предпочтительно применять в качестве биологически активного ингредиента культуры микроорганизмов, поддер- живающие соотношение уксусной и 10 пропионовой кислот в области (2,0-3,5):1, например 2:1. Для молочной продукции оптимальное соотношение усусной и пропи- оног ой кислот составляет примерно 3,0:1, для периода стельности 4,0:1, в то время как 15 при выращивании телок{2,0-3,0):1. Пример 1.
А. Селекция штаммов микроорганизмов, выделенных из рубца животных, вскармливаемых сеном.20
-Овэц в течение месяца кормят сеном, затем через оперативно введенную в рубец закрывающуюся фистулу отбирают пробу. Пробу непосредственно после взятия отбора селекционируют на специальной пита- 25 тельной среде.
Для получения питательной среды используют 7,5 мл солевого раствора I, содержащего:
Дикалийгидрофосфат, м0,630
Дистиллированная вода, мл До 100 7,5 мл солевого раствора II, содержащего: Хлорид натрия, г1,2
Сульфат аммония, г1,2
Дигидрофоифат калия, г0,6 35
Хлорид кальция, г0,12
Гептагидрат сульфата магния, г0,25
Дистиллированная вода, мл До 100 а также40
0,01%-ный раствор резазурина, мл0,1
Агар (бакто), г2,5
Жидкость рубца, мл10,0
Глюкоза, г0,05 45
Целлюбиоза, г0,05
Моногидрат гидрохлорида цистеина,г0,05
8%-ный раствор карбоната натрия, мл5,0 50
Дистиллированная вода, мл До 100 Обозначение питательной среды RGCA. Отобранная из рубца проба фильтруется через рыхлый марлевый фильтр, фильтрат затем хранится при -20° в атмосфере СОа. 55 РН питательной среды устанавливают 6,8, затем среду стерилизуют. Стерилизацию осуществляют в атмосфере С02.
Предварительно среду разбавляют стерильной смесью следующего состава:
Солевой раствор I, мл7,5
Солевой раствор II, мл7,5
Моногидрат гидрохлорида цистеина, г0,05
Карбонат натрия, г0,3
0,1%-ный раствор резазурина, мл0,1 Дистиллированная вода, мл До 100 Обозначение смеси НВ. Культуры инкубируют в течение 120 ч в анаэробных условиях при 35°С,
Затем отдельными колониями засевают содержащую сенной экстракт питательную среду следующего состава, %:
Солевой раствор 15,0
Солевой раствор II15,0
0,1%-ный раствор резазурина0,1 Триптон I 421,5 Дрожжевой экстракт 0,5 Рубцовая жидкость10,0 Карбонат натрия 0,4 Моногидрат гидрохлорида цистеина 0,05 Сенной экстракт10,0 Обозначение RGCF. Для приготовления сенного экстракта разрезанные на мелкие кусочки части растений cycnes-.дируют в воде, кипятят и затем отфильтровывают. Остаток на фильтре перед стерилизацией добавляют к питательной среде.
рН питательной среды устанавливают 6,5 с помощью сонной кислоты, затем среду стерилизуют.
Стерилизованные в пробирках питательные среды объемом 5 мл засевают суспензией клеток, полученной из изолированных колоний, выросших на твердой питательной среде RGCA. Культуры инкубируют в течение 5 дней при 35°С при анаэробных условиях. Рост контролируют микроскопмрованием, затем культуру селекционируют на питательной среде RGCA указанного состава. Однако в среду не добавляют глюкозу, целлюбиозу, используют вместо этого 2% бакто-целлюлозы.
Культуры инкубируют при 35°С в течение 120ч, затем отдельные колонии, развившиеся на способных усваивать целлюлозу клетках, изолируют путем центрифугирования в атмосфере СОа.
Б. Генетическая маркировка полученных бактерий.
Генетическую маркировку осуществляют с помощью EschericWa coll Плазмида р.1011.
Плазмидную ДНК изолируют и растворяют в смеси следующего состава, ммоль: Хлорид кальция75
Хлорид магния Трис-гидрохлоридный буфер, рН7,5
10
(Трис)-(оксиметил)-{аминометан)-гид- рохлорид.
Полученные в разделе А клетки суспендируют в смеси следующего состава, ммоль: Хлорид кальция75
Хлорид магния5
Трис-гидрохлоридный буфер, рН7,510
Моногидрат гидрохлорида цистеина1
Тиосульфат натрия1
В суспензии содержится 5Х 109 клеток на миллилитр. Суспензию клеток разбавляют в соотношении 1:1 (0,1 мкг/мкл) смесью, содержащей р.1011 плазмидную ДНК, затем инкубируют при 4°С в течение 60 мин. Далее инкубацию продолжают 2 мин при 41 °С, после чего культуру наносят на плотную питательную среду, содержащую в качестве источника углерода целлюлозу, с добавлением перед стерилизацией 500 мкг/мл канамицина В. Культуры инкубируют 120 ч при 35°С и при анаэробных условиях, затем колонии, способные расти в присутствии 500 мкг/мл канамицина В, исследуют.
Плазмида р1011 несет гены, определяющие резистентность к канамицину и хлорамфениколу и ori-участок, обеспечивающий репликацию плазмиды в клетках E.coli. Так как плазмида ДНК способна ре- плицироваться только в E.coli тона, она теряется после того, как попадает в другие бактерии, однако полностью или частично встраивается в хромосомы, т.е. происходит генетическая рекомбинация. Встроенный в хромосом ген проявляется в благоприятном случае и обеспечивает устойчивость к канамицину и хлорамфениколу.
Таким образом получают резистентные к канамицину В колонии, частота трансфер- мации которых составляет 3 Х10 .
Некоторые резистентные колонии изолируют и определяют чувствительность к антибиотикам исходных штаммов и резистентных по отношению к кэнамицину Б (KmR) штаммов. Получены следующие результаты:
Микроорганизмы Минимальная подавляющая рост концентрация кана- мицина В, мкг/мл Содержимое рубца31
Исходные штаммы4,0-7,5
Генетически маркированные KmRштаммы: Hh-GVOK1-1,8 500
27250
91 500
1231000
142 500
Штамм Hh-GVOK1-1-123/K наносят на содержащую целлюлозу питательную среду R GCA с добавлением 1000, 5000 и 10000 мкг/мл канамицина В. Культуры инкубируют 168 ч при 35°С в анаэробных условиях, затем изолируют выросшие в присутствии 10000 мкг/мл антибиотика штаммы. Таким образом селекционированный штамм, обозначенный как Hh-GYOK-1-123 Sz, синтезируют пропионовую кислоту. Бактерия является грамположительной и имеет палочковидную форму. Глюкоза и крахмал сбраживаются этой бактерией в пропионовую и уксусную кислоты, причем образуется также немного масляной кислоты и углекислоты. На комплексных питательных средах появляются молодые микроорганизмы клеток палочковидной формы, которые позднее превращаются в полиморфные формы различной величины и содержания, не имеющие ресничек и часто расширяющиеся на вершине, становятся шире. Организм также хорошо растет в анаэробных и полуанаэробных условиях, он факультативно анаэробный. Поэтому штамм, обозначенный как Hh-GVOK1-1-123 Sz (как и. происходящий от него штамм Hh-GYOK 1-48a) относят к роду Propionibacterium. Штамм Propionibacterium sp. (Hh-GYOK-1-123 Sz) депонирован в Национальной коллекции микроорганизмов при Венгерском государственном институте здравоохранения под номером 00287.
В. Внесение генетически маркированных микроорганизмов в рубец.
Штаммом Propionibacterium sp. HNCMB № 00287 засевают стерильную питательную среду RGCFa следующего состава, мл:
Гидрофосфзт калия 0,3%45
Сульфат аммония
Хлорид натрия
Моногидрат сульфата
магния 45
Дигидрат хлорида кальция
Дигидрофосфат калия
Бакто-целлюлоза
Агар (бзкто)65
Дрожжевой экстракт20
Моногидрат гидрохлорида
цистеина20
Тиосульфат натрия20
Карбонат натрия
Рубцовая жидкость20
Разведение культуры осуществляют при анаэробных условиях в колбах объемом 500 мл, содержащих 150 мл питательной среды. Спустя 48 ч контролируют рост, затем культуру примешивают в корм овец, получающих сено. Перед кормлением и в последующие дни через введенную путем операции в рубец фистулу отбирают пробы объемом 50-200 мл.
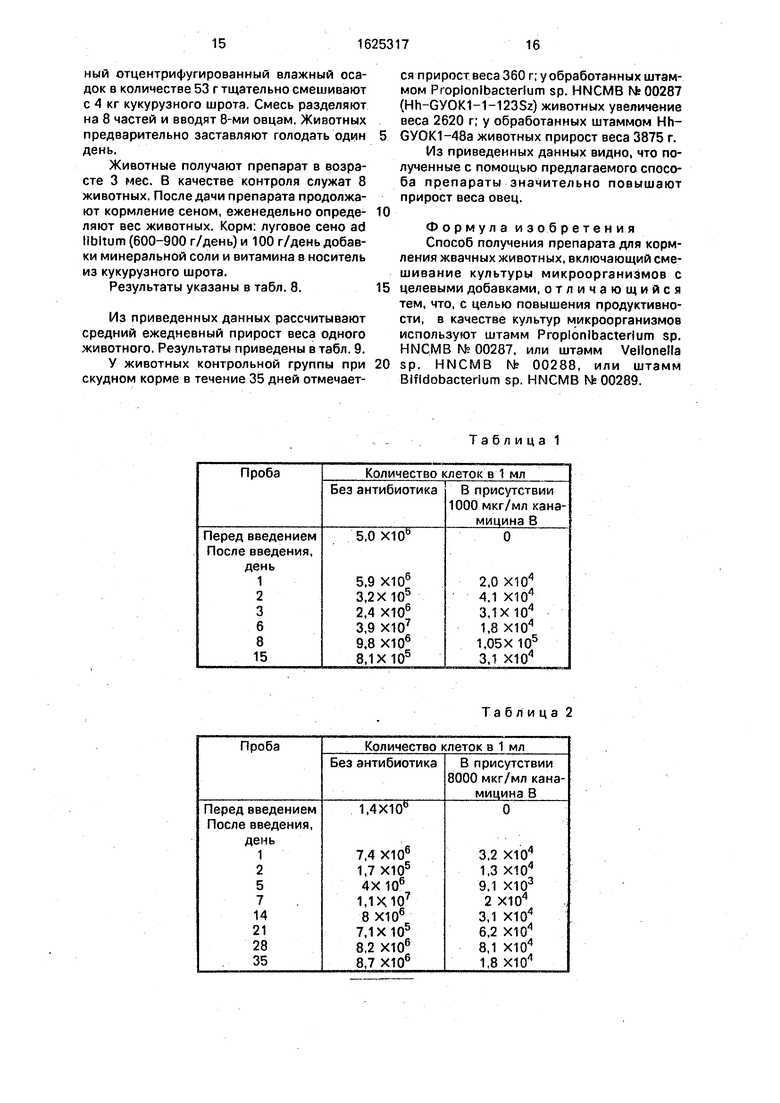
Пробы после соответствующего разбавления НВ-расгвором наносят на RGCA-пи- тательные среды, не содержащие канамицина и других анти5иотиков. Культуры инкубируют 72 ч при 35°С в анаэробных условиях, затем определяют число развившихся колоний бактерий. Животному вводят орально 340 мп культуры, содержащей 4,7 X 10 бактерии на миллилитр. Результаты представлены в табл. 1.
Из данных табл. 1 следует, что введенный микроорганизм длительное время существует в рубце и размножается,
Животному также вводят орально 140 мл культуры Propionibacterium sp., содержащей 2 X 10 клеток на миллилитр. Результаты представлены в табл. 2.
Из данных табл. 2 следует, что введенные микроорганизм имеется в значительном количестве в рубце, а также размножается.
Пример 2.
А. Селекция штаммов микроорганизмов, выделенных из рубца животных, вскармливаемых зерновыми продуктами.
Культуру получают аналогично п. А примера 1 с тем различием, что исходную пробу отбирают из рубца животных, вскармливаемых зерновыми продуктами, Отдельные изоляты высевают HaRGCF-среду, содержащую вместо сена измельченное в порошок зерно (2%). Выросшие в жидкой RGCF-cpe- де культуры наносят на плотную RGCA-cpe- AV и из такой питательной среды изолируют колонии, развившиеся из клеток, усваивающих зерновое продукты.
Б, Генетическая маркировка бактерий, разрушающих крахмал.
Осуществляют анэпогично п. Б примера 1.
Резистентность по отношению к кана- мицин.у В некоторых трансформированных и KmR штаммов следующая:
Микроорганизм Минимальная подавляющая рост концентрация канамицина В, мкг/мл
Содержимое желудка31
Исходные ш гаммы1,8
Генетически маркированные Km -штаммы: Hh-GYOK1-2-4 14 Ab 37
81
250 250 250 125
Селекционированный штамм, обозначенный как Hh-GYOK1-2-14Ab, неподвижный, грамотрицательный, не вырабатывает
пигментов.
Хорошо растет в анаэробных условиях при 37°С. В большом количестве появляются сферические клетки и располагаются одна рядом с другой. Их средняя величина
составляет 0,3-0,4 мкм, Сбраживает углеро- ды до кислоты и углекислого газа. На комплексных питательных средах образует сероводород, не разжижает желатину, гемолиза не вызывает. Поэтому штамм, обозначенный как Hh-GVOK1-2-14Ab, относят к роду Veilonella.
Штамм Vellonella sp. (Hh-GV ОК1-2- 14АЬ) депонирован под номером 00288 в Национальной коллекции микроорганизмов
при Венгерском государственном институте здравоохранения.
В. Внесение генетически маркированных микроорганизмов в рубец.
Определяют аналогично пункту В примера 1 с тем различием, что используют штамм Veilonella sp, (Hh-GYOK1-2-14Ab) и засевают стерильную RGCFa-среду, содержащую вместо бактоцеллюлозы 1,8% растворимого крахмала. Затем культуру
примешивают в корм животных, получающих зерно. Перед введением и затем ежедневно через фистулу отбирают пробу. Животному вводят орально 310 мл культуры, содержащей в целом 7,1Х 105 бактерий.
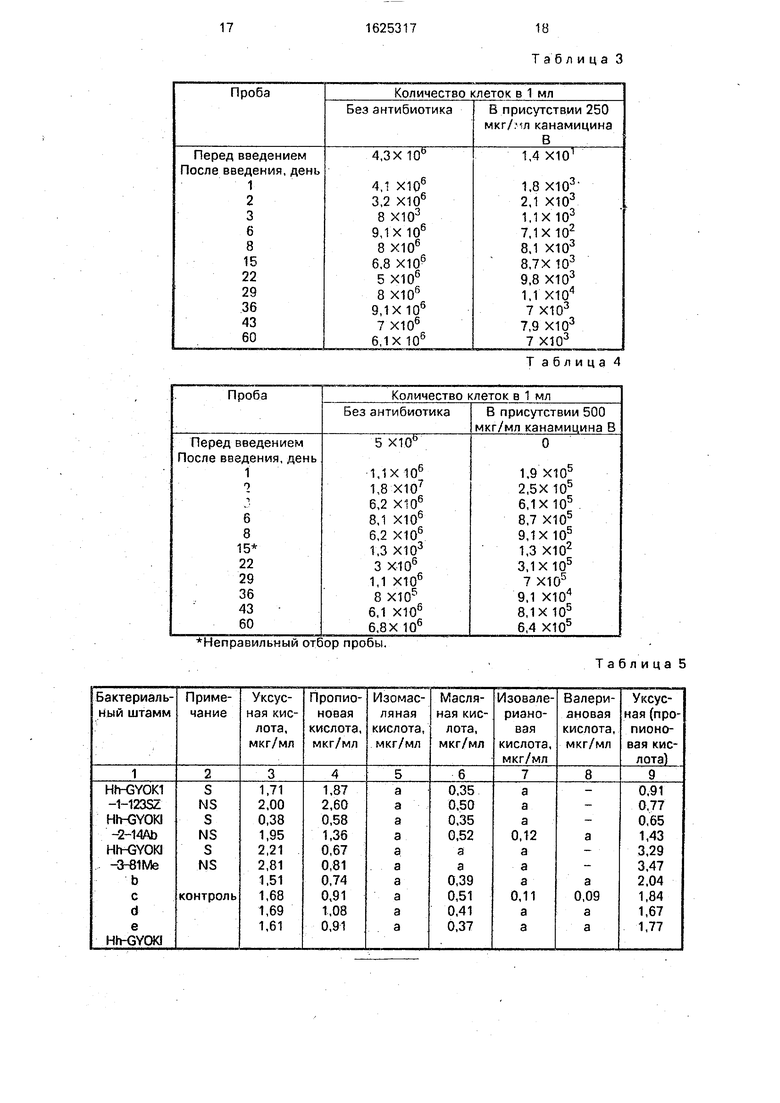
Число содержащихся в пробах KmR клеток указано в табл. 3.
Из табл. 3 видно, что введенный микроорганизм длительное время остается живым и размножается.
. П р и м е р 3.
А, Селекция штаммов микроорганизмов, выделенных 1.з рубца животных, вскармливаемых мелассой.
Культуру получают аналогично пункту А примера 1 с тем различием, что исходную пробу отбирают из рубца животных, которых кормят мелассой. Отдельные изоляты высевают на R GCF-среду, содержащую вместо дрожжевого экстракта глюкозу. Развившиеся в жидкой питательной среде культуры наносят на R GCA-среду. На такие же питательные среды высевают колонии, которые развились из клеток способных усваивать мелассу.
Таким образом получают происходящие из рубца микроорганизмы, которые могут метаболизировать мелассу.
Б. Генетическая маркировка использующих мелассу бактерий.
Осуществляют аналогично пункту Б примера 1.
Резистентность некоторых КпАклегок по отношению к канамицину В следующая:
Микроорганизм Минимальная подавля- ющая рост концентрации канамицина В, мкг/мл .
Содержимое рубца31
Исходные штаммы7,5
Генетически мэр-
кированные Кт -штаммы: Нп-СУОК1-3-2250
14500
34250
81 Me500
132500
Селекционированный штамм, обозначенный как Hh-GVOK1-3-81 Me, факультативно анаэробный, грамположительный. Клетки имеют палочковидную форму, не- подвижны. Концы палочек сдавлены. Образует уксусную кислоту, ферментирует глюкозу до молочной кислоты. Палочки растут на различных питательных средах, редко по отдельности, в большинстве случаев в форме цепочек. Не образует пигмента. Поэтому штамм относят к роду Bifidobacterium. Штамм Bifidobacterium sp. (Hh-GVOK1- 3-81 Me) депонирован под номером 00289 в Национальном собрании микроорганизмов при Венгерском государственном институте здравоохранения.
В. Внесение генетически маркированных клеток в рубец.
Поступают согласно п. В примера 1 с тем же различием, что штаммом Bifidobacterium sp. HNCMB № 00289 (Hh- GYOK-3-81 Me) засевают R GCF-a-среду, содержащую вместо целлюлозы 1,8% глюкозы. Культуру примешивают в корм жи- вотных, получающих мелассу. Перед кормлением и затем ежедневно через введенную в рубец фистулу отбирают пробы, Животно му вводят орально 380 мл культуры, которая содержит 1,6 X 107 клеток на миллилитр.
Число содержащихся в пробах Ктк-кле- ток указано в табл. 4.
Из данных табл. 4 видно, что введенный микроорганизм длительное время находится в рубце животного.
Пример 4. Изменение соотношения продуцируемых в рубце летучих жирных кислот при использовании полученных бактерий.
Две овцы получают комплексный корм (смесь из сена и овечьего корма), затем спустя 14 дней через фистулу отбирают из рубца пробу. 2 л рубцового сока фильтруют через многослойную марлю, фильтрат отделяют. Остающиеся на марле кусочки Суспендируют в 1 л физиологического буфера, затем после перемешивания также фильтруют. Оба фильтрата объединяют, оставляют стоять, спустя 1 ч удаляют абсорбирующиеся на поверхности твердые вещества, дл исследования используют только жидкости Состав физиологического буфера следу ющий, г/л:
Динатрийгидрофосфат (гидрофосфат натрия0,316
Дигидрофосфат калия0,152
Гидрокарбонат натрия2,260
Хлорид калия0,375
Сульфат магния0,112
Дигидрат хлорида кальция0,050
Геп та гидрат сульфата железа (II)0,08
Моногидрат сульфата магния0,004
Гептагидрат сульфата цинка 0,004 Пентагидрат сульфата меди 0,002 Гексагидрат хлорид кобальта (II)0,001 рН смеси контролируют, в случае необходимости устанавливают равным 7,2 с помощью разбавленного водного раствора соляной кислоты или раствора гидроксида натрия.
Полученную смесь в соотношении 1:1 разбавляют указанным выше физиологическим буфером, и в 1 л раствора добавляют 4 г кормовой смеси. По 30 мл полученной суспензии заполняют в колбы Эрленмейерз объемом 100 мл, затем 200 порций предварительно подготовленной питательной среды стерилизуют, 200 следующих порций не стерилизуют и засевают полученными по примерам 1-3 бактериями,
Исследуемые бактерии инкубируют при 37°С в анаэробных условиях в течение 48 ч на R GCA + CG-питательных средах следующего состава1 %:
Солевой раствор I15
Солевой раствор II15
Раствор микроэлементов0,3
.Дрожжевой экстракт0,5
Отфильтрованная жидкость рубца10,0
Карбонат натрия0,4
Моногидрат гидрохлорида цистеина0,05
Тиосульфат натрия0,008
Целлюлоза (бакто)0,3
Глюкоза2,0 Состав раствора микроэлементов следующий, мг:
Хлорид цинка40
Дигидрат хлорида меди (It)10
Декагидрат тетрабората натрия10
Тетрагидрат молибдата аммония10
Гексагидрат трихлорида железа200
Тетрагидрат хлорида мар-
ганца (II)10
Свободная от ионов , мл До 1000 Культурами засевают предварительно приготовленные, как указано выше, питательные среды в колбах Эрленмейера. Посев осуществляется в соотношении 2 мл культуры на 50 MJI питательной среды. Так же высевают нестирильную культуру.
Посев инкубируют в течение 40 ч при анаэробных условиях, затем размножение прекращают с помощью 10% концентрированной муравьиной кислоты и исследуют содержание летучих жирных кислот. Для этого культуры фильтруют через марлю и затем в течение 15 мин центрифугируют в роторе с числом оборотов 4000. Смесь еще раз фильтруют и затем для определения жирных кислот с 2-5 С-атомами вносят в разделительную колонку.газового хроматографа, снабженного плазменно-ионизационным детектором. Температура колонки 150°С. Разделительная колонка длиной 2 м, стеклянная трубка с внутренним диаметром 4 мм; заполнение: 1С% зтиленгликольадипи- нат + 2% ортофосфорной кислоты на сила- низированном силикагелевом носителе (0,2-0,3 мм). Температура инжектора 190°С. Скорость потока Na 50 мл/мин. Скорость потока На 50 мл/мин. Скорость потока воздуха 200 мл/мин. Скорость бумаги 160 см/ч. Время хроматографирования 20 мин. Количество пробы 1 м;;л.
Для каждой пробы осуществляют 4 параллельных измерения.
Стандартный раствор содержит уксусную, пропионовую, изомасляную, масляную, изовалериановую и валериановую кислоты.
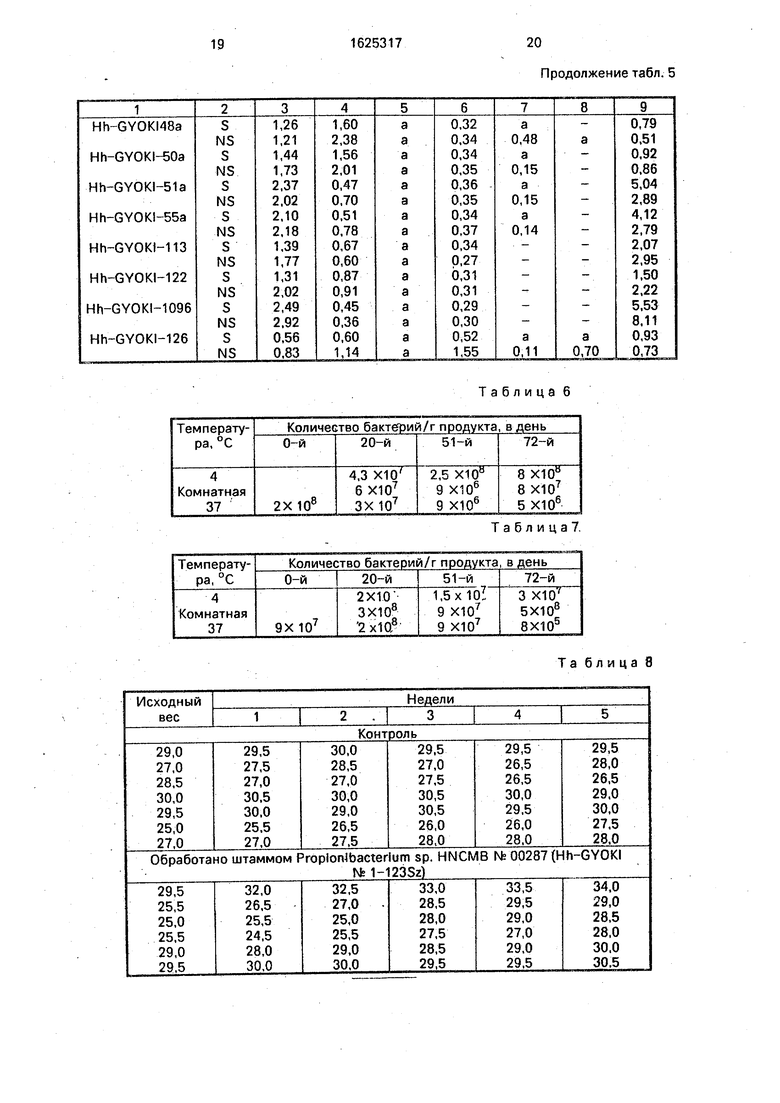
Полученные результаты представлены в табл. 5. В табл. 5 использованы следующие обозначения:
+S - высевается после стерилизации; NS - высевается из пробирки, содержащей живую флору рубца;
а - незначительное количество;
Ь - отрицательный контроль: содержание в питательной среде (жидкость рубца.
физиологический буфер и корм) летучих жирных кислот (среднее из 12 измерений);
с - положительный контроль: содержание в содержащей первоначальные бактерии рубца и инкубированной культуре (питательная среда из жидкости рубца, физиологического буфера и корма) летучих жирных кислот (среднее из 12 измерений); d - аналогично с, но в питательной сре0 де с добавлением 5 ррт моненцинз (натриевая соль), среднее из 6 измерений;
е - как и с, но в питательной среде с добавлением 100 ррт моненцина (натриевая соль), среднее из 6 измерений.
5 Из данных табл. 5 видно, что при введении предлагаемых культур микроорганизмов соотношение образующихся в рубце летучих жирных кислот может изменяться в широких пределах. С помощью полученной
0 из штамма Hh-GVOK-48a культуры можно, например, повысить количество образующейся пропионовой кислоты, одновременно благодаря культуре микроорганизма Hh-GVOK1-109e повышается количество
5 образующейся уксусной кислоты. Увеличение количества образующихся отдельных жирных кислот можно наблюдать также на питательных средах, которые не содержат никаких других микроорганизмов (S) или в
0 присутствии обычных бактерий рубца (NS). В используемой опытной системе с натриевой солью моненцина соотношение уксусная кислота/пропионовая кислота (d, e) уменьшается на 1 -2 десятых.
5 П р и м е р 5. Получение бактериального препарата для кормления животных.
Вводимую бактзрию выращивают на R GCA + CG-питательных средах указанного в примере 4 состава в анаэробных условиях.
0 После выращивания клетки известным образом отделяют, например, путем фильтрации ипи центрифугирования. Отделенные клегки суспендируют в физиологическом буфере (см. пример 4) и подвергают сушке
5 вымораживанием. Лиофилизированный бактериальный препарат собирают и при известных условиях в виде соответствующего препарата БВОД..Т(задают)животным. Разведение культуры микроорганизмов
0 можно осуществлять также на других известных питательных средах, например на питательных средах, содержащих в качестве источника углерода глюкозу, крахмал и т.д., в качестве источника азота - неорганиче5 ские соли.
Препарат можно вводит в смеси с кормом, питьевой водой, самостоятельно или вместе с другими биологическими активными веществами, например с антибиотиками, витаминами.
Кроме лиофилизированного препарата можно приготовлять также другие продукты. Микроорганизм можно вводить также после смещения отделенной путем центрифугирования или фильтрации массы бактерий с соответствующими носителями или разбавителями, например с карбонатом кальция, зерновыми культурами, премик- сом или другими кормовыми средствами.
В зависимости от применяемого корма и от направления выработки устанавливают, какой из приготовленных с помощью предлагаемого способа и благоприятно влияющих на флору рубца микроорганизмов воспринимается и в каком количестве. Если нужно снизить частное уксусная кислота - пропионовая кислота, то вводят, например, культуру штамма Proplonibacterium sp. HNCMB N2 00287, если нужно увеличить это частное, то дают, например, культуру микроорганизма Bifidobacterium sp HNCMB № 00289 (Нп-СУОК1-3-81Ме). Если вводят связывающие азот бактерии, то количество вводимого жвачным животным органического источника азота может уменьшаться. Культуру вводят в таком количестве, чтобы в 1 мл содержимого рубца функционировало около 5 X 102 и 5 X Ю7 клеток.
Пример 6.
A.Получение сухого замороженного препарата.
Полученная в соответствии с примером 5 путем центрифугирования влажная бактериальная паста ОЕ-950 весом 100 г ли- офилизируется в установке для сушки сублимацией. Затем полученные 54 г продукта тщательно смешивают с 486 г пшеничных отрубей и помещают в обеспечивающий защиту бактерий мешок (непроницаемый для бактерий). Получают препарат, содержащий 10% биологически активного вещества.
Б. Получение препарата, содержащего в качестве носителя пшеничные отруби.
100 г полученной в соответствии с примером 5 путем центрифугирования влажной пасты микроорганизма равномерно перемешивают со 100 г или 900 г пшеничных отрубей, затем помещают в обеспечивающий защиту бактерий мешок или контейнер. Таким образом получают содержащий 5 или 10% биологически активного вещества препарат.
B.Получение препарата, содержащего в качестве носителя бантонит.
100 кг бентонитного порошка стерилизуют при 160° С в течение 2 ч, затем после охлаждения до комнатной температуры помещают в смеситель. Смеситель приводят в действие, с помощью дозатора жидкостей
распыляют 10 кг полученной в соответствии с примером 5 суспензии микроорганизмов. Полученную суспензию высушивают при 30°С до достижения влажности 6-8% и по- мещают в обеспечивающие защиту бактерий мешки (емкости).
5 г продукта хранят при 4°С, при комнатной температуре или при 37°С, на нулевой, 20-й, 51-й и 72-й день берут пробы,
затем препарат суспендируют в стерильный НВ-смеси и после соответствующего разбавления засевают на агар RGCA. Выращивание осуществляют 48 ч в анаэробных условиях, затем определяют количество выращенных колоний.
Результаты приведены в табл. 6. Из данных табл. 6 видно, что количество бактерий в продукте, содержащем бентонит, практически не изменяется.
Г. Получение препарата, содержащего в качестве носителя аттапульгит.
100 кг коллоидного аттапульгита стерилизуют 2 ч при 160°С, затем после охлаждения до комнатной температуры помещают в
смеситель.
Смеситель приводят в действие, и через насадку дозатора жидкостей полученная в соответствии с примером 5 распыляемая суспензия микроорганизмов в количестве
10 кг распрыскивается на аттапульгит.
Полученную дисперсию высушивают при 30°С до достижения влажности 6% и помещают в обеспечивающие защиту бактерий мешки (емкости).
По 5 г продукта хранят при 4°С, при
комнатной температуре или при 37°С, затем на нулевой, 20-й, 51-й и на 72-й день берут пробы. Препарат суспендируют в стерильной НВ-смеси и после соответствующего
разбавления засевают на агар RGCA. Выращивание осуществляют 46 ч в анаэробных условиях, затем определяют количество выращенных колоний.
Результаты приведены в табл. 7.
Из данных табл. 7 видно, что количество
бактерий в продукте, содержащем аттапульгит, не изменяется.
Пример 7, Питательную среду RGCA + CG указанного в примере 4 состава засевают культурой штамма Propionibacterium sp. HNCMB N2 00287 (Hh-GYOK1-1-123Sz). Выращивание осуществляют в двух ферментерах с полезным объемом 5 л при 37 °С в анаэробных условиях. Ферментацию начинают с посева 10 мл приготовленного на питательной среде такого же состава иноку- лята и продолжают в течение 48 ч. Затем клетки отделяют центрифугированием в роторе с числом оборотов 5000/мин и полученный отцентрифугированный влажный осадок в количестве 53 г тщательно смешивают с 4 кг кукурузного шрота. Смесь разделяют на 8 частей и вводят 8-ми овцам. Животных предварительно заставляют голодать один день.
Животные получают препарат в возрасте 3 мес. В качестве контроля служат 8 животных. После дачи препарата продолжают кормление сеном, еженедельно опреде- ляют вес животных. Корм: луговое сено ad libitum (600-900 г/день) и 100 г/день добавки минеральной соли и витамина в носитель из кукурузного шрота.
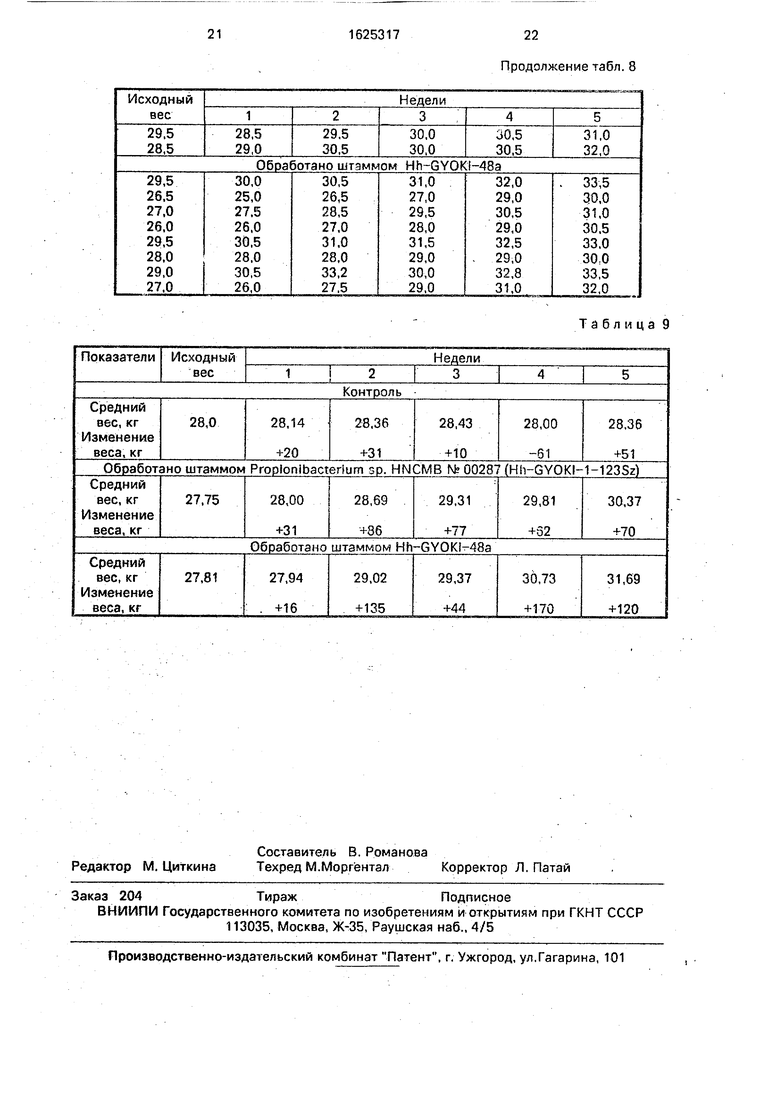
Результаты указаны в табл. 8.
Из приведенных данных рассчитывают средний ежедневный прирост веса одного животного. Результаты приведены в табл. 9.
У животных контрольной группы при скудном корме в течение 35 дней отмечается прирост веса 360 г; у обработанных штаммом Propionibacterium sp. HNCMB Nb 00287 (Hh-GVOK1-1-123Sz) животных увеличение веса 2620 г; у обработанных штаммом Нп- 6УОК1-48а животных прирост веса 3875 г. Из приведенных данных видно, что полученные с помощью предлагаемого способа препараты значительно повышают прирост веса овец.
Формула изобретения Способ получения препарата для кормления жвачных животных, включающий смешивание культуры микроорганизмов с целевыми добавками, отличающийся тем, что, с целью повышения продуктивности, в качестве культур микроорганизмов используют штамм Propionibacterium sp. HNCMB N2 00287, или штамм Vellonella sp. HNCMB № 00288, или штамм Bifldobacterium sp. HNCMB Ns 00289.






Изобретение относится к сельскохозяйственной биотехнологии и может быть использовано в животноводстве для кормления животных. Цель изобретения - повышение продуктивности. Для этого в качестве биологически активного ингредиента в препарате используют штамм Prapionlbacterium sp. HNCMB № 00287 или штамм Veilonella sp. HNCMB fsfe 00288 или штамм Blfldobacterlum sp. HNCMB . N 00289. Штаммы получают следующим образом: бактерии изолируют из отобранной из рубца пробы и исследуют способность отдельных изолятов к биосинтезу летучих жирных кислот. На дополненной соответствующим кормом (сено, овес, меласса) содержащей рубцовую жидкость комплексной питательной среде при анаэробных условиях выращивают полученные изоляты. Затем с помощью газохроматографического анализа определяют концентрацию уксусной, пропионовой и масляной кислот в культуре. Изоляты, продуцирующие указанные органические кислоты в предпочтительном соотношении, генетически маркируют. Далее исследуют их размножение в рубце жвачных животных. Полученные таким образом штаммы способны длительное время (не менее 60 дней) размножаться в рубце жвачных и поддерживать соотношение уксусной и пропионовой кислот в области (1,5-4,0): 1, Полученные культуры микроорганизмов сами по себе или смешанные с используемыми в животноводстве носителями, разбавителями и/или консервантами и/или с другими обычно вводимыми жвачным животным веществами формулируют в оральный препарат. 9 табл. (Л ю ел Сл
Таблица 1
Таблица 2
17
Неправильный отбор пробы.
1625317
18 Таблица 3
Т аблица 4
Таблица 5
Продолжение табл. 5
Таблица 6
Таблица
Та блица 8
Продолжение табл. 8
Таблица 9
| Первичный элемент | 1973 |
|
SU489367A3 |
| Нивелир для отсчетов без перемещения наблюдателя при нивелировании из средины | 1921 |
|
SU34A1 |
Авторы
Даты
1991-01-30—Публикация
1985-08-15—Подача