9-Карбазолилсодержащий полиоргано- силтриметилен получают полимеризацией карбазолилсодержащего органо-1 -силацик- лобутана в среде органического растворителя в присутствии регулятора молекулярной массы в вакууме или в инертной атмосфере. Мономе р-карбазол ил содержащий органо- 1-силациклобутан получают взаимодействием Mg-органического соединения из карбазолилалкил(арил)галогенидов с 1- хлор-1-алкил(арил)-1-силациклобутаном в среде эфира и тетрагидрофурана при температуре кипения растворителя. В свою очередь, карбазолилалкил(арил)-галогенид получают взаимодействием избытка а,а) -дигалогенидалкана с карбазолом в условиях межфазного катализа.
П р и м е р 1. Синтез CI(Br) (€N2)3- МС12Н8(хлор-бром-пропилкэрбазола).
К смеси 167 г (1,0 моль) карбазола и 630 г (4,0 моль) 1-хлор-З-бромпропана в 2 л толуола добавляют равный объем 50%-ного раствора КОН и тетрабутиламмонийбромид (7 мольн,% от карбазола). Смесь нагревают до 80-90°С и перемешивают до отрицательной реакции пробы на карбазол - обычно не менее 4 ч. Слои разделяют, органический промывают водой до нейтральной реакции. Сушат гранулированным или безводным сульфатом натрия. После удаления растворителя остаток хроматографируют в колонке с AlaOa или перегоняют в вакууме. Т кип, 161-165°С (0,008 мм). ПМР ( б м.д. в CCU от ТМС): 2,03 м (2Н,ССН2С), 3,2 м (2Н, CH2CI), 4,15 т (2Н, NCH2), 6,77-7,9 м (8НЧ ароматич.). Масс-спектр m/z, %: 243 М (100), Clf (14), 180 CrcHaNChfcf (5).
Найдено, %: С 73,9; Н 5,8; N 5,7; C115,1.
CisHnNCI
Вычислено, %: С 73,9; Н 5,7; N 5,7; CI 14,7.
Выход 192 г (83%), считая на хлорпро- пилкарбазол.
Синтез мономера 1-метил-1-у (9-карба- золилпропил)-1-силациклобутана.
К 30 г магния добавляют 70 мл абсолютированного тетрагидрофурана (ТГФ), 15 мл раствора 243,5 г (1,0 моль, считая на чистый) у-хлорпропилкарбазола в 0,45 л абсолютированного ТГФ и 2 мл дибромэтана. После того как реакция начнется, добавляют оставшийся раствор хлорпропилкарбазола так, чтобы температура была 40-55°С. По окончании добавления греют при 60°С 1 ч и, охладив до комнатной температуры, добавляют 1,1 моль 1-метил-1-хлор-1-силацикло- бутана в 200 мл ТГФ за 1 ч. Далее греют при 60°С 6 ч. и в вакууме удаляют растворитель и избыток метилхлорсипациклобутана. Ос0
таток суспендируют в 0,6 л сухого бензола и фильтруют. Операцию повторяют и осадок промывают на фильтре бензолом. Фильтраты концентрируют и хроматографируют в колонке с AlaOa (элюент гексан) бензол-2(1).
Выход 205 г( 70%). Масло, $°1,6136. Найдено, %: С 77,9; Н 7,9; N 4,6; SI 9.5.
C19H23NSI
Вычислено, %: С77,8; Н 7,8; N 4,8; SI 9.6.
Масс-спектр, m/z, %: 293 МТ(34), 265 M-C2H4f (29), 250 М-СНз-С2Н4Г(29), 180 Ci2H8NCH2f(100).
ПМР (б , м.д. вСС 40тТМС):0,18с(ЗН, CH2Si), 0,6-1,23 м (4Н, СН2 - а цикла, 5 2H,SiCH2CCN), 1,6-2,15 м (2Н, СН2-/3 цикла, 2Н, ССН2СМ), 4,12 т (2Н. CH2N), 6,87-7,42 м (4Н, карбазолил без о-протонов), 7,77-8,02 м (2Н, о-протоны карбазолила). ПК-спектр: 930, 1125, 1185 (силациклобутановое кольцо).
Получение полимера
0
31-СНг-СНг-СНг8 мл сухого углеводороднополи-1-метил-1-у -(9-карбазолилпропил)-1- силтриметилена.
A.В ампулу помещают 10 г мономера
С12Н8Н(СН2Ц()
СН3
го растворителя(бензол,толуол, ксилол, ди- кумилметан) и 3,5-5 мас.% высшего спирта (регулятор молекулярной массы, от СбЖзОН до ). Содержимое ампулы дегазируют и ампулу запаивают в вакууме. Нагревают 12-15 ч при 220-250°С до постоянной вязкости. Охлажденную ампулу вскрывают и полимер высаживают спиртом. Вновь растворяют полимер и переосаждают гексаном, промывают горячим спиртом. Сушат в вакууме при 50°С до постоянного веса. Выход 75-95%. Молекулярная масса 2,8 х 10 -1 104, которая здесь и далее определялась эбулиометрически в бензоле, х 9 , В ПК-спектре полосы моносила- циклобу анового кольца (930, 1125 и 1185 ) отсутствуют.
Б. Аналогично пункту А, но в качестве, регулятора молекулярной массы используют прокаленный КОН (концентрация КОН 0,05-0,08 мол/л). Температура 60-80°С,. время 72 ч. Выход 70-85%.
B.Аналогично пункту А, но используют инициатор полимеризации бутиллития (концентрация бутиллития 0,05 мол/л, концентрация мономера 1,0-2,0 мол/л).
0
5
0
5
5
Температура 20°С, время 48 ч. Молекулярная масса 2,5 хЮ3 (х 9). Выход 80-95%.
В случаях Б и В растворы полимеров эффективно отмывают водой от щелочности. 5
П р и м е р 2. Синтез 9-(д- бромбутил}- карбазола Br(CH2)4NCi2H8.
Аналогично примеру 1, но используют 5,0 моль 1,4-дибромбутана. Выход д -бром- бутилкарбазола после хроматографирова- 10 ния в колонке с 78%. Температура плавления 115,7-116,7°С.
Найдено, %: С 63,7; Н 5,2; N 4,8; Вг 26,8.
CiHHieNBr
Вычислено, %: С 63.6; Н 5,3; N 4,6; Вг 15 26,5.
Масс-спектр, m/z, %: 301/303 (18), 180 Ci2HeNCH2fa(100). ПМР(3 .м.д. в COj от ТМС): 1,73 м (4Н, ССН2СН2-С), 3,1 т (2Н, СН2Вг), 4,05 т(2Н, CH2N), 7,18 м (карбазолил 20 без о-протонов), 7,93 м (2Н, о-протоны кар- базолила).QI
I / 1-метил-1-8- CWH8U(CH2) Si У
425
(9-карбазолилбутил)-1-силациклобутана.
Аналогично примеру 1, но магнийорга- ническое соединение готовят из бромбутил- карбазола. Выход маслообразного
СН330
(CHz),,k)75% ° 16095
Найдено, %: С 78,1; Н 8,2; N 4,4; SI 9,2 C20H25NSI
Вычислено, %: С78.1; Н 8,1; N4,6; SI9.1. Jb ИК-спектр,930, 1125 и 1195 см сила- циклобутаное кольцо).
Масс-спектр m/z, %: 307 Mf(50), 279 M-C2H4f (23), 180 Ci2H8NCH2f (100). ПМР ( д м.д., в CCCI4 от ТМС): 0,17 с (ЗН, CH3SI), 40 0,71-2,5 м (6Н, SICH2CH2CH2C; 6Н, СН2 цикла), 4,1 т (2Н, CH2N), 6,8-8,01 м (8Н, карбазолил).
Получение полимера С12Н8И(СН2)4
45
$1 СН. СНч Iг г г
СН3
поли-1-метил-1 (9-карбазолилбутил(-1- силтриметилена.
Аналогично 1Б. Выход 77%. Молекулярная масса 2,9-103 ().
Полосы 930, 1125 и 1185 в ИК-спек- тре отсутствуют.
ПримерЗ. Синтез Br{CH2)sNCi2H8 9- (Е-бромпентил)карбазола.
Аналогично примеру 2 с использованием 1,5-дибромпентана. Выход Br(CH2)sNCi2H8
после хроматографирования 74%. Температура плавления 50,5-52,5°С.
Найдено, %: С 64.5; Н 5,55; N 4,5; Вг 25,6,
CiyHieNBr
Вычислено, %: С 64.6; Н 5,7; N 4,4; Вг 25,3
Масс-спектр, m/z, %: 315/317 Mf (35). 235 M-HBrf (18), 180 (HeNC f OOO). ПМР(с5 , м.д. в ССЦ от ТМС): 1,12-2,05 м(6Н. С(СН2)зС),3.1т(2Н,СН2Вг),4,1т(2Н,СН2М), 6,87-8,03 м(8Н, карбазолил).
Синтез 1-метил-1- Ј -(9-карбазолилпен СН3тил) илациклобутана 12Н(СН2)5 ..у
Аналогично примеру 1, но магнийорга- ническое соединение готовят из е -бромпен- тилкарбазола. Выход маслообразного СН3
с12н8жснг)ДО 67% ТемпеРатУРа
застывания 16-23°С.
Найдено, %: С 78,65; Н 8,3; N 4,5; Si 8,6.
C2iH2 N5i
Вычислено; %: С78,5; Н 8,4; N 4,4; Si 8,7.
ИК-спектр содержит полосы 930, 1125, 1180 (силациклобутановое кольцо).
Масс-спектр m/г, %: 321 Mf (41), 293 M-C2H4f (24), 278 M-CH3-C2H4f(20), 180 Ci2H8NCH2f (100).
ПМР ( д , м.д. в ССЦ от ТМС): 0,165 м (ЗН, CHsSi), 0,62-2,56 м (6Н, цикла; 8Н. Si(CH2)4C), 4,05 т(2Н, CH2N), 6,9- 8,01 м (8Н, карбазолил).
Получение полимера поли-1-метил-1- к- (9-карбазолилпентил)1-силтриметилена
.С,2Нвй(СН2)5
: Xsi-CH2-CH2-CH2 -4
СЧ3
Аналогично примеру 1А. Выход 72%.
Мол. масса 3,6-10 ().
П р и м е р 4.
Синтез
sHCH -NCuHe 1-фенил-1- у-(9-карбазолил- пропил)-1-силациклобутана.
Аналогично примеру 1, но в качестве хлорсилациклобутанового компонента используют 1-хлор-1-фенил-1-силациклобутан
С,Н5
О:
ci
Выделение хроматографированием и перекристаллизацией из смеси гексан (бен- зол-3)1. Выход 64%. Температура кипения 69-70, 5°С.
Найдено, %; С 81,3; Н 7,25; N 4,2; SI 8,2.
C24H25NSI
Вычислено, %: С 81.1; Н 7,05; N 3,95; Si 7,9.
ИК-спектр содержит полосы 930, 1125, Н 7,0 1190 (силациклобутановое кольцо). Масс-спектр, m/z, %: 355 (100), 327 M-C2H4f (57), 328 M-C2H5f (34), (22), 180 Ci2H8NCH2f (74).
ПМР((5 .м.д., вССиотТМС):0,91-1,44 м(4Н,а-СН2цикла;2Н. CH2SI), 1,73-2,38 м (2Н, уЗ-СН2 цикла, 2Н, ССН2С). 4,23 т (2Н, CH2N), 6,88-7,6 м (5Н, фенил, 6Н, протоны м- и п-положений карбазолила), 7,98 м (2Н, о-протоны карбазолила).
Получение полимера
Ci2H8H(CH2)j
tsi-CHj-CHj-CHz j- iBH5J
JA
поли-1 фенил-1--у -(9-карбазолилпропил)-1- силтриметилена ().
Аналогично примеру 1А. Выход 91%. Мол.массаЗ,8103(). ИК-спектр полимера не содержит полосы 930,1125 и 1185 см 1.
сен5
Пример5.Синтез 1(
1-фенил-1- 5 -(9-карбазолилбутил)-1 сила- циклобутана.
Аналогично примеру 4, но в качестве алкилирующего агента используют б -бром- бутилкарбазол. Выход маслообразного - (9-кэрбазолилбутил)-1-фенил-1-силацикло
бутана62%, г$ 1,6183.
Найдено, %: С 81,5; Н 7,5; N 4,1; Si 7,7.
C25H27NSi
Вычислено, %: С 81,3; Н 7,3; N 3,8; SI 7,6.
ИК-спектр содержит полосы 930, 1120, 1185 (силациклобутановое кольцо). Масс-спектр, m/z, %: 369 Mf (23), 341 М- С2Н4(15), 180 С12Н8МСН2(100). ПМР(б, м.д., в ССЦ от ТМС): 0,75-2,5 м (6Н, Si(CH2)3C, 6H, а- и/3 -СН2 цикла), 4,18 т (2H,CH2N), 6,95-8,25 м (13Н карбазолил и фенил),
Получение полимера C12H8N(CH2)4
--$i-CH2-CH2-CHj
С6Н5
поли-1-фенил-1-б -(9-карбазол ил бутил )-1- силтриметилена.
Аналогично примеру 1А. Выход 88,5%. Мол. масса 3,3«103 (х 10). Полосы 930, 1125 и 11,85 в ИК-спектре отсутствуют. Примерб. Синтез
C12H8N(CH2)3Si-Cl
-(9-карбазолилпропил)-диметилхлорсилана,
0
5
0
5
0
В колбу с обратным холодильником и капельной воронкой помещают 5 мл раствора 103,5 (0,5 моль) аллилкарбазола и 0,55 моль диметилхлорсилана в 250 мл абсолютного бензола и 0,1 мл 0,1 М раствора H2PtCle 6H20 в изопропаноле. Нагревают до начала реакции (резкое потемнение раствора) и в течение 12 ч добавляют оставшийся раствор при непрерывном кипячении. Добавляют 0,05 мл свежего раствора катализатора и 0,2 моль диметилхлорсилана и кипятят еще 16ч. После удаления растворителя и избытка диметилхлорсилана остаток перегоняют в вакууме. Выход 76,5%. Температура плавления 164,5-167°С (0,003
мм), ° 1,6135.
Найдено, %; С67,9; Н 6,75; N4,5; Si 9,5; C111,5.
Ci7H2oNSfCI
Вычислено, %: С 67,7; Н 6,6; N 4,6; Si 9,3; CI 11,8,
Масс-спектр, m/z, %: 369/371 Mjt 2.5(1,0), 354/356 М-СНз Ц1,6), 234 М-СН2- С1 (3,6), 180 Ci2H8NCH2p(100).
ПМР (д , м.д., в CCI4 от ТМС): 0,71 с (6Н, CH3Si), 1,09 м (2Н, CH2SI), 2.04 м (2Н, ССН2С), 4,2 т (2Н, CH2N), 6,8-8,06 м (8Н. карбазолил).
Синтез мономера 1-метил-1-п- у-(9-кар- базолилпропил)-диметилсилилфенил)-1-си- лациклобутана СН7СН
.I 3
( Si-(CH2)3-NC12H8 СН3
5
0
5
0
5
К 12 г (0,5 r-ат) магния в 50 мл абсолютного ТГФ добавляют 5 мл раствора 105 г (0,41 моль) п-бромфенилметилсилациклобу- тана в 350 мл ТГФ. После начала реакции добавляют оставшийся раствор так, чтобы температура поддерживалась 35-40°С. По окончании добавления 4 ч) греют при 50,- 55°С 1 ч. К раствору добавляют в течение 2,5 ч раствор 107 г (0,34 моль) Ci2H8N(CH2)3Si(CH3)2C в 250 мл ТГФ. По окончании добавления греют при 65°С 6 ч. Добавляют 0,5 л толуола и разлагают водой. Слои разделяют и водный экстрагируют толуолом. После высушивания удаляют в вакууме толуол и другие легколетучие и остаток хроматографируют в колонке с А12Оз(1И степень активности, элюирование смесью бен- зол/гексан-1/3 по объему). Выход 57,5%. Температура плавления 44,5-47°С.
Найдено, %: С75,85; Н 7,8; N3,5; S113,1.
C2yH33Si2N
Вычислено, %: С 75,9; Н 7,7; N 3.5; SI 13,1.
Масс-спектр, m/z, %: 427 М (100), 399 М-С2Н (18), 385 М-СзНеГ (18), 180 Ci2H8NCH2lt (56).
10
15
ПМР (д , м.д., В ССЦ от ТМС) :0,2 с (6Н (СНзЬЗ), 0,52 с (ЗН, CHaSi), 0,65-1,4 м (2Н, SICH2CC, 4Н, «-СН2 цикла), 1,5-2,35 м (2Н, .NCCH2CSi, 2Н, Д-СН2 цикла). 4,09 м (2Н, CH2N), 6,83-7,48 м (4Н, фенилен; 6Н, карба- золил), 7,75-7,97-м (2Н, о-протоны карбазо- лила).
Получение полимера c,jHeW(CH2)3-sKCHj)2 свн4
-81-СН2-СН2-СНг-- СН3
поли-1-метил-1-п у -(9-карбазолилпро- пил)диметилсилилфенил}-1-силтриметиле - на.
Аналогично примеру 1А. Выход 90%. Мол.масса 3,1 103 ().
Полосы силациклобутанового кольца 930, 1125 и 1185 в ИК-спектре отсутст- 20 вуют.
Для всех полученных полимеров ПМР- спектры имеют следующие значения:
1.0.1 с (ЗН, SICH3), 0.6-1,07 .м (4Н. Si. СН2 основной и 2H.SI-CH2 боковой цепи). 25 1.1-1,85 м (2Н, С-СН2-С основной цепи и 2Н, С-СН2-С боковой цепи). 4,2 м (2Н, CH2N), 6.9-8,1 м(8Н протоны карбазолила).
2.0.08 с (ЗН, Si-СНз). 0,6-2,1 м (6Н, SI- СН2СН2 СН-С с боковой цепи и 6Н, Si- 30 CH2CH2CH2S основной цепи), 4,17 м (2Н. CH2N), 6,95-8,12 с (8Н, протоны карбазолила).
3.0,06 с (ЗН, SI-СНз), 0.53-2,17 М (8Н. 35 SI-CH2-CH2-CH2- с боковой цепи и 6Н, SICH2CH2CH2SI основной цепи), 4.06 м (2Н, CH2N), 0,9-8.15 (8Н, карбазолил).
4.0,66-1,16m (4H.SICH2 основной цепи 2Н,51-СН2 боковой цепи), 1,15-1,8 м (2Н; 40
С-СН2С боковой цепи), 4.2 м (2Н, CH2N), 6.87-8,07 м (8Н, протоны карбазолила и 5Н, фенил).
0
5
0
5
0
5.0,67-2,18 м (6Н. S CH2CH2CH2 с боко- ьой цепи и 6Н, SICH2CH2SIC основной цепи), 4,2 м (2Н, CH2N), 6,95-8.3 м (13Н, карбазолил и фенил).
6.0.1-0,62 (9H.SI-CH3 и 5(СНз)Д 0.65- 1,96 м (6Н, SICH2CH2CH2SI основной цепи, 4Н, SI-CH2-CH2 боковой цепи), 4.1 м (2Н, CH2N), 6,81-8,00 м (8Н, карбазолил и 4 м фенилен).
Полученные соединения испытывают при изготовлении электрофотографических материалов.
На полиэтилентерефталатную металлизированную подложку наносят раствор сополимера метилфенилсилоксана с 9-эпоксипропилкарбазолом (известное соединение), а также каждое из соединений, полученное в примерах 1-6 (в 90 г толуола растворяют 9,5 г полимерного соединения и 0,5 г тринитрофлуорена - ТНФ).
Полученный слой сушат до постоянного веса. Толщина высушенного слоя составляет 1,7-1,8 мкм.
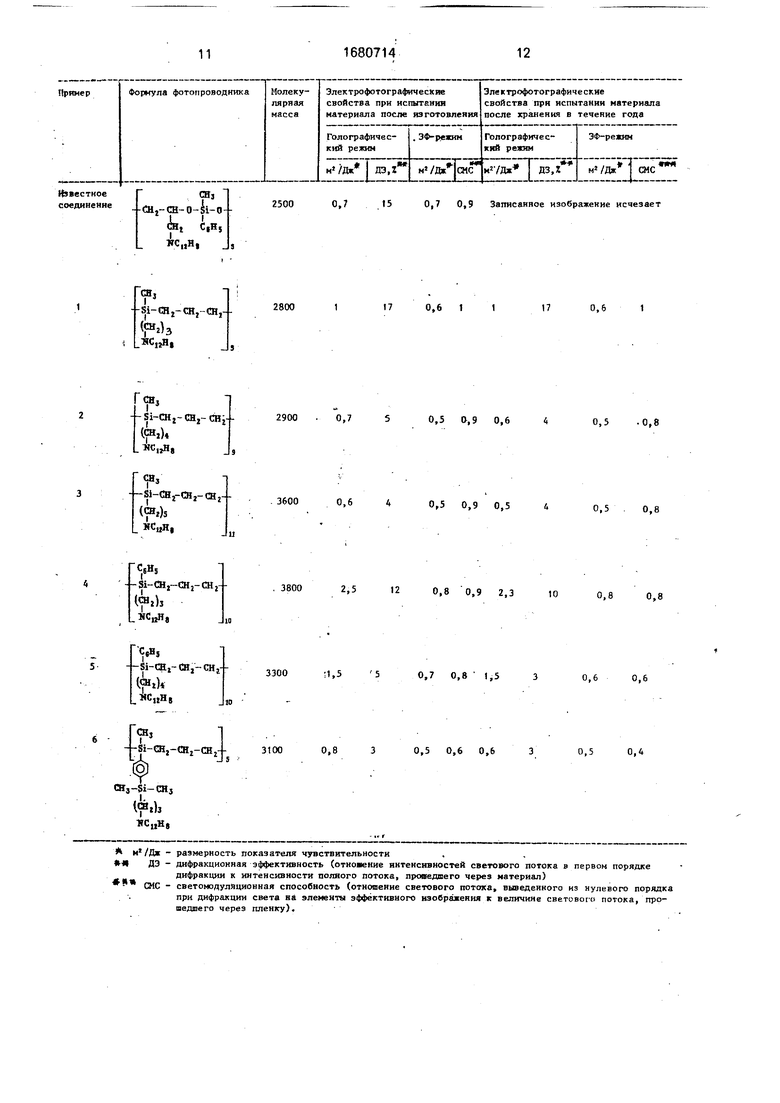
Полученный материал испытывают на частоте 200 мм . Результаты испытаний образцов в голографическом и электрофотографическом (ЭФ) режимах после изготовления материала и после хранения в течение 1 года представлены в таблице.
Формула изобретения
9-Карбазолилсодержащий полиоргано- силтриметилен формулы
I Г
где х 5-11;
Р-(СН2)п.,(СН2)з51(СНзКбН4:
Ri СНз.СбНб.
в качестве фотопроводника электрофотографического материала.




| название | год | авторы | номер документа |
|---|---|---|---|
| ФОТОТЕРМОПЛАСТИЧЕСКИЙ НОСИТЕЛЬ ЗАПИСИ | 1991 |
|
RU2035063C1 |
| Способ получения азонийспиронортропанолового сложного эфира | 1986 |
|
SU1711674A3 |
| КАТИОННЫЕ ДИМЕРНЫЕ АМФИФИЛЫ В КАЧЕСТВЕ АГЕНТОВ ТРАНСФЕКЦИИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2002 |
|
RU2233834C2 |
| 1-ОМЕГА-АРИЛОКСИАЛКИЛ- И 1-БЕНЗИЛЗАМЕЩЕННЫЕ 2-ИМИНОБЕНЗИМИДАЗОЛИНЫ И ИХ ФАРМАКОЛОГИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ОБЛАДАЮЩИЕ ПРОТИСТОЦИДНОЙ И АНТИМИКРОБНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2514196C1 |
| 5-АМИНО-3-(2-АМИНОПРОПИЛ)-[1,2,4]ТИАДИАЗОЛЫ | 2011 |
|
RU2449997C1 |
| Способ получения (S)-3Z-додецен-11-олида | 1990 |
|
SU1773913A1 |
| Способ получения эфиров 2,6-диметил1,4-дигидропиридин-3,5-дикарбоновой кислоты | 1977 |
|
SU740768A1 |
| Способ получения S-триметилсилиловых эфиров дитио- или тетратиофосфорных кислот | 1990 |
|
SU1735300A1 |
| Способ получения алкил(арил)производных 5,6-бензо-1,7-нафтиридина | 1990 |
|
SU1766918A1 |
| Способ получения 2,2-диалкил-2Н-имидазол-1-оксидов | 1988 |
|
SU1770321A1 |
Изобретение относится к химико-фотографической промышленности, в частности к новому веществу - 9-карбазолилсодержа- щему полиорганосилтриметилену формулы -1 Изобретение относится к химико-фотографической промышленности, в частности к новому веществу - 9-карбазолилсодержа- щему поллорганосилтриметилену формулы где х 5-11; -IX где х 5-11; R (СН2)п; где п 3-5, (СН2)з5(СНз)2СбН4; RI СНз, СбН5, которое может быть использовано в качестве фотопроводника для электрофотографических материалов. Изобретение позволяет повысить стабильность записанного изображения на электрофотографическом материале - чувствительность исходная в голографическом режиме составляет 0,6- 2.5 м /Дж и в электрофотографическом режиме 0,5-0,8 м /Дж, после хранения материала в течение года она составляет в этих режимах соответственно 0,5-2,3 м2/Дж и 0.5-0,8 м2/Дж; дифракционная эффективность исходная в голографическом режиме составляет 3-17%, после хранения материала в течение года - также 3-17%; светомодуляционная способность исходная в электрофотогрзфическом режиме составляет 0,6-0,9, после хранения материала в течение года - 0,4-0,8. 9-Карбазолилсодер- жащий полиорганосилтриметилен получают полимеризацией карбазолилсодержащего органо-1-силациклобутана в среде органического растворителя в присутствии регулятора молекулярной массы в вакууме или инертной атмосфере, 1 табл. R (СНа)п, . где п 3-5, (СН2)з51(СНз)2СбН4; R СНз, СеН5, которое может быть использовано в качестве фотопроводника для электрофотографи- ческих материалов. Целью изобретения является повышение стабильности записанного изображения на электрофотографическом материале в процессе хранения. fe О 00 о X Ј 

| Гетманчук Ю.П., Соколов П.И | |||
| О структуре и спектральной чувствительности некоторых олигомерных фотопроводниКов, сенсибилизированных различными акцепторами электронов, - Фундаментальные основы оптической памяти и среды, вып | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
Авторы
Даты
1991-09-30—Публикация
1989-05-22—Подача