Изобретение относится к непредельным кетонам, конкретно к усовершенствованному способу получения непредельных /5-дикетонов, которые являются ценным сырьем для получения полимеров с заранее заданными свойствами.
Известен способ получения метакрои- лацетона путем конденсации метилметак- рилата и ацетона в присутствии метилата натрия.
Процесс проводят при эквимолярном соотношении реагентов, смешивают свежеприготовленный метилат натрия, ацетон и метилметакрилат (с ингибитором) при 0° С. Смесь выдерживают ночь в холодильнике, затем выливают на лед с кислотой, экстрагируют эфиром, сушат, отгоняют растворитель, фракционируют в вакууме. Ме- такроилацетон, содержащийся в первой фракции, выделяют в виде медного комплекса, который после перекристаллизации из 90% этанола разлагают 10% серной кислотой, экстрагируют эфиром, сушат отгоняют растворитель и опять фракционируют в вакууме. Выход целевого продукта составляет 5%.
Наиболее близким из известных является способ, получения непредельных дикето- нов, в частности кротонилацетофенона, при помощи взаимодействия хлррангидрида непредельной карбоновой кислоты с натрий- кетоном, приготовленном из амида натрия и кетона в среде диэтилового эфира.
Методика состоит в следующем.
а) Получение амида натрия.
К 300 мл жидкого аммиака прибавляют при перемешивании небольшими порциями металлический натрий и кристаллическое железо в качестве катализатора. После прибавления всего количества натрия (переход голубой окраски раствора в серую) смесь перемешивают еце 15 мин. Жидкий аммиак выпаривают над паровой баней до 100 мл и прибавляют 200 мл безводного эфира. Пол4 f
Ё
ю
Ј
XI
кэ
ученный раствор амида натрия в эфире нагревают при перемешивании с обратным холодильником в течение 0,5 ч и охлаждают до комнатной температуры. Получают 0,3 моль амида натрия в эфире.
б)Получение натрий-кетона.
К 0,3 моль амида натрия в безводном эфире прибавляют 0,3 моля кетона в 75 мл безводного эфира и перемешивают в течение 20 мин. Затем пропускают сухой газообразный азрт для полного удаления аммиака.
в)Получение непредельного / -дикето- на.
Эфирную суспензию натрий-кетона (0,3 моля) охлаждают до -40° С и прибавляют при быстром перемешивании 0,15 моля хло- рангидрида непредельной карбоновой кислоты в эфире. После перемешивания в течение 20 мин при (-30)-(-40)° С, реакционную смесь подкисляли путем добавления 27 мл конц. HCI в 100 г льда. Реакционную смесь встряхивают и отделяют два слоя. Эфирный слой, соединенный с эфирной вытяжкой водного слоя, промывают насыщенным раствором бикарбоната натрия, затем сушат и удаляют растворитель. Неацилиро- ванный кетон удаляют перегонкой, а остаток фракционируют в вакууме. Получают 49% кротонилацетофенона.
Этот способ обладает целым рядом существенных недостатков, основными из которых является препаративная сложность, взрыво- и пожароопасность, длительность процесса.
Получение амида натрия требует особых условий работы: низкая температура (около -40° С), так как температура кипения жидкого аммиака составляет - 33,5° С; взрыво- и пожароопасность как исходных веществ (аммиак, образующий с воздухом взрывоопасные смеси, и металлический натрий), так и продукта реакции - амида натрия. Взрыво- и пожароопасность работ с этими веществами ведет к ограничению объема (массы) синтеза и сложности контроля реакции на протяжении всех стадий получения непредельного / -дикетона, а также не дзет возможности использовать этот процесс в производстве.
Многостадийность процесса, препаративная сложность, обеспечение низких температур и постепенных загрузок обуславливают значительную длительность процесса (более 50 ч).
Далее, реакция конденсации является сильно экзотермической и необходимость проведения ее в условиях сильного охлаждения (-30)-(-40)° С и поддержания ее в ходе реакции является процессом трудоемким.
Обработка продукта реакции на стадии очистки насыщенным раствором бикарбоната натрия может привести к образованию натрийпроизводных / -дикетонов, что загрязняет целевой продукт и значительно снижает его выход.
Кроме того, выход 49% вряд ли можно
считать высоким.
Целью изобретения является повышение выхода продукта, упрощение и повышение безопасности проведения процесса. Поставленная цель достигается тем, что
для получения непредельных ациклических /3-дикетонов взаимодействием хлорангид- рида непредельной карбоновой кислоты и производного кетона, в качестве последнего используюттриалкиламмонийкетон и гексан.
Сущность предлагаемого метода состоит в том, что к триалкиламмонийкетону, полученному при взаимодействии триал- киламина и кетона, прибавляют в среде
абсолютного гексана хлорангидрид непредельной карбоновой кислоты.
П р и м е р 1. Получение метакроилаце- тона.
К 0,5 моля (36,7 мл) сухого ацетона прибавляют постепенно при перемешивании 0,5 моля (69,7 мл) триэтиламина. Смесь нагревают при 30° С в течение 20 мин и охлаждают до 0-(-5)° С при помощи ледяной бани. К полученному триэталаммонийкетону прибавляют по каплям 0,5 моля (48 мл) хлоран- гидрида метакриловой кислоты в 60 мл абсолютного гексана с ингибитором. В качестве ингибитора используют гидрохинон - 2% от массы ангидрида. Реакционную
смесь перемешивают в течение 10-15 мин при ледяном охлаждении и в течение 2 ч без ледяного охлаждения. Затем реакционную смесь отделяют от выпавшего в осадок три- этиламмонийхлорида, добавляют 100 г размельченного льда, отделяют два слоя. Органический слой, соединенный с эфирной вытяжкой водного слоя сушат .над сульфатом натрия и удаляют растворитель. Остаток фракционируют в вакууме.
Получают 73,2 г (58%) метакроилацетона.
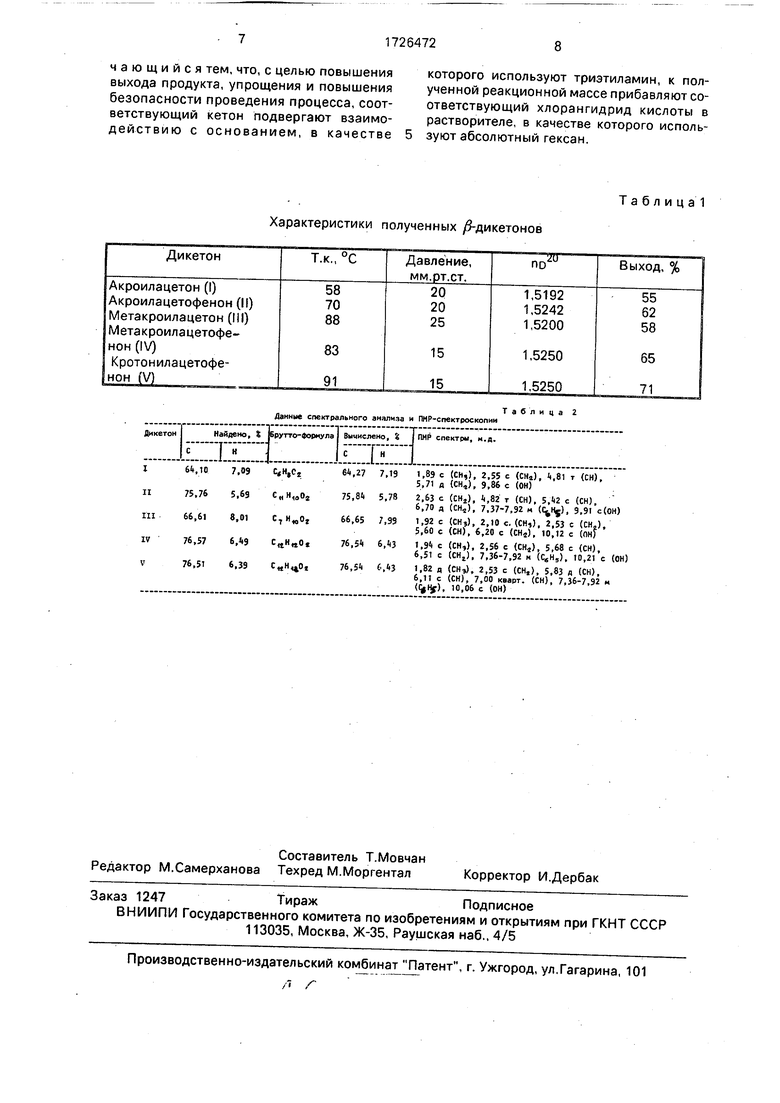
Характеристики полученного продукта приведены в табл. 1 и 2.
П р и м е р 2. Получение метакроилацетона.
Получают по аналогичной методике. Берут 0,5 моля (36,7 мл) сухого ацетона, 0,5 моля (58 мл) N-метилдиэтиламина и 0,5 моля (48 мл)хлорангидрида метакриловой кислоты (с ингибитором) в 60 мл абсолютного гек- сана.
Получают 72,1 г (57,2%) метакроилаце- тона.
П р и м е р 3. Получение метакроилаце- тона.
Получают по аналогичной методике. Берут 0,5 моля-(36,7 мл) сухого ацетона, 0,5 моля (70,2) N.N-диметилбутиламина и 0,5 моля (48 мл)хлорангидрида метакриловой кислоты (с ингибитором) в 60 мл абс. гексана.
Получают 72 г (57%) метакроилацетона.
П р и м е р 4. Получение метакроилаце- тофенона.
Получают по аналогичной методике. Берут 0,5 моля (58,4 мл) сухого ацетофенона, 0,5 моля (69,7 мл) триэтиламина и 0,5 моля (48 мл) хлорангидрида метакриловой кислоты в гексане.
Получают 122,2 (65%) метакроилацето- фенона.
Характеристики продукта приведены в табл. 1 и 2.
П р е р 5. Получение метакроилаце- тофенона.
Получают по аналогичной методике. Берут 0,5 моля (58,4 мл) сухого ацетофенона, 0,5 моля (58 мл) N-метилдиэтиламина и 0.5 моля (48 мл) хлорангидрида метакриловой кислоты (с ингибитором) в гексане.
Получают 121,8 г (64,8%) метакроилаце- тофенона;
Примерб. Получение метакроилаце- тофенона.
Получают по аналогичной методике. Берут 0,5 моля (58,4 мл) сухого ацетофенона, 0,5 моля (70,2 мл) М,М-диметилбутиламина и 0,5 моля (48 мл) хлорангидрида метакриловой кислоты (с ингибитором) в гексане.
Получают 121 г(64,4%)метакроилацето- фенона.
П р и м е р 7. Получение акроилацетона.
Получают по аналогичной методике. Берут 0,5 моля (36,7 мл) сухого ацетона, 0,5 моля (69,7 мл) триэтиламина и 0,5 моля (40,6 мл) хлорангидрида акриловой кислоты (с ингибитором) в абсолютном гексане.
Получают 61,5 г (55%) акроилацетона.
Характеристики продукта даны втабл. 1 и 2.
ПримерЗ. Получение акроилацетофе- нона.
Получают по аналогичной методике. Берут 0,5 моля (58,4 мл) сухого ацетофенона, 0,5 моля (69,7 мл) триэтиламина и 0,5 моля (40,6 мл) хлорангидрида акриловой кислоты (с ингибитором) в абс.гексане.
Получают 108 г(62%)акроилацетофенона.
Характеристики продукта приведены в табл. 1 и 2.
П р и м е р 9. Получение кротонилацето- фенона.
Получают по аналогичной методике.Берут 0,5 моля (58,4 мл) сухого ацетофенона,
0,5 моля (69,7 мл) триэтиламина и 0,5 моля (52,25 мл) хлорангидрида кретоновой кислоты в гексане.
Получают 133,6 г (71%) кротонилацето- фенона.
Характеристики продукта приведены в табл. 1 и 2.
Чистота продуктов контролировалась газохроматографическим методом на хроматографе ЛХМ-8МД-5 в следующих условиях: газ-носитель - гелий, скорость 30 мл/с с детектированием по теплопроводности при температуре колонки 190° С, испарителя 250° С, детектора - 250° С. Длина колонки 3 м, фаза 10% СКТФВ-803 на хромосорбе G.
ПМР-спектры записывались на приборе Bruker WM с рабочей частотой 250 МГц в растворе .
Как видно из приведенных данных, предлагаемый способ содержит ряд существенных преимуществ по сравнению с известным:
Упрощение метода состоит в том, что реакция практически проходит в одну стадию, в мягких условиях, устраняет взрыво- и
пожароопасные реагенты, прост в препаративном отношении. Синтез протекает при 0° С, в отличие от температуры (-30)-(-40)° С, указанной с прототипе.
Сокращение времени синтеза от г 50 ч
до 6 ч и отсутствие ограничений на массу реагирующих веществ дает возможность получить значительные количества непре- дельных/5-дикетонов, т.е. открывает путь их использования не только для лабораторных
исследований, но и широкого применения в различных областях техники.
Применение гексана в этом способа увеличивает выход целевого продукта, так как делает основную реакцию образования
непредельного/ -дикетона необратимой и выделение триалкиламмонййгидрохлорида из сферы реакции в виде осадка значительно упрощает очистку конечного продукта. Предложенный способ значительно повышает выход целевого продукта: в 1,43 раза больше, чем по методу прототипа.
Формула изобретения
Способ получения непредельных Д-ди- кетонов с использованием хлорангидрида непредельной карбоновой кислоты, алифатического или ароматического кетона, основания и органического растворителя, отл ичающийся тем, что, с целью повышения выхода продукта, упрощения и повышения безопасности проведения процесса, соответствующий кетон подвергают взаимокоторого используют три ученной реакционной масс ответствующий хлоранги растворителе, в качестве
действию с основанием, в качестве 5 зуют абсолютный гексан.
которого используют триэтиламин, к полученной реакционной массе прибавляют соответствующий хлорангидрид кислоты в растворителе, в качестве которого исполь


| название | год | авторы | номер документа |
|---|---|---|---|
| Эфиры или амиды 3-метил-3-(4-метилпентен-3-ил)-фенилпропен-2-овой кислоты как инсектициды с ювенильной активностью | 1975 |
|
SU681044A1 |
| СПОСОБ ПОЛУЧЕНИЯ ФТОРСОДЕРЖАЩИХ ТЕТРАКЕТОНОВ | 2010 |
|
RU2421442C1 |
| Способ получения акриловых или метакриловых эфиров алканоламидов перфторированных кислот | 1975 |
|
SU549461A1 |
| Способ получения хлорсодержащих олигоэфиракрилатов с симм-триазиновым циклом | 1974 |
|
SU546612A1 |
| 3-ФЕНОКСИФЕНИЛСОДЕРЖАЩИЕ 1,3-ДИКЕТОНЫ В КАЧЕСТВЕ ИСХОДНЫХ СОЕДИНЕНИЙ ДЛЯ ПОЛУЧЕНИЯ ИХ ХЕЛАТНЫХ КОМПЛЕКСОВ С ИОНАМИ МЕДИ (II) И СПОСОБ ПОЛУЧЕНИЯ 3-ФЕНОКСИФЕНИЛСОДЕРЖАЩИХ 1,3-ДИКЕТОНОВ | 2012 |
|
RU2475473C1 |
| Способ получения макроциклических кетонов | 1958 |
|
SU120841A1 |
| Акриловый или @ -замещенные акриловые эфиры 4-оксиметилкарена-2, обладающие фунгистатической, бактериостатической и гербицидной активностью | 1980 |
|
SU926900A1 |
| ОЖЙТНО-ИХКЙЧЕСИБИБЛИОТЕКА | 1971 |
|
SU309933A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЦЕТИЛЕНОВЫХ КЕТОЭПОКСИДОВ | 1991 |
|
RU2021265C1 |
| ПРОИЗВОДНЫЕ 1Н-3-АРИЛ-ПИРРОЛИДИН-2,4-ДИОНА, ИСХОДНЫЕ И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ИХ ПОЛУЧЕНИЯ И СРЕДСТВО ДЛЯ БОРЬБЫ С ПОВРЕЖДАЮЩИМИ РАСТЕНИЯ НАСЕКОМЫМИ И КЛЕЩАМИ | 1994 |
|
RU2144034C1 |
Изобретение касается кетонов, в частности получения непредельных /3-дикетонов, которые могут быть использованы в качестве мономеров для получения полимеров с заранее заданными свойствами. Цель - упрощение, сокращение длительности и повышение безопасности процесса. Его ведут добавлением к смеси триэтиламина с соответствующим кетоном раствора в гексане хло- рангидрида ненасыщенной кислоты. Полученный кетон выделяют вакуумной разгонкой. Эти условия обеспечивают повышение выхода целевого продукта с 40 до 55-64% при проведении процесса в одну стадию с использованием невысокого нагревания (0° С против -40° С), пожаробезопасных реагентов и сокращения времени синтеза с 50 до 6 ч. 2 табл.
Характеристики полученных / -дикетонов
Данные спектрального анализа и ПМР-спектроскопии
Таблиц а 1
Таблица 2
| Ph | |||
| Teyssie u G.Smets Makromol | |||
| Chem | |||
| Прибор для получения стереоскопических впечатлений от двух изображений различного масштаба | 1917 |
|
SU26A1 |
| Льночесальная машина | 1923 |
|
SU245A1 |
| B.O.LInu u C.R.XauserJ | |||
| Amer, Chem | |||
| Soc | |||
| v | |||
| Парный автоматический сцепной прибор для железнодорожных вагонов | 0 |
|
SU78A1 |
| Двухлопастной водяной или воздушный гребной винт | 1926 |
|
SU6066A1 |
Авторы
Даты
1992-04-15—Публикация
1989-09-15—Подача