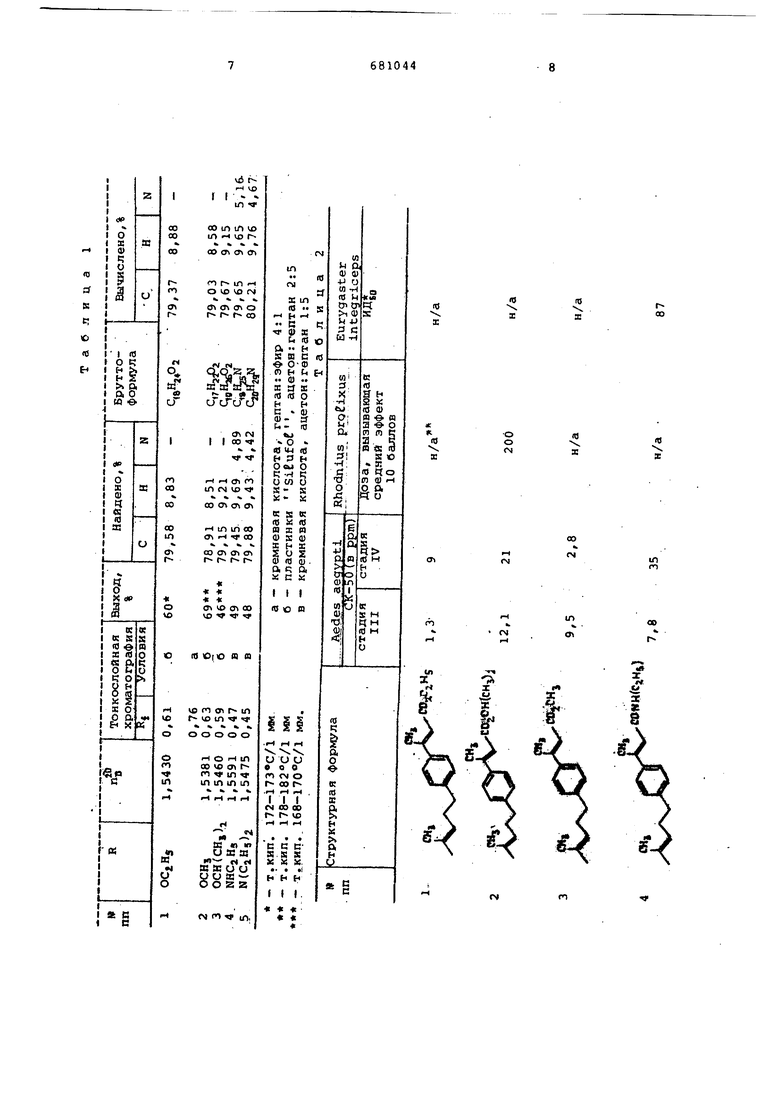
Изобретение относится к новым пр изводным коричной кислоты, а именно к эфирам или амидам 3-метил-3-(4-метилпентен-З-ил)-фенилпропен-2-овой кислоты формулы I где R - OR, NHR, NR R - CHs, CjHs, CH(CHj)a , обладающим избирательной ювенильной ги тивностью (Ш) на комарах Aedes aegypti. Известные вещества с ЮА, как правило, обладают широким спектром действия на различных группах насекомых, хотя степень активности может различаться. Примером такого вещест ва являются смесь Лоу, которая проявляет приблизительно одинаковую ;активность на комарах, клопах и вре 1ной черепашке 1. Основной компонент ее известен в качестве инсектицида с ЮА; смесь .Лоу служит удобным эталоном при б рлогическнх испытаниях 2. Известны также некоторые производные замещенной коричной кислоты обСНгщей формулы R-O- CH-COOR, где R-Н, алкил, R - Зс1мещенные или незамещенные фенил и циклогексил, применяющиеся как инсектициды, нарушающие метаморфоз насекомых различных видов 3 . Однако эти соединения так же, как и производные замещенной коричной кислоты общей формулы f-.СИ, -R../ -(CH2)rt-C CH-CC)OR ,3) 4 имеют слишком широкий диапазон действия, и их нельзя применять против определенного вида насекомых. Цель изобретения - получение эфиров или амидов замещенной 3-метил-З-фенилпропен-2-овой кислоты общей формулы (I) как инсектицидов к избирательной ГОАс Полученные производные формулы (I) , отличаиотся солективным действием против комаров Aedes aegypti, что позволяет расширить ассортимент избирательно действукчцих соединений с ЮА. Соединений формулы .(I), где R -- , OCjHg получают из этилового эфира п-ацетил-д-фенилмасляиой кислоты (И) взаимодействием с этиленгликолем, полученный при этом этиленкеталь подвергают взаимодействий с метилмагнийодидом с последующим гидролизом и дегидратацией до кетона (IV). Полученный кетон подвер-гают ззаимодейст(MjOHb JC%0)s,fCU где Эфиры общей (I)f где R - OCHj, ОСН{СН5)2 получают перетерефикацией этилового эфира формулы со.отнетствующими спиртами. Агхшды общей формулы (I), где R NCCjHg),, получают амидирова пнем хлорангидрида кислоты (), где К OCjHg, Константы синтезированных соедине ний общей формулы (I) приведенЕл в табл. 1. Биологические испытания синтезированных соединений, проведенные на комарах и на двух видах клопов, показали, что хотя производные этой группы не Превосходят эталон {Смесь- Лоу), они обладают высокой специфичностью действия для кома ров,. Так, наиболее активным среди них являетсясоединение I, где К ОСз Н. Кроме того, соединения форму.пы (I), где R г , и (I), где Н NiCjHsJjf оказывают на личинок кома ров токсическое действие. На клопах Rhodnius proEixus и вредной черепаш ке EXirygaster integriceps эти вещества практически не активны. Результаты биологических испытаний синтезированных соединений приведены в табл. 2. Ниже приводятся примеры получени свойства и методика проведения испы тания на ЮА для полученных.соединений, (пример 1. Смесь 33,0 г эти лйвогоэфира п-ацетил-у-фенилмасля- ной кислоты (II), 46 мл этиленглико ля, 250 МП бензола и 0,2 г п-толуол сульфокислоты нагревают с насадкой Дина-Старка в .течение. 60 час. После этого реакционную массу охлаждают, промывают раствором-соды, водой, су -шат сернокислым натрием. Растворите отгоняют, а остаток фракционируют. Получают 26 г (66%) этиленкеталя эт лового эфира п ацетил- фенилмаслян кислоты (III) с т, кип. 175-178 С/ВИЮ с зтиловым эфиром диметйлфосфонуксус1иэй к1- слоть (реакция Виттига-Хорнера) с последующим выделением целевого продукта (I), где R - в свободном виде или в виде эфиров общей формулы {I), где ОСН(СНз)2, или в виде кислоты, или в виде амида. Схема реакций: DCHjIVi a SlgjOjJ: /2 мм, п|°1, 5058, Тонкослойная хроматография (тех) на пластинках SiEufoE в системе ацетон: гег/тан - 2:5 (Rf 0,54), Время удерживания 2015 (Г/КЗС, прибор Цвет-З; колонка 3 м, циаметр 3 мм, 5% на хроматоне (60-80 меш) . Те 4пература колонки , скорость газа-носителя 80 jvui/MHH; в последующих примерах температура колонки и скорость газаносителя указывааотся в каждом конкретном случае). ИК-спектр (прибор UR-20): 1060, 1610, 1735 см1 Найдено,%: С 68,74; Н 8,05. С 16 22Р4 Вычислено,%: С 69,04; Н 7,96, К реактиву гриньяра, полученному из 7,35 г Мд 18,8 мл йодистого метила в 100 мл сухого эфира, при в течение 30 мин прибавляют раствор 32 г (III) в 40 гп эфира. Перемешивают 1 ч при 20°С и 3 ч при кипении. Экстрагируют эфиром, эфирные экстракты про.1ывают водой, суыат сернокислым натрием, эфир отгоняют. Остаток 30 .г растворяют в 60 мл ацетона, прибавляют 10 MI7 10%-ной НС и перемешивают 4 ч при комнатной температуре.. Ацетон отгоняют, остаток разбавляютвбдой и экстрагируют эфиром. Эфирные экстракты промывают водой, сушат сернокислым натрием, затем эфир отгоняют, остаток 24 г растворяют в 60 мл ксилола, добавляют 0,25 г кристгшлического йода и нагревают в течение 4 ч с насадкой Дина-CfapKa - Охлаждают, промывают раствором оисульфита натрия, водой и сушат сернокисльгм натрием. Растворитель отгоняют, а остаток фракционируют и получают 14,7 г (60%) п - (4-мегилпентен-З-. -ил)-ацетофенона (IV), т. кип. 14815ГС/1 f/iM, п2° 1,5359, R, 0,49 (ТСХSlEufot, условия аналогичны III. Время удерживания 614(условия аиалогачны(111) .ИК-спектр5847,1610,1685 см . Найдено,%: С 82,87; Н 8,93.
Вычислено,%: С 83,12; Н 6,96.
2 , 4-ЛД1НИТрофенилгидразон , т. пл „ 1.50-1С (из спирта).
Найдено,%: 62,96; Н 5,66; 14,93.
C oHjjN.O.
Вычислено,%: С 62,81; Н 5,79; 14,65,
В атмосфере сухого азота к суспензии гидрида натрия в тетрагидрофуране (ТГФ), полученной из 1,07 г 50%ной суспензии гидрида натрия в минеральном масле и 1-0 мл ТГФ, при 5С прибавляют 4,37 г этилового эфира диметилфосфонуксусной кислоты и перемешивают при комнатной температуре 3 ч Затем вновь охлаждают до и прибавляют 4,5 г кетона (IV) в 5 мл ТГФ Перемешивают 1 ч при 5°С, 1ч при , 3 ч при кипении и оставляют на
Н ОЧ Ь а
ТГФ отгоняют, остаток разбавляют водой и экстрагируют эфиром. Эфирные экстракты промывают водой, 21-ной , снова водой и сушат сернокислым натрием. Эфир отгоняют, остаток перегоняют и получают этидовый эфир 3-метил-З-(4-метилпентен 3-ил)- фенилпропен-2-овой кислоты. Время удерживания 10 22 (цис--) , 1325 (транс-), температура колонки 210°С, S2 90 мл/мин.
ИК-спектр: 847, 1610, 1635, 1715 СМ-П р и м е. р 2. К раствору метилата натрия, полученному из 0,1 г натрия и 30 мл метилового спирта, прибавляют 10 г эфира (I) и кипятят 5 ч. Охлаждают, выливают в воду, подкисленную соляной кислотой, экстрагируют эфиром. Эфирные экстракты проNuJBaK)T водой и сушат сернокислым натрием. После отгонки растворителя остаток фракционируют и получают метиловый эфир 3-метил-З-(4-метилпентен 3 ил)-фенилпропен-2-овой кислоты. Условия ГЖХ аналогичны эфиру (II). Время удерживания 1015 (транс-), 8 30 Чцис-).
ИК-спектр: 847, 1610, 1715 см
Соединение (I), где R - ОСН(СНз)2, получают аналогично с использованием изопропилата натрия. Время удерживания 1418 (транс-), 1145(цисУсловия ГЖХ см. эфир (II).
ИК-спектр: 847, 1610., 1635, 1715 CM-J
Пример З.К раствору 2,0 г эфира (I) в 30 мл CjHsOH и 8 мл %О прибавляют 3 мл 50%-ной NaOH и оставляют на 20 ч при комнатной температуре. Спирт отгоняют в вакууме, остаток разбавляют водой и экстрагируют эфиром. Водный слой при 0°С подкисляют 10% НрЗО, экстрагируют эфиром, зфирные экстракты промывают водой и суша.7 сернокислым натрием. Эфир отгоняют, остаток перекристаллизовывают из гексана и получают 3-метил-З-(4-метилпентен-3-ил)-фенилпропен-2 -овую кислоту.
ИК-спектрг 847, 1610, 1635, 1690, 2800-3300 см/
Пример 4. К раствору 1,0 г кислоты примера 3 в 20 мл сухого хлороформа прибавляют О,7 мл триэтиламина, охлаждают до 0°С и прибавляпот 0,5 мл хлоругольного эфира в 2 мл хлороформа. Перемешивают при 30 мин, затем при 20С 2 ч. Охлажда0 ют, прибавляют 0,6 мл диэтиламина в 2 мл хлороформа, перемешивают при 0°С 30 мин и 3 ч при . Реакционную массу промывают водой,разбавленной серной кислотой, снова водой,
5 хлороформ отгоняют, остаток раэбавляют эфиром, прогнивают раствором соды, водой, сушат сернокислым натрием, эфир отгоняют, остаток (1,0 г) чистят с помощью препаративной ТСХ и получают N-диэтиламид-З-мётил-З-(4-метилпентен-3 -ил)-фенилпропен-2-овой кислоты.
ИК-спектр: 847, 1610, 1630, 1650 см-. .
Время удерживания 2350 (темпе ратура колонки 220С, N2 100 мл/мин) .
Соединение (I), где R - , получают аналогично с.использованием этиламина.
ИК-спектр: 847, 1230, 1550, 1610,
0 1630, 1655, 3300
Время удерживания 2045 (температура колонки , N2 100 мл/мин) . Пример 5. При испытании на комарах Aedes aegypti личинки четвертой стадии за 1-2 дня до окукливания помещают на 24 ч в растворы различных концентраций. Вещества добавляют в воду в 0,1 мл ацетона, для каждой концентрации используют не менее 100 личинок (по 25 в одной повторности). При испытании на личинках третьей стадии экспозиция была продолжительной (с момента обработки до окукливания). Эффект определяют по числу погибших насекомых, а СК-50 по линиям регрессии на пробитлографической бумаге.
При испытании на клопах Rhodnius Q proEixus соединения наносились топикально в 1 мкл ацетона на тергиты . брюшка нимф через сутки после .кормления кровью, после имагинальной линьки по 19тбалльной шкале оценивалась степень остаточности у.имаго личиночных черт, а затем графически уста-навливалась доза, вызывающая средний эффект (т. е. 10 баллов).
При испытании на вредной черепашке Eurygaster integriceps растворы 0 веществ наносились на личинки пятой стадии. Степень ювенилизирующего эффекта оценивалась после линьки по 5балльной шкале. В качестве эталона применялась смесь Лоу.
го v
Г
оо
Х





лз
«
X
X
1Г1 го
со
%
г
л} R
t
I
К А
§.
И О
с Формула изобретения Эфиры или амиды 3-метил-3-(4 тилпентен-3-ил)-фенилпропен-2кислоты обцей формулы где R - OR, -NHR, -NR2, СНа, СдНз, СН(СН5)2 J как инсектициды с ювенильной акт ностью. Источники информации, приняты внимание при экспертизе 1.Кример М, 3., Шамшурин А. А. Химия ювенильиого гормона и его аналогов , Кишинев, 1972 ,с. .; 2.Патент Франции № 2121260, кл, С 07 С 121/00,опуезлик. 1972. 3.Авторское свидетельство СССР 282811, кл. А 01 N 119/30,оЪублик. 4.А. Franke und an. Synthetische. TuveniEhormone III, p-Substituirte 4 phenyEbuten-l-carbonsaure derivative, und IV, p-Substituirte 5-pheny penten-l-carbonsanre derivative, HeEv. chim, acta, 1975, 58. 1, c. 283, 293.
Авторы
Даты
1979-08-25—Публикация
1975-09-04—Подача