Ё

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения ацилированных дикетоновых соединений | 1985 |
|
SU1697591A3 |
| Способ получения цис- и транс-изомеров замещенных дигалоидвинилциклопропанкарбоновых кислот или их эфиров | 1976 |
|
SU940644A3 |
| Способ получения простых гликолевых эфиров | 1973 |
|
SU541428A3 |
| Способ получения 5-бромвалериановой кислоты | 1985 |
|
SU1268565A1 |
| Способ получения производных @ -дигалоидвинилциклопропана | 1978 |
|
SU1075972A3 |
| Способ получения производных 3-(бензотиазол-2-илалкил)-4-оксо-3Н-фталазин-1-илуксусных кислот или их сложных алкиловых эфиров | 1988 |
|
SU1678208A3 |
| Способ получения 5-бромпентановой кислоты | 1988 |
|
SU1594169A1 |
| Способ получения сложных эфиров этиленгликоля | 1969 |
|
SU441702A1 |
| СПОСОБ ПОЛУЧЕНИЯ СПИРОБЕНЗОЦИКЛАНУКСУСНЫХ | 1973 |
|
SU379082A1 |
| Способ получения 2-арилпропионовой кислоты | 1978 |
|
SU963462A3 |
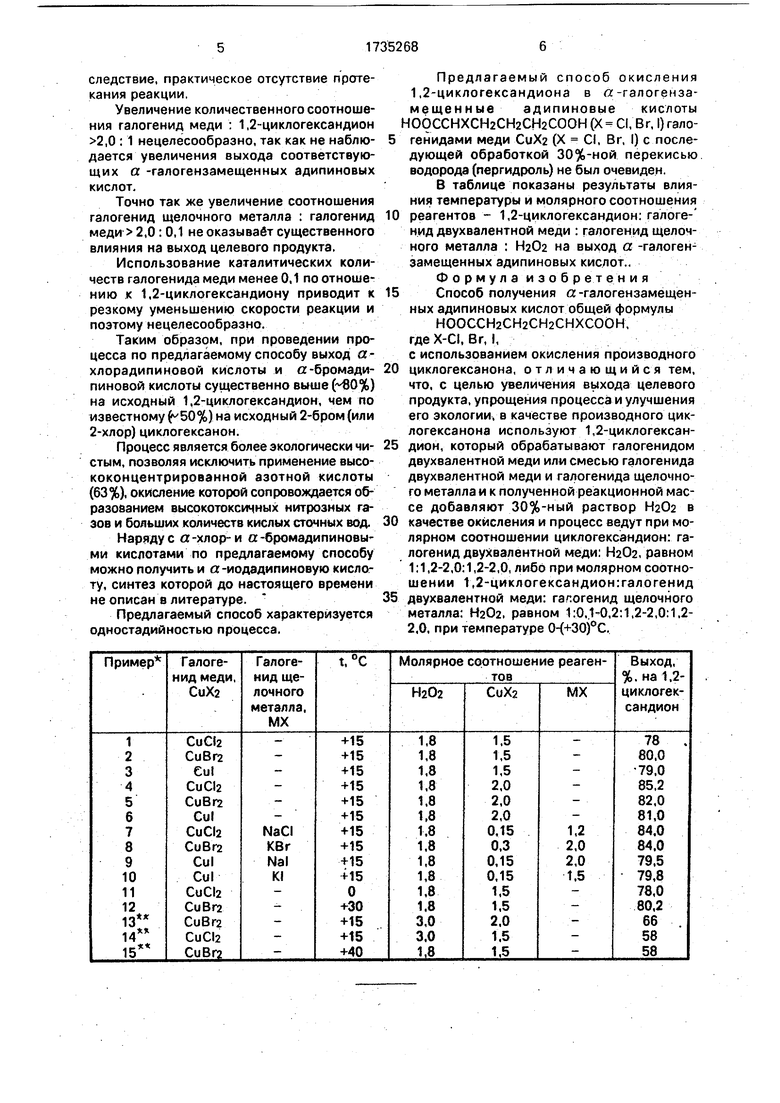
Сущность изобретения: Продукт - а- хлорзамещенная адипиновая кислота, БФ СеНдОдС ; т. пл. 93°С пр. Продукт - а -бром- замещенная адипиновая кислота БФ СбНэ04Вг;т.пл. 122-123°С. Продукт -а-иод- замещенная адипиновая кислота БФ СбН9041.т. пл. 129-130°С, пр. Реагент 1:1,2- циклогександион. Реагент 2: галогенид двухвалентной меди. Реагент 3: смесь гало- генида двухвалентной меди и галогенида щелочного металла. Реагент 4: 30%-ный Н202. Условия реакции: при 0 - 30°С молярное соотношение циклогександион : галогенид двухвалентной меди: Н202 1 : 1.2-2,0 : :1,2-2,0 или молярное соотношение 1,2- циклогександион : галогенид двухвалентной меди : галогенид щелочного металла : Н202 - 1 : 0.1-0,2 : 1.2-2.0 : 1,2-2,0. 1 табл.
Изобретение относится к органической химии, и касается, в частности, способа получения а-хлор,- а-бром-и а -иодздипино- вых кислот. Эти кислоты находят применение в тонком органическом синтезе, в производстве гербицидов, в синтезе ft -оксикислот по реакции Реформатского.
Известен способ получения сг-брома- дипиновой кислоты прямым бромировани- ем адипиновой кислоты при +160°С. Выход а -бромадипиновой кислоты составляет 5%. Наряду с ct-бромзамещенной адипиновой кислотой образуются также и/ -бром- замещенные продукты, ч го в значительной степени затрудняет выделение целевого продукта.
Наиболее близким по технической сущности и достигаемому результату является
способ получения а -бром или «-хлоради- пиновых кислот путем окисления 2-бром- или 2-хлорциклогексанона азотной кислотой в присутствии МЩУОз и NaN02 при +38°С при перемешивании в течение 15 ч. Получают а -бромадипиновую кислоту с выходом- 50%.
сс-Иодциклогексанон при прямом иодировании ввиду большой неустойчивости выделен не был и в связи с этим а-иодади- пиноновая кислота не получена.
Недостатками данного способа являются относительно невысокий выход целевого продукта, а также образование больших количеств сточных вод кислого характера и выброс в атмосферу вредных нитрозных газов, двухстадийкость процесса.
Цель изобретения - повышение выхода целевого продукта и экологической безМ
OJ
ел
NJ О 00
опасности окружающей среды, а также упрощение процесса.
Поставленная цель достигается способом получения а -галогензамещенных адипи- новых кислот НООССНХСН2СН2СН2СООН (X CI, Вг, I) путем обработки 1,2-циклогек- сандиона галогенидом двухвалентной меди или смесью галогенида двухвалентной меди с галогенидом щелочного металла и 30%- ным раствором перекиси водорода при молярном соотношении 1,2-циклогександион: галогенид двухвалентной меди : НгОа, равном 1 : 1,2-2,0 : 1,2-2,0, либо при молярном соотношении 1,2-циклогександион : галогенид двухвалентной меди : галогенид щелочного металла : НаОа, равном 1 : 0,1-0,2 : .-1,2-2,0 : 1,2-2,0, при температуре 0 - +30°С. Выход целевого продукта 78-85%.
Отличительными признаками процесса являются : использование в качестве исходного 1,2-циклогександиона и обработка его галогенидом двухвалентной меди и галогенидом щелочного металла с добавлением к реакционной массе 30%-ного раствора На02 в качестве окислителя и проведение процесса при молярном соотношении 1,2- циклогександион : галогенид двухвалентной меди : Н202, равном 1 : 1,2-2,0 : 1,2-2,0, либо при молярном соотношении 1,2-циклогександион : галогенид двухвалентной меди: : галогенид щелочного металла : HaOz. равном 1 : 0,1-0,2 : 1,2-2,0 : 1,2-2,0, при температуре 0 - +30°С, что позволяет упростить процесс, улучшить экологию и повысить выход целевого продукта.
Пример 1. К 11,2 г (0,1 моль) 1,2-циклогександиона, растворенных в 150 мл воды, добавляют 25,5 г CuCh x 2 Н20 и к этому раствору при перемешивании добавляют в течение 45 мин 18,0 мл. 30%-ното раствора Н202, поддерживая температуру +15°С охлаждением водяной баней. После этого раствор подкисляют 2NH2S04 до рН 2 и перемешивают еще 30 мин, затем экстрагируют эфиром 3 х 100 мл и эфирный экстракт обрабатывают насыщенным раствором Na2COa. Водный слой отделяют, подкисляют 2N H2S04 до рН 2 и экстрагируют эфиром 3 х 100 мл.
После удаления эфира выделяют 14,05 г а -хлорадипиновой кислоты (78%). После перекристаллизации из воды т. пл. +93°С. Найдено,%: С 40,22; Н 5,02; CI - 19,62 Вычислено,%: С 39,91; Н 5,02; C119,63 По данным ГЖХ чистота продукта 8%. Пример 2. К 11,2 г (0,1 моль) 1,2-циклогександиона, растворенных в 150 мл воды, добавляют 36,0 г СиВгг х НаО и к этому раствору при перемешивании в течение
45 мин добавляют 18,0 мл 30%-ного раствора Н202, поддерживая температуру +15°С охлаждением водяной баней. После этого раствор подкисляют 2N H2S04 до рН 2 и перемешивают еще 30 мин, затем экстрагируют эфиром 3 х 100 мл и эфирный экстракт обрабатывают насыщенным раствором Ма2СОз. Водный слой отделяют подкисляют 2N H2S04 до рН 2 и экстрагируют эфи- ром 3x100 мл.
После удаления эфира выделяют 17,85 г а -бромадипиновой кислоты (80%). После перекристаллизации из воды т. пл. +122- 123°С. Найдено,%: С 32,03; Н 4,02; Вг 35,71
Вычислено,%: С 31,95; Н 3,96; Вг 35,93. По данным ГЖХ чистота продукта - 97,9%.
Пример 3. К 11,2 г (0,1 моль) 1,2-цик- логександиона, растворенных в 150 мл воды, добавляют 47,8 г Cul и к этому раствору при перемешивании в течение 45 мин добавляют 18,0 мл 30%-ного раствора N262. поддерживая температуру -4-15°С охлажде- нием водяной баней. После этого раствор подкисляют 2N H2S04 до рН 2 и перемешивают еще 30 мин, затем экстрагируют эфиром 3 х 100 мл и эфирный экстракт обрабатывают насыщенным раствором Ма2СОз. Водный слой отделяют, подкисляют 2N H2S04 до рН 2 и экстрагируют эфиром 3 х 100 мл.
После удаления эфира выделяют 2t,4 г а -иодадипиновой кислоты (79%). После перекристаллизации из воды т. пл. +129- 130°С.
Найдено,%: С 26,32; Н 3,41; J 47.11 Вычислено,%: С 26,46; Н 3,32; J 46,70 По данным ГЖХ чистота продукта 97,4%.
Примеры 4-23 проводят по методике примеров 1-3.
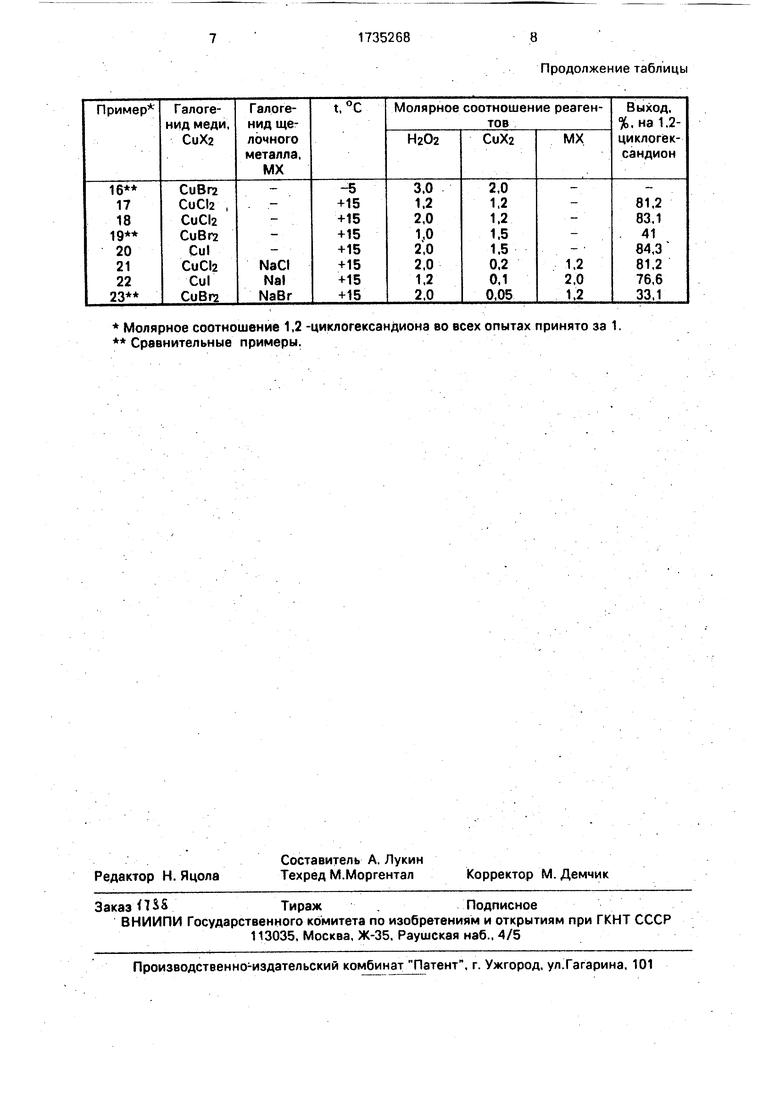
Сравнительные примеры 13-16, 19 и 23 свидетельствуют о том, что примеры 1-12, 17, 18 и 20-22 являются оптимальными условиями синтеза а-галогензамещенных адипиновых кислот.
Увеличение избытка Н202 более двукратного является нецелесообразным, по- скольку приводит к уменьшению выхода целевых продуктов (примеры 13 и 14).
При этом повышение температуры свыше +30°С также нецелесообразно (пример 15), так как приводит к уменьшению выхода целевого продукта.
Нецелесообразно проведение реакции и при температурах ниже 0°С (пример 16), так как наблюдается уменьшение растворимости веществ, выпадение их в осадок и, как
следствие, практическое отсутствие протекания реакции,
Увеличение количественного соотношения галогенид меди : 1,2-циклогександион 2,0 : 1 нецелесообразно, так как не наблюдается увеличения выхода соответствующих а -галогензамещенных адипиновых кислот.
Точно так же увеличение соотношения галогенид щелочного металла : гаяогенид меди 2,0 : 0,1 не оказывает существенного влияния на выход целевого продукта.
Использование каталитических количеств галогенида меди менее 0,1 по отношению к 1,2-циклогександиону приводит к резкому уменьшению скорости реакции и поэтому нецелесообразно.
Таким образом, при проведении процесса по предлагаемому способу выход о,- хлорадипиновой кислоты и а-бромади- пиновой кислоты существенно выше|ЧЮ%) на исходный 1,2-циклогександион, чем по известному 50%) на исходный 2-бром (или 2-хлор) циклогексанон.
Процесс является более экологически чистым, позволяя исключить применение высококонцентрированной азотной кислоты (63%), окисление которой сопровождается образованием высокотоксичных нитрозных газов и больших количеств кислых сточных вод.
Наряду с а-хлор-и а-бромадипиновы- ми кислотами по предлагаемому способу можно получить и а-иодадипиновую кислоту, синтез которой до настоящего времени не описан в литературе.
Предлагаемый способ характеризуется одностадийностью процесса.
Предлагаемый способ окисления 1,2-циклогександиона в «-галогенза- мещенные адипиновые кислоты HOOCCHXCH2CH2CH2COOH(, Вг, )гало- 5 ген идами меди СиХ2 (X CI, В г, I) с последующей обработкой 30%-ной перекисью водорода (пергидроль) не был очевиден.
В таблице показаны результаты влияния температуры и молярного соотношения
0 реагентов - 1,2-циклогександион: галоге- нид двухвалентной меди : галогенид щелочного металла : НаОа на выход а -галогензамещенных адипиновых кислот.. Формула изобретения
5 Способ получения а-галогензамещенных адипиновых кислот общей формулы
НООССН2СН2СН2СНХСООН, где X-CI, Вг, I, с использованием окисления производного
0 циклогексанона, отличающийся тем, что, с целью увеличения выхода целевого продукта, упрощения процесса и улучшения его экологии, в качестве производного циклогексанона используют 1,2-циклогексан5 дион, который обрабатывают галогенидом двухвалентной меди или смесью галогенида двухвалентной меди и галогенида щелочного металла и к полученной реакционной массе добавляют 30%-ный раствор НаОз в
0 качестве окисления и процесс ведут при молярном соотношении циклогександион: галогенид двухвалентной меди: НаОз, равном 1:1,2-2,0:1,2-2,0, либо при молярном соотношении 1,2-циклогександион: га л о ген ид
5 двухвалентной меди: галогенид щелочного металла: Н202, равном 1:0,1-0,2:1,2-2,0:1,2- 2,0. при температуре 0-(+30)°С.
Молярное соотношение 1,2 -циклогександиона во всех опытах принято за 1. Сравнительные примеры.
Продолжение таблицы
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Органическая химия | |||
| - Изд-во | |||
| Химия, М., 1979, с | |||
| Способ приготовления пластического взрывчатого состава | 1913 |
|
SU439A1 |
| Gal W., Gay-Lussac С | |||
| Канатное устройство для подъема и перемещения сыпучих и раздробленных тел | 1923 |
|
SU155A1 |
| Катодное реле | 1921 |
|
SU250A1 |
| Nasaki N. | |||
| Terno L., Masajasu Sh., Hlro- shl G., Janan Kokal | |||
| 7399115, кл | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| Приспособление для склейки фанер в стыках | 1924 |
|
SU1973A1 |
| Капельная масленка с постоянным уровнем масла | 0 |
|
SU80A1 |
| Устройство для дистанционного измерения высоты, периода и скорости распространения волн в прибрежных мелководных пунктах водоема | 1951 |
|
SU95273A1 |
Авторы
Даты
1992-05-23—Публикация
1990-06-22—Подача