Изобретение относится к производным сульфаминовой кислоты, а именно к N,N-бис-(полифторалкил)амидосульфофторидам общей формулы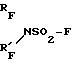
 где RF - CF3, CHF2, R
где RF - CF3, CHF2, R - CF3, CHF2, проявляющим инсектицидную активность фумигационного действия, которые могут найти применение в сельском хозяйстве.
- CF3, CHF2, проявляющим инсектицидную активность фумигационного действия, которые могут найти применение в сельском хозяйстве.
Известно применение в качестве фумигантов различных хлорсодержащих органических соединений, например, гексахлорбутадиена, который используется для фумигации почвы виноградников против филлоксеры. Гексахлорбутадиен имеет высокую температуру кипения (215оС) и выпускается в жидком или гранулированном виде.
В настоящее время разработана специальная система внесения гексахлорбутадиена, обеспечивающая внесение препарата в количестве до 200 кг/га на глубину до 50 см. Гексахлорбутадиен при фумигации почвы виноградников не полностью освобождает их от филлоксеры, причем на богатых гумусом черноземах норму расхода препарата необходимо увеличить в 3-4 раза.
Недостатки гексахлорбутадиена как фумиганта - невысокая эффективность действия при значительных удельных нормах расхода, необходимость использования специальной системы для внесения препарата в почву, а также высокая токсичность для теплокровных: ЛД50 для крыс при оральном воздействии составляет 165±2,3 мг/кг.
Для обработки зерна с целью освобождения от вредителей используют металлилхлорид (3-хлор-2-метилпропен-1). Нормы расхода препарата составляют до 100 г/м3. Металлилхлорид представляет собой бесцветную жидкость с характерным запахом, т.кип. 72оС, препарат обладает слезоточивым действием. Среднетоксичен для теплокровных: ЛД50 для лабораторных животных при оральном воздействии составляет 580-1350 мг/кг. Работу с металлилхлоридом проводят в противогазах марки "А".
Недостатки препарата - сравнительно невысокая эффективность, наличие специфического запаха и необходимость использования индивидуальных средств защиты (противогаза) при работе с ним.
Для фумигации семян, зерна, сеянцев, сушеных овощей и фруктов, сушеных рыбы и мяса, пушнины, а также для дезинсекции складов, холодильников, элеваторов, мельниц и жилищ применяется бромистый метил. Препарат выпускается в форме сжиженного газа (т.кип.4оС), упакованного в стальные баллоны. Бромистый метил образует с воздухом взрывоопасные смеси при концентрации препарата в воздухе 13,5-14,5 об.%. Высокотоксичен для теплокровных, действует на нервную систему, почки и легкие: ЛД50 для крыс при 30-минутной экспозиции 11 г/м3, для мышей - 6,6 г/м3. Нормы расхода составляют 40-60 г/м3. Предельно допустимая концентрация бромметила в воздухе рабочей зоны составляет 1 мг/м3, поэтому при работе с ним пользуются фильтрующим промышленным противогазом марки "А", а при высоких концентрациях - изолирующими шланговыми противогазами ПШ-1, ПШ-2, ДПА-4 и другими.
Для газации пустых складских помещений используется дихлорэтан. Норма расхода составляет 300 г на 1 м3. При обработке зерна расходуют 300-450 г дихлорэтана на 1 м3 в зависимости от толщины слоя, продолжительность - до 8 сут. Дихлорэтан кипит при 84оС, горюч: температура вспышки 9оС. Дихлорэтан относится к высокотоксичным веществам, смертельные концентрации для лабораторных животных составляют 8-35 г/м3. Предельно допустимая концентрация в воздухе рабочей зоны 10 мг/м3. Работу с дихлорэтаном для газации зернохранилищ проводят в противогазах.
Имеются сведения о возможности использования фторсодержащих винилсульфофторидов общей формулы RCF=CHSO2F в качестве инсектицидов. Однако данные об их испытаниях в качестве фумигантов отсутствуют. Синтез этих соединений отличается сложностью аппаратурного оформления процесса и необходимостью выделения целевых продуктов из реакционной смеси с использованием хроматографического оборудования.
Наиболее близким к предлагаемым соединениям является препарат фуммет (метансульфофторид), выбранный в качестве аналога по структуре и действию.
Недостатки фуммета - высокая токсичность (ЛД50 = 3,5 мг/кг) и низкая летучесть (т.кип. 121-123оС).
Общим предлагаемых соединений и прототипа является то, что эти вещества относятся к классу сульфофторидов, проявляющих инсектицидную активность против различных насекомых. Структурные отличия заключаются в замене алкильного радикала у атома серы фторированной диалкиламиногруппой, что создает положительный эффект, заключающийся в значительном снижении токсичности по отношению к теплокровным и повышении летучести при сохранении достаточно высокой активности.
В качестве базовых объектов сравнения используют применяемый в отечественной практике дихлорэтан ClCH2CH2Cl и специально синтезированный метансульфофторид.
Цель изобретения - изыскание в ряду сульфофторидов новых соединений, проявляющих высокую инсектицидную активность фумигационного действия и обладающих низкой токсичностью.
Предлагаемые соединения общей формулы получают путем фторирования исходных диалкиламидосульфофторидов или сульфохлоридов, например диметиламидосульфофторида и диметиламидосульфохлорида. Для фторирования могут быть использованы два метода: электрохимическое фторирование в растворе жидкого безводного фтористого водорода и фторирование с помощью CuF3. При электрохимическом фторировании получают преимущественно перфторированные соединения.
В случае использования в качестве фторирующегоо агента CuF3образуются преимущественно частично фторированные соединения, например N,N-бис-(дифторметил)амидосульфофторид.
Изобретение иллюстрируется следующими примерами.
П р и м е р 1. N,N-Бис-(трифторметил)амидосульфофторид (1) и N-дифторметил-N-трифторметиламидосульфофторид (2).
104 г (0,82 моль) N-диметиламидосульфофторида (А) добавляют порциями в электрохимическую ячейку, содержащую 400 мл жидкого безводного фтористого водорода. Полученный раствор подвергают электролизу при напряжении на электродах 5-5,5 В и силе тока 3-9 А (плотность тока составляет при этом 1-3 А/дм2). В течение электролиза пропускают 250 А ч электричества. Первую порцию исходного вещества (А) в количестве 39,2 г добавляют в ячейку до начала электролиза, вторую порцию вещества (А) в количестве 20,4 г вводят в ячейку после прохождения 107,5 А ч. После пропускания 157 А ч электричества в ячейку добавляют еще 27,6 г исходного вещества. Последнюю порцию вещества (А) вводят в ячейку после прохождения 218,4 А ч. Электролиз ведется с использованием электродного пакета, состоящего из четырех никелевых анодов и пяти никелевых катодов. Расстояние между анодом и катодом составляет 4,5 мм, а эффективная площадь анода - 3 дм2. Расход фтористого водорода в процессе электрохимического фторирования контролируются визуально и по мере необходимости восполняют добавлением свежего фтористого водорода таким образом, чтобы общий объем электролита в ячейке составлял 400-500 мл. Температуру электролита поддерживают в интервале 10-20оС, а температуру обратного холодильника -20оС. Продукты фторирования конденсируют в трех последовательных медных ловушках, охлаждаемых до -20оС, -50оС и -78оС соответственно. После окончания электролиза содержимое ловушек доводят до температуры 0оС, объединяют и получают 85 г двухфазной смеси, состоящей из фторированных продуктов и фтористого водорода. После отделения фтористого водорода остается 48 г сырого продукта, который подвергают фракционной перегонке. Получают 33,6 г (70%) фракции, кипящей при 29-35оС (I фракция), 2,4 г (9%) фракции, кипящей при 35-50оС. (II фракции), 7,2г (15%) фракции, кипящей при 50-55оС (III фракция), 1,9 г (4%) фракции, кипящей при 55-57оС (IV фракция), 2,4 г (5%), фракции, кипящей при 75-100оС (V фракция). По данным спектра ЯМР19F и газовой хроматографии (I фракция) представляет собой преимущественно N, N-бис-(трифторметил)амидосульфофторид (85-90% частоты), а третья фракция - преимущественно N-дифторметил-N-трифторметиламидосуль-фофторид (85% -ной чистоты). После дополнительной перегонки указанные соединения получают в индивидуальном состоянии.
N, N-Бис-(трифторметил)амидосульфо-фторид (1), т.кип. 32-33оС. Строение целевого продукта доказано соответствием определенных экспериментально результатов элементного анализа рассчитанным величинам, а также с помощью спектра ЯМР19F, записанного на приборе "Bruker WP-200" в растворе дейтероацетона относительно трихлорфторметана. Спектр ЯМР19F, δ, м.д.: -53,23 д (6F, CF3), 62,06 м (1F, SO2F) J = 5,9 Гц.
= 5,9 Гц.
Найдено, % : С 10,29, 10,19, F 56,33, 56,45, N 5,28, 5,49, O 14,41, 14,27, S 13,69, 13,61.
C2F7NO2S.
Вычислено, %: С 10,22, F 56,57, N 5,96, О 13,61, S 13,64.
N-Дифторметил-N-трифторметиламидосульфофторид (2), т. кип. 52-53оС. Строение целевого продукта доказано с помощью спектроскопии ЯМР19 F и ПМР. Спектры ЯМР19F и ПМР записаны на приборе "Bruker WP-200" в растворе дейтероацетона относительно трихлорфторметана и гексаметилдисилоксана соответственно. Спектр ЯМР19F, δ, м.д.: 61,62 м (1F, SO2F), - 53,50 м (3F, CF3), -97,10 дм (2F, СНF2) J = 6,0 Гц J
= 6,0 Гц J = 54,5 Гц.
= 54,5 Гц.
С2НF6HSO2. ПМР-спектр, δ, м.д.: 7,69 тк (1Н,СНF2), JHF=54,5 Гц, J = 1,4 Гц.
= 1,4 Гц.
Найдено, %: С 11,11, 11,03, Н 0,44, 0,47; F 52,28, 52,37; N 6,04, 6,17; O 15,43, 15,14; S 14,70, 14,82.
C2HF6NO2S
Вычислено,%: С 11,06, Н 0,46, F 52,51, N 6,45, O 14,74, S 14,77.
П р и м е р 2. N,N-Бис-(дифторметил)амидосульфофторид (3).
90 г (0,7 моль) N,N-диметиламидосульфофторида в течение 3 ч прикапывают в испаритель, нагретый до 200оС, совмещенный с реактором, содержащим 3 мк CuF3. Пары исходного вещества пропускают через реактор с CuF3 при 200-250оС. В качестве газа-носителя используют азот (20 л/ч). После прохождения всего количества исходного вещества через реактор продувка газообразным азотом продолжается еще 30 мин. Продукты фторирования конденсируют в трех ловушках из меди, охлаждаемых до 50оС (-20оС) и (-78оС) соответственно. Содержимое всех ловушек объединяют, отделяют от фтористого водорода, получают 102 г сырого продукта, который перегоняют, разделяя на три основные фракции: смесь N,N-бис-(трифторметил)амидосульфофторида и N-дифторметил-N-трифторметиламидосульфофторида 20г (19,6%) (I фракция, т.кип. 30-65оС), N, N-бис-(дифторметил)амидосульфофторид 54,5 г (53,4%) (II фракция, т.кип. 80-90оС), N-дифторметил-N-фторметиламидосульфофторид 17,3 г (17,0%) (III фракция, 90-105оС).
Для выделения индивидуального целевого продукта N,N-бис-(дифторметил)амидосульфофторида (3) вторую фракцию дополнительно перегоняют, выделяя продукт с т.кип. 86-88оС. Строение целевого продукта доказано соответствием определенных экспериментально результатов элементного анализа рассчитанным величинам, а также с помощью спектроскопии ЯМР 19F и ПМР. Спектры ЯМР 19F и ПМР записаны на приборе "Bruker WP-200" в растворе дейтероацетона относительно трихлорфторметана и гексаметилдисилоксана соответственно. Спектр ЯМР 19F, δ, м.д.: 61,05 м (1F, SO2F), (-97,04 дд) (4F, CHF2) J = 56,7 Гц, J
= 56,7 Гц, J = 6,6 Гц, J
= 6,6 Гц, J = 56,7 Гц, J
= 56,7 Гц, J = 6,6 Гц.
= 6,6 Гц.
Найдено, % : С 12,01, 12,03; Н 0,97, 1,03; F 47,13, N 6,99, 7,04, О 16,73, 16,55, S 16,03, 16,12.
С2Н2F5NO2S.
Вычислено,%: С 12,07, Н 1,01, F 47,71, N 7,04, O 16,70, S 16,10.
П р и м е р 3. N,N-бис-(дифторметил)амидосульфофторид (3).
53 г (0,37 моль) N,N-бис-(диметил)-амидосульфофторида прикапывают в течение 1,6 ч в испаритель, нагретый до 220оС и совмещенный с реактором, содержащим 3 кг CuF3. Фторирование исходного вещества проводят при температуре реактора 220-250оС, используя в качестве газа-носителя азот.
Фторированные соединения конденсируются в ловушке, как описано в примере 2. Получают 65 т сырого продукта, который по данным газовой хроматографии содержит 54% N,N-бис-(дифторметил)амидосульфофторида и другие фторированные соединения, как описано в примере 2. Целевой продукт выделяют из смеси фракционной перегонкой. Идентичность полученного продукта с образцом, синтезированным, как описано в примере 2, подтверждают данными газо-жидкостной хроматографии и спектрами ЯМР 19F и ПМР.
Инсектицидная активность N,N-бис-(полифторалкил)амидосульфофторидов в качестве фумигантов.
Испытания соединений 1-3 на инсектицидную активность фумигационного действия проводят статическим способом путем дозирования веществ в определенный замкнутый объем без учета фактического постепенного изменения изначальной концентрации в опытной среде. Биологическими тест-объектами служат различные насекомые-вредители: злаковая тля, паутинный клещ, рисовый долгоносик, комнатные мухи.
Активность соединений 1-3 оценивают по гибели насекомых после трехчасовой экспозиции их в парах веществ в стеклянном эксикаторе. Температуру на протяжении всего опыта поддерживают постоянной (22оС) с помощью термостата.
В эксикаторы объемом 1500 см3 помещают насекомых в чашках Петри, закрытых марлевыми салфетками. Количество особей в каждой чашке в зависимости от вида составляет 20-30 единиц. Края эксикаторов в целях герметизации смазывают вазелиновым маслом.
В предварительных опытах вещества испытывают в трех произвольно выбранных дозах 150, 100, 50, 10 мкл.
После установления границ активности осуществляют дозировку вещества в более узком интервале 150, 100, 80, 60, 40, 25 мкл на объем 1500 см3.
Техника нанесения испытуемого соединения (фумиганта) заключается в следующем: микропипеткой отбирают соответствующую дозу соединения по объему и наносят на кружочки обеззоленной фильтровальной бумаги, помещенной в эк-сикатор. Эксикатор закрывают крышкой.
Спустя 3 ч после внесения фумиганта проводят учет выживших и погибших насекомых и рассчитывают процент погибших насекомых в сравнении с контрольным опытом.
В качестве эталонного препарата в опытах используют дихлорэтан. Сравнение проводят с препаратом фуммет.
Математическую обработку результатов опытов проводят с учетом удельной массы испытываемых соединений.
Результаты испытаний представлены в табл.1.
Токсичность N,N-бис-(полифторалкил)амидосульфофторидов (1-3) для теплокровных животных.
Острую токсичность определяют на белых беспородных мышах (самцах и самках) массой 18-21 г при внутримышечном введении соединений в чистом виде в различных дозах. Учет гибели животных проводят через 24 ч после аппликации препарата. Токсичность препаратов выражают величинами ЛД50(среднесмертельные дозы) по методу М.Л.Беленького.
Результаты опытов представлены в табл.1.
Инсектицидную активность N, N-бис-(дифторметил)амидосульфофторида в качестве фумиганта для борьбы с вредителями хлебных злаков определяют по следующей методике.
Жуков рисового и амбарного долгоносиков, зернового точильщика, булавоусого хрущака и суринамского мукоеда в количестве по 33 экземпляра в каждой из трех повторностей помещают в стеклянные посуды емкостью 0,5 л с небольшим количеством (около 0,5 г) раздробленного зерна пшеницы. На дно сосуда помещают кусочек фильтровальной бумаги 1х1 см.
С помощью микрошприца на фильтровальную бумагу наносят фумигант в дозе 1,3,5,6,7,10,15,17,20,25,40 г/м3. Сосуды герметизируют и оставляют на 24 ч при 20оС, периодически переворачивая несколько раз, чтобы мешать газ внутри сосуда.
Через 24 ч сосуды открывают и проветривают.
Насекомых переносят в пробирки и через 48 ч проводят подсчет количества погибших жуков. Полученные данные обрабатывают методом пробит и вычисляют СК-50.
Результаты приведены в табл. 2.
Таким образом, предлагаемые соединения формулы обладают низкой токсичностью 500-1000 мг/кг против 3,5 мг/кг для известного и проявляют высокую инсектицидную активность. (56) Шамшурин А.А. и др. Справочник "Физико-химические свойства пестицидов".М.: Химия, 1976, с 35, 118.
Патент США N 3492348, кл. 260-543, 1971.
Мельников Н. Н. Синтетические регуляторы роста растений и гербициды. Успехи химии, т. 45, вып. 8, 1976.
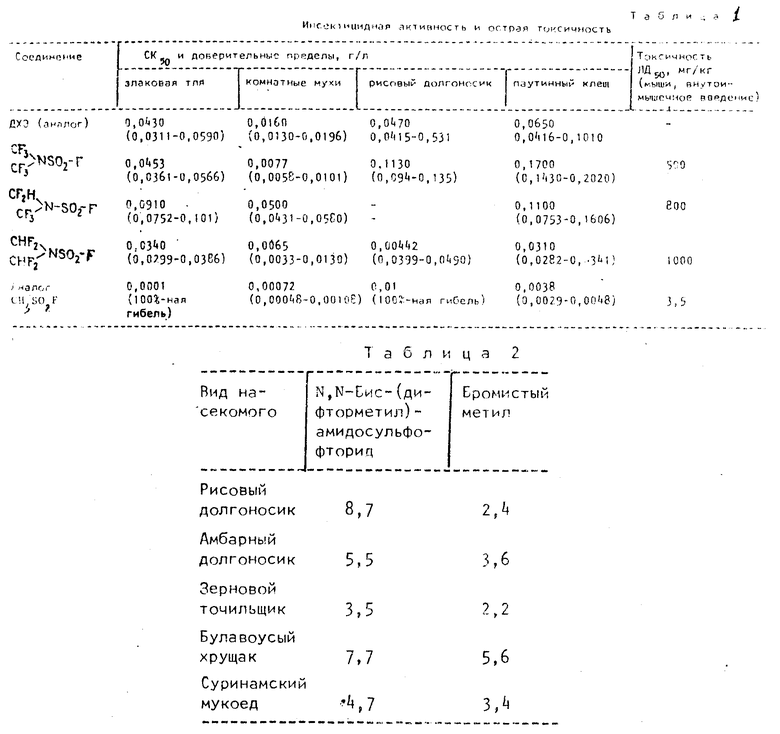
Изобретение касается производных сульфаминовой кислоты, в частности, N, N-бис-(трифторметил)амидосульфофторида или N-дифторметил-N-трифторметиламидосульфофторида, проявляющих инсектицидную фумигантную активность. Цель - создание новых соединений с лучшей инсектицидной активностью и низкой токсичностью. Синтез ведут фторированием соответствующего диалкиламидосульфофторида электрохимически или в растворе жидкого безводного фтористого водорода. Соединения имеют низкую токсичность (500 - 1000 мг/кг против 3,5 мг/кг для известного) и проявляет высокую инсектицидную активность. 2 табл.
N,N-Бис-(полифторалкил)амидосульфофториды общей формулы
где RF-CF3, CHF2, R -CF3, CHF2 ,
-CF3, CHF2 ,
проявляющие инсектицидную активность фумигационного действия.
Авторы
Даты
1994-06-15—Публикация
1989-12-28—Подача