Изобретение относится к усовершенствованному способу получения 3,3,5,5 -тет- ратретбутил-4,4 -дифенохинона (ТТБДФХ), который может быть использован для синтеза 4,4 -бис(2,6-дитретбутилфенола) (Агидола-5) - эффективного стабилизатора полимерных материалов.
Известен способ получения ТТБДФХ окислением 2,6-дитретбутилфенола двуокисью свинца или марганца. Процесс проводят в среде органического полярного растворителя (например, метанола) при 25- 70°С.
Существенным недостатком этого способа является использование дорогостоящих и малодоступных окисляющих агентов: двуокиси свинца и двуокиси марганца, а также большой расход окислителей (на 1 моль 2,6-дитретбутияфенола берут 2-3 моль указанных окислителей) и относительно малый выход целевого продукта (85-90%).
Известен также способ получения ТТБДФХ окислением 2,6-дитретбутилфенола перекисью водорода в молярном соотношении в присутствии катализатора трехокиси вольфрама или молибдена, или ванадиевого ангидрида, или молибденовой кислоты, или вольфрамовой кислоты, взятых в количестве 1,5-6% от массы 2,6- дитретбутилфенола, в среде полярного органического растворителя.
Данный способ имеет несколько недостатков, в том числе при реализации используется не менее, чем 30%-ная перекисью водорода, которая, как известно, не может храниться долго и в течении нескольких месяцев теряет свою активность за счет разложения. Кроме того, недостатком известного способа является использование соединений тяжелых металлов, присутствие которых, являющихся кроме всего прочего высокотоксичными вещества2 2
ы
ми, снижает стабилизирующие свойства стабилизатора полимеров Агидола-5, Чтобы этого не происходило, необходима дорогостоящая специальная очистка целевого продукта от примесей тяжелых металлов,
.Известен также способ получения ТТБДФХ окислением 2,6-дитретбутилфено- ла чистым кислородом или кислородом воздуха, в качестве катализатора используют комплекс двухлористой меди с морфоли- ном, Чтобы получить чистый ТТБДФХ необходимо провести его спецочистку от соединений меди, которые накапливаются в нем во время реакции и впоследствие снижают эффективность Агидола-5.
Наиболее близким к предлагаемому является способ получения ТТБДФХ путем окисления 2,6-дитретбутилфенола кислородом воздуха при 200°С и давлении 13 атм в присутствии КОН.
Недостатками этого способа являются периодичность процесса и использование повышенного давления для получения ТТБДФХ, что удорожает способ и делает его малопригодным для промышленности.
Цель изобретения - упрощение технологии процесса и повышение выхода целевого продукта.
Поставленная цель достигается тем, что согласно способу получения 3,3,5,5 -тет- ратретбутил-4,4 -дифенохинона окислением 2,6-дитретбутилфенола кислородом воздуха в растворителе в присутствии щелочи, окисление 2,6-дитретбутилфенола ведут в смеси толуола или бензола и воды при объемном соотношении толуол (или бензол): вода, равном 1:0,5-1, процесс ведут а присутствии катализатора межфазного переноса, выбранного из групп 18-краун-6, 18-дибензокраун-6, триэтилбензиламмонийхлорид при массовом соотношении 2,6-дитретбутилфенол:ще- лочьжатализатор, равном 50:10-15:1-1,5, и процесс ведут при 20-110°С.
Пример. А. В двухфазную систему, состоящую из раствора 50 г 2,6-дитретбутилфенола, 10 г NaOH в 50 мл толуола и раствора 1,0 г 18-краун-6 в 50 мл НаО, пропускают в интервале температур 20-40 С воздух со скоростью 0,06 л/мин так, чтобы реакционная смесь спокойно кипела. Через 1,5 ч отделяют органический слой от водного, от органического слоя отфильтровывают образовавшиеся темно-красные кристаллы, промывают двумя порциями по 2,5 мл воды. Выход полученного ТТБДФХ 47.0 г (95%).
Б. 50 г 2,6-дитретбутилфенола растворяют в фильтрате органического слоя и
добавляют к нему 5 мл толуола. Полученный раствор объединяют с водным слоем и 5 мл промывных вод и используют, как показано в примере 1А, для получения новой порции
ТТБДФХ выход 45,5 г (92 %).
В. Затем в фильтрате органического слоя с добавлением 5 мл толуола растворяют новую порцию 50 г 2,6-дитретбутилфенола и проводят третий цикл превращений,
как показано в примере 1А, Б. Выход ТТБДФХ 42,1 г (85%).
В одной и той же двухфазной системе с добавлением каждый раз по 5 мл толуола и
промывной воды можно провести до 10 и более циклов превращений, при этом выход ТТБДФХ после десятого цикла составляет 12,4 г (25%). Толуол и промывные воды (по 5 мл) добавляют для того,
чтобы нейтрализовать убыль растворителей за счет их испарения.
Пример 2. А В двухфазную систему, состоящую из раствора 50 г 2,6-дитретбутилфенола, 15 г NaOH в 50 мл толуола и раствора 1,5 г 18-краун-6 в 50 мл Й20, в интервале температур 20-40°С пропускают воздух со скоростью 0,06 л/мин так, чтобы реакционная смесь спокойно кипела. Через 1,5 ч отделяют органический слой от водного, от органического слоя отфильтровывают образовавшиеся темно-красные кристаллы, промывают двумя порциями по 2,5 мл воды. Выход полученного ТТБДФХ
47,0 г (95%).
Б. 50 г 2,6-дитретбутилфенола растворяют в фильтрате органического слоя и добавляют к нему 5 мл толуола. Полученный раствор объединяют с водным слоем
и 5 мл промывных вод и используют, как показано в примерах 1А и 2А для получения новой порции ТТБДФХ. Выход 47,0 г (95%).
В, Затем в фильтрате органического
слоя с добавлением 5 мл толуола растворяют новую порцию 50 г 2.6-дитретбутилфено- ла и проводят третий цикл превращений, как показано в примерах 1.2(А,Б) Выход ТТБДФХ 43,6 г (88%).
В одной и той же двухфазной системе можно провести до 10 и более циклов превращений, при этом выход ТТБДФХ после десятого цикла составляет 13,9
(28%).
П р и м е р 3. Проводят аналогично примеру 1А, отличие состоит в гом. что скорость пропускания воздуха увеличена до 0,6 л/мин. Выход ТТБДФХ составляет 47,0 (95%).
При скорости пропускания воздуха меньше 0,05 л/мин выход ТТБДФХ сокращается до 32,7 г (66%).
П р и м е р 4, Проводят аналогично примеру 1 А, отличие состоит в том, что вместо толуола используют бензол. Выход ТТБДФХ составляет 45,5 г (92%).
П р и м е р 5. Проводят аналогично примеру 1 А, отличие состоит в том, что объемное соотношение толуола и воды составляет 1:1,5 (50 мл толуола и 75 мл воды). Выход ТТБДФХ составляет 44,1 г (89%).
Примерб. Проводят аналогично примеру 1А, отличие состоит в том. что объемное соотношение толуола и воды составляет 1:0,3 (50 мл толуола и 15 мл воды); Выход ТТБДФХ составляет 22,3 г (45%).
Пример. Проводят аналогично примеру 1А, отличие состоит в том, что температуру реакционной смеси поддерживают в интервале 80-110°С. Выход ТТБДФХ составляет 41,6 г (84%).
Примерз. Проводят аналогично примеру 1А, отличие состоит в том, что соотношение 2,6-дитретбутилфенола, NaOH и 18-краун-6 е массовых частях составляет 50:5:1 (50 г 2.6-дитретбутилфенола, 5 г NaOH и 1 г 18-краун-6). Выход ТТБДФХ 24,7 г (50%).
П р и м е р 9. Проводят аналогично примеру 1А, отличие состоит в том, что соотношение 2,6-дитретбутилфенола, щелочи и 18-краун-6 в массовых частях составляет 50:10:10,5 (50 г 2,6-дитретбутилфенола, 10 г щелочи и 0,5 г 18-краун-6). Выход ТТБДФХ 40,1 г (81%).
Пример 10. Проводят аналогично примеру 1 А, отличие состоит в том, что вместо едкого натра используют едкое кали. Выход ТТБДФХ 44,1 г (89%).
ПримерИ. Проводят аналогично примеру 1А, отличие состоит в том, что вместо катализатора 18-краун-6 используют 18- дибензокраун-6. Выход ТТБДФХ 39,6 г (80%).
Пример 12. Проводят аналогично примеру 1 А, отличие состоит в том, что вместо катализатора 18-краун-б используют триэтилбензиламмонийхлорид. Выход ТТБДФХ 32.2 г (65%).
Пример 13. Проводят аналогично примеру 1А, отличие состоит в том, что продолжительность пропускания воздуха составляет 1 ч. Выход ТТБДФХ 39,6 (80%).
П р и м е р 14. Проводят аналогично примеру 1 А, отличие состоит в том, что продолжительность пропускания воздуха составляет 2 ч. Выход ТТБДФХ 47,0 (95%).
П р и м е р 15. Проводят аналогично примеру 1А, отличие состоит в том, что температура реакционной смеси 15°С. Выход ТТБДФХ составляет 22.3 г (45%). П р и м е р 16. Проводят аналогично
примеру 1А, отличие состоит в том, что температура реакционной смеси 20°С. Выход ТТБДФХ составляет 47,0 г (95%).
ПримерП. Проводят аналогично примеру 1А, отличие состоит в том, что тем- пература реакционной смеси 30°С. Выход ТТБДФХ составляет 47,0 г (95%).
Пример 18. Проводят аналогично примеру 1 А, отличие состоит в том, что тем- 5 -.пература реакционной смеси 40°С. Выход ТТБДФХ составляет 47,0 г (95%).
П р и м е р 19. Проводят аналогично примеру 1 А, отличие состоит в том, что температура реакционной смеси 50°С. Выход 2о, ТТБДФХ составляет 43,6 г (88%).
П р и м е р 20. Проводят аналогично примеру 1 А, отличие состоит в том, что процесс проводят при 60°С. Выход ТТБДФХ . 94%.
25 П р и м е р 21. Проводят аналогично примеру 1А, отличие состоит в том, что процесс проводят при 80°С. Выход ТТБДФХ 93%.
П р и м е р 22. Проводят аналогично Зо примеру 1А, отличие состоит в том, что процесс проводят при 100°С. Выход ТТБДФХ 90%.
П р и м е р 23. Проводят аналогично примеру 1А, отличие состоит в том, что со- с отношение реагентов 50:8:1. Выход ТТБДФХ 2.7 г (66%).
П р и м е р 24. Проводят аналогично примеру 1А, отличие состоит в том, что соотношение реагентов 50:10:0,8. Выход 0 ТТБДФХ 32,2 г (65%).
П р и м е р 25. Проводят аналогично примеру 1А, отличие состоит в том, что соотношение реагентов 50:8:1,5. Выход ТТБДФХ 32,7 (66%).
с П р и м е р 26. Проводят аналогично примеру 1А, отличие состоит в том, что соотношение реагентов 50:15:0,8. Выход ТТБДФХ 32,2 г (65%).
П р и м е р 27. Проводят аналогично -, примеру 1А, отличие состоит в том, что соотношение реагентов 50:12:1. Выход ТТБДФХ 47,0 (95%).
П р и м е р 28. Проводят аналогично примеру 1А, отличие состоит в том, что соотношение реагентов 50:12:1,2. Выход ТТБДФХ 47,0 г (95%).
П р и м е р 29. Проводят аналогично примеру 1А, отличие состоит в том, что соотношение реагентов 50:15:1,2. Выход ТТБДФХ 47,0 г (95%).
П р и м е р 30. Проводят аналогично римеру 1А, отличие состоит в том, что сотношение реагентов 50:17:10. Выход ТБДФХ46,5г(94%).
П р и м е р 31. Проводят аналогично римеру 1А, отличие состоит в том, что сотношение реагентов 50:17:1,8. Выход ТБДФХ 46,5 г (94%).
П р и м е р 32. Проводят аналогично примеру 1А, отличие состоит в том, что соотношение реагентов 50:10:1,8. Выход ТБДФХ 45,5 г (92%).
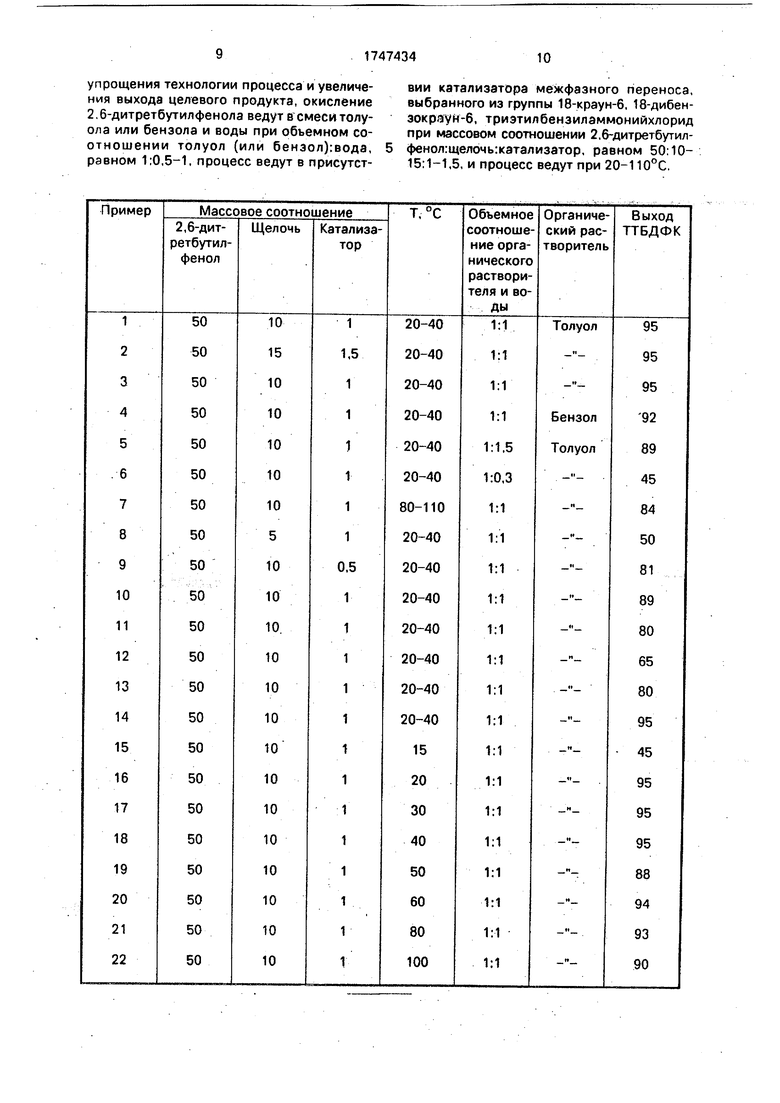
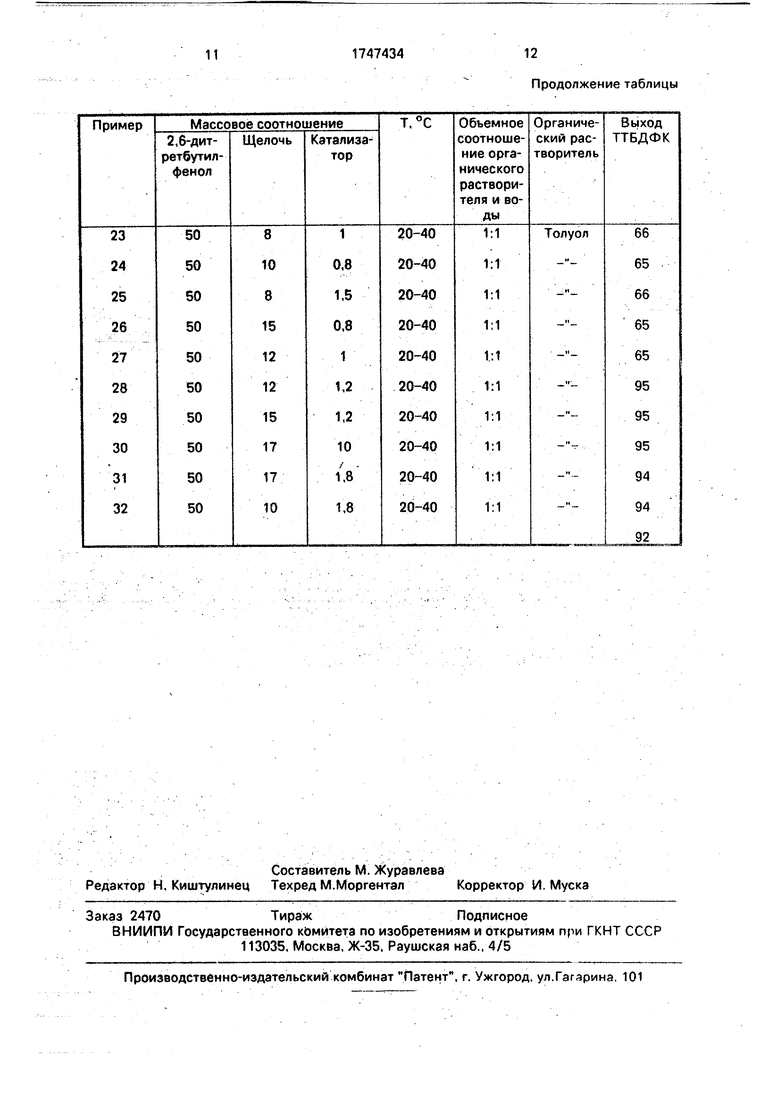
Обобщенные параметры ведения процесса по примерам 1-32 приведены в таблице.
Как видно из приведенных экспериментальных данных, оптимальным соотношением 2,6-дитретбутилфенола : :щелочи:межфазного катализатора является 50:10-15:1-1,5 мас.ч. Уменьшение или увеличение массовой части щелочи и межфазного катализатора нецелесообразно, так как ведет в первом случае к уменьшению выхода ТТБДФХ, а во втором случае не увеличивает выход ТТБДФХ (примеры 1,2,8,9). Предпочтительнее использовать в качестве щелочи более дешевую №аОН, чем КОН (пример 10), а из межфазных катализаторов - 18-краун-б, так как в случае дибен- зо-18-краун-би
триэтилбензиламмонийхлорида ТТБДФХ получается с меньшим выходом (примеры 11,12).
Предлагаемый способ характеризуется непрерывностью процесса, положенного в основу получения целевого продукта. После проведения процесса и отделения образовавшегося ТТБДФХ в фильтрат добавляют новую порцию 2,6-дитретбутилфенола, не добавляя при этом другие компоненты реакционной смеси, и ведут реакцию вновь. Выход образовавшегося ТТБДФХ после второго цикла превращений несколько ниже 92%. После третьего цикла выход составляет 85%. Для получения ТТБДФХ с выходом 25% можно использовать одну и ту же реакционную смесь десять раз (примеры 1,2).
Очистка образующегося ТТБДФХ не представляет затруднений, так как состоит лишь в отделении образующегося осадка ТТБДФХ от раствора реакционной смеси и промывании его небольшим количеством воды, которую добавляют затем в реакционную смесь и возвращают таким образом в маточный раствор следы щелочи и межфазного катализатора (пример 1). Следы щелочи или межфазного катализатора, оставшиеся в плохо
промытом ТТБДФХ, не снижают эффективность действия полученного ТТБДФХ Аги- дола-5, как, например, в случае применения катализаторов с тяжелыми металлами.
При температуре меньше 20°С 2,6-дитретбутилфенол, находящийся в растворе реакционной смеси, выпадает в виде осадка, что ведет к снижению выхода дифенохинона (пример 1).
0 Если температуру реакционной смеси поддерживают в интервале 20-40°С, то достигается максимальный выход ТТБДФХ (примеры 2-4). При температурах 50-80°С наблюдается меньший выход ТТБДФХ
5 (пример 5). При температуре 80-110°С выход ТТБДФХ еще меньше (пример 7).
Уменьшение выхода ТТБДФХ при увеличении температуры реакционной смеси, очевидно, связано с протеканием побоч0 ных процессов, При соотношении 2,6-дитретбутилфенола: щелочи: межфазного катализатора 50:10:1 выход ТТБДФХ составляет 95% (пример 1А). При уменьшении массовой части щелочи или
5 межфазного катализатора выход ТТБДФХ снижается (примеры 8,9 и 6-9). При увеличении массовой части щелочи или межфаз- ного катализатора выход ТТБДФХ составляет 95% вплоть до соотношения
0 50:15:1,5 (примеры 10-12, 2А). Увеличение массовой части щелочи и межфазного катализатора нецелесообразно, так как не увеличивает выход ТТБДФХ (примеры 13- 15).
5 Отклонение от оптимального соотношения реагентов и катализатора 50:10-15:1- 1,5 в меньшую или большую сторону ведет к уменьшению (хоть и незначительному) выхода ТТБДФХ, что объясняется нарушением
0 равновесной концентрации гидроксид-ани- она в системе. Полученный ТТБДФХ имеет т.пл. 246°С.
ИК-спектр (вазелиновое масло): , (1580, 1610, 1640см 1), трет-С Нэ(1050,
5 1090см 1).
ПМР-спектр: трет-СзНэ 1,5 м.д.(с). СН 6,8 м.д.(с).
Таким образом, предлагаемый способ обладает следующими преимуществами: не0 прерывность процесса в связи с возможностью использования фильтрата, отсутствие высокого давления при получении целевого продукта по сравнению с прототипом, выход целевого продукта достигает 95%.
5 Формула изобретения
Способ получения 3,3,5,5 -тетратрет- бутил-4,4 -дифенохинона окислением 2,6- дитретбутилфенола кислородом воздуха в растворителе в присутствии щелочи, отличающийся тем, что, с целью
упрощения технологии процесса и увеличения выхода целевого продукта, окисление 2.6-дитретбутилфенола ведут в смеси толуола или бензола и воды при объемном соотношении толуол (или бенэол):вода, равном 1:0,5-1, процесс ведут в присутствии катализатора межфазного переноса, выбранного из группы 18-краун-6, 18-дибен- зокраун-6, триэтилбензиламмонийхлорид при массовом соотношении 2,6-дитретбутил- фенол:щелочь:катализатор, равном 50:10- 15:1-1,5, и процесс ведут при 20-110°С.
Продолжение таблицы



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 3,3 @ , 5,5 @ -тетратрет-бутил-4,4 @ -дифенохинона | 1990 |
|
SU1810325A1 |
| Способ получения 3,3 @ ,5,5 @ -тетратретбутил-4,4 @ -дифенохинона | 1990 |
|
SU1740368A1 |
| Способ получения стирола | 1983 |
|
SU1143739A1 |
| Способ получения 3,3,5,5-тетратретбутил-4,4-дифенохинона | 1977 |
|
SU687063A1 |
| Способ получения моно- или дизамещенных @ - или @ - карборанов | 1980 |
|
SU888493A1 |
| Способ получения спиро[2.4]гепта-4,6-диена | 2017 |
|
RU2657871C1 |
| Способ получения алкил(фенилэтинил)селенидов | 1990 |
|
SU1728237A1 |
| Способ дезактивации катализатора полимеризации продукта взаимодействия галогенида металла переменной валентности с триалкилалюминием | 1977 |
|
SU696026A1 |
| Способ получения и разделения транс-син-транс- и транс-анти-транс-изомеров дициклогексано-18-краун-6 | 1985 |
|
SU1270152A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИХИНОНОВ | 2014 |
|
RU2552516C1 |
Сущность изобретения: продукт - 3,3. 5.5 тетратретбутил-4,4 -дифенохинон. Реагент 1: 2,6 дитретбутилфенол. Реагент 2- кислород воздуха. Условия реакции: при 20- 40°С в среде неполярного органического растворителя и воды при объемном соотношении 1:(0,5-1) в присутствии катализатора межфазного переноса 18-краун-6 и щелочи, 1 табл.

| Патент США N 3281435, кл 260-396, 1963 | |||
| Способ получения 3,3,5,5-тетратретбутил-4,4-дифенохинона | 1977 |
|
SU687063A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| 1971 |
|
SU413140A1 | |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Патент США № 4238627, кл | |||
| Нефтяная топка для комнатных печей | 1923 |
|
SU568A1 |
Авторы
Даты
1992-07-15—Публикация
1990-04-04—Подача