азотнокислого, 18% (5,6 М) раствора перок- сида водорода и 11% (6,1 М) раствора водного аммиака, а также ухудшается степень отмывки осадка от примесей.
Цель изобретения - ускорение процесса.
Поставленная цель достигается тем, что водные растворы соликальцил с концентрацией 0,8-2,5 М, пероксида водорода и гид- роксида аммония параллельно влияют в водную суспензию кристаллического окта- гидрата пероксида каЖция при охлах дении и молярных соотношениях СаС(2(Са(ЫОз)2 : Н202 : (NHUOH 1 ; (1.3-1.4) : (2,6-2,8). Образовавшуюся суспензию кристаллогидрата пероксида кальция выдерживают при перемешивании, после чего осадок отделяют от маточного раствора, промывают от примесей и подвергают термической дегидратации.
При молярной концентрации указанных растворов солей кальция меньшей 0,5 М, и большей 2,5 М, поставленная цель по заявленному способу не достигается,-независимо от массовой концентрации кристаллического октагидрата пероксида кальция в исходной суспензии. При использовании разбавленных растворов съем пероксида кальция с 1 кг массы, введенной в синтез, меньше, чем в прототипе. При использовании очень концентрированных растворов солей кальция качество пероксида кальция хуже. В отсутствии первоначальной водной суспензии кристаллического октагидрата пероксида кэльция резко снижается скорость фильтрования полученной в результате взаимодействия реагентов суспензии и качество целевого продукта, Это объясняется образованием в указанных условиях пастообразного вязкого дигидрата пероксида кальция. Последний значительно труднее отмывается от анионов, присутствующих в жидкой фазе, и легче разлагается в маточном растворе с образованием гидро- ксида кальция, чем кристаллические октз- и дигидраты пероксида кальция, которые образуются в присутствии водной суспензии кристаллического октагидрата пероксида кальция. Однофазный кристаллический ок- тагидрат пероксида кальция при температуре до 10°С образуется только при взаимодействии 1-2 молярного раствора кальция хлористого или кальция азотнокислого с 2,5-3,5%-ным раствором пероксида водорода и 2,0-2.5% -ным раствором гидро- ксида аммония.
Таким образом, при отсутствии исходной водной суспензии кристаллического октагидрата пероксида кальция интенсифика0
5
0
5
0
ция процесса при сохранении качества продукта не обеспечивается.
Массовая концентрация кристаллического октагидрата пероксида кальция в первоначальной суспензии на достижение поставленной цели не оказывает влияния.
Обьем первоначальной водной суспензии кристаллического октагидрата пероксида кальция должен обеспечить интенсивное перемешивание реакционной массы в начале процесса и зависит от нижнего уровня мешалки в реакторе и его диаметра,
Съем пероксида кальция с 1 кг введенной в синтез массы рассчитывают только по массе образовавшегося из водных растворов (Са(МОз)2, H2U2 и NM/iOH кристал- логидратор пероксида кальция (смеси очта- и дигидрата пероксида кальция). В расчет пе принимают массу пероксида кальция, образовавшуюся из специально введенного в ре- акционную массу кристаллического октагидрата пероксида кальция. Ее вычитают из общей массы пероксида кальция, полученной в опыте, а затем разницу относят ко всей реакционной массе при расчете съема продукции с 1 кг введенной в синтез массы.
Пример 1. В стеклянный реактор, вместимостью 20 дм3, снабженный мешалкой и водяной рубашкой, заливают дистиллированную воду в количестве 2,0 дм3 и охлаждают ее до 8-10°С подачей охлажденной воды в рубашку. Затем всыпают 200 г кристаллического октагидрата пероксида кальция и при перемешивании со скоростью 110±20 об/мин, в течение двух часов параллельно сливают 6,27 дм3 раствора кальция хлористого с концентрацией 2,2 М (21%), 2,05 дм3 раствора пероксида водорода с концентрацией 9,0 М ( 27%) и 3,03 дм3 раствора гидроксчда аммония с концентрацией 12,0 М ( 22%). При этом скорость введения исходных растворов 3,14; 1,03; 1,52 дм /ч соответственно. В указанных условиях обеспечивается молярное соотношение СаОД . 1 : 1.3: 2,6 и рН порядка 9,3. По окончании слива растворов суспензию перемешивают в течение 15- 20 мин, а затем фильтрацией под вакуумом отделяют осадок кристаллогидрата от маточного раствора, промывают 20 дмЗ охлажденной до 8-10°С дистиллированной воды и сушат в слое 15-25 мм при периодическом перемешивании при 95-120°С и непрерывном отводе выделяющихся водяных паров 5 до массовой доли влаги не более 0,5%. Полученный продукт содержит, мас.%: Са02 90,6, влаги 0,0, С 0,4, N 0,08, С 0,005, K+Na 0,01. Ре 0,009, нерастворимых в HCL примеси - 0,01, РЬ - 0.005%. Выход пероксида кальция составляет 78%. При этом расход
5
0
5
0
пероксида водорода равен 2,9 кг/кг СаС)2. а гидроксида аммония 3,55 кг/кг Са02. Относительная скорость фильтрации кристаллогидрата пероксида кальция равна 135 дм /ч. Съем пероксида кальция с 1 кг массы, введенной в синтез 54 г.
Пример 2. В стеклянный реактор вместимостью 20 дм3, снабженный мешалкой и водяной рубашкой, заливают дистиллированную воду в количестве 2 дм3 и охлаждают ее до 8-10°С подачей охлажденной воды в рубашку. Затем всыпают 185 г кристаллического октагидрата пероксида кальция и при перемешивании со скоростью 110+20 об/мин в течение полутора ча- сов параллельно сливают 5,52 дм3 раствора кальция хлористого с концентрацией 2,5 М (23%), 1,66 дм3 раствора пероксида водорода с концентрацией 11,5 М ( 35%) и 2,7 дм раствора гидроксида аммония с концен- трацией 14,5 М (27%). При этом скорость слива исходных растворов составит 3,68: 1,11; 1,8 дм /ч соответственно. В указанных условиях обеспечивается молярное соотношение CaCfc : NH4OH 1 :1,4 : 2,8 и рН порядка 9,2. По окончании слива растворов суспензию перемешивают в течение 15-20 мин, а затем фильтрацией под вакуумом отделяют осадок кристаллогидрата от маточного раствора, промывают 20 дм3 ох- лажденной до 8-10°С дистиллированной воды и сушат в слое 15-25 мм при периодическом перемешивании при 95- 120°С и отводе выделяющихся водных паров до массовой доли влаги не более 0,5%. Полученный продукт содержит, мас.%: Са02 89,0, влаги 0,5, С 0,5, N 0,07, С 0,005, К + Na 0,02, Fe 0,009, нерастворимых в HCI примесей - 0,01, РЬ 0,005. Выход пероксида кальция составляет 80,0%. При этом расход раствора пероксида водорода составляет 2,35 кг/кг Са02, а раствора гидроксида аммония 3,04 кг/кг СаОа. Относительная скорость фильтрации кристаллогидрата равна 136 дм /ч. Съем пероксида кальция с 1 кг массы, введенной в синтез, 58 г.
Пример 3. В стеклянный реактор вместимостью 20 дм3, снабженный мешалкой и водяной рубашкой, заливают дистиллированную воду в количестве 2 дм и охлаждают ее до 8-10°С подачей охлажденной воды в рубашку. Затем всыпают 215 г кристаллического октагидрата пероксида кальция и при перемешивании со скоростью 110±20 об/мин в течение полутора часов параллельно вводят 5,52 дм3 раствора кальция азотнокислого с концентрацией 2,5 М (32%), 1,898 дм3 раствора пероксида водорода с концентрацией 9,8 М (30%) и 2,79 дм раствора гидроксида аммония с
концентрацией 13,35 М (25%). При этом скорость введения исходных растворов составляет 3,68; 1.27; 1,86 дм3/ч соответственно. В указанных условиях обеспечивается мольное отношение Са(МОз)2 : Н202 : МЩОН - 1 : 1,35 : 2,7 и рН порядка 9,2. По окончании слива растворов суспензию перемешивают в течение 15-20 мин, а затем фильтрацией под вакуумом отделяют осадок кристаллогидрата от маточного раствора, промывают 20 дм охлажденной до 8-10°С дистиллированной воды и сушат в слое 15-25 мм при периодическом перемешивании при 95-110°С и непрерывном отводе выделяющихся водяных паров до массовой доли влаги не более 0,5%.
Полученный продукт содержит, мас.%: -Са02 91,9, влаги 0,5, С 0,5, N 0,08. CI 0,005, K+Na 0,02, Fe 0,009, нерастворимых в HCI примесей - 0,01, РЬ 0,005. Выход пероксида кальция составляет 80%. При этом расход 30% пероксида водорода равен 2,64 кг/кг Са02, раствора гидроксида аммония 3,2 кг/кг Са02. Относительная скорость фильтрации кристаллогидрата пероксида кальция равна 150 дм3/ч. Съем пероксида кальция с Т кг массы, введенной в синтез, 58 г.
Последующие опыты проводят в аналогичных условиях, меняя молярное соотношение реагентов.
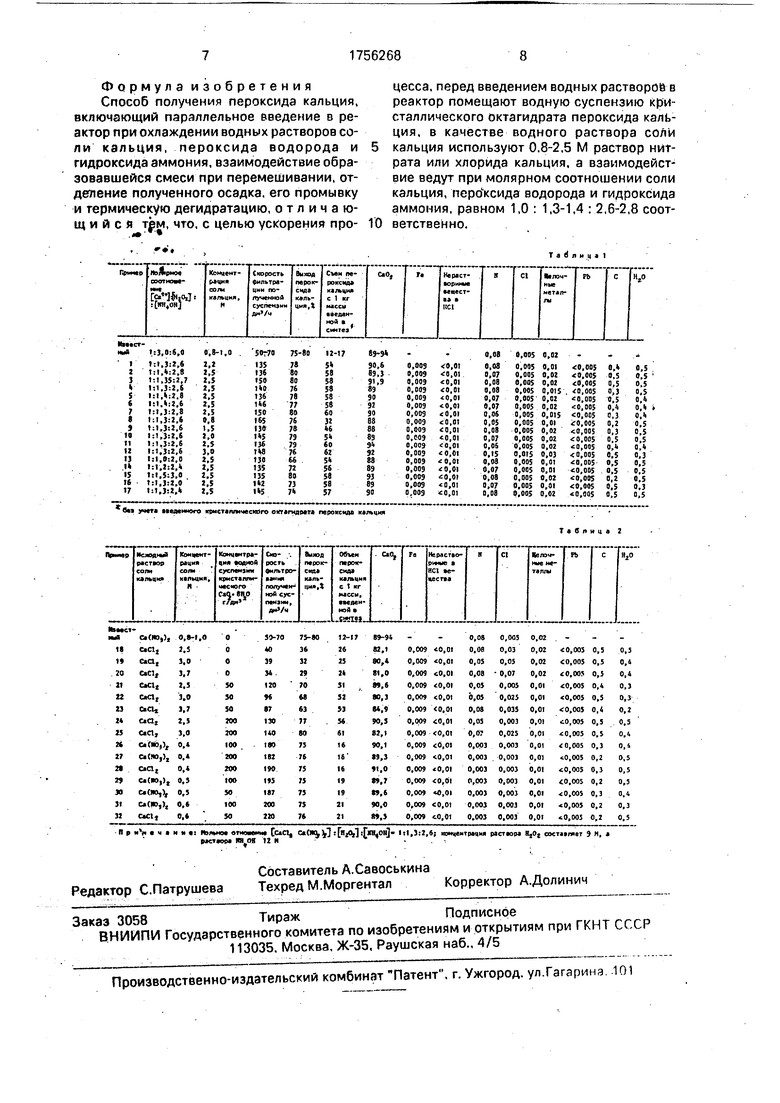
Результаты опытов представлены в табл. 1, 2.
При проведении процесса осаждения при молярных соотношениях, меньших, чем Н202 : NH40H 1 ; 1.3 : 2.6, поставленная цель не достигается, так как либо уменьшается выход пероксида кальция, либо съем продукции.
Увеличение молярного соотношения Са2+ : Н202 : МЩОН более 1 : 1,4 ; 2,8 экономически нецелесообразно. При увеличении концентрации соли кальция больше 2,5 моль/дм3 ухудшается качество пероксида кальция.
Предлагаемый способ обеспечивает увеличение выхода пероксида кальция с 1 кг массы, введенной в синтез, до 54-60 г (у прототипа 12-17 г), скорости фильтрации водной суспензии кристаллогидрата пероксида кальция в идентичных условиях до 130- 150 дм3/ч (у прототипа 50-70 дм3/ч), уменьшение расхода пероксида водорода 30%-ного до 2,50-2.95 кг/кг Са02, (у прототипа 5,8-6,3 кг/кг Са02) и гидроксида аммония 25%-ного до 3,1-3,5 кг/кг СаОа (у прототипа 7,1-7,5 кг/кг Са02), при сохранении выхода пероксида кальция 75-80% и его качества.
Формула изобретения Способ получения пероксида кальция, включающий параллельное введение в реактор при охлаждении водных растворов со- ли кальция, пероксида водорода и гидроксида аммония, взаимодействие образовавшейся смеси при перемешивании, от- детение полученного осадка, его промывку и термическую дегидратацию, отличающийся тем, что, с целью ускорения про- «
0
цесса, перед введением водных растворов в реактор помещают водную суспензию кристаллического октагидрата пероксида кальция, в качестве водного раствора соли кальция используют 0,8-2,5 М раствор нитрата или хлорида кальция, а взаимодействие ведут при молярном соотношении соли кальция, перо ксида водорода и гидроксида аммония, равном 1,0 : 1,3-1,4 : 2,6-2,8 соответственно,
Таблица 1


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения пероксида кальция | 1990 |
|
SU1778068A1 |
| Способ получения пероксигидратов пероксида кальция | 1988 |
|
SU1643453A1 |
| Способ получения пероксигидратов пероксида кальция | 1988 |
|
SU1643455A1 |
| Способ получения пероксигидратов пероксида кальция | 1988 |
|
SU1643456A1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЗВОДНОГО ПЕРОКСИДА КАЛЬЦИЯ | 2007 |
|
RU2341449C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ВЫСОКОКРЕМНЕЗЕМНОГО ЦЕОЛИТА | 2010 |
|
RU2457179C2 |
| Способ получения пероксида кальция | 1987 |
|
SU1532547A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРАТОВ ХЛОРИДОВ ЩЕЛОЧНО-ЗЕМЕЛЬНЫХ МЕТАЛЛОВ | 2006 |
|
RU2338689C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОБАЛЬТ (II) СУЛЬФАТА | 1998 |
|
RU2141452C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕКСАГИДРАТА НИТРАТА МАРГАНЦА ВЫСОКОЙ ЧИСТОТЫ | 2009 |
|
RU2410329C1 |


Авторы
Даты
1992-08-23—Публикация
1990-06-25—Подача