(21)
(22)10.12.90
(46)30.12.92. Бюл. № W
(71)Институт терапии СО АМН СССР
(72)М.И.Душкин
(56)Journal of BioloRical Chemistry, 1980, 255, 9344.
( СПОСОБ ПОЛУЧЕНИЯ ПЕНИСТЫХ КЛЕТОК ИЗ МАКРОФАГОВ МЫШИ
(57)Использование: биология, медицина. Сущность изобретения: на четвертые сутки после внутрибрюшинного введения 10% гликогена мышам внутри- брюшинно вводят среду Хенкса, содержащую ацетилированные липопротеиды низкой плотности или окисленный холестерин из расчета 2 и 1мг холестерина на 18 г веса живого. Через 2 ч из перитонеальной полости мышей извлекают макрофаги, трансформированные в пенистые клетки. 3 табл.



Изобретение относится к биологии и медицине, в частности к методам исследования патогенеза и профилактики атеросклероза.
Известен способ получения пенистых клеток, схожих с клетками в атероскле- ротической аорте, из макрофагов, заключающийся в том, что полученные из перитонеальной полости мышей резидентные макрофаги культивируют в пластиковых чашках Петри в среде ЕРМУ-1640, содержащей 2 мМ глутати- она, 10% делипидированную сыворотку крови человека, 100 ЕД/мл пенициллина, 100 мкг/мл стрептомицина и 100 мкг белка модифицированных ацетилляцией липопротеидов низкой плотности (ЛПНП) в 1 мл среды, в течение 2Ц часов при 37°С в атмосфере С0а (5%) и воздуха (95%). В конце исследования монослой клеток промывают средой 199 и исследуют влияние антиатерогенных фармакологических препаратов на скорость включения 4С-олеата в эфиры
холестерина и содержание холе стерина в полученных пенистых клетках.
Недостатки указанного способа заключаются в невысокой точности воспроизведения условий культивирования макрофагов, вариабельности использования различных серий среды RPMI - , делипидизации сыворотки крови, в различии материалов применяемой культуральной посуды, в трудоемкости метода культивиро§ания макрофагов в стерильных условиях, в использовании дорогостоящих питательных сред и оборудования для клеточных культур. Кроме того, культивирование макрофагов in vitro не позволяет моделировать процессы образования холестерин-обогащенных пенистых клеток в организме,
Предлагаемый способ получения пенистых клеток в перитонеальной полости организма живых мышей позволяет значительно упростить процедуру метода, устранив выше перечне- ,
5
енные недостатки. Преимущества Предагаемого способа достигаются в результате способности макрофагов живых мышей накапливать большие коли- чества холестерина и трансформироваться в пенистые клетки при внутри- рюшинном введении эмульсии окисленного холестерина или ацетилированных липопротеидов низкой плотности (эце- JQ тил-ЛПНП).
Палуч Йе пени с тых клеток с высоким содержанием холесте рина и скоростью его эст ерификации осуществляют с помощью следующего метода: 15
Окисление холестерина проводим на воздухе при температуре 60°С в течение 6 недель. 20 мг окисленного холестерина растворяем в 60 мкл ацетона . при температуре 60°С и быстро вносим 20 в 10 мл раствора Хенкса, содержащего 50% бычий сывороточный альбумин (БСА). Раствор перемешиваем на магнитной мешалке под током азота, поступающего из баллона с азотом, в течение 25 часа для удаления ацетона. Полученная эмульсия стабильная в течение 2 часов. Липопротеиды низкой плотности (019-1,055 г/мл) выделяем из плазмы доноров методом ультрацентри- 30 фугирования ЛПНП (5 мг белка в 1 мл раствора Хенкса) разбавляем (1:1. V:V) насыщенным раствором ацетата натрия при температуре 0°С. К разбавленному таким образом раствору ЛПНП gg (10 мг в мл) периодически,один раз в 15 мин в течение часа, вносим по 2 мкл уксусного ангидрида с помощью микрошприца. Ацетилированные ЛПНП диализуем против 20 л 0,05 М 40 фосфатного буфера, рН 7,, 0,85% хлористого натрия в течение часов при °С. Полученные ацетилиро- ванные ЛПНП храним в течение трех суток при 4°С.45
Для стимуляции выхода макрофагов в перитонеальную полость 5-8 недельным мышам линии С57В1 внутрибрюшин- но вводили 1 мл раствора Хенкса, содержащего 10% гликоген. На четвертые -п сутки после введения гликогена мышам внутрибрюшинно вводим раствор ацетилированных ЛПНП или эмульсию окисленного холестерина из расчета 2 или 1 мг холестерина на 18 г веса мыши, соответственно. Через 2k часа после последнего введения из перито- неальной полости мышей получаем пенистые клетки. Для этого мышей забивали
55
п
5
и в перитонеальную полость вводили в мл среды RPMI - , содержащую 10%, эмбриональную сыворотку телят, 2 мМ глютатиона, 100 Ед/мл гентамицина, брюшную стенку массировали в течение 1 мин и аспирировали шприцом Ь мл перитонеальной жидкости, в которой с помощью камеры Горячева подсчитывали количество клеток. 2 мл среды, содержащей 2-Ю6 клеток, вносим в пластиковые чашки Петри диаметром 35 мм и инкубируем при 37°С в течение 2-х часов в атмосфере СО (5%) и воздуха (95%). Клеточный монослой отмываем раза средой RPMI - 16AO и полученные пенистые клетки характеризуем по скорости эстерификации холестерина и содержанию свободного и общего холестерина.
Определение содержания свободного и общего холестерина в пенистых клетках. Экстракцию липидов из клеток проводим, добавляя k мл гексана и изопропанола в объемном соотношении 3:2 в каждую чашку Петри, в течение 30 мин. Экстракт сливаем в стеклянные пробирки и органический растворитель упариваем в токе азота при 60°С. В сухом остатке определяем содержание общего и свободного холестерина в макрофагах энзиматическим методом с помощью набора, реактивов Bio-Lab- sistero (Финляндия)
Оставший на чашках Петри после экстракции липидов клеточный белок растворяем в 1 мл 0,2 М NaOH и определяем концентрацию белка методом Лоури. Содержание холестерина выражаем в мкг в расчете на 1 мг белка.
Определение скорости эстерификации холестерина в пенистых клетках. К полученному клеточному монослою вносим 2 мл среды КРМУ - , содержащей 0,2% альбумин и 0,2 мМ (1 -t+c) олеата радиоактивностью 1 мкКи/мл среды. Клетки инкубировали в течение 6 часов при температуре 37°С в атмосфере С0г (5%) и воздуха (95%). После инкубации клетки промываем охлажденным до °С раствором Хенкса и проводим экстракцию липидов гексаном и изопропанолом в объемом соотношении 3:2 описанным выше способом. Разделение эфиров холестерина осуществляем методом тонкослойной хроматографии на пластинах ( см) Силуфол (ЧССР) в двух системах растворителей :гексан:диэтиловый эфир:
:уксусная кислота в объемных соотношениях 6П А():1 и 90:10:1, Пластину проявляем в парах йода и радиоактивность эфиров холестерина подсчитываем в толуольном сцинтилляторе (k г
|РРО,0, 3 г РОРОР на 1 л толуола) в жидкостном сцинтилляционном счетчи ке Марк-Ill (США) по программе 2. Скорость эстерификации холестерина выражаем в кмоль включения С-олеата в эфиры холестерина на 1 мг клеточного белка за 6А инкубации по следующей формуле:
ЭДл 5Л Ј 1 § i Ј § .г 1У-MO.Ј fe РадТСуб:
: клеточный белок в мг,
где Рад.кл - радиоактивность Эфиров холестерина клеток в имп./мин,
Рад.Суб - радиоактивность добавляемого субстрата 4С- олеата в имп/мин-, (С) Суб. - концентрация субстрата (олеата) в среде инкубации в нмоль.
Определив таким образом концентра- (цию холестерина и его эфиров и скорость эстериЛикации холестерина в полученных клетках, можно определить степень трансформации макрофагов перитонеаль- нрй полости мышей в пенистые клетки и динамику накопления эфиров холестерина в клетках.
Пример 1. Исследование сравнительного влияния натиеных ЛПНП (1-2 мг холестерина/18 г массы живот10
окисленного холестерина и ацетил-ЛПНП повышает концентрацию эфиров холестери на в клетках в 60 раз и уровень свободного холестерина в 2 раза по сравнению с контролем. Десятикратное повышение скорости 5стериЛикации холе стерина и 60-кратное повышение содержания эфиров холестерина в перито- неальных макрофагах свидетельствует об их трансформации в типичные пенистые клетки, характерные для ранних стадий развития атеросклероза. г Предлагаемый способ позволяет по15 лучить пенистые клетки, которые могут быть использованы для изучения механизмов антиатерогенного действия фармакологических препаратов.
Пример 2. Исследование дей20 ствия антагониста кальция верапамила на скорость эстерификации холестерина в пенистых клетках. Пенистые клетки получаем,как описано выше после внутри- брюшинного введения окисленного холе25 стерина (1 мг/18 г массы мыши) и последующего культивирования их в чашках Петри. К среде для определения скорости эстерификации холестерина, которое подробно изложено выше,микро30 шприцом вносим верапамил в 5 мкл этилового спирта fla 1 мл среды культивирования в конечных концентрациях 25, 50, 75 и 100 мкМ. Табл.3 демонстрирует, что верапамил дозозависимо ингибирует
35 скорость эстерификации холестерина в
пенистых клетШэх, что, вероятно, свя- зано с его антиатерогенным действием.
Таким образом, предлагаемый способ
позволяет получить пенистые клетки в
ного), эцетилированных ЛПНП (0,f-2 мг 40 условиях их естественной трансформа- холестерина/ 18 г массы животного), Чии из перитонеальныхмакрофагов живых очищенного перекристаллизацией холе- мышей, которые могут быть использова ньг для изучений механизмов атерогене- за и действия антиатерогенных преластерина (1-2 мг холестерина/18 г массы животного) на содержание холестерина и скорость его эстерификации в пе- ритонеальных макрофагах мыши. Через 2k часа после внутрибрюшинного введения препаратов ЛПНП и холестерина получаем перитонеальные макрофаги и исследуем скорость эстерификации холестерина. Результаты исследования, представленные в табл.1, показывают, что наиболее высокое (десятикратное) повышение скорости эстериЛикации хо45 ратов. Форм
ула изобретения
Способ получения пенистых клеток из макрофагов мыши, включающий воз- 50 действие на макрофаги мышей окисленным холестерином или минопротеида- ми низкой плотности, отличающийся тем, что, с целью повышения выхода жизнеспособных клеток,
лестерина наблюдается при введении м н-55воздействие осуществляют in vivo
шам ацетил-ЛПНП и окисленного холе г внутрибрюшинным введением вещества
стерина в концентрации 2 и 1 мг холе-в дозе 1-2 мг/18 г массы мыши,затем
стерина/18 г массы мыши, соответстт выдерживают в течение суток и целевённо. Как видно из табл.2, введениевой продукт извлекают аспирацией.
ь х -
10
окисленного холестерина и ацетил-ЛПНП повышает концентрацию эфиров холестерина в клетках в 60 раз и уровень свободного холестерина в 2 раза по сравнению с контролем. Десятикратное повышение скорости 5стериЛикации холе стерина и 60-кратное повышение содержания эфиров холестерина в перито- неальных макрофагах свидетельствует об их трансформации в типичные пенистые клетки, характерные для ранних стадий развития атеросклероза. г Предлагаемый способ позволяет по15 лучить пенистые клетки, которые могут быть использованы для изучения механизмов антиатерогенного действия фармакологических препаратов.
Пример 2. Исследование дей20 ствия антагониста кальция верапамила на скорость эстерификации холестерина в пенистых клетках. Пенистые клетки получаем,как описано выше после внутри- брюшинного введения окисленного холе25 стерина (1 мг/18 г массы мыши) и последующего культивирования их в чашках Петри. К среде для определения скорости эстерификации холестерина, которое подробно изложено выше,микро30 шприцом вносим верапамил в 5 мкл этило- вого спирта fla 1 мл среды культивирования в конечных концентрациях 25, 50, 75 и 100 мкМ. Табл.3 демонстрирует, что верапамил дозозависимо ингибирует
35 скорость эстерификации холестерина в
пенистых клетШэх, что, вероятно, свя- зано с его антиатерогенным действием.
Таким образом, предлагаемый способ
позволяет получить пенистые клетки в
45 ратов. Форм
ула изобретения
Способ получения пенистых клеток из макрофагов мыши, включающий воз- действие на макрофаги мышей окисленным холестерином или минопротеида- ми низкой плотности, отличающийся тем, что, с целью повышения выхода жизнеспособных клеток,
178А922
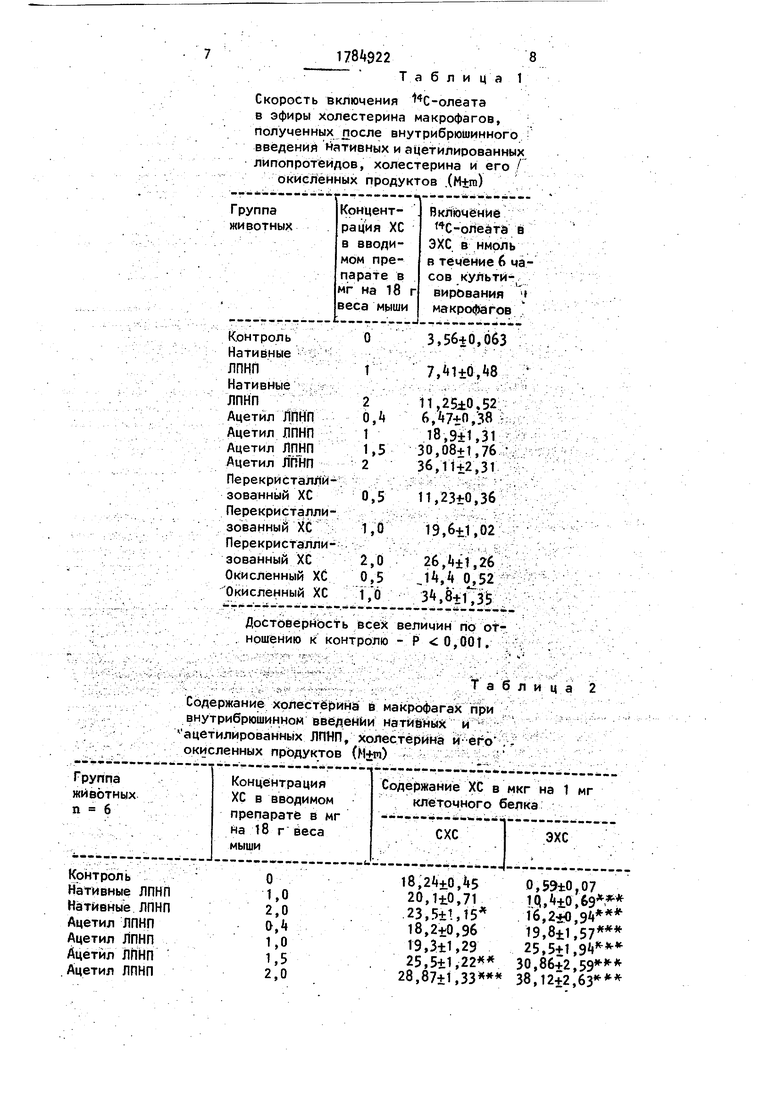
Таблица 1
Скорость включения 4С-олеата в эфиры холестерина макрофагов, полученных после внутрибрюшинного введений нативных и ацетилированных липопротеидов, холестерина и его окисленных продуктов (М+го)
Достоверность всех величин по отношению к контролю - Р 0,001,
Т а 6 л
Содержание холестерина в макрофагах при внутрибрюшинном введении нативных и ацетилированных ЛПНП, холестерина и-его , - окисленных продуктов (М+го)
О
1,0
2,0
М 1,0
1,5 2,0
8
ц а 2
8,24+0,It5 20,1±0,71 23,5+,15 18,2±0,96 19,3±1,29 25,5+1,22
8,87+1,33
0,5Э±0
16,
19,8±1
25,5-И
30,86+2
38,12+2
,07
;9/|
,57 ,91 ,59 ,63
Перекристаллизованный ХС0,5 Перекристаллизованный ХС1,0 Перекристаллизованный ХС 2,0 Окисленный ХС 0,5 Окисленный ХС 1,0
Достоверность отличий по отношению к контролю: , одна звездочка ,01 две ,002
три 0,001
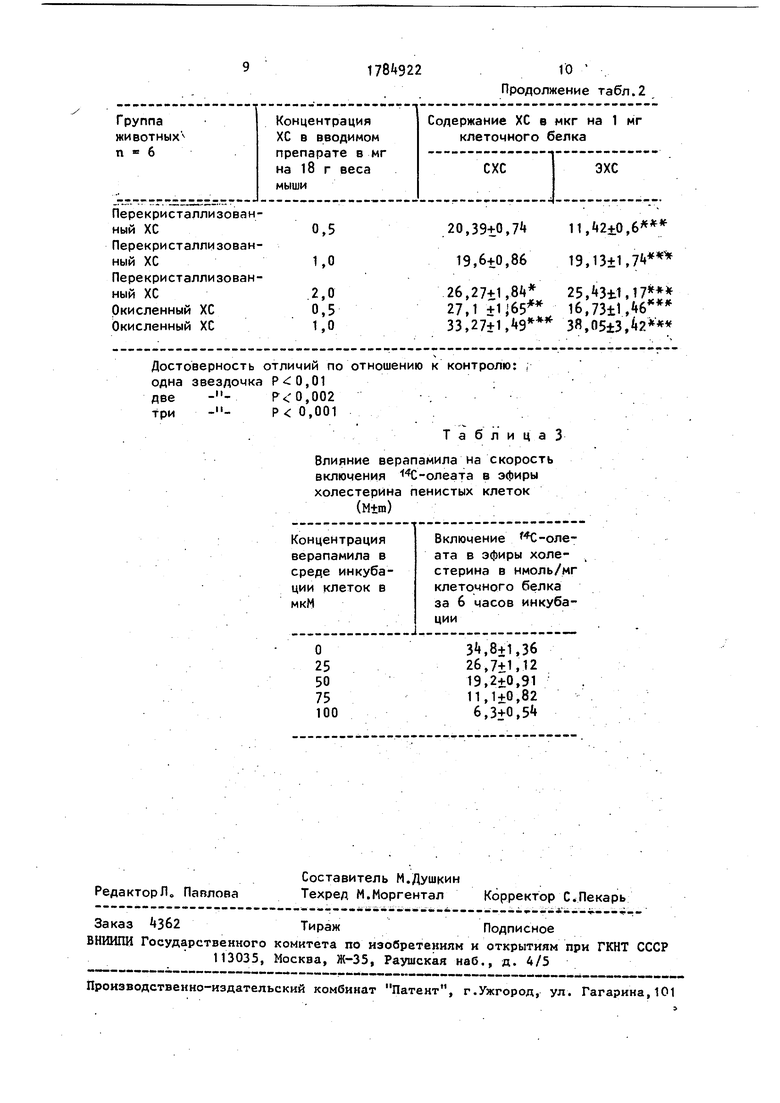
Таблица
Влияние верапамила на скорость включения -олеата в эфиры холестерина пенистых клеток (М±т)
Концентрация верапамила в среде инкубации клеток в мкМ
О
25
50
75
100
10 Продолжение табл.2
20,39±0,74 19,6tO,86
11,i42±0,6 19,13±1,7
26,27+1,8 25,,17 27,1 +1j65 16,73±1,46 33,27±М9 ЗЯ,05±ЗЛ2 «
Включение С-оле- ата в эфиры холестерина в нмоль/мг клеточного белка за 6 часов инкубации
3, 8+1,36 26,7+1,12 19,2±0,91 11,1+0,82 6,3+0,5
Авторы
Даты
1992-12-30—Публикация
1990-12-10—Подача