Изобретение относится к области ферментативного анализа и может быть использовано в клинических исследованиях при диагностике атеросклероза, диабета, мочекаменной болезни, функциональных расстройств печени и некоторых инфекционных заболеваний.
Известен также способ определения холестерина, основанный на измерении скорости выделения пероксида водорода. Определение холестерина данным способом, который по своей сути наиболее близок к заявляемому изобретению, выполняется следующим образом. Аликвота исследуемого образца, например сыворотки крови, вносится в измерительную кювету спектрофотометра, содержащую реакционную смесь следующего состава: Буферная смесь 0,1 М, рН 5-9 Субстраты пероксидазы Соли желчных кислот 1-20 мМ, Неионные детергенты - 0,1-10 г/л Холестеринэстераза 100 - 30000 ед/л Холестериноксидаза 100 - 30000 ед/л
Пероксидаза2500 ед/л. Далее проводят регистрацию изменения оптической плотности при температуре 20- 40°С в течение 2-15 мин.
Недостатки рассматриваемого способа определения холестерина заключаются в следующем.
Оптимальные условия проведения реакций гидролиза и окисления не идентичны (не совпадают оптимум рН, температурный оптимум, концентрации детергентов), что приводит к использованию больших количеств ферментов.
Проведение определения холестерина рассматриваемым способом основано на одновременном проведении 3-х последовательных реакций. Исходно в исследуемых образцах содержится как этерифицирован- ный, так и неэтерифицированный холестерин, причем соотношение .этих форм холестерина может меняться в зависимости отсыворотки. Кроме того, скорость гидролиза этерифицированного холестерина холе- стеринэстеразой зависит от длины и
ел
С
vj
00
00
4
о VJ
степени насыщенности остатка жирной кислоты. Поэтому начальная скорость образования пероксида водорода зависит не только от общей концентрации холестерина, но и от соотношения разных форм холестерина в образце, что приводит к снижению точности определения.
Целью изобретения является повышение точности определения.
Поставленная цель достигается предложенным способом, заключающимся в том, что исследуемую пробу добавляют в водную среду инкубации состава: не менее 0,01 м/л буфера с рН 6,5-8,0; не менее 5 г/л холево- кислого натрия и не менее 10 ед/л холесте- ринэстеразы, инкубируют не менее 2 мин при 25-55°С,после чего аликвоту инкубационной смеси вносят в измерительную кювету, содержащую не менее 0,01 м/л при рН 8,0-8,6, не менее 0,003 ед/л пероксидазы, не менее 0,5 ед/л холестериноксидазы, не менее 0,1 г/л п-йодфенола и не менее 0,1 г/л люминола, с последующей регистрацией скорости образования пероксида водорода хемилюминесцентным методом.
Предложенный способ отличается от известного порядком проведения операций, а именно, разделением стадии гидролиза и экстракции со стадией окисления, что дает возможность осуществлять гидролиз в оптимальных условиях при температуре 25- 55°С не менее 2 мин, соотношением реагентов в гидролизующей и окисляющей смесях, а также тем, что регистрация скорости образования пероксида водорода осуществляется хемилюминесцентным методом.
Указанные отличительные признаки позволяют повысить чувствительность определения.
Пример 1. К 0,02 мл сыворотки крови добавили 1,8 мл гидролизующей смеси (смесь 1 : 0,1 М трис-НС., 15,0 г/л холево- кислого натрия, 0,05 ед/мл холестеринэсте- разы, рН 7,2). После перемешивания инкубировали 20 минут. Затем из полученного раствора отбирали 0,1 мл и добавляли в измерительную кювету люминометра LKB 1250, доводили до объема 1,0 мл смесью 2 (смесь 2: буфер 0,1 М трис-HCI, рН 8,2, содержащий 3,0 г/л холевокислого натрия, 0,5 ед пероксидазы, 0,05 ед холестериноксидазы, 0,1 г/л п-иодфенола, 0,1 г/л люминола). Перемешивали и через одну минуту фиксировали интенсивность люминесценции.
Пример 2. Условия измерений те же, что и в примере 1, за исключением того, что изменяли концентрацию пероксидазы. данные, приведенные в таблице 2, получены
для стандартной сыворотки с концентрацией холестерина 6,1 мкМ.
Из данных, приведенных в табл. 2, сле- 5 дует, что оптимальными концентрациями пероксидазы.при анализе являются концентрации не менее 0,003 ед/л.
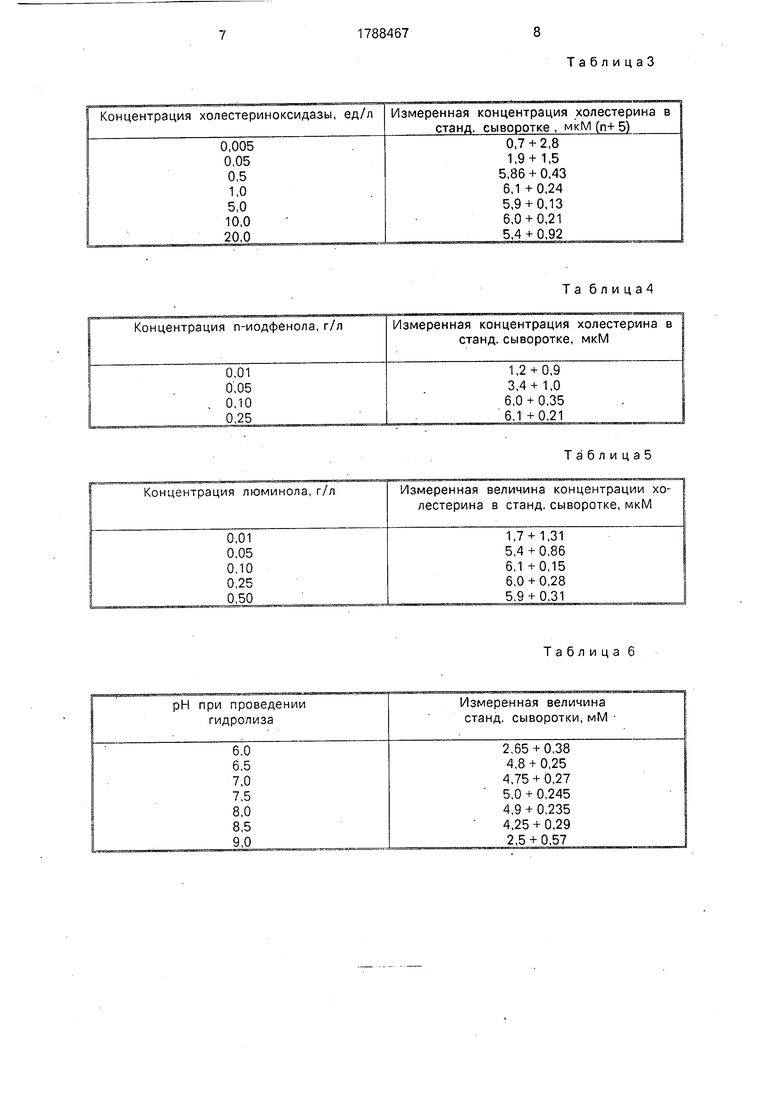
Пример 3. Условия измерения те же, что и в примере 1, за исключением того, что 10 изменяли концентрацию холестериноксидазы. Результаты измерений приведены в таблице 3 для стандартной сыворотки с концентрацией 6,1 мкМ.
Из данных, приведенных в табл. 3, сле- 15 дует, что оптимальными являются концентрации холестериноксидазы не менее 0,5 ед/л.
Пример 4. Условия измерений те же, что в примере 1, за исключением того, что 20 изменяютконцентрацию п-йодфенола. Данные приведены в табл. 4.
Из данных, приведенных в табл. 4, следует, что оптимальной концентрацией п- йод фенола является концентрация не менее 5 0,1 г/л.
Пример 5. Условия измерения те же, что в примере Т, за исключением того, что изменяют концентрацию люминола. Данные представлены в табл. 5. 30 Из данных, приведенных в табл. 5, следует, что оптимальной концентрацией люминола является концентрация не менее 0,1 г/л.
Пример 6. Условия проведения зкс5 перимента аналогичны таковым в примере
1, за исключением того, что при анализе
стандартной сыворотки (5 мМ) используют
различные значения рН при проведении
первой стадии реакции гидролиза. Резуль0 тэты измерений приведены в табл. 6.
Из полученных данных следует, что оптимальные значения рН для проведения реакции гидролиза составляют 6,5-8,0.
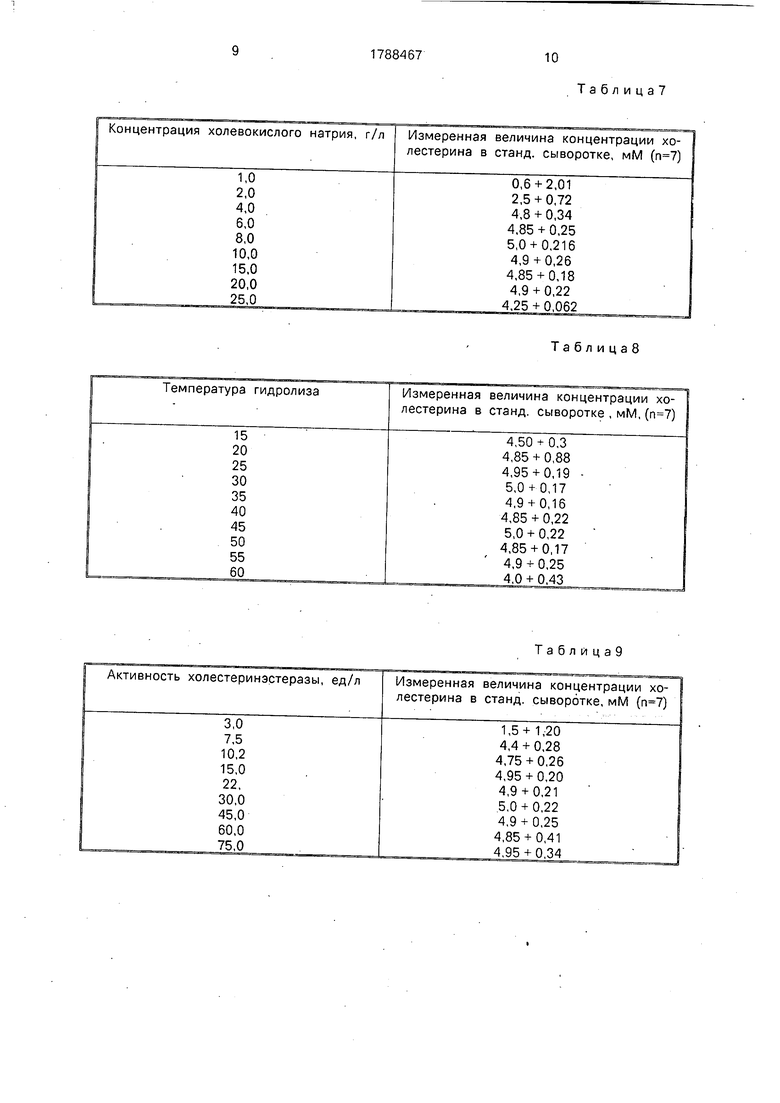
Пример 7. Условия эксперимента 5 аналогичны условиям в примере 1, за исключением того, что используют различные кон- центрации холевокислого натрия в гидролизующей смеси. Результаты измерений приведены в табл. 7.
0 На основании данных, приведенных в табл. 3, оптимальная концентрация холевокислого натрия в гидролизующей смеси составляет 5-20 г/л.
Пример 8. Условия проведения экс- 5 перимента аналогичны таковым в примере 1, за исключением того, что изменяют температуру, при которой проводится гидролиз (табл. 8).
Из данных, приведенных в табл. 8 следует, что полный гидролиз этерифицирован- ного холестерина достигается при
температуре 25-55LlC при концентрации хо- лестеринэстеразы из поджелудочной железы в гидролизующей смеси 2 г/л (активность холестеринэстеразы 30 ед/л).
Пример 9. Условия эксперимента те же, что в примере 1, за исключением того, что изменяют концентрацию холестеринэстеразы в смеси. Данные представлены в табл.9,
На основании данных, приведенных в табл. 9, оптимальная концентрация холестеринэстеразы составляет не менее 10 ед/л при температуре и времени гидролиза 10мин.
Формула изобретения
Способ определения холестерина, включающий инкубацию исследуемой пробы в среде, содержащей буфер, субстрат пероксидазы, соль желчных кислот, холесте- ринэстеразу, холестериноксидазу и пероксидазу и последующую регистрацию скорости образования перекиси водорода, отличающийся тем, что, с целью повышения точности способа, исследуемую пробу добавляют в водную среду инкубации, содержащую буфер с рН 6,5-8,0 в концентрации не менее 0,01 М, холевокислый натрий в концентрации не менее 5 г/л, холестеринэ- стеразу не менее 10 ед/л, инкубируют не менее 2 мин при 25-55°С, затем аликвоту инкубационной смеси вносят в измерительную кювету, содержащую буфер с рН 8,0-8,6 в концентрации не менее 0,01 М, холевокислый натрий в концентрации не менее 1 г/л, пероксидазу не менее 3 ед/л, холестериноксидазу не менее 0,5 ед/л, п-иодфенол в концентрации не менее 0,1 г/л и люминол в концентрации не менее 0,1 г/л, а регистрацию проводят путем измерения хемилю- минесценции.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения холестерина | 1990 |
|
SU1788466A1 |
| Реактив для определения общего холестерина в сыворотке крови | 1974 |
|
SU717994A3 |
| СПОСОБ, РЕАГЕНТ И НАБОР ДЛЯ ОПРЕДЕЛЕНИЯ ХОЛЕСТЕРИНА В ОСТАТОЧНО-ПОДОБНЫХ ЧАСТИЦАХ | 2006 |
|
RU2403577C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТКАНЕВОГО ХОЛЕСТЕРИНА КОЖИ | 1997 |
|
RU2130189C1 |
| Способ определения общего холестерина в сыворотке крови | 1974 |
|
SU1168103A3 |
| Способ получения холестериноксидазы | 1989 |
|
SU1678831A1 |
| Способ получения фосфолипидного носителя холестерина | 1986 |
|
SU1690769A1 |
| Реактив для ферментативного определения холестерина | 1974 |
|
SU613731A3 |
| Способ определения свободного связанного холестерина в биологических жидкостях | 1973 |
|
SU637097A3 |
| СПОСОБ ДИАГНОСТИКИ ДИАБЕТИЧЕСКОЙ РЕТИНОПАТИИ | 2005 |
|
RU2304786C2 |
Использование: медицина, ферментативный анализ. Цель изобретения - повышение точности способа. Сущность изобретения: процесс осуществляют в две стадии, на первой из которых ведут обработку образца при температуре 20-55°С в течение 2-20 мин реагентом, содержащим холесте- ринэстеразу, буферную смесь и детергент, при этом происходит гидролиз этерифици- рованного холестерина. На второй стадии осуществляют окисление холестерина с помощью холестериноксидазы и регистрацию скорости образования пероксида водорода. Регистрацию ведут хемилюминесцент- ным методом. 9 табл.
Концентрация пероксидазы, ед/л
0,001
0,003
0,01
1,00
10,0
25
Т а б л и ц а 1
Таблица2
Измеренная концентрация холестерина в станд. сыворотке, мкМ
1,2 + 0,70 6.0 + 0,35 5,9 + 0,27 6,1 +0,23 5,95 + 0.33
Концентрация холестериноксидазы, ед/л
0,005
0,05
0,5
5,0
10,0
20,0
Концентрация люминола, г/л
0,01
0,05
0,10
0,25
0,50
рН при проведении гидролиза
6,0 6,5 7,0 7.5 8,0 8,5 9,0
ТаблицаЗ
Измеренная концентрация холестерина в станд. сыворотке , мкМ (п+ 5)
0,7 + 2,8
1,9 + 1,5
5,86 + 0,43
6,1 +0,24
Та блица4
Таблица5
Измеренная величина концентрации холестерина в станд. сыворотке, мкМ
1,7 + 1,31 5,4 + 0,86 6,1 +0,15 6,0 + 0,28 5,9 + 0,31
Таблица 6
Измеренная величина станд. сыворотки, мМ
2,65 + 0,38 4,8 + 0,25 4,75 + 0,27 5,0 + 0,245 4,9 + 0,235 4,25 + 0,29 2,5 + 0,57
Концентрация холевокислого натрия, г/л
2,0
4,0
6,0
8,0
10,0
15,0
20,0
25,0
Температура гидролиза
15
20
25
30
35
40
45
50
55
60
Активность холестеринэстеразы, ед/л
3,0
7,5
10,2
15,0
22,
30,0
45,0
60,0
75,0
Таблица
Измеренная величина концентрации холестерина в станд. сыворотке, мМ ()
0,6 + 2,01 2,5 + 0,72 4,8 + 0,34
4,85 + 0,25
5,0 + 0,216 4,9 + 0,26
4,85 + 0,18 4,9 + 0,22
4,25 + 0,062
ТаблицаЗ
Измеренная величина концентрации холестерина в станд. сыворотке , мМ, ()
4,50 + 0,3
4,85 + 0,88
4,95 + 0,19
5,0+0,17
4,9 + 0,16
4,85 + 0,22
5,0 + 0,22
4,85 + 0,17
4,9 + 0,25
4,0 + 0,43
ТаблицаЭ
Измеренная величина концентрации холестерина в станд. сыворотке, мМ ()
1,5+ 1,20
4,4 + 0,28
4,75 + 0,26
4,95 + 0,20

| УСТРОЙСТВО ДЛЯ АВТОМАТИЧЕСКОГО СОСТАВЛЕНИЯ ПРЯМОГО КАНАЛА СВЯЗИ | 0 |
|
SU265933A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
1993-01-15—Публикация
1990-05-22—Подача