спектр: М+ 191 (30), 190 (8), 174 (3), 173 (2,5), 162 (2,5), 146 (9), 114 (5), 105 (100), 99 (20), 86 (7,5), 85 (10), 77 (50), 70 (70), 57 (15), 56 (25), 55(15); спектр ПМР: 1.76-2.16 (ЗН, м, 3-Н и 4-Н), 3.40-3.83 (4Н, м, 2-Н и 5-Н), I - -46.56° (С 1.89, зтанол). Хроматографиче- ская подвижность на еилйкагеле Merk Kieseigei 60 F254 Art. 5554 - Rf - 0.26.
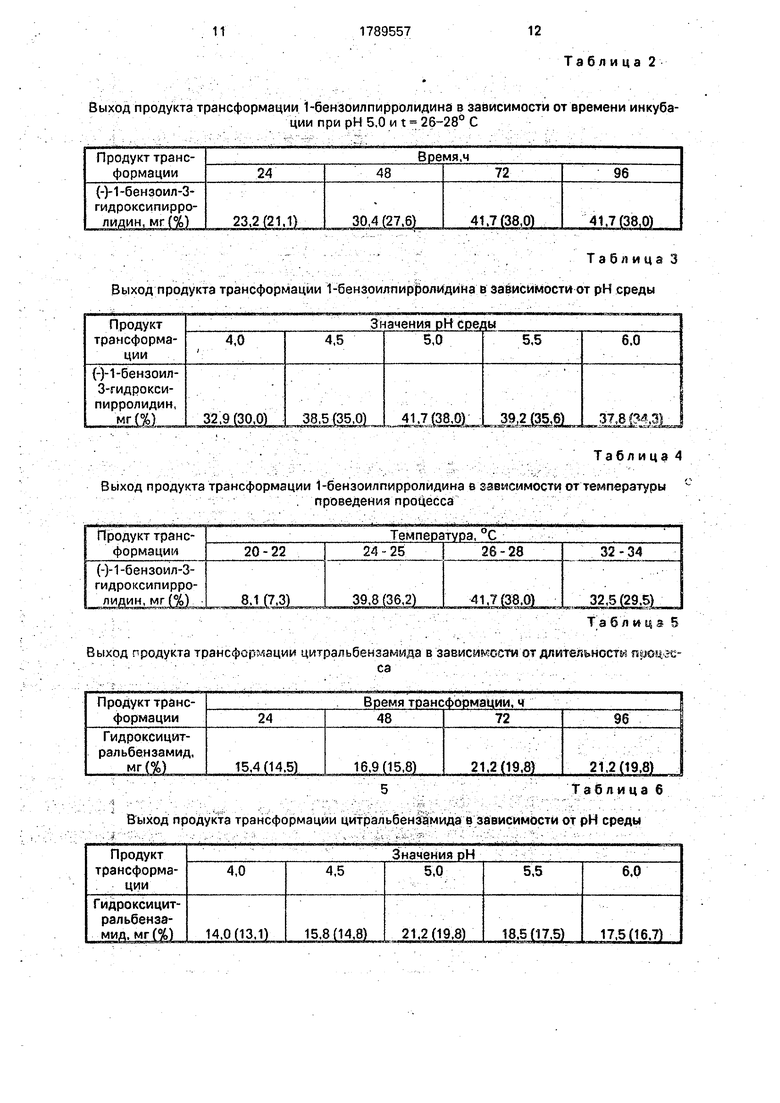
Выход продукта трансформации 1-бен- зоилгтирролидина в зависимости от времени инкубации при рН 5,0 и t 26-28° С.
Из табл. 2 видно, что реакция полностью проходит за 3 сут и увеличение времени трансформации до 4 сут не приводит к увеличению выхода продуктов трансформаций,
Пример 2. Реакцию е 1-бензоилпир- ролидмном проводят аналогично примеру 1 при t 26-28° С в течение 3 сут, но при разных значениях рН, как показано в табл. 3
Из табл. 3 видно, что увеличение или уменьшение рН приводит к увеличению выхода продуктов, и наилучший выход мы имеем при рН 5,0.
. Прим е-р 3. Реакцию с 1-бензоилпир- ролидином проводят аналогично примеру 1 при рН 0,5 в течение 3 сут, но при разных температурах, как показано в табл. 4.
Из табл. 4 видно, что процесс микробиологического окисления протекает при темг пературе 20-34° С, но оптимальным является интервал 26-28° С, наиболее благоприятный для роста гриба и работы фер ментных систем.
Пример 4. Реакцию с дитральбен- замидом проводят аналогично примеру 1 при рН 5,0 и t 26-28° С, но при разном времени трансформации, как показано в табл. 5.
Из табл, 5 видно, что из 100 мг цитраль- бензамида за 3 сут трансформации получают21,2 мг (19,8 %) гидроксицйтральбензамида и увеличение
времени трансформации до 4 сут не приводит к увеличению выхода продукта. Хрома- тографическаяподвижность гидроксицйтральбензамида на еилйкагеле Merk, Klesefgel 60 F254. Art. 5554 - R f -0,40
Масс-спектр: М 273 (25), 232 (40), 214 (15), 187 (100). 152 (55). 134 (9), 77 (50).
П р и м е р 5. Реакцию с цитральбенза- мидом проводят аналогично примеру Т при t 26-28° С в течение 3 сут, но при разных
значениях рН, как показано в табл. 6.
Из табл. 6 видно, что увеличение или уменьшение рН не приводит к увеличению выхода продукта, и наибольший выход мы имеем при рА 5,0.
Пример 6. Реакцию с цитральбен- замидом проводят аналогично примеру 1 при рН 5,0, в течение 3 сут, но при разных значениях темггературы. как показано в табл. 7. .
Из табл. 7 видно, что процесс микробиологического окисления протекает от 20 до 34° С, но оптимальным является интервал 26-28° С, наиболее благоприятный для роста гриба и работы ферментных систем.
:-.-.. :.-,::,, . -..;-: ;;: .,,-
Выделен новый гриб CunnlnghameHa verticflfata ВКПМ F-430. Штамм способен стереоселехтивно гидроксилмровать 1- бёнзоилпирролидйн, что ранее не было отмечено у других грибов; кроме того, он способен трансформировать соединения терпеновогО ряда, в частности цитраль- бензамид, что расширяет область его прм- менения;




| название | год | авторы | номер документа |
|---|---|---|---|
| Штамм гриба BeaUVeRIa ваSSIаNа BaLS в качестве трансформатора для гидроксилирования 1-бензоилпиперидина и 1-бензоиламино-3,7-диметилоктадиена-2,6 | 1990 |
|
SU1822886A1 |
| Способ получения (-)-(1-оксиэтил) пиридинов | 1986 |
|
SU1364621A1 |
| Способ получения оптически активного (-) 2-метил-5-(1-оксиэтил)пиридина | 1973 |
|
SU615652A1 |
| Штамм гриба ЕRемотнесIUт аSнвYI - продуцент эфирного масла | 1987 |
|
SU1454845A1 |
| Способ получения замещенных 2-окси-3-/1-(1н-имидазол-4-ил)алкил/-бензамидов или их нетоксичных фармацевтически приемлемых солей кислот | 1990 |
|
SU1836353A3 |
| СПОСОБ ПОЛУЧЕНИЯ 1 -> 3, 1 -> 6-БЕТА-D-ГЛЮКАНА, ОБЛАДАЮЩЕГО ИММУНОСТИМУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1993 |
|
RU2095417C1 |
| СПОСОБ ЗАЩИТЫ ТЕХНИЧЕСКИХ МАСЕЛ ОТ ВОЗДЕЙСТВИЯ МИКРОМИЦЕТОВ | 1992 |
|
RU2074250C1 |
| КОНСЕРВАЦИОННЫЙ СМАЗОЧНЫЙ МАТЕРИАЛ | 1992 |
|
RU2029779C1 |
| Способ получения 1-(2 @ , 4 @ , 6 @ -трихлорфенил)-3-(3-аминобензамидо)-пиразолона-5 | 1988 |
|
SU1505935A1 |
| СПОСОБ ТВЕРДОФАЗНОЙ ФЕРМЕНТАЦИИ ТРАВЯНОГО ЖОМА ЛЮЦЕРНЫ | 1991 |
|
RU2048518C1 |

cb о р му л а и з о б р е t е н и я Штамм гриба Cunnighamella vertlcUlata В КПМ F-430 - трансформатор для гйдроксилиррвания 1-бензоилпирролидина и 1- бензоиламино-3, 7-диметилоктадиена-2,
6;:- .:.. .... . .,...-.
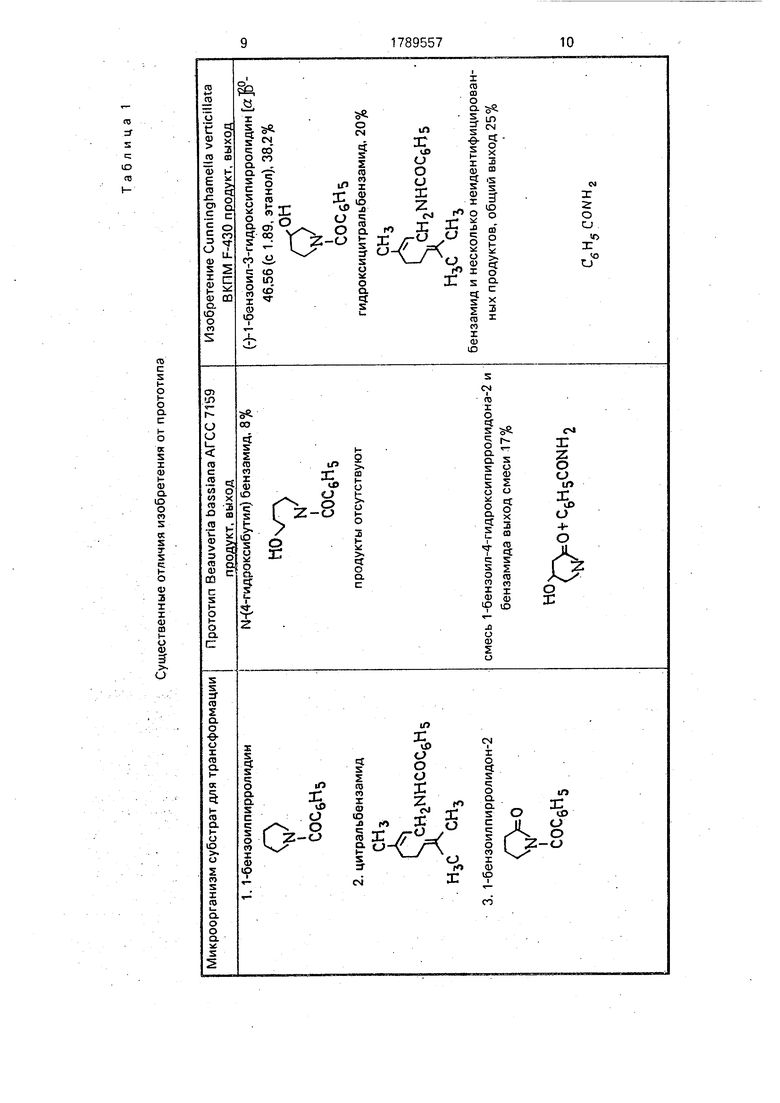
Микроорганизм субстрат для трансформации
9
СОС6Н5
Si
4CH2NHCOC6H5
НчС СН,
4i
СОС6Н;
Существенные отличия изобретения от прототипа
Прототип Beauveria bassiana АГСС 7159 продукт, выход
Изобретение Cunninghamella verticillata ВКПМ F-430 продукт, выход
М-(4-гидроксибутил) бензамид. 8%
HOv-y N7 СОС6Н5
продукты отсутствуют
смесь 1-бензоил-4-гидроксипирролидона-2 и бензамида выход смеси 17%
(-)-1-бензоил-3-гидроксипирролидин - 46,56 (с 1.89, этанол), 38,2%
V
СОС6Н5 гидроксицитральбензамид, 20%
СН3
1
CH2NHCOC6H5
НЪС СНЪ. бензамид и несколько неидентифицированных продуктов, общий выход 25%
СО
-J
оо со ел ел
-д
Q O C6H5CONH2
C6H5CONH,
Выход продукта трансформации 1-бензоилпирролидина в зависимости от времени инкубации при рН 5,0 и t 26-28° С
Т а б п и ц а 3 Выход продукта трансформации 1-бензоияпирр лмдина в зависимости от рН среды
Таблица 4
Выход продукта трансформации 1-бензоилпирролидина в зависимости от температуры
. проведения процесса
;. ; . - . . : . : Та б л и ц а 5
Выход продукта трансформации цитральбензаммда в зависимости от длительности пуоц-эс- ; - - са .. ..
5Таблица 6 Выход продукта трансформации цитральбензамида в зависимости от рН среды
Таблица 2
Таблица Выход продукта трансформации цитральбензамида в зависимости от температуры
Авторы
Даты
1993-01-23—Публикация
1990-11-15—Подача