Изобретение относится к способу получения нового комплексного соединения платины, обладающего противоопухолевой активностью.
Цель изобретения - получение нового Платийоорганического комплексного соединения с более высокой активностью и более низкой токсичностью по сравнению с известными противоопухолевыми препаратами.
Способ получения соединения PtOH- ДН К заключается в том, что предварительно нагретые до температуры плавления н-ДНК водные растворы н-ДНК и цис-дихлордиамминплатины (II) (ДДП). гидролизованной до заданной степени превращения, смешивают при молярном соотношении Pt:P 1,5:1 и термостатируют при той же температуре до окончания реакции.
Температуру плавления н-ДНК определяют из спектрофотометрической кривой плавления.
Нативную ДНК растворяют в воде при комнатной температуре и нагревают в термостате.
Гидролиз ДДП проводят в воде, соблюдая режим нагревания, обеспечивающий заЯ
v|
ГО ГО
данную степень гидролиза, которую контролируют по электронному спектру в области 250-350 нм, характеризуемому максимумом поглощения, А макс, изменяющимся в интервале 273,5-276,7 нм, с ошибкой 0,5 нм и с максимальным молярным коэффициентом экстинкции Емакс 110 ± 10 л-моль см 1.
Окончание взаимодействия н-ДНК и г- ДДП контролируют спектрофотометриче- ски по достижению параметров УФ-спектра поглощения Я макс 265,7 ±0,1 ими ,7 а 10000 ± ЮОл-моль см 1.
Предлагаемое вещество получают в водном растворе или в индивидуальном состоянии. В последнем случае образующийся в результате реакции аммоний хлористый и избыток воды удаляют лио- фильной сушкой.
П р и м е р 1. На спектрофотометре Specord M 40 с использованием держателя кюветы, снабженного блоком управления температурой, и программы измерений, обеспечивающей линейное возрастание температуры, определяют Тпл н-ДНК. Регистрируют экстинкцию как функцию температуры в диапазоне 60-95°С при градиенте температуры 1°С/мин. Применяемая для получения предла гаемого соединения н- ДНК имеет ТПл - 78.0 ± 0,5°С.
Растворы 405 мг цис-РгС 2(МНз)2 в 250 мл воды (концентрация 1620 мкг/мл) и 300 мг н-ДНК в 250 мл воды (концентрация 1200 мкг/мл), приготовленные при комнатной температуре, каждый в отдельности, помещают в термостат и равномерно повышают температуру до 78,0 ±0,5°С со скоростью 1°С/мин как при плавлении н-ДНК. Реагенты смешивают в молярном соотношении Pt:P 1,5:1, тщательно перемешивают и те.рмостатируют при той же температуре в .течение 15 мин.
П р и м е р 2, Опыт проводят как в примере 1, только реакционную смесь подвергают лиофильной сушке по методике изготовления сухой плазмы крови.
Раствор соединения PtOH-ДНК при постоянном вращении охлаждают до -40°С в течение 40 мин, а затем выдерживают при этой температуре 12 ч. После этого температуру повышают до -20°С. образец откачивают в течение 40 «, нагревают до 40°С и снова откачивают 26 ч. Полученные после лиофильной сушки соединения PtOH-ДНК в дальнейшем хранят в закрытой стеклянной посуде в холодильнике или на воздухе. Выход целевого продукта PtOH-ДНК практически соответствует теоретическому.
Для экспериментальной проверки предлагаемого способа получения соединения PtOH-ДНК было проведено 19 опытов, восемь из которых показали положительные результаты. В положительных опытах получен продукт, УФ-спектры которого имеют
параметры, характерные для предлагаемого соединения.
Результаты опытов сведены в табл,1, где приведены характеристики полученных продуктов в зависимости от способа их получения.
Способы получения охарактеризованы следующими параметрами: выбором концентрации исходных растворов ДДП и н- ДНК, степенью гидролиза ДДП, молярным
соотношением Pt:P, временем и температурой проведения реакции.
Из данных табл. 1 (опыты 1-4) видно, что выбор исходной концентрации ДДП в интервале 2520-1200 мкг/мл позволяет получить продукт с параметрами, характерными для предлагаемого соединения PtOH-ДНК. Снижение исходной концентрации ДДП приводит к отрицательному результату (опыты 5-7). Из зависимости
А макс растворов ДДП от концентрации препарата следует, что при концентрации меньшей, чем 1080 мкг/мл, резко изменяется степень гидролиза ДДП, что и не позволяет получить целевое соединение платины с
ДНК. Таким образом, интервал исходной концентрации ДДП обусловлен тем, что максимальная концентрация ДДП ограничена ее растворимостью в воде при 20°С, а минимальная - величиной, ниже которой
резко изменяется степень гидролиза ДДП. Эта величина равна 1080 мкг/мл.
Выбор концентрации н-ДНК обусловлен выбором концентрации ДДП и необходимостью соблюдать молярное
соотношение Pt:P 1,5:1. Отклонение от соотношения Pt:P 1,5:1 не позволяет получить целевое соединение с вышеуказанными параметрами (опыты 8 и 9).
Результаты о.пытбв 10-13, приведенные
в табл. 1, указывают, что взаимодействие реагентов протекает быстро и заканчивается за время, не превышающее 5 мин. Увеличение времени термостатирования реакционной смеси до 30 мин не влияет на параметры
продукта реакции.
Температура проведения реакции существенно влияет на такой параметр продукта реакции как Е265.7. На это указывают результаты опытов 14-19. Из зависимости
Е265.7 от температуры видно, что для получения предлагаемого соединения PtOH-ДНК термостатирование реакционной смеси надо вести при 78,0 ± 0,5°С. Отклонение от температуры больше, чем в указанном пределе, не дает возможности получить продукт с необходимыми параметрами УФ-спектра.
Опытами установлено, что заданная степень гидролиза ДДП обеспечивается нагреванием водного раствора ДДП в определенном режиме.
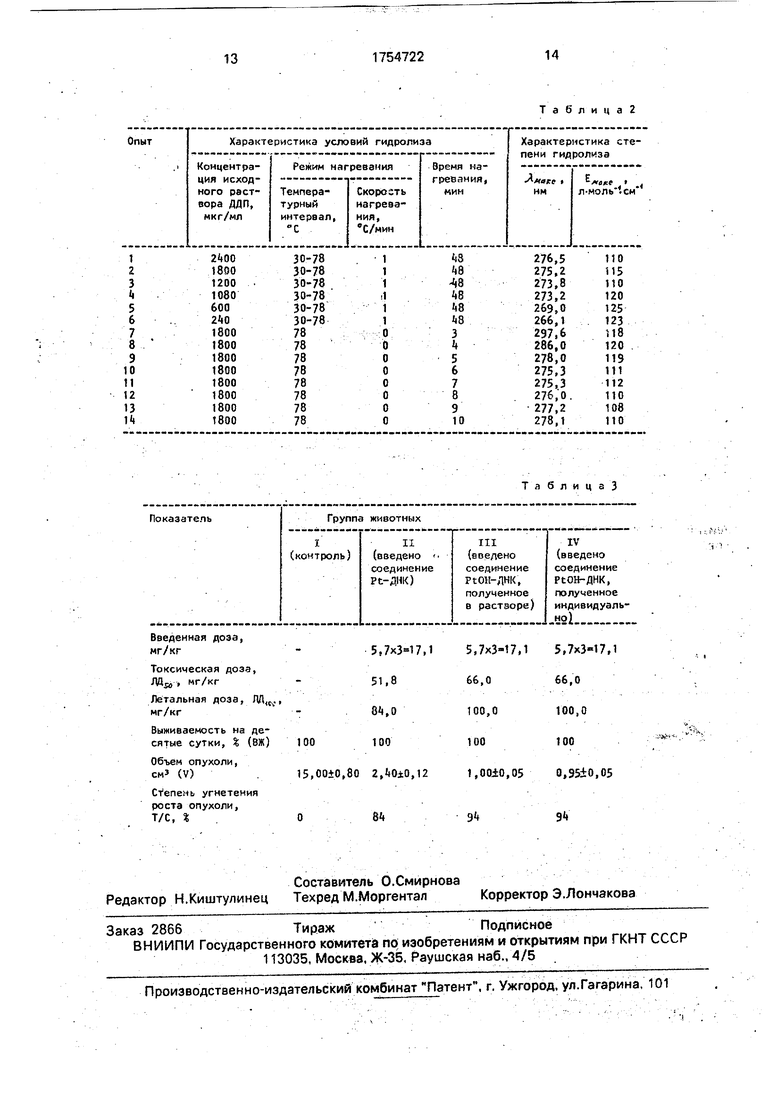
В табл.2 приведены характеристики способа гидролиза и полученного в результате продукта гидролиза ДДП.
Гидролиз проводили при разных исходных концентрациях ДДП и в разных режимах нагревания. В первых шести опытах навески ДДП растворяли в воде при 30°С и раствор нагревали до 78,0 ± 0,5°С в термостате в том же режиме, как и нагревали н-ДНК, т.е. со скоростью 1°С/мин в течение 48 мин. Результаты этих опытов показывают, что указанный режим нагревания обеспечивает получение продукта с заданными А макс и Емакс для растворов с исходными концентрациями ДДП 2400, 1800, 1200 и 1080 мкг/мл (опыты 1-4). Понижение исходной концентрации ДДП (опыты 5 и 6) не позволяет достигнуть заданных параметров УФ-спектра.
В опытах 7-14 навески ДДП растворяли в воде, нагретой до 78,0 ± 0,5°С, и полученные растворы выдерживали в термостате при этой температуре в течение 3-10 мин. Из результатов, приведенных в табл 2, и зависимости Я макс от времени видно, что необходимые параметры спектров, соответствующие заданному интервалу степени гидролиза ДДП, также достигаются, если ДДП растворять в горячей воде (температура 78,0 ± 0,5°С) и раствор термостати- ровать в течение 5-9 мин.
Приведенные выше данные позволяют заключить, что смешение предварительно нагретых до температуры плавления н-ДНК водных растворов н-ДНК и гидролизован- ной до заданной степени цис-дихлородиам- минплатины (II) при молярном соотношении 1,5:1 и термостатировании смеси реагентов при этой температуре в течение времени, необходимого для окончания реакции, позволяет получить соединение, характеризуемое формулой
{ Pt pH)CI(NH3XH20MPtCI(NH3XH20)
х Ц -ДНК,
где ± 100; / -ДНКНСзэН ОзМбР, с описанными физико-химическими свойствами. Отклонение от вышеуказанных параметров способа получения: интервала исходных концентраций ДДП и н-ДНК, степени гидролиза ДДП, соотношения реагентов и температуры проведения реакции, не
дает возможности получить предлагаемое соединение с указанными характеристиками,
Предлагаемое соединение РЮН-ДНК как индивидуальный препарат представляет собой мелкокристаллический порошок желтого цвета. Оно устойчиво в водных растворах и в твердом виде, способно длительное время храниться на воздухе при комнатной температуре и в холодильнике без изменения свойств. Состав и строение соединения РЮН-ДНК определены на основе химико-аналитических и физико-химических исследований растворов и твердых образцов.
Элементный анализ твердого образца подтверждает состав синтезированного целевого соединения РЮН-ДНК.
Найдено, %: Pt 38,97: CI 7,38; С 15,53; N 9,83; Н 7,17; Р 2,98.
Вычислено, %; Pt 38,19; CI 6,95; С 15,27; N 9,59; Н 4,05; Р 2,97.
Измеренная вискозиметрическим методом молекулярная масса соединения К составляет 6,0 106 дальтон. Исходя из молекулярной массы соединения РЮН-ДНК и массы мономерной единиц этого полимера, имеющей эмпирическую формулу
(OH)CI)NH3XH20)HPtCt(NH3XH20)2} x
X (C39H51032N15P4).
можно рассчитать среднестатистическую
величину п в соединении. Она равна 2000 ± 100. Следовательно, в среднем на 2000 нуклеотидных квартетов ДНК, состоящих из пар аденин-тимин, гуанин-цитоэин, приходится примерно 4000 комплексных частиц Pt(OH)CI(NH3XH20)l и 8000 комплексных частиц PtC1)NH3XH2O)f.
УФ-спектр поглощения соединения РЮН-ДНК, полученного в водном растворе и выделенного индивидуально, характеризуется максимальным поглощением при 265,7 нм, а свободная н-ДНК максимально поглощает свет при 258,0 нм. Молярный коэффициент поглощения РЮН-ДНК, рассчитанный на моль нуклеотида, Езет.з в 10000
л (у свободной н-ДНК Ease 7000 л моль -см ). Длинноволновое смещение максимума поглощения, ДА макс, на 7,7 нм у соединения РЮН-ДНК по сравнению с н-ДНК говорит об образовании ковалентных связей между атомами платины (II) и донорными атомами азотистых оснований биомакромолекулы. Длинноволновое смещение s УФ-спектре соединения Pt-ДНК, ДА макс, составляет 10,8 нм. Более низкая
величина АЯ мэкс для PtOH-ДНК по сравнению с АЛ макс для Pt-ДНК указывает, что ковалентные связи между металлом и основаниями ДНК в предлагаемом соединении в среднем слабее, чем в соединении Pt-ДНК, Повышение интенсивности поглощения для PtOH-ДНК, составляющее 30%, говорит о том, что присоединение металла к ДНК вызывает сильные конформационные изменения ее двухцепочечной структуры, УФ-спектр соединения PtOH-ДНК, полученного в растворе, и его идентичность спектру раствора, приготовленного из твердого образца, свидетельствует об одинаковой химической природе соединения PtOH-ДНК, образующегося в растворе и выделенного в твердом виде. Об этом же говорят одинаковые результаты биологических испытаний,
Растворимость кристаллического образца PtOH-ДНК в воде при 20°С, составля- ющая 0,0075% (75 мкг/мл), показывает, что максимально достижимая концентрация PtOH-ДНК при растворении твердого соединения в 35 раз ниже максимально достижимой концентрации соединения, полученного в растворе. Низкая растворимость индивидуального вещества свидетельствует о его необратимой десолызатации при выделении в кристаллическом виде, что обуславливает необходи- мость использовать его в виде суспензии при биологических испытаниях.
Водный раствор РЮН-ДНК практически не проводит электрический ток, что свидетельствует о том, что при растворении соединение не подвергается электролитической диссоциации.
Изменение в ИК-спектрах соединения РЮН-ДНК по сравнению со свободной ДНК свидетельствует о наличии химических свя- зе й между атомами платины (М) и атомами кислорода фосфатных групп, В ИК-спектрах имеются полосы-при 1060 и 1220 , соответствующие валентным колебаниям груп- , полосы в области 1500-1700 , соответствующие валентным колебаниям групп , , азотистых оснований, полосы в области 3100-3700 см , соответствующие валентным колебаниям С-Н, N-H, 0-Н, входящих в состав ДНК и молекул во- ды. Кроме того, при 340 наблюдается валентное колебание Pt-Ci, при 1340 - деформационное колебание координированной олекулы МНз, при 3295 - валентное колебание координированной гидроксильной группы.
По данным термогравиметрии соединение PtOH-ДНК теряет молекулы воды только при нагревании до 200°С. Высокая
температура удаления молекул воды свидетельствует об их прочном связывании а соединении.
Данные элементного анализа, вискозиметрии, кондуктометрии, УФ- и ИК-спект- ров поглощения подтверждают, что синтезированное соединение действительно высокомолекулярное вещество - поли {бис гидроксохлороамминак вал патина (М)тетракис хлороамминдиакваплатина О )} / -дезоксирибонуклеат формулы
{ PtCKOHXNH3XH20)b(PtCI(NH3XH20)2j4K
-р-ДНК где п 2000 ± 100.
В табл.3 представлены результаты испытаний токсичности и противоопухолевой активности известного соединения Pt-ДНК и предлагаемого соединения PtOH-ДНК, полученного в растворе и выделенного в индивидуальном состоянии. Опыты проводили на мышах и крысах обоего пола разведения питомника Столбовая.
Токсичность изучали на группах животных из половозрелых нелинейных мышей массой 30,0 ± 2,0 г, прошедших карантин 20 дней (в каждой группе по 10 животных). Препараты вводили трехкратно внутрибрюшмн- но с интервалами в 2 ч в виде водного раствора или водной суспензии объемом 0,5 мя. Суммарные дозы составляли 34,0; 68,0 и 84,0 мг/кг, Количество животных, погибших в каждой группе, отмеизли через 24-48 ч после введения препаратов. Расчет токсической дозы, ДJlgo, проводили по методике, летальную дозу, ЛДюо, определяли экспериментально,
Установлено, что для Pt-Д Н К Л Дзо 51,8 мг/кг, ЛДюо 84,0 мг/кг, для предлагаемого соединения PtOH-ДНК ЛДзо 66,0 мг/кг, ЛДюо 100 мг/кг независимо от формы введения, Из сравнения приведенных величин следует, что токсичность РхОН-ДНК ниже, чем токсичность соединения Pt-ДНК.
Согласно гистологическим исследованиям гибель животных, получивших токсические дозы препаратов, обусловлена их энтеротоксичностью.
Противоопухолевую активность каждого из препаратов оценивали из экспериментов, проведенных на четырех группах животных (в каждой группе по 10 животных). Опыты проводили дважды.
Белым беспородным крысам массой 150-200 г под кожу бедра трансппантирова- ли 2 108-2 10 клеток перевивного штамма лейкоза Швеца. Животные I группы служили для контроля. Животные III и IV групп получали соединения Pt-ДНК и PtOHДНК в растворе или в суспензии соответственно. Препараты вводили внутрибрюшин- но трехкратно на 4-6 сут после трансплантации опухоли, второй и третий раз с интервалом в 1 су г Суммарные дозы составляли 17,1 мг/кг.
Противоопухолевую активность оценивали по выживаемости животных (ВЖ. %) на десятые сутки после перевивки опухоли, по объему опухопи (V, см и степени угнетения роста опухоли (Т/С, %), Расчеты производили по формулам
ВЖ(%) ,
где А - число животных на десятые сутки после трансплантации опухоли;
N - число животных в данной группе;
V (см3) 4/3 гс R3,
, m i + m 2 + гп з R
где mi, ГП2 и тз - три взаимно перпендикулярных измерения опухолевого узла.
V кон V оп
Т/С(%)100.
V кон
где VKOH. и Von. - объем опухоли в контрольной группе и в опытной соответственно.
Результаты экспериментов обрабатывали статистически, Вероятнее пая ошибка ,05
Анализ данных, представленных в (абл.З, показывает, что введение соединения PtOH-Д IK обеспечивает 100%-ную выживаемость животных. Вместе с тем, оно тормозит рост опухоли на 94% по сравнению с контролем. Сравнительный анализ данных, приведенных в табл.3, позволяет заключить, что предлагаемое соединение PtOH-ДНК обладает лучшей эффективностью, чем известное соединение Pt-ДНК, так как, не уступая ему по такому показателю как выживаемость животных, превосходит его по уровню степени угнетения роста опухоли на 10%. Кроме того, оно менее токсично, чем известное вещество.
Таким образом, создание нового высокомолекулярного соединеьия платины с ДНК привело к получению вещества с ценными свойс вами: противоопухолевой активностью при малой токсичности. По этим
показателям предлагаемое соединение выгодно отличается от соединения Pt-ДНК, превосходя или будучи сопоставимо с ним по показателям физиологической активности. Таксой комплекс свойств делает предлэгаемое соединение перспективным в качестве основы для создания препаратов, эффективных для лечения злокачественных опухолей.
Дополнительным преимуществом предлагаемого противоопухолевого вещества является обеспечение их возможности продолжить ряд платиносодержаи .их противоопухолевых препаратов и тем самым обеспечить преодоление эффекта привыкания организма к платиновым противоопухолевым средствам.
Формула изобретения Способ получения комплексного соединения платины (И) с н-ДНК, обладающего
противоопухолевой активностью, взаимодействием цис-дихлородиамминплатичу с дезоксмрибонуклеиновой кислотой (выделенной из селезенки крупного рогатого скотз, марки А) в воде при нагревании до
78,0 ± 0,5°С, отличающийся тем, что с целью получения соединения с более высокой активностью и более низкой токсичностью цис-дихлородиамминплатину и ДНК используют в молярном соотношении 1,51
и процесс ведут в течение 15 мин.
Таблица





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения комплексного соединения платины (II) с Н-ДНК, обладающего противоопухолевой активностью | 1988 |
|
SU1813089A3 |
| Способ получения комплексного соединения платины (II) с высокомолекулярной н-ДНК из селезенки крупного рогатого скота марки А, обладающего противоопухолевой активностью | 1988 |
|
SU1685944A1 |
| ЦИС-ХЛОРДИАММИН-1,3-ДИМЕТИЛКСАНТИНПЛАТИНЫ (II) ХЛОРИД ДИГИДРАТ, ПРОЯВЛЯЮЩИЙ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 1990 |
|
SU1790190A1 |
| ЦИС-ХЛОРО-N, -(2' -ТЕТРАГИДРОФУРИЛ) -5-ФТОРУРАЦИЛАТОДИАММИНПЛАТИНА II, ПРОЯВЛЯЮЩАЯ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 1992 |
|
RU2028301C1 |
| КОМПЛЕКСНОЕ СОЕДИНЕНИЕ ЦИС-ДИАММИНОПЛАТИНЫ (П) С СОПОЛИМЕРОМ NA-СОЛИ МАЛЕИНОВОЙ КИСЛОТЫ И 1,4-ДИИЗОПРОПОКСИБУТЕНА-2, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ С ШИРОКИМ ИНТЕРВАЛОМ ТЕРАПЕВТИЧЕСКИХ ДОЗ ПРИ ПОЛНОМ ОТСУТСТВИИ НЕФРОТОКСИЧНОСТИ И ИММУНОДЕПРЕССАНТНОГО ДЕЙСТВИЯ | 1990 |
|
RU2034856C1 |
| ПРОИЗВОДНЫЕ ДИХЛОРИДА ЦИС-ДИАММИНДИИМИДАЗОЛИЛ ПЛАТИНЫ, ПРОЯВЛЯЮЩИЕ АНТИПРОЛИФЕРАТИВНУЮ АКТИВНОСТЬ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1995 |
|
RU2114858C1 |
| КОМПОЗИЦИЯ ДЛЯ ПРИГОТОВЛЕНИЯ ПРОТИВООПУХОЛЕВОГО СРЕДСТВА И СПОСОБ ПРИГОТОВЛЕНИЯ ПРОТИВООПУХОЛЕВОГО СРЕДСТВА НА ЕЕ ОСНОВЕ | 2016 |
|
RU2667128C2 |
| КОМПЛЕКСНОЕ СОЕДИНЕНИЕ ЦИС-ДИАМИНОПЛАТИНЫ (II) С СОПОЛИМЕРОМ NA-СОЛИ МАЛЕИНОВОЙ КИСЛОТЫ И ФУРАНА, ОБЛАДАЮЩЕЕ ИММУНОСТИМУЛИРУЮЩЕЙ И ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ, С ШИРОКИМ ИНТЕРВАЛОМ ТЕРАПЕВТИЧЕСКИХ ДОЗ ПРИ НИЗКОЙ НЕФРОТОКСИЧНОСТИ | 1990 |
|
RU2033998C1 |
| Цис-диамминдихлороаквагидроксоплатина (1У)-сульфат и способ его получения | 1988 |
|
SU1557106A1 |
| Цис-дихлороаквогуанозинплатина ( @ ),моноэтанол,проявляющая антиканцерогенную активность | 1980 |
|
SU886472A1 |
Изобретение касается комплексных соединений платины (2+), в частности получения комплекса соединения платины (2+) с н-ДНК (дезоксирибонуклеиновой кислотой), обладающего противоопухолевой активностью, что может быть использовано в фармацевтической промышленности. Цель - повышение активности и снижение токсичности целевого продукта. Синтез последнего ведут реакцией цис-дихлордиамминплатмны с н-ДНК (выделенной из селезенки крупного рогатого скота, марки А) при их молярном соотношении 1.5:1 и 78 ± 0,5°С в среде воды 
Введенная доза,
ТаблицзЗ
Авторы
Даты
1992-08-15—Публикация
1988-06-30—Подача