ел
с
магния и выпаривают в вакууме. Остаток хроматографируют на 40 г силикагеля с использованием хлороформа в качестве элю- ента. Фракции, содержащие целевое соединение, объединяют и .выпаривают в вакууме с получением 1,30 г 1-/3-/2-фенил- пиразоло/1,5-е/пиридин-3-ил/-акрилоил/- 2-этилпиперидина (транс-изомер) в виде маслоподобного продукта.
Это соединение подвергают конверсии в полуфумарат с получением 0,96 г желтых кристаллов 1- 3-/2-фенилпиразоло/1,5-е/- пиридин-3-ил/-акрилоил -2-этилпипериди нполуфумарата (транс-изомер). Т.пл. 121- 122°С (из смеси н-гексана с диэтиловым эфиром).
ИК-спектр (вазелиновое масло), см : 1705, 1635, 1580. 1530Л510.
ЯМР-спектр(ОМСО-о б)(5, м.д.):0,77(ЗН, т, 7,0 гц), 1,30-1,83 (8Н. м.), 6,66 (1Н, с.), 6,83 (1Н, д., 16.0 гц), 7.00-7.83 (8Н, м.), 8.07 (1Н, д.. 9,0 гц). 8,77 (1.Н, д.. 7,0 гц).
Данные элементного анализа для
C23H25N30-0.5С4Н404.
Вычислено: С 71.92; Н 6,52; N 10,06. Найдено: С 72,01; Н 6,60; N 10,03. П р и м е р 2.
сн сн-соон
гЛ4-N-N
и
При охлаждении льдом 1,79 г хлористого тионила по каплям добавляют в перемешиваемую смесь 2,0 г 3-(2-фенилпи- разоло/1,5-е/ пиридин-3-ил)-акриловой кислоты (транс-изомер) с 4 каплям Ы,М-ди- метилформамида в 10 мл хлористого метилена..
После перемешивания при комнатной температуре в течение 3 ч растворитель выпаривают в вакууме, получая производное хлорангидрида кислоты.
С другой стороны, при охлаждении льдом и 6,80 г бис-(триметилсилил)-ацетами- да по каплям добавляют 6,48 /R/-2- (2-окси- этил)-пиперидина. Смесь нагревают до комнатной температуры в течение 20 мин при перемешивании.
Затем в смесь добавляют 1,53 г триэ- тиламина и 40 мл хлористого метилена. В эту смесь далее при охлаждении льдом добавляют вышеуказанное производное хлорэнгидрида кислоты и всю массу перемешивают при комнатной температуре в течение 1 ч. Растворитель упаривают в вакууме и в смесь добавляют 10 мл 1н раствора соляной кислоты и 10 мл этила- цетата.
Полученную смесь перемешивают в течение 30 минут, а затем добавляют 12 мл 1Н раствора окиси натрия и экстрагируют 60 мл хлористого метилена. Экстракт сушат над сульфатом магния и упаривают растворитель. Остаток хроматографируют на 40 г силикагеля с использованием смеси хлористого метилена с этилацетатом в coot- ношении 5:1. Фракции, содержащие целе- вое соединение, объединяют и упаривают в вакууме, с получением 1,83т (2Р)-1-/3-(2-фе- нилпиразоло/1,5-а/пиридин-3-ил)-акрило ил/2-/2-оксиэтил/- пиперидина (транс-изомер), т.пл 145-146.5°С.
+ 39,61° (с - 1,04, 95%-ный этанол).
ИК-спектр (вазелиновое масло), см : 3350,1640,1575,1520см 1.
ЯМР-спектр (CDC 1 з) б, м.д.: 1,23-2,20
(8Н, м), 2,63-3,90 (4Н, м.), 4,00-4,40 (1Н. м).
4,67-5,10 (1Н, м.), 6,63 (1Н, д.. 16.0 гц), 8,50
(1 Н, т., 7,0 гц), 7,77 (7Н, м.), 7,92 (1 Н, д., 16,0
гц), 8,47(1 Н, д., 7,0гц).
Данные элементного анализа для С2зН25Мз02:
Вычислено: С 73,58; Н 6,71; N 11,19. Найдено: С 73,98; Н 6,76; N 11,24. Масс-спектр: 375 (М+4). В соответствии с процедурой, аналогич- ной вышеизложенной в примере 2, получили нижеследующие соединения (примеры 3-18).
Пример 3, ,-. CONQ J А
J Ц./
Г он
0
5
0
5
/25/-1-/3-(2-Фенилпиразоло/1,5-а/пи ридин-3-ил)-акрилоил/-2-(2- оксиэтил)-пипе- ридин/транс-изомер). т.пл. 98-99,5°С.
a D23 0 -41,20°(c- 1,0, 95%-ный этанол).
ИК-спектр (хлороформ), см : 3330, 1635, 1570, 1520.
ЯМР-спектр (СОС1з) 5, м.д.: 1,17-2,20 (8Н. м.), 2,67-4,00 (4Н, м.), 2,73 (1 Н, с), 4,67- 5,10(1 Н, м.), 6,70 (1 Н, д., 16,0 гц), 6.89 (1 Н. т., 7,0 гц), 7,25-7,87 (7Н, м.), 8,00 (1Н, д., 16,0 гц), 8,57(1 Н, д., 7,0гц).
Данные элементного анализа для C23H25N302:
Вычислено: С 73,58; Н 6,71; N 11,18.
Найдено: С 73,68; Н 6,81; N 11,21.
Масс-спектр: 375 (М4).
Приме р 4. CONQ
f он
Аг-О
N-N
Самцов крыс расы SD весом по 200-300 г умертвляют спусканием у них крови и удаляют торакальную аорту. В ванне для органов, заполненной 25 мл раствора Тирода, подвешивают спиральные полоски размерами 2,0 х 15 мм. Эти полоски соединяют с тензометром и измеряют изометрические натяжения. Через раствор в ванне пропускают ток пузырьков смеси 95% кислорода с 5% углекислого газа, а его температуру поддерживают на уровне 37°С. После доведения натяжения покоя до 0,5 г вызывают сокращение артериальных полосок с помощью раствора норэпинофрина концентрацией 3,2 х М.
Испытываемое вещество добавляют в ванну для органов кумулятивно. В конце каждого испытания в ванну для органов добавляют раствор папаверина концентрацией М с целью достижения максимальной релаксации.
(II) Испытываемое соединение.
(2Р)-1/3-/2-Фенилпиразоло/1,5-а/пир идин-3-ил/-акрилоил/2-/2-оксиэтил/-пиперидин (транс-изомер) (соединение примера
2).
(III) Результаты испытания. Величина MKgo 5,3 х г/мл. Испытание 2.
Действие по усилению тока почечной крови.;
(I) Методика испытания.
Испытание проводят на взрослых особях собак породы гончая обоих полов весом 8-15 кг. Под анестезией с помощью 35 мг/кг пентобарбитала натрия, вводимое внутри- брюшинно, трахею интубируютдля искусственного дыхания; В бедренную вену вводят катетеры для подачи в организм лекарственного средства.
Боковым надрезом обнажают короткий сегмент левой почечной артерии и удаляют прилегающую ткань для освобождения места для установки электромагнитного датчика скорости потока. Ток почечной крови измеряют соединением датчика скорости с расходомером.
(II) Испытываемое соединение.
То же самое соединение, что и использованное в испытании I.
() Результаты испытания,
Доза мг/кг увеличение расхода тока почечной крови, %
0,2 крови % + 19,7
Испытание 3. Диуретическое действие. (I) Методика испытания.
Испытание проводят на крысах расы FCLSD в возрасте 6 недель массой 170-206 г после выдержки животных на голодном режиме в течение 18 ч. Непосредственно
после перорального введения в организм испытываемого вещества, суспендирован- ного в 0,5%-ной метилцеллюлозе (0,5% МЦ), животным через рот вводят по 20 мл/кг физиологического раствора. Крыс рассажива0 ют по три особи в клетку для изучения метаболизма. Мочу собирают в течение 3 часов. Объем мочи измеряют мерным цилиндром, а мочевую кислоту в моче определяют с помощью прибора Determiner
5 UAKit (выпускается фирмой Киова медекс Ко., Лтд). Испытания проводят на 3 группах животных по 3 особи в каждой.
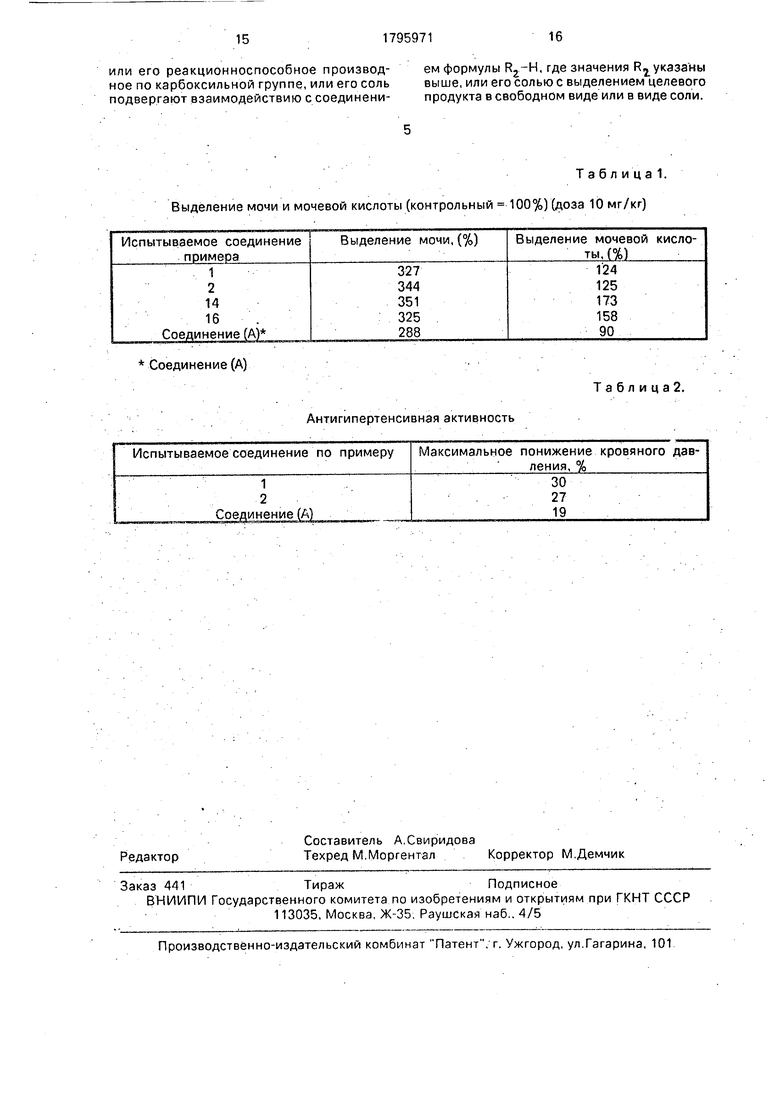
Результаты испытания представлены в табл.1.
0 1-/3-(2-Метил-б-фенилимидазо/2,1-Ь/ -1,3,4-тиадиазол-5-ил)акрилоил/-2- этилпи- перидин (транс-изомер)(соединение примера 35 патента ЕР-0041215, кл. С 07 D 513/04, 1981). .
5Испытание 4. Антигипертенсивная активность.
Метод испытания.
У самцов крыс породы Вистар в возрасте 11 недель удаляют одну почку под ане0 стезией. Дезоксикортикостеронацетат (ДОСА), субсидированный в арахисовом масле, вводят подкожно в количестве 30 мг/кг 2 раза в неделю/Питьевую воду заменяют 1%-ным солевым раствором,
5 Для эксперимента используют животных со средним кровяным давлением ISO- 200 мм ртутного столба в течение от 5 до 11 недель после операции.
Испытываемое соединение (дозировка
0 10 мг/кг) назначают для приема через рот ежедневно в течение 5 дней крысам, у которых кровяное давление повышено ДОСА.
Кровяное давление измеряют у бедренной артерии посредством датчика давления
5 и регистрируют в виде электрически интегрированных значений среднего артериального давления.
Результаты испытания представлены в табл.2.
0 Испытание 5,. . . . Ингибирование процесса агрегирования кровяных пластинок. (I) Методика испытания. Из сонной артерии самцов японских бе5 лых кроликов весом 2.5-3,0 кг собирают кровь и смешивают ее в объемном соотношении 1:10 с 3,8%-ным раствором цитрата натрия. После центрифугирования смеси при 150 g в течение 15.мин получили богатую кровяными пластинами плазму (КПП).
Способность пластин агрегироваться измеряют с помощью агрегометра (nikohklzal NKK НЕМА TRACER модель РАТ-4А). В кювету последовательно добавляют 0,24 мл КПП, содержащую 6,5-7,5 х 108 пласти- нок/мл, и 5 мкл испытываемого раствора или смеси полиэтиленгликоля 200 с этано- лом и водой в соотношении 1:1:2. Всю смесь перемешивают в течение 2 мин при температуре 37°С и для инициирования процесса агрегирования добавляют 125 мкг/мл коллагена. Испытание провели с использованием КПП, полученной от 3 других кроликов.
(II) Испытываемое соединение. То же самое соединение, что и использованное в испытании I.
(III) Результаты испытания. Ингибирующее действие на процесс агрегирования пластин. Величина ИКбо 7,9 х г/мл. Испытание 6. Кардиотоническое действие.
(I) Методика испытания.
Самцов морских свинок расы Хартли ве- сом по 500-600 г умертвляют спусканием крови, после чего у каждого животного удаляют сердце. Удаляют артериальную полоску и подвешивают ее в ванне для органов, содержащей 50 мл раствора Тирода, темпе- ратуру которого поддерживают на уровне 30° при аэрировании газовой смесью, содержащей 95% кислорода и 5% углекислого газа. Предсердие соединяют с датчиком натяжения с первоначальным натяжением 0,4-0,6 г. После достижения постоянной подвижности в раствор ванны добавляют лекарственный агент ив течение 30 мин наблюдают влияние на усилие сжатия и скорость пульсации. Эффективность выражают в процентных величинах до и после введения лекарственного агента. Для каждой концентрации используют по 3 отдельных препарата.
(II) Испытываемое соединение, То же самое соединение, что и использованное в испытании I.
() Результаты испытания приведены ниже.
Концентрация испытываемого соединения 10 г/мл Процентное увеличение сжимающего усилия 10,0 Процентное усиление сердечной пульсации -10,7 Испытание 7. Антигипертоническое действие.;
(I) Методика испытания.
Под анестезией у крыс рамы Вистар в одиннадцатинедельном возрасте удаляют по одной почке. Подкожно дважды в неделю животным вводят по ЗОмг/кг дезоксикарти- костеронацетата (ДОСА), суспендированно- го в арахисовом масле, а в качестве питьевой воды дают 1%-ный солевой раствор. . .
Для определения эксперимента используют животных со средним кровяным давлением 150-200 мм рт.ст. в течение от 5 до 13 недель после операции.
Испытываемое соединение (в дозе 3,2 мг/кг) вводят перорально ежедневно в течение 5 дней животным, страдающим от гипертонии, вызванной применением ДОСА.
На бедренной артерии с помощью датчика давления измеряют кровяное давление, которое фиксируют в виде электрически интегрированных величин средне1 го артериального давления.
(II) Испытываемое соединение.
1-/3-(2-Фенилпиразоло/1,5-а/пириди н-3-ил)акрилоил/-2- этилпиперидинполуфу- ма рат (транс-изомер) (соединение примера
1).
(Ill) Результаты испытания.
Максимальная степень снижения кровяного давления - 32%.
Представленные данные доказывают преимущество соединения I перед известными соединениями ЕР № 0041215, полезными в качестве средств, понижающих кровяное давление, мочегонных средств.
По категории токсичности соединение формулы I относится к низкотоксичным.






Изобретение касается гетероциклических веществ, в частности получения пираэолопиридинового соединения общей ф-лы: СН CH-DH CH-ty-C (0)- 1 N, где R1 фенил, R2 пиперидин, замещенн ый низшим алкилом, окси(ни- зшим)алкилом, или его соли, обладающего диуретическим и антигипертоническим действием, что может быть использовано в медицине. Цель - создание новых более активных веществ указанного класса, Синтез ведут реакцией соответствующей кислоты или реакционноспособного производного с соединением с последующим выделением целевого продукта в свободном виде или в виде соли. Новые соединения малотоксичны и по активности лучше известных аналогов. 2 табл.
Формул а изобретения Способ получения пиразолопиридино- вого соединения формулы
CH CH-COR2
v TRi N-N
СИ
где Ri-фенил;
R2 пиперидин, замещенный низшим алкилом, окси(низшим) алкилом, низшим ал- каноилокси(низщим) алкилом или низшим алкокси(низшим) алкилом, или его соли, отличающийся тем, что
соединение формулы
сн сн-соон
.QsVv
где значения Rt указаны выше.
или его реакционноспособное производ-ем формулы , где значения R указаны
мое по карбоксильной группе, или его сольвыше, или его солью с выделением целевого
подвергают взаимодействию с соединени-продукта в свободном виде или в виде соли.
Таблица. Выделение мочи и мочевой кислоты (контрольный 100%) (доза 10 мг/кг)
Соединение (А)
Антигипертенсивная активность
Таблица 2.
| Ступенчатый отражатель | 1933 |
|
SU41215A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Приспособление для изготовления в грунте бетонных свай с употреблением обсадных труб | 1915 |
|
SU1981A1 |
Авторы
Даты
1993-02-15—Публикация
1988-06-14—Подача