Изобретение относится к способу получения легированного тетрабората лития и может быть использовано в пьезо- и пиротехнике, а также при получении термолюми- йофоров и материалов акустоэлектронных устройств.
Целью изобретения является упрощение процесса, снижение энергозатрат и обеспечение возможности однофазного продукта.
Поставленная цель достигается тем, что в известном способе получения тетрабората лития, легированного ионами редкоземельных элементов и/или ионами переходных металлов, включающем смешивание бор и литий содержащих компонентов с метанольным раствором легирующей добавки, метанольный реактор легирующей добавки смешивают с 8,0-11,2 мас.% водным раствором гидроксида лития, содержащим борную кислоту в количестве, обеспечивающем
мольное соотношение ее к гидроксиду лития и легирующей добавке равное (2,0- 2,1):(1 .0-1 ,05)-.(0,00005-0,0 15) соответственно, а объемное содержание метанола в смеси выбирают из уравнения
V снзон - И.ЗСион ± 43,75(Сион - :-С°ион),
где V снзон объем метанола в см3 на 100 см3 водного раствора;
Сион - концентрация гидроксида лития в водном растворе, мас.%;
С°ион - наименьшая допустимая концентрация гидроксида лития в водном растворе (8,0 мас.%).
Способ осуществляют следующим образом.
В стеклянную или емкость из нержавеющей стали с мешалкой вводят определенные количества твёрдых борной кислоты и
00
о
со со
со
гидроксида лития при их мольном соотношении 2:1,а также воду а количестве, достаточном для достижения концентрации гидроксида лития а образующемся растворе н.б. 3,0-7,1 мас.%.
Смесь перемешивают при слабом нагревании до полного растворения твердой фазы. Полученный раствор выпаривают до достижения заданной (8,0-11,2 мас.%) концентрации гидроксида лития, В водную фазу вводят рассчитанный обьем метанола, содержащего определенное количество солей РЗЭ и/или солей переходных металлов в двух или трехвалентном состоянии из группы: О. Mn, Fe, Co, Ni, Си, V.
Образовавшийся в результате реакции осадок легированного тетрабората лития отфильтровывают, сушат при 150°С и прокаливают при 600-700°С в течение 1 ч.
Процесс получения легированного 1(26467 nMe+z происходит по следующей схеме: - растворение исходных твердых компонентов LiOH, НзВОз в водном растворе, доведение содержания воды и твердой фазы до нужного соотношения, введение легирующей добавки в виде метанольно- го раствора, синтез легированного LJ2B407 nMe+z и его выделение из водноспиртовой системы в твердом виде за счет определенного соотношения воды и метанола.
Все вышеуказанные параметры получения легированного тетрабората лития существенны для достижения цели изобретения.
Экспериментально установлено, что оптимальное содержание гидроксида лития в водной фазе, при котором происходит образование достаточного количества тетрабората лития для его выделения в твердом виде из воДноспиртовой системы составляет 8,0-11,2 мас.%.
При этих концентрациях и заданном мольном соотношении компонентов, в том числе легирующей добавки, а также необходимом объемном содержании метанола, происходит образование и последующее выделение легированного тетрабората лития LiaB/jO nMe+z в твердом виде из вод- носпиртовой системы.
При концентрациях LiOH в водной фазе CLIOH 8,0 мас.% процесс синтеза LiaB-iO nMe+z протекает медленно, а его выделение в твердом виде незначительно, ввиду малого содержания последнего по отношению к объему водноспиртовой фазы. Указанные факторы лимитируют выход nMe+z. Так, при концентрациях LiOH 7,5-7.9 мас.% выход LJ2B407 пМе+г составляет н.б. 15-40 мас.% от возможного.
При концентрациях Сион 11.2 мас.% значительное содержание LbBtOi приводит к нестабильности водной фазы и преждевременному выделению Li2B/)07 в твердом виде
5 до введения легирующей добавки. В результате чего происходит самопроизвольное образование осадка нелегированного , что резко снижает выход легированных кристаллов Li2B407 nMe+z.
Ю При подборе спиртовой фазы и, особенно, ее объемного соотношения с водной фазой исходили из следующих условий: необходимость наличия хорошей (достаточной) растворимости в спирте исходных со15 лей легирующих добавок и.,.плохой растворимости образовавшегося легированного тетрабората лития в конечной водо- спиртовой системе.
Этим условиям удовлетворяет спирт ме- 0 тиловый СНзОН (метанол). Действительно, в метаноле хорошо растворяются нитраты, хлориды, ацетаты и др. соли РЗЭ и переходных металлов (хрома, марганца, железа, кобальта, никеля, меди и т.д.), что позволяет
5 использовать их метанольные растворы в широком диапазоне концентраций и тем самым обеспечивает получение LJ2B407 с содержанием легирующей добавки до 3-5 моль.%.
0 Такое содержание добавок практически превышает их предельно допустимые значения в твердых растворах на основе . Объемное содержание метанола в водноспиртовой системе было подобрано
5 экспериментально. При этом установлено, что объем метанола, обеспечивающий оптимальный выход легированного LJ2B407, висит от концентрации гидроксида лития в водной фазе (Сион).
0 с другой стороны, интервал значений содержания метанола в системе определяется разностью между Сион и наименьшей заявляемой концентрацией в водной фазе (С°ион), равной 8,0 мас.%1 LIOH,
5 Если концентрация LiOH;в ыpaжeнa в мас.%, то объем метанола, приходящийся на 100 см водной фазы равняется
V сн3он 14.3CLIOH ± 43,75(Сион - . - С°ион). где C°LIOH 8,0 мас.%.
0
В целом, объем метанола, приходящегося на 100 см3 водной фазы заявляемого диапазона концентраций LiOH (8,0- 11,2 мас.%) может меняться в пределах от 20 до 300 см3. Установлено, что как верхнее (300 см3), так и нижнее значение (20 см3) интервала количества метанола соответствуют концентрации Сион эт 11.2 мас.%. т.е.
верхнему значению заявляемого диапазона концентрацией UQH в водной фазе.
С уменьшением концентрации LIOH в водной фазе, интервал значений объемов метанола сужается и при нижнем значении заявляемого диапазона концентраций С°ион 8,0 мас.%, объем спиртовой фазы приближается к объему водной фазы (Уснзон ).
В случае, если V снзон 300 см3 возрастание содержания метанола в системе приводит к затруднению переноса легирующей добавки в реакционную зойу вследствие сольватирующего эффекта спирта и изменения растворимости соли легирующей добавки. При этом конечный продукт представляет собой смесь легированного и чистого UzBaQ с неопределенным содержанием первого.
При V сизом 20 см3 (при Сион ;Ц 11,2 мас.%)относительно большое содержание воды в системе существенно повышает растворимость легированного LiaBAOv в водноспиртовой системе и тем самым приводит к резкому снижению выхода LisBflOv (до 5-30%).
Мольное отношение исходных компонентов НзВОз и LiOH, а также легирующей добавки Мё(МОз)г(МеС1г) в пределах 2,0- 2,1:1.0-1,05:0,00005-0,015 является существенным для синтеза легированного nMe+z без образования побочных фаз и соединений.
Если, например, изменить указанный интервал соотношений в сторону увеличения количества НзВОз и уменьшения содержания LIOH, то в процессе синтеза, кроме тетрабората лития, будут образовываться также полибораты лития.
При уменьшении содержания НзВОз и, соответственно, увеличении количества UOH в системе образуются орто- и метабо- раты лития.
Изменение мольного соотношения легирующей добавки Ме(МОз)г(МеС1г) в сторону ее увеличения приводит к образованию в процессе синтеза побочных фаз оксидов этих металлов.
Нижний предел легирующей добавки лимитируется только практическими потребностями, так как при более низких со- держаниях легирующих добавок ( 0,00005) их влияние на электрофизические, оптические и др. свойства Li2B40y может не проявляться, хотя их введение в количествах менее нижнего предела заявляемым способом возможно.
Предложенный способ позволяет синтезировать легированный ионами РЗЭ
и/или ионами переходных металлов тетра- борат лития с выходом 50-92% от теоретического и содержанием легирующей добавки Me+z.до 3,0 мас.%.
Пример1,В стеклянную емкость с мешалкой объемом 3000 см помещают 494,7 г НзВОз и 95,8 г LiOH, взятых в мольном отношении 2:1. В емкость заливают 956 см3 воды, достаточной для обеспечения
концентрации гидроксида лития в образующемся растворе равной 6,2 мас.%. Полученную смесь нагревают (60-70°С) при перемешивании до полного растворения твердой фазы. Раствор выпаривают до содержания гидроксида лития в растворе равном 8,0 мас,%. При этом упаривается 356 см3 воды. К полученному водному раствору добавляют определенное количество метанола 115 см3, содержащего 4,74 г хлорида
меди (CuCla 2H20), что соответствует мольному отношению борная кислота : гидро- ксид лития : хлорид меди в системе 2:1; :0,005.. ,
Выпавший осадок легированного
LiaB/iO отфильтровывают, сушат при 150°С и прокаливают при 700°С в течение 1 ч. Выход легированного LI2B40 составляет 50% от теоретически возможного. Состав легированного тетрабората лития соответствует LI2B407 0,02Си .
П р и м.е р 2. В стеклянную емкость Объемом 3000 см3 помещают 742,0 г НаВОз и 143,7 г LIOH, взятых в мольном отношении 2; 1 и заливают 1432см3 воды, необходимой
для создания концентрации гидроксида лития в системе 6,2 мас.%. Полученную смесь перемешивают при слабом нагревании до полного растворения твердой фазы. Раствор выпаривают до концентрации LiOH в
водной фазе равной 11,2 мас.%. При этом упаривается 1035 см3 воды. К полученному раствору добавляют заданное количество метанола (200 см3), содержащего 3,29 г нитрата неодима (Nd(NCs)3 бНаО). Мольное
отношение компонентов В : Li : Nd составляет 2 : 1,0 : 0,00125. Выпавший осадок отфильтровывают, сушат и прокаливают при 700°С в течение 1,5ч. Выход конечного продукта составляет 50%. Состав легированного неодимом тетрабората лития соответствует формуле LI2B40 O.OOSNd3. ПримерЗ. Готовят водный раствор исходных компонентов в количестве и с концентрацией LIOH как указано в примере 2.
К полученному водному раствору добавляют определенное количество метанола (3000 см3), который содержит 9,51 г хлорида хрома (). Мольное отношение борная кислота : гидроксид лития : хлорид хрома
составляет 2:1: 0,01. Выпавший осадок легированного отфильтровывают, сушат и прокаливают 1 ч при температуре 700°С. Выход продукта составляет 65%. Состав легированного хромом тетра- бората лития соответствует формуле LI2B407 0,ОЗСг3+.
П р и м е р 4. В стеклянную емкость объемом 3000 см3 вносят 618,3 г НзВОз и 119,7 г LiOH с мольным отношением 2,1 : :1,05 и заливают водой в количестве 1194 см3, необходимой для достижения концентрации LiOH в растворе 6,2 мас.%. Полученную смесь нагревают при перемешивании до полного растворения твердой фазы. Раствор выпаривают до концентрации LiOH 9,7 мас.%. При этом упаривают 700 см3 воды: К полученному водному раствору добавляют определенное количество метанола (1315 см3), содержащего 0,452 г хлорида меди (CuCte 2Н20), Мольное отношение при этом в системе борная кислота : гидроксид лития : хлорид меди составляет 2,1 : 1,05 : 0,00056. Выпавший осадок образовавшегося легированного тетрабората лития отфильтровывают, сушат и прокаливают при температуре 700°С в течение 1,5ч.
Выход легированного медью тетрабората лития при этом составляет 70% от теоретического. Состав продукта соответствует формуле L12B407 O.OOISCu2 1,
Приме р 5. Готовят водный раствор с концентрацией гидроксида лития 9,7 мае. % с соотношением компонентов и их количествах, как указано в примере 4. К получен- ному водному раствору добавляют необходимое количество (1315 см ) метанола, содержащего 0,452 г СиС(2 2НО и 0,159 г . Мольное соотношение исходных компонентов - борная кислота : гидро- ксид лития : хлорид меди : хлорид тербия при этом в системе составляет 2,1 : 1,05 : :0,00056: 0,000126. Образовавшийся осадок легированного тетрабората сушат, прокаливают при температуре 700°С в течение 1 ч. Выход легированного тетрабората лития состава LI2B407- 0,001 SCu2 0,00034ТЬ3+ составляет 70%.
Примерб. Готовят водный раствор с содержанием LiOH равным 11,2 мас.% и количествах исходных компонентов как указано в примере 2. После чего к водному раствору добавляют строго определенное количество метанола (1600 см3), содержащего 0,10 г нитрата неодима (Nd(N03J3 6Н20). Мольное отношение компонентов борная кислота : гидроксид лития : нитрат неодима в водно-спиртовой системе составляет 2 :1: : 0,00005. Выпавший в результате реакции
осадок легированного тетрабората лития отфильтровывают, сушат и прокаливают при температуре 700°С в течение 1 ч. Выход продукта составляет 75% от возможного. Состав легированного неодимом тетрабората лития соответствует L B-iOy 0,0001 Nd3+. П р и м е р 7 (вне заявляемого диапазона). В стеклянную емкость объемом 3000 см3 вносят 470 г борной кислоты и 91 г гидроксида лития, взятых в мольном отношении 2 : 1, а также 905 см1 воды, взятом в количестве необходимом для достижения в образовавшемся растворе концентрации LiOH, равной 6,2 мас.%. Смесь нагревают до полного растворения твердой фазы, после чего раствор выпаривают до концентрации равной 7,7 мас.%. При этом выпаривается 285 см воды. К полученному водному раствору добавляют рассчитанное количество метанола 1100 см , содержащего 3,47 г хлорида меди (CuCte 2Н20). что соответствует мольному соотношению НзВОз : LiOH : CuCte в системе равному 2 : 1: : 0,0053. В указанных условиях компоненты реагируют в водноспиртовой системе с оЬ- разованием тетрабората лития/часть которого выделяется в твердом виде. Выход легированного тетрабората лития LI2 640 О.ОЗБСи2 30 % от возможного.
Прим е.р 8 (вне заявляемых условий). В стеклянную емкость объемом 3000 см3 добавляют 767 г Н2ВОз и 148,2 г LiOH, взятых в мольном соотношении 2:1, а также
з. .
1475 см воды, в количестве обеспечивающем концентрацию LiOH в образующемся растворе равную 6,2 мас.%, Смесь нагревают до растворения твёрдой фазы. После чего раствор выпаривают до концентрации равной 11,4 мас.%. Образовавшийся водный раствор нестабилен и при охлаждении до комнатной температуры возможно выпадение осадка в виде тетрабората лития: К полученной водной фазе добавляют определенное количество метанола (180. см3), содержащего 0,107 г NdCl3 6Н20. Мольное отношение компонентов при этом в системе составляет борная кислота : гидроксид лития : хлорид неодима 2:1: 0,00004, В указанных условиях эксперимента, кроме легированного тетрабората лития в осадок выделяется также некоторая часть чистого LJ2B407, а само количество твердой фазы невелико. Выпавший осадок фильтруют, сушат и прокаливают 1 ч при температуре 700°С, Образовавшийся продукт представляет собой смесь L12B407 и LJ2B407 Nd3. Выход твердой фазы 20% от массы исходных компонентов.
П р и м е р 9 (вне заявленных условий). Готовят водную фазу, содержащую 11,4 мас.% LiOH в количествах и по методу, указанному в примере 7. К полученной водной фазе добавляют рассчитанное количество метанола (3120 см, содержащего 34,435 г NdCla БНаО (мольное отношение В : Li : Nd 2 : 1 : 0,016). В указанных условиях эксперимента в твердую фазу выделяется чистый LJ2B407, а также частично гидроксид неодима, снижающие выход легированного тетрабората лития. Образовавшийся осадок фильтруют, сушат и прокаливают 1 ч ПРИ температуре 700°С. Образовавшийся продукт представляет собой смесь nNd°+ с примесью ШаОз.
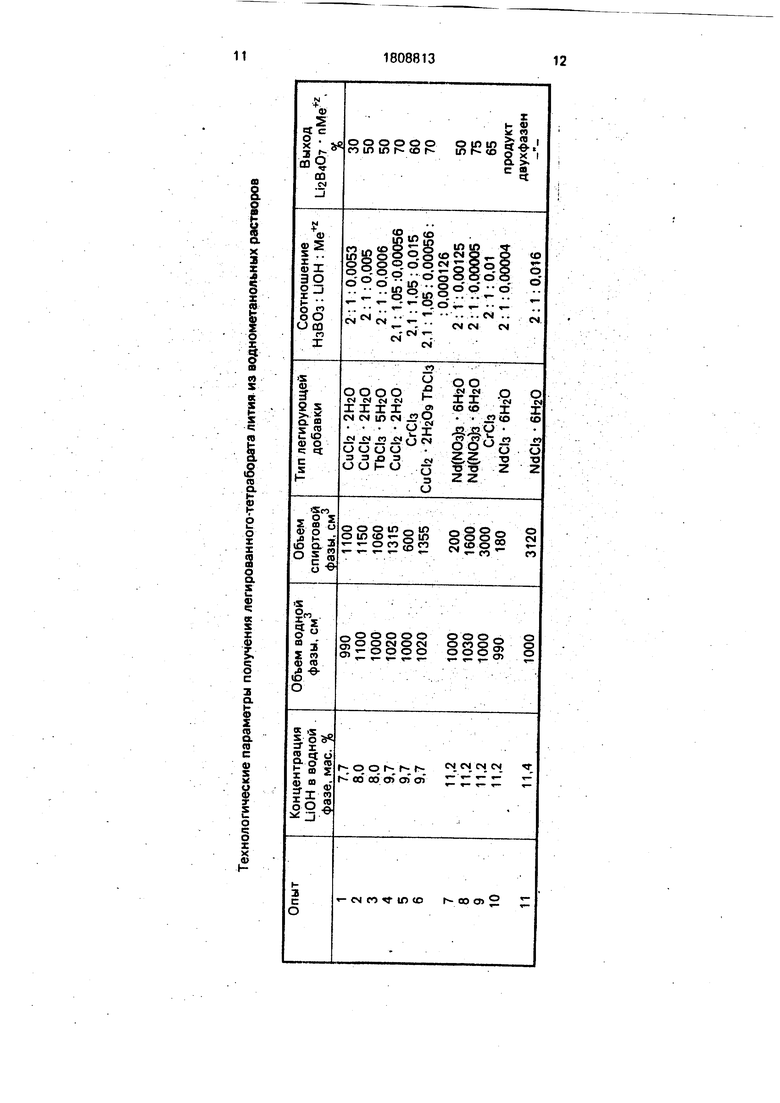
Основные технологические данные по получению легированного тетрабората лития L12B407 представлены в таблице (опыты 1, 10 и 11 вне заявляемых условий).
Полученный легированный тетраборэт лития nM«+z представляет собой белый или окрашенный в тот или иной цвет, в зависимости от типа легирующей добавки, мелкокристаллический порошок. По данным рентгенографического анализа U2B407 nMe+,z кристаллизуется в тетрагональной сингонии и относится к полярной
.-...- . -. . 19
группе симметрии, пр.гр. 14icd С 4V . которая совпадает с пространственной группой симметрии чистого L12B40. Параметры элементарной ячейки легированного лежат в пределах а 9,46- 9,48 А, с 10,26-10,29 А, Число формульных единиц U2B40 . nMe+z в элементарной ячейке г 8, плотность рентгенографическая р 2,44 г/см , что близко к кристаллографическим характеристикам чистого U2B407 : а 9,46 А: с 10,26 А, г - 8,/э 2,44 г/см3.
Рентгенографические данные, таким образом, указывают на принадлежность легированных кристаллов LJ2B407 к структуре LJ2B407, т.е. подтверждают образование твердых растворов на основе матрицы LI2B407.
Принадлежность легированного LJ2B407 к фазам типа твердых растворов замещения подтверждается также плавными и линейным изменением параметров элементарной ячейки и, соответственно отсутствием скачка в их значениях в зависимости от содержания легирующей добавки. В случае отсутствия образования твердых растворов, параметры элементарной ячейки LI2B407 оставались бы без изменений не зависимо от количества вводимой добавки.
Возможность количественно изменять содержание легирующей добавки в тетрабо- рате лития представляет несомненный практический интерес для создания новых термолюминофоров, материалов акустоэ- лектронных устройств, а также для регулирования, в том числе повышения, пьеэо- и пироэлектрических характеристик в функциональных материалах на оснрве LI2B407.
Таким образом, использование предлагаемого способа получения легированного d- и f-металлами тетрабората лития L|2B4)7 пМе+: обеспечивает по сравнению с известными способами следующие преимуществу: получение легированного тетрабората лития с различным и регулируемым содержанием добавки; возможность введения в матрицу LI2B407 практически любой легирующей добавки из классов переходных и редкоземельных металлов и их сочетания; отсутствие в конечных образцах примесей других боратов и побочных фаз; упрощение технологического процесса пол- .учения..
Предлагаемый способ эффективен, так как позволяет получать легированный Li2B4U7 nMe+z (где Me+z d- и/или f-эле- менты) в количествах, лимитируемых только емкостью рабочей аппаратуры,
Формула изобретения
Способ получения тетрабората лития, легированного ионами редкоземельных элементов и/или ионами переходных металлов, включающий смешивание бор и
литийсодержащих компонентов с мета- нольным раствором легирующей добавки, отличающийся тем, что, с целью упрощения процесса, снижения энергозатрат и обеспечения возможности получения
однофазного продукта, метанольиый раствор легирующей добавки смешивают с 8,0- 11,2 мас.% водным раствором гидроксида лития, содержащим борную кислоту в количестве, обеспечивающем молярное соотношение ее и гидроксиду лития и легирующей добавке (2.0-2,1):(1,0-1,05):(0,00005-0,015) соответственно, а объемное содержание метанола в смеси выбирают из уравнения
V снзбн - 14,3Cuoh ± 43,75(Сион - - C°LIOH),
где V снзон объем метанола в 1 см3 на 100 см3 водного раствора;
Сион - концентрация гидроксида лития в водном растворе, мас.%;
C°LIOH наименьшая допустимая концентрация гидроксида лития в водном растворе (8,0 мас.%).




| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ШИХТЫ НИОБАТА ЛИТИЯ ДЛЯ ВЫРАЩИВАНИЯ МОНОКРИСТАЛЛОВ | 2015 |
|
RU2576641C1 |
| Способ получения пероксида лития | 2017 |
|
RU2678026C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТА ДЛЯ РЕГЕНЕРАЦИИ ВОЗДУХА | 2015 |
|
RU2596770C1 |
| Способ получения продукта для регенерации воздуха | 2017 |
|
RU2669857C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ЛИТИРОВАННОГО ОКСИДА КОБАЛЬТА С ЛЕГИРОВАННОЙ СТРУКТУРОЙ И МОДИФИЦИРОВАННОЙ ПОВЕРХНОСТЬЮ | 2020 |
|
RU2755526C1 |
| СПОСОБ ОЧИСТКИ ЛИТИЕВЫХ СОЛЕЙ | 2020 |
|
RU2834777C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОКСИДА ЛИТИЯ | 2006 |
|
RU2322387C1 |
| Способ получения моногидрата гидроксида лития высокой степени чистоты из материалов, содержащих соли лития | 2021 |
|
RU2769609C2 |
| Технологическая линия для получения соединения-предшественника активного катодного материала для литий-ионных аккумуляторов на основе слоистых оксидов лития и переходных металлов | 2024 |
|
RU2838244C1 |
| Катодный материал с высокой объемной плотностью энергии для литий-ионных аккумуляторов | 2021 |
|
RU2776156C1 |
Сущность изобретения: способ получения тетрабората лития, легированного ионами РЗЭ или ионами переходных металлов путем смешения бор и литййсодержащих компонентов с метанольным раствором легирующей добавки, предварительно сме- шанным с 8,0-11,2%-ным водным раствором гидроксида лития, содержащим борную кислоту в количестве, обеспечиваю щим мольное соотношение ее к гидроксиДу лития и легирующей добавке, равное (2,0- 2,1):(1,0-1,05):(0,00006-0,015). При этом объемное содержание метанола в смеси выбирают из уравнения V снзон .- 14,3 Сион ± 43,75(Сион - C°LIOH), гдб V снзон объем метанола в 1 см на 100 см водного раствора; Сион - концентрация гидроксида лития в водном растворе, мае. %; С°ион- наименьшая допустимая концентрация LIOH в водном растворе (8,0 мас.%). 1 табл.

| 0 |
|
SU161626A1 | |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Сплав для отливки колец для сальниковых набивок | 1922 |
|
SU1975A1 |
| Kutoml Y.,Takeuchi N.Thermolumlnescence In lithium tetraborate doped with activators // // J.Mater, Soh Lett, 1986, 5, 51,53 | |||
Авторы
Даты
1993-04-15—Публикация
1990-11-19—Подача