Изобретение относится к способу выделения нового биологически активного соединения - птеринового кофермента ферментной системы необратимого окислительного деза- минирования L-глютамата, который может найти применение в энзимологии и биохимии.
Поставленная цель достигается опиЫва- емым способом выделения птеринового кофермента ферментной системы необратимого окислительного дезаминирования L-глютамата, заключающийся в том, что семена злаковых и бобовых растений экстрагируют водой при весообьемном соотношении 1:1-10, гомоге- нат центрифугируют, очищают гель-хрома- тографией на декстрановых гелях с последующей ионообменной хроматогра- фией на заряженном ионообменнике типа QAE-сефадексе или адсорбционной хрома- тографией на окиси алюминия.
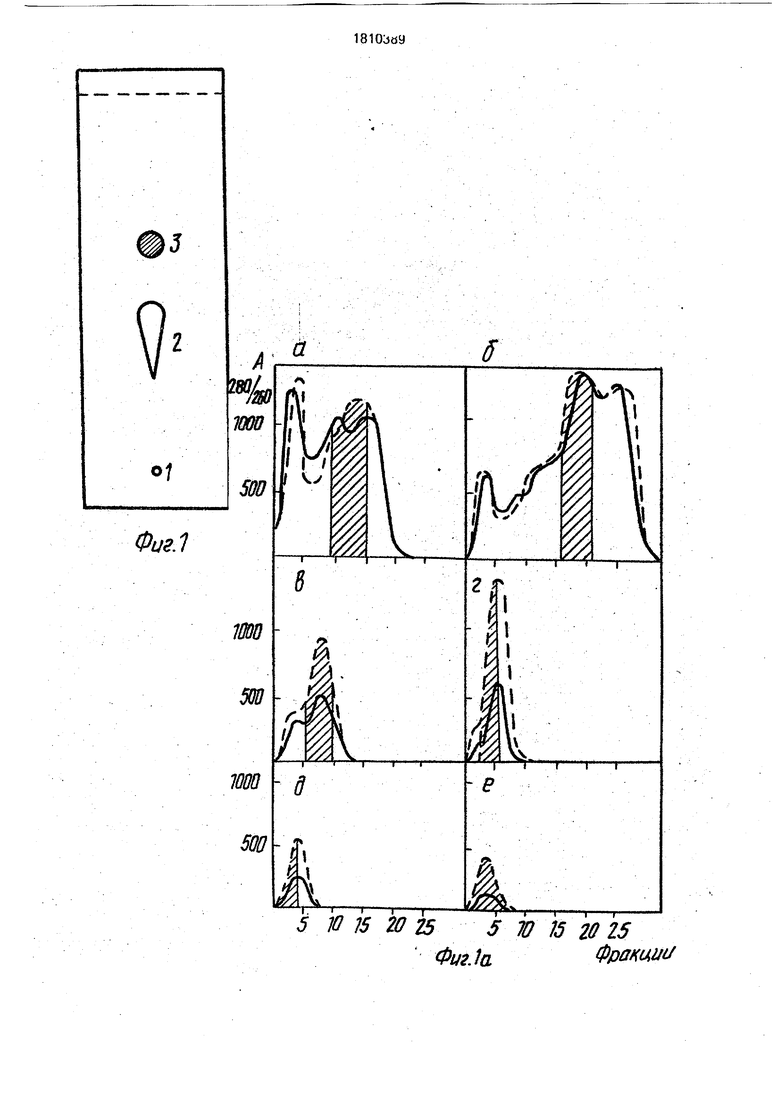
На фиг. 1а - изображена последовательная гель-хроматографическая очистка фактора на: а - сефадексе G-50; б - сефадексе G-15; в, г - молселекте G-10: д, е - сефадексе G-10. (Адсорбция при 280 нм --сплошная
линия, при 260 нм - пунктирная линия; фракции, содержащие фактор - заштрихованы); на фиг. i - тонкослойная хроматог- рафия гидролизованного фактора в системе растворителей: бутанол-уксусная кислота-вода (4:1:1), здесь 1 - старт, 2 - аминокислотный, компонент, 3 - флюоресцирующий компонент; на фиг. 2 - спектр флюоресценции фактора: 1 - спектр возбуждения; 2 - спектр эмиссии; фиг. 3 - ИК-спектр фактора; на фиг, 4 - дифференциальный спектр фактора; на фиг. 5 - тонкослойная хроматография фактора и птериновых соединений, окисленных перманганатом калия: 1 - 6-птерин карбоновая кислота, 2 - эрит- роптерин, 3 - фактор (в системе растворите-, лей: А - пропанол-аммиак (2:1), Б - бутанол-уксусная кислота-вода (4:1:1); ка фиг. 6 - тонкослойная хроматография фактора (пятно 2) и эритроптерина (пятна 1, 3), окисленных перманганатом калия (в системах растворителей: А - пропанол-аммиак (2:1), Б - бутанол-уксусная кислота-вода (4:1:1); на фиг, 7 - полерография неокислены
00
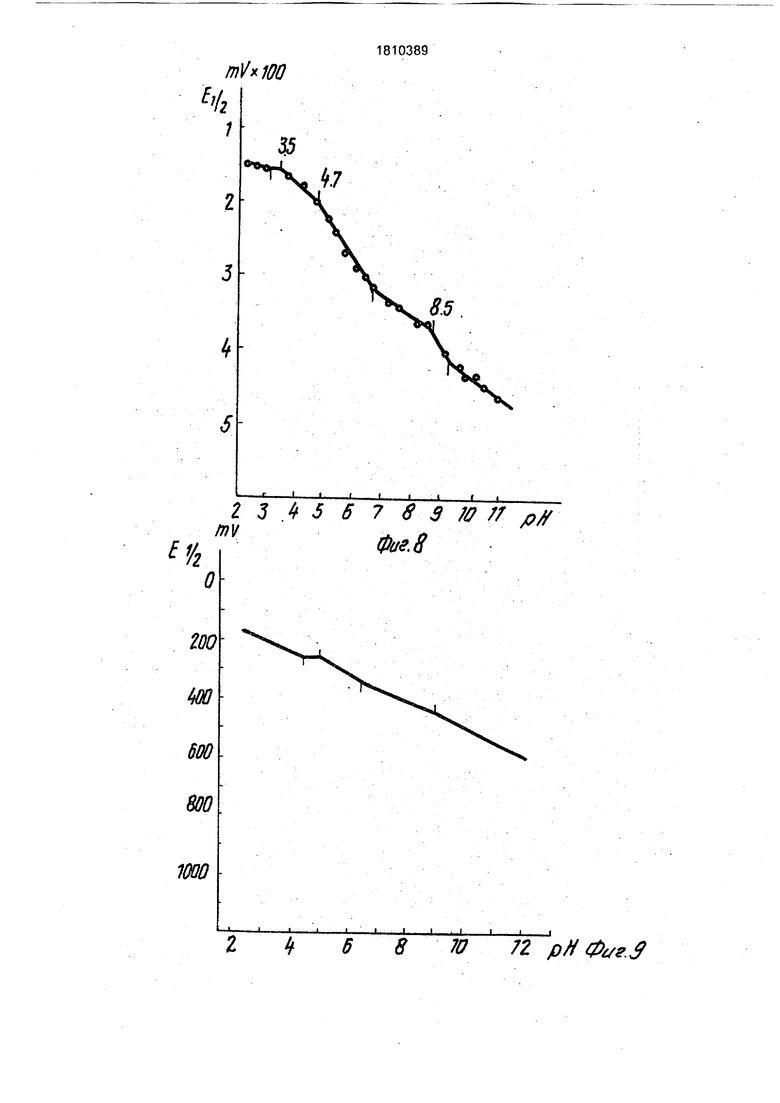
ного эритроптерина; на фиг. 8 - полярогра- фия неокисленного кофермента; на фиг. 9- полярография кофермента и эритроптерина, окисленных перманганатом калия в щелочных условиях.
Пример1.50г зерна пшеницы сорта Саратовская 29 растирают в дистиллированной воде в соотношении 1:1 (масса семян к объему диет, воды) - выход кофермента в таком соотношении составляет 10%, при экстракции зерна пшеницы в соотношении 1:5, выход кофермента - 95%; экстракция семян в дистиллированной воде в соотношении 1:10 - выход кофермента составляет 15%. Затем гомогенат центрифугируют при ускорении силы тяжести, равной 1000 д, выход кофермента составляет 15%; при ускорении силы тяжести, равной 8000 д, выход кофермента составляет 75%; а при ускорении силы тяжести, равной ЮОООд, выход кофермента составляет 95%. В дальнейшем надосадочную жидкость подвергают гель-хроматографии на колонке с сефадексом G-50, Как показано на фиг. 1а, фракции содержащие коферментную актив ность, заштрихованы. Следующим этапом очистки кофермента явилась ступенчатая хроматография на анионообменнике QAE- сефадексе А-50, фракции содержащие ко- фермент объединяют и выпаривают досуха.
На последней стадии очистки кофермента используют адсорбционную хрома- тографию, на щелочной окиси алюминия. Для работы используют колонку размером 1,2 х 5 см, уравновешенную бидистиллятом. Не связавшиеся с сорбентом вещества сначала элюируют бидистиллированной водой, а затем кофермент элюируют с колонки 0,5 н раствором аммиака. Фракции, содержащие кофермент, объединяют и выпаривают на вакуумно-роторном испарителе.
Аналогичным образом, как описано в примере 1, выделяют кофермент из злаковых растений (овес, ячмень) и бобовых (сои, гороха, люпина). Выход кофермента зависит от взятого соотношения веса растительного материала к объему диет, воды (примеры приводятся ниже).
П р и м е р 2. Выделение кофермента из овса.
Соотношение массы
к объему1:1 1:5 1:10
Выход кофермента, % . 10.90 20
Примерз. Выделение кофермента из ячменя.
Соотношение массы
к объему1:1 1:5 1:10
Выход кофермента, % 20 98 40 .
П р и м е р 4. Выделение кофермента из люпина,
Соотношение массы к объему1:1 1:5 1:10 Выход кофермента, % 10 87 18 П р и м е р 5. Выделение кофермента из гороха.
Соотношение массы к объему1:1 1:5 1:10 Выход кофермента, % 7 80 10 Прим е р б. Выделение кофермента из 0 сои.
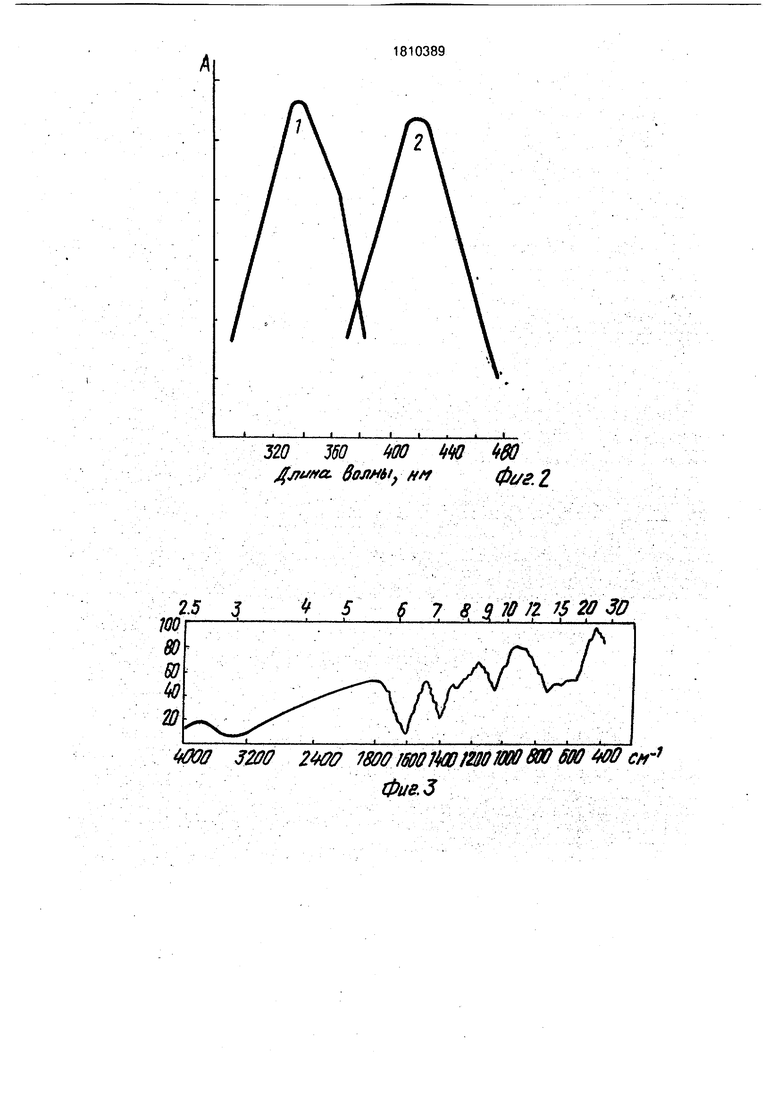
Соотношение массы к объему1:1 1:5 1:10 Выход кофермента, % 9 85 8 Физико-химические свойства кофер- 5 мента. Для того, чтобы полностью исключить сомнения о белковой природе кофермента были испытаны каждая аминокислота, из содержащихся в коферменте, в отдельности и всумме. Ни по отдельности, ни 0 в сумме они не оказывали активирующего действия на кофермент-чувствительный фермент. Была проведена тонкослойная хроматография в системе растворителей: бу- танол-уксусная кислота-вода (4:1:1) гидролизо- 5 ванного в соляной кислоте кофермента. Хроматограмма была проявлена нингидри- ном. Как видно из фиг. 1, на хроматограмме имеются два пятна, одно из которых проявляется нингидрином; а другое - нет. Эти пят- 0 ная были выделены и испытаны на коферментную активность, Как мы и предполагали, активацию кофермент-чувствитель- ного фермента проявляло пятно, не окрашиваемое нингидрином, т.е. вещество 5 неаминокислотной и небелковой природы. При освещении хроматограммы ультрафиолетом наблюдалась интенсивная флюоресценция активного компонента кофермента. Для этого с хроматограммы было 0 выделено флюоресцирующее пятно неаминокислотной природы злюированием бидистиллятом и был снят спектр флюоресценции. Спектр флюоресценции активного кофермента приведен на рис. 2, Как видно из рисунка, 5 активный компонент кофермента имеет лишь один пик поглощения с максимумом длины волны 330 нм и симметричный ему пик возбуждения с максимумом - 450 нм. Симметричность пиков свидетельствует о 0 том, что препарат кофермента не загрязнен другими флюоресцирующими веществами. Так как по спектру флюоресценции невозможно делать выводы о природе активного компонента кофермента, необходимо было 5 провести комплексное его изучение. Был снят спектр ИК-спектр на спектрофотометре Спекорд 75 ИР. Из фиг.З, видны выраженные пики в областях 1585, 1395, 1305, 1090,1045см . При сравнительном анализе известных стандартных соединений, приведенных в центре по спектроскопии Института органической химии СО АН СССР (г. Новосибирск) было обнаружено некоторое сходство его со спектром 2-амино-4-гидро- кси-7-птеридина.
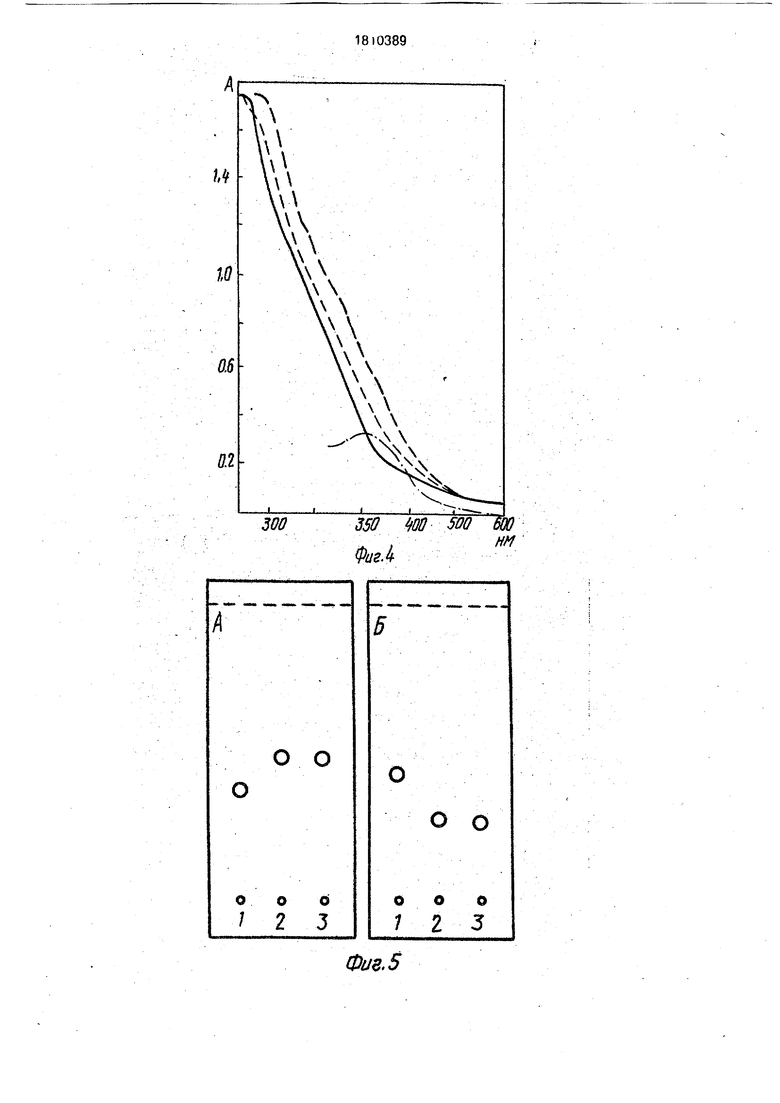
Были изучены ультрафиолетовые и дифференциальные ультрафиолетовые спектры. Кофермент, элюированный с щелочной окиси алюминия анализировали в щелочной (1), кислой (2) и нейтральной (3) среде. На рисунке 4 показан дифференциальный спектр (4) щелочного раствора кофермента (1) относительно кислого (2). Дифференциальный спектр кофермента с максимумом поглощения при 360 нм указывает на его птериновую природу. На основании полученных данных сделан вывод о том, что выделенный из зерна пшеницы коферент, участвующий в реакции окислительного де- заминирования . глютамата, относится к классу птериновых соединений.
Для того, чтобы определить к каким производным птеринов относится выделенный коферент, было проведено в щелочных -условиях перманганатное окисление кофермента. Для этого используют активный компонент кофермента после тонкослойной хроматографии. Окисление проводят в 0,1 н NaOH в присутствии 0,1 н КМпОз. Затем эту смесь прогревают при 100° Сна водяной бане в течение 30 минут. После этого добавляют этанол и полученный коричневый осадок отфильтровывают и фильтрат используют для дальнейшей работы. Окисленный препарат кофермента разделяют тонкослойной хро- матографией на широкопористых пластинках Силуфол в двух системах растворителей: 1) пропанол-аммиак 1 % (2:1), 2)бутанол-уксусная кислота-вода (4:1:1). Данные хроматографиче- ского анализа щелочного окисления кофермента приведены на рисунке 5. Как видно из рисунка, на хроматограмме имеется пятно, продукт щелочного окисления кофермента в системе: бутанол-уксусная кислота-вода (,23 ±0,02); пропанол-аммиак 1% (RHJ.4 ± 0,03).
Данный способ идентификации позволяет провести достоверное разделение и идентификацию соединения, относящихся к 6- и 7-производным птеринам. Для этого параллельно с анализируемым продуктом шелочного окисления кофермента были разделены продукты щелочного окисления синтетических маркеров: 6-птерин карбоновой
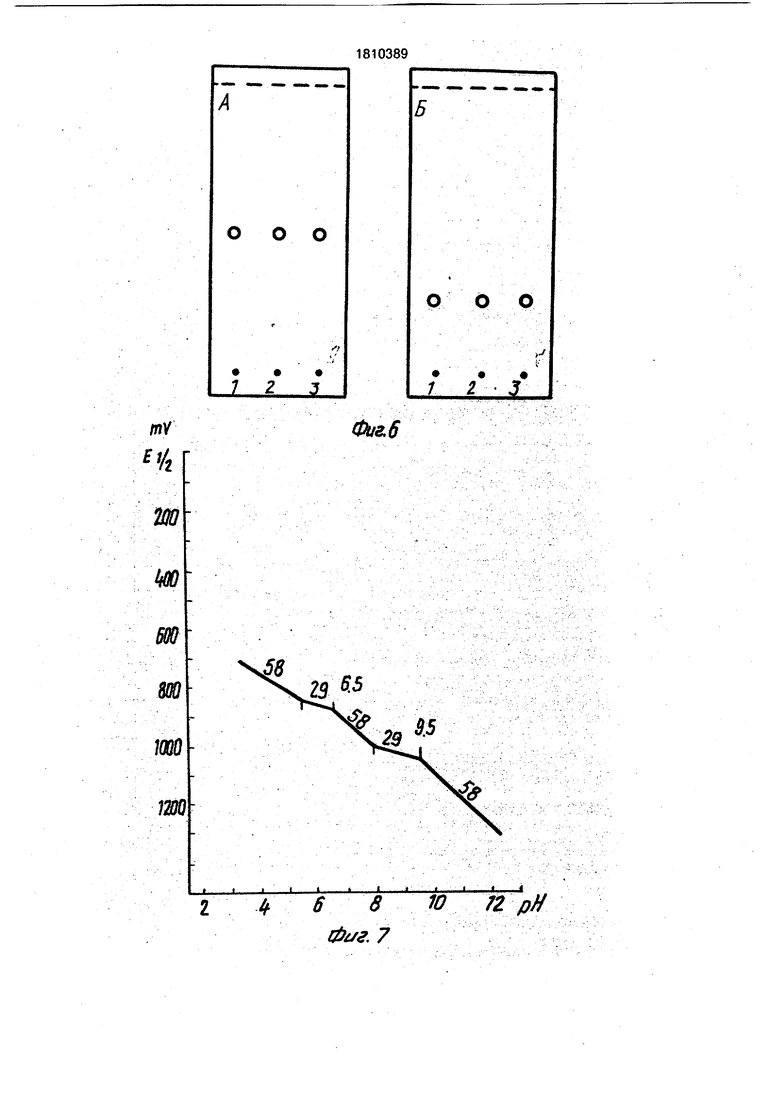
кислоты, ксантоптерина, 7-метил птерина и 7 производного птерина - эритроптерина. Как видно из рисунка б продукт окисления кофермента имеет одинаковую подвижность с продуктом окисления эритроптерина. Это свидетельствует о том, что кофермент относится к 7-замещенным птеринам и по всей вероятности, продукты щелочного окисления кофермента и эритроптерина идентичны и этим продуктом
является ксантоптерин-7-карбоновая кислота.
о н
0. Н
о к-Ј HMJUU)
НК| П№NaOH H2N N N СН2-С-СООН
АХ
HjN N ьГСООН
. Данные полярографического анализа кофермента, продукта щелочного окисления кофермента перманганатом калия,
эритроптерина, продукта щелочного окисления эритроптерина перманганатом калия (ксантоптерина-7-карбоновая кислота) представлены на рисунках 7-9. Как видно из рисунков 7 и 8, полярографические характеристики неокисленного коферментэ и неокисленного эритроптерина не совпадают, хотя после щелочного окисления их перманганатом калия они имеют идентичные полярографические характеристики, На этом
основании сделан вывод, что кофермент, хотя и близок по свойствам к эритроптерину, отличается от него и является 7-замещенным птериновым соединением.
Формул а изобретения
Способ выделения птеринового кофермента ферментной системы необратимого окислительного дезаминированмя L-глюта- мата, отличающийся тем, что семена
злаковых или бобовых растений экстрагируют водой при массообъемном соотношении 1:1-10, гомогёнат центрифугируют и очищают гель-хроматографией на декстрановых гелях с последующей ионообменной хроматографией на заряженном ионообменнике типа QAE-сефадексе или адсорбционной хроматографией на окиси алюминия.
9101 Я П 9 $1 01 Si 01 9


| название | год | авторы | номер документа |
|---|---|---|---|
| БЕЛОК, СОДЕРЖАЩИЙ МОЛИБДОКОФАКТОР, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1995 |
|
RU2100370C1 |
| Способ получения антибиотика @ -19393 @ и/или @ -19393 @ | 1980 |
|
SU1075984A3 |
| Способ получения антибиотического комплекса | 1978 |
|
SU1039446A3 |
| Фармацевтическая композиция иммуностимулирующих веществ мурамилпептидной природы | 2021 |
|
RU2768484C1 |
| Способ выделения ингибитора ангиотензин-1-превращающего фермента из яда животного происхождения | 1990 |
|
SU1730088A1 |
| СПОСОБ ПОЛУЧЕНИЯ СУБСТАНЦИИ L-ЛИЗИН-АЛЬФА-ОКСИДАЗЫ | 2011 |
|
RU2471866C1 |
| Способ получения клавулановой кислоты и ее солей | 1976 |
|
SU695565A3 |
| Способ хроматографического анализа органических веществ | 2019 |
|
RU2719638C1 |
| Способ получения антибиотика | 1978 |
|
SU738517A3 |
| Способ получения производных 7-аминоцеф-3-ем-4-карбоновой кислоты | 1971 |
|
SU468428A3 |
Использование: в биохимии и энзимоло- гии. Сущность изобретения: способ выделения птеринового кофермента ферментной системы необратимого окислительного дезз- минирования L-глютамата. Семена злаковых и бобовых растений экстрагируют водой при массо-обьемном соотношении 1:1-10, гомо- генат центрифугируют, очищают гель-хрома- тографией на заряженном ионообменнике типа QAE-сефадекс или адсорбционной хро- матографией на окиси алюминия. 9 фиг.
6Т0181
т: ж т w w
fat/#a. волны, н ttФиг. 2
W J5W
ш тотшто м s® °G
фиа.З
300
350 Ш 500 Ш
,/НМ ФигА
Фив, 5
о о о
7 2 3
tnV
f
№ Ш
2 Ю 72 0# Фг/г. 7
Q О О
J
/г
| Диксон М., Уэбб Э | |||
| Ферменты, т | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Устройство для видения на расстоянии | 1915 |
|
SU1982A1 |
| - М.: Мир, с | |||
| Железобетонный фасонный камень для кладки стен | 1920 |
|
SU45A1 |
| ...;.., | |||
| г ..;.; .., | |||
Авторы
Даты
1993-04-23—Публикация
1990-02-05—Подача