Изобретение относится к способам получения ариловых эфиров аренкарбоновых кислот, в частности способа получения эфиров n-замещенных бензойных кислот и гидрохинона - жидкокристаллических веществ, которые находят применение в электронооп- тическихустройствах в качестве компонентов высокотемпературных нематических жидкокристаллических материалов.
Известен способ получения ариловых эфиров аренкарбоновых кислот, заключающийся в обработке гидроксиароматического соединения хлорангидридом или ангидридом карбоновой кислоты в присутствии основания. Наиболее близким по технической сущности и достигаемым результатам является способ получения эфиров п-замещен- ных бензойных кислот и гидрохинона общей формулы I
X- -C-0-Q-O-CHQ-X ,
где X N02, CI, алкокси Ci-Сю нормального строения. Получают I обработкой гидрохинона хлорангидридом карбоновой кислоты формулы л-ХСбН4СОС1(М) в пиридине, который играет роль растворителя и основания при 25° С в течение 24 ч при молярном соотношении хлорангидрид: гидрохинон 3 : 1 (II) получают при действии избытка SOCI2 на карбоновую кислоту n-XCeH4COOH (III). В случае Х-алкокси Ci-Сю HI получают алки- лированием этилового эфира п-оксибензой- ной кислоты алкилгалогенидом Ci-Cio нормального строения в присутствии 2 экв. КОН и молярном отношении алкилгалоге- нид: эфир 1,1 : 1 с последующим гидролизом сложного эфира III. Общий выход I
оо
««
°5
sj О 00
полкилгалогениду по четырем стадиям составляют 13-32 %.
Недостатками известного способа являются многостадийность, и, как следствие, большая трудоемкость, низкий общий выход, л.
Целью изобретения является увеличение выхода I и упрощение процесса за счет того, что I можно получить, минуя стадию соответствующих кислот III или хлорангид- ридов II. Поставленная цель достигается за счет способа получения эфиров п-замещен- ных бензойных кислот и гидрохинона общей формулы I, заключающегося во взаимодействии соответствующих алкоксииодбензо- лов, полученных алкированием иодфенола алкилгалогенидами в присутствии основания, или хлориодбензола или иоднитробен- зола с гидрохиноном в среде деметилформамида, содержащего 16-23 % по объему основания - триэтиламина в атмосфере окиси углерода в присутствии катализатора формулы PdY2. где Y - остаток низшей алифатической карбоновой кислоты при температуре 50-70° С и молярном соотношении компонентов арилиодид:гидрохинон : палладий 200-250 : 80-100 : 1 соответственно. Выход целевого продукта достигает 50-76 %.
Отличительными признаками процесса являются следующие. В качестве арилгало- генида используют алкоксииодбензол, полученный аклилированием иодфенола алкилгалогенидом в присутствии основания, или хлориодбензол или иод нитробензол, использование в качестве основания триэтиламина, а в качестве растворителя диметилформамида с добавлением 16-23 % основания и проведение процесса в атмосфере окиси углерода в присутствии катализатора формулы PdY2, где Y - остаток низшей алифатической кислоты при 50-70° С, молярном соотношении компонентов арилиодид: гидрохинон : палладий 200-250 : 80-100 : 1 соответственно, что позволяет упростить процесс и повысить выход целевого продукта.
Замещенный иодбензол необходим для осуществления катализируемой комплексами палладия реакции карбонилирования с образованием I и иодоводорода, Соединения палладия выполняют при этом роль предшественника катализатора реакции карбонилирования, применение комплексов с фосфиновыми лигандами приводит к увеличению продолжительности процесса, кроме того такие соединения палладия менее доступны. Применение других соединений палладия, например PdCla не приводит к упрощению процесса или повышению выхода продукта. Диметилформамид необходим для создания контакта между реагентами и для активации реагентов. Применение воды, гексана, бензола, дихлорэтана не приводит к получению I. Триэтиламин необходим для связывания образующегося в реакции иодоводорода. Проведение реакции с применением триэтиламина в количестве, меньшем 16 % по обьему приводит к
снижению выхода I. Увеличение содержания триэтиламина выше 23 % приводит к вытеснению окиси углерода и, вследствие этого, кснижению выхода). Увеличение температуры реакции выше 70° С приводит к
снижению выхода I, понижение температуры ниже 50° приводит к увеличению продолжительности процесса.
При уменьшении соотношения арилиодид : гидрохинон : ниже 200-250 : 80-100
образуется побочный продукт формулы
О
Х4°)-с-о-(о}-он
Увеличение указанного соотношения приводит к неоправданному увеличению расхода арилиодида.
При соотношении арилиодид: палладий более 250:1 выход 1 снижается, увеличение
соотношения выше 200 : 1 нецелесообразно, т. к. не приводит к увеличению выхода I, кроме того, неоправданно возрастает расход палладия.
Предлагаемый способ иллюстрируется
следующими примерами.
Пример 1. В термостатируемый реактор, заполненный осушенной окисью углерода, снабженный магнитной мешалкой, помещают 5 мл сухого диметилформамида, 1,01 г триэтиламина (23 % по объему), 0,22 г (2 ммоль) гидрохинона, 1,19г(5ммоль) п- хлориодбэнзола, перемешивают до полного растворения в атмосфере СО, добавляют 0,0056 г (0,0025 ммоля) Pd(OAc)2.
Соотношение иодхлорбензол: гидрохинон: катализатор - 200 : 80 : 1. Перемешивают реакционную смесь при 60° С, через 36 ч реакционную смесь разбавляют ацетоном (5 мл), охлаждают до 0° С, выпавшие кристаллы отфильтровывают, промывают МеОН, сушат над PaOs. Выход n-CICeH-iCOOCeH-t ОСОСеН4С1-п 0,73 г (94 %), т. пл. 226° С.
Пример 2-5 сведены в табл. 1. процесс проводят аналогично примеру 1.
Пример 6. В колбу, снабженную магнитной мешалкой, помещают 100 мл хлористого метилена, 100 мл воды, 4,4 г (0,02 моль) п-иодфенола, 6,63 г (0,03 моль) бромистого н-гептила, № 1,68 г (0,03 моль) КОН, перемешивали при 20-25° С 48 ч, экстрагировали, промыли КОН и водой, высушили, перегнали в вакууме, получили 5,04 г (выход 70 %) н-децилокси-п-иодбензола,В реактор (см, пример 1) помещают 7.5 мл сухого ди- метилформамида, 1,01 г триэтиламина, 0,22 г (2 ммоль) гидрохинона, 1,62 г (4,5 ммоль) n-децилоксииодбензола, перемешивают до полного растворения в атмосфере СО, добавляют 0,0045 г (0,02 ммоль) Pd(OAc)2. соотношение алкоксииодбензол :гидрохинон : катализатор 200 :100 : 1. Перемешивают при 70° С 30 ч, подкисляют СНзСООН, разбавляют водой до 50 мл, экстрагируют горячим гексаном (4-х 50 мл). Гексан промывают водой, отгоняют при атмосферном давле- нии до объема 30 мл, охлаждают до 0° С, выпавшие кристаллы отфильтровывают, сушат на воздухе. Выход (X n-CioH2iO) 1,17 г (93 %),т. пл. 120-1° С.
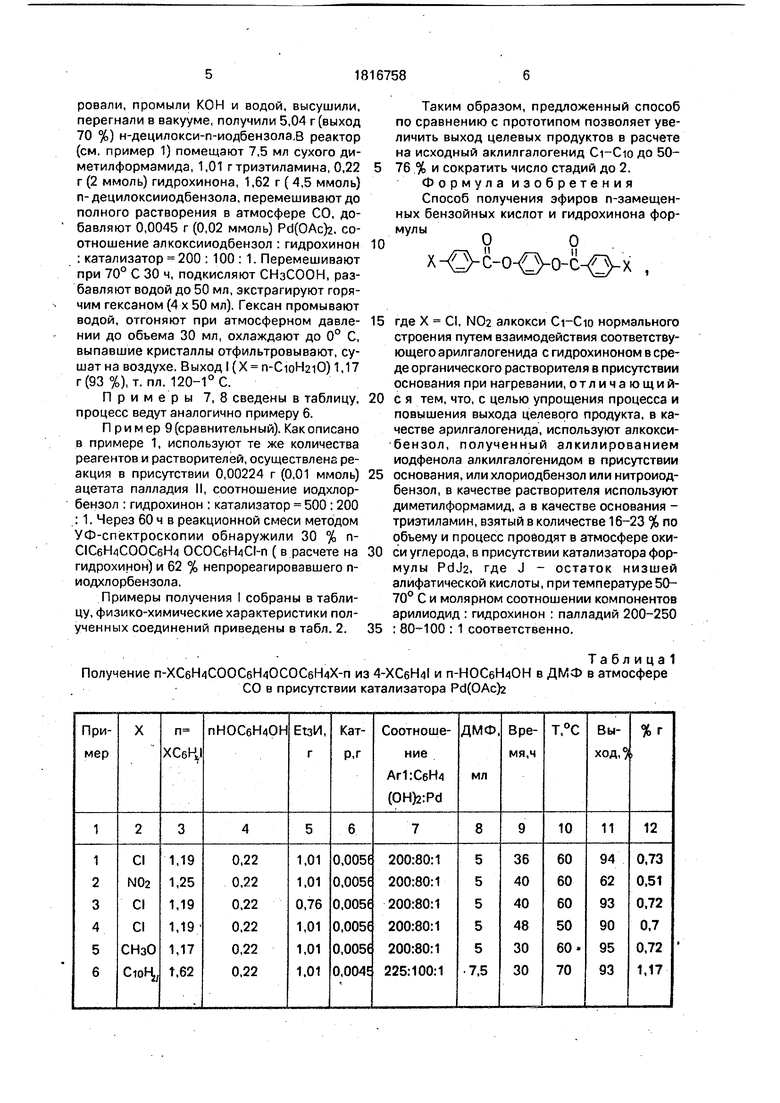
Примеры 7, 8 сведены в таблицу, процесс ведут аналогично примеру 6.
П р и м ер 9 (сравнительный). Как описано в примере 1, используют те же количества реагентов и растворителей, осуществлена реакция в присутствии 0,00224 г (0,01 ммоль) ацетата палладия II, соотношение иодхлор- бензол : гидрохинон : катализатор 500 : 200 .: 1. Через 60 ч в реакционной смеси методом УФ-спёктроскопии обнаружили 30 % п- С СбН4СООСбН4 ОСОСбН Оп ( в расчете на гидрохинон) и 62 % непрореагировавшего п- иодхлорбензола.
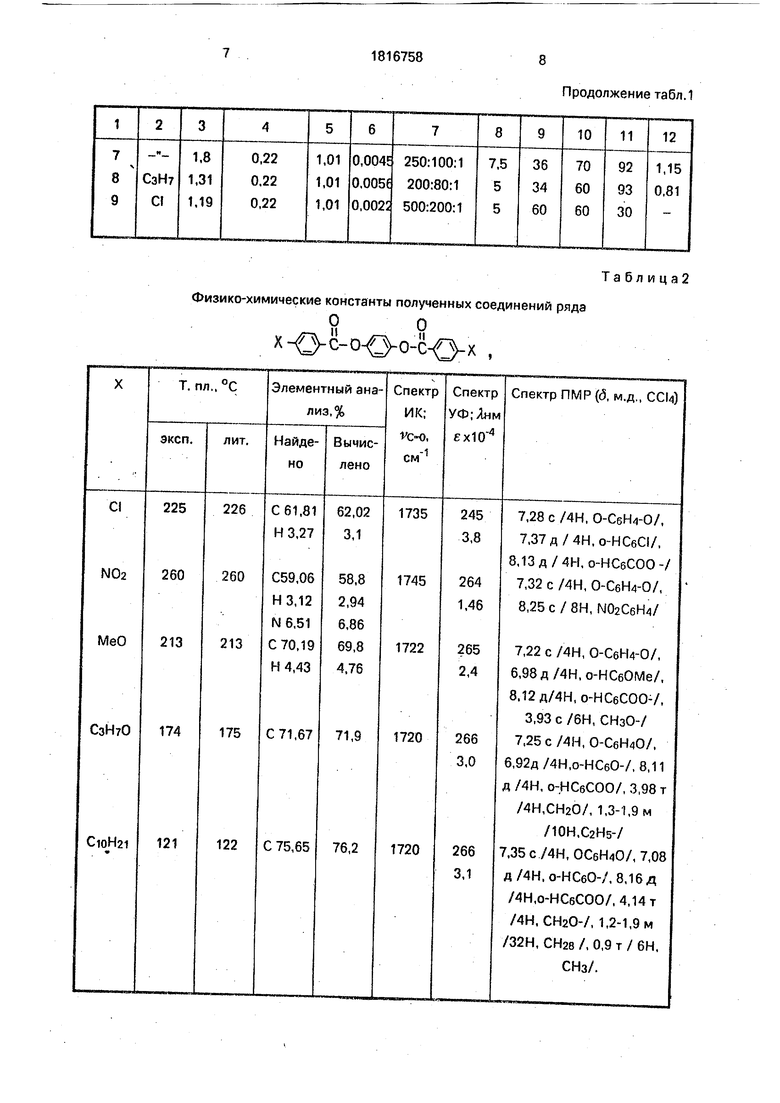
Примеры получения I собраны в таблицу, физико-химические характеристики полученных соединений приведены в табл. 2.
Таким образом, предложенный способ по сравнению с прототипом позволяет увеличить выход целевых продуктов в расчете на исходный аклилгалогенид Ci-Сю до 50- 76 % и сократить число стадий до 2. Ф о р м у л а и з о б р е те н и я Способ получения эфиров п-замещен- ных бензойных кислот и гидрохинона формулы
оо
где X С, N02 алкокси Ci-Сю нормального строения путем взаимодействия соответствующего арилгалогенида с гидрохиноном в среде органического растворителя в присутствии основания при нагревании, отличающий- с я тем, что, с целью упрощения процесса и повышения выхода целевого продукта, в качестве арилгалогенида, используют алкокси- бензол, полученный алкилированием иодфенола алкилгалогенидом в присутствии основания, илихлориодбензол или нитроиод- бензол, в качестве растворителя используют диметилформамид, а в качестве основания - триэтиламин, взятый в количестве 16-23 % по объему и процесс проводят в атмосфере окиси углерода, в присутствии катализатора фор- мулы PdJa, где J - остаток низшей алифатической кислоты, при температуре 50- 70° С и молярном соотношении компонентов арилиодид : гидрохинон : палладий 200-250 : 80-100 : 1 соответственно.

| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ САЛИЦИЛОВОЙ КИСЛОТЫ, ИХ АЛКИЛОВЫЕ ЭФИРЫ, СОДЕРЖАЩИЕ ОТ 1 ДО 6 АТОМОВ УГЛЕРОДА В ЭФИРНОЙ ГРУППЕ, СОЛИ И СОЛЬВАТЫ | 1992 |
|
RU2124501C1 |
| ПРОИЗВОДНЫЕ ХИНОКСАЛИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И СРЕДСТВО С КВИСКВАЛАТ-АНТАГОНИСТИЧЕСКИМ ДЕЙСТВИЕМ НА ИХ ОСНОВЕ | 1992 |
|
RU2117663C1 |
| БИАРИЛОКСИМЕТИЛАРЕНОВЫЕ КАРБОНОВЫЕ КИСЛОТЫ | 2004 |
|
RU2373187C2 |
| Способ получения 1-алкил-1( -алкоксикарбонилэтил)1,2,3,4,6,7,12,12в-октагидроиндоло (2,3-а) хинолизина или его солей | 1976 |
|
SU619107A3 |
| СПОСОБ ПОЛУЧЕНИЯ 5-(АЛЬФА-ГАЛОГЕНАЦЕТИЛ)-8-(ЗАМЕЩЕННЫЙ ОКСИ)-(1Н)-ХИНОЛИН-2-ОНОВ | 2004 |
|
RU2339621C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ВИНИЛОВЫХ ЭФИРОВ КИСЛОТ ФОСФОРА | 1971 |
|
SU420182A3 |
| ИМИДАЗОЛИЛЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ЦИКЛОГЕКСАНА ИЛИ ИХ СОЛИ | 1993 |
|
RU2110514C1 |
| АНТРАНИЛАМИДПИРИДИНАМИДЫ ИЗБИРАТЕЛЬНОГО ДЕЙСТВИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ VEGFR-2 И VEGFR-3 | 2002 |
|
RU2299208C2 |
| Способ получения производных аминокислот или их физиологически совместимых солей | 1987 |
|
SU1836335A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЦВЕТНЫХ ФОТОГРАФИЧЕСКИХ ИЗОБРАЖЕНИЙ | 1973 |
|
SU383336A1 |
Способ получения эфиров л-замещен- ных бензойных кислот и гидрохинона. Сущность изобретения: продукт -эфиры п-заме- щенных бензойных кислот и гидрохинона формулы оО x-sQ -c-o-0-o-c-0-x , где X CI; N02, алкокси Ci-Сю. Продукт 1 : БФ С20Н120 т. пл. 226° С. Продукт 2: БФ С40Н5406, т. пл. 120 + 1° С. Продукт 3: С22Н1806, т. пл. 213° С. Продукт 4: С26Н2606, т. пл. 175° С, пр. Реагент 1: ал- .коксииодбензол Ci-Сю или хлориодбензсл или нитроиодбензол. Реагент 2: гидрохинон. Условия реакции: диметилформамид, триэтиламин, взятый в количестве 16-23 % по объему, атмосфера СО. Катализатор Pdya, у -остаток низшей алифатической кислоты, температуры 50-70° С, молярное соотношение компонентов арилиодид : гидрохинон : палладий 200-250 : 80-100 : 1 соответственно. 2 табл. ел с
Таблица
Получение п-ХСбНзСООСбЩОСОСбН Х-п из 4-XCeH4l и п-НОСеН/ЮН в ДМФ в атмосфере
СО в присутствии катализатора Pd(OAc)2
Физико-химические константы полученных соединений ряда
оо x-O-c-i O 0-c-fVx ,
Продолжение табл.1
Таблица2
| Dewar M.I.S., Goldberg R.S | |||
| // Effects of Central and Terminal Groups on Nemati Mesophase Stobitlty | |||
| I.Org | |||
| Chem., V | |||
| Скоропечатный станок для печатания со стеклянных пластинок | 1922 |
|
SU35A1 |
| No | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Подставка для мыла | 1924 |
|
SU2711A1 |
| Пономарев А.Б | |||
| Катализируемое комплексами палладия кросссочетание и карбо- нилирование с участием производных Zn, AI, Си и органических галогенидов | |||
| Дисс | |||
| на Соискание ученой степени К.Х.Н | |||
| Пневматический водоподъемный аппарат-двигатель | 1917 |
|
SU1986A1 |
Авторы
Даты
1993-05-23—Публикация
1991-05-08—Подача