где R1-R5- как указано выше, и полученный продукт выделяют в виде аддитивной соли уксусной кислоты.
3. Способ получения цианпроизводных нафталинкарбоновых кислот общей формулы 111
соон
В:
а5
где. R и R вместе образуют метилендиок- сигруппу; R3 и R - низший алкоксил и R - низший алкоксил, отличающийся тем. что расщепляют изоксазольное кольцо соединения общей формулы Н
где R - галоген; R -R- - как указано выше, путем метал лирования.



Изобретение относится к химии гетероциклический соединений, в частности к способу получения производных эпиподофиллотоксина, которые могут быть использованы в качестве полупродуктов в синтезе аитинеопластических средств.
Целью изобретения является упрощение процесса.
Предлагаемый способ получения производных эпиподофиллотоксина общей формулы , Qli КТ
И;
где R1 и R2 вместе образуют метилендиок- сигруппу; R и R5 - низший алкоксил; и - низший а л кил, или его фармацевтически пригодной аддитивной соли состоит в том, что расщепляют изоксазольное кольцо соединения общей формулы Н
й
где R -R - как указано выше; R - галоген и R7- Н или алкил, путем метал лирования с образованием нитрила общей формулы Ж
Эй
где R1 - R5 и R7 - как указано выше, избирательно восстанавливают полученный нитрил формулы 1И с получением соединения общей формулы IV
Ч ЗШг
to
ft
где R1 - R4. R5 и R7 - как указано выше, при необходимости выделяют его в виде его аддитивной соли уксусной кислоты. Полученнов соединение формулы IV в форме кислоты подвергают циклизации путем диа- зотйрованип аминового радикала с последующей его лактонизацией.
Для получения аминометилпроизводных нафталинкарбоновых кислот формулы
IV избирательно восстанавливают нитрил
формулы Hi и полученный продукт выделяют
в виде аддитивной соли уксусной кислоты.
Для получения цианпроизводных нафталинкарбоновых кислот формулы Ш расщепляют изоксазольное кольцо соединения формулы tt путем металлирования.
И р и м е р 1. В суспензию хлоризокса- эолиновой кислоты (ГТд, где R и R вместе
-ОСНаО; R3 и R5 - ОСКз; R4 - СНз; R6 - a Л - Н) (2,00 г, 0.43 ммоль) б метаноле (100 мл) вводят никель Ренея («0.5 см3), взбалтывают в аппарате Парра при давлении водорода 2,94 кг/см в течение 4ч. В раствор
вводят окись платины рО мг), взбалтывают еще 2.5 ч, фильтруют через слой диатомовой земли, фильтрат выпаривают до получения твердого остатка (2 г). Анализ твердого остатка методом ТСХ (20% метанола в хлористом метилене) показывает, кроме исходной кислоты с Rf 0,53, два дополнительные компонента: основной с Rf 0,30 и неосновной с Rf 0,09. Основной компонент с Rf 0,30 выделяют в виде белого твердого вещества (0,9 г) на хроматографической колонке, элюируя смесью метанол-хлористый метилен (1:5). По- еле перекристализации из метанола получают аналитически чистый dl-{1 а , 2а , З/б , 4/2 -1,2,3,4-тетрагидро-3-циан-4-окси-1-{3,4,5- триметоксифенил)-нафталин-2-карбоновую кислоту (ША, где R1 и R2 вместе - OCHizO; R3 и R5 - ОСНз; R4 - СНз, R7 - Н), т.пл. 245- 246,5°С (разл.).
Вычислено, %: С 61,82; Н 4,95; N 3,28.
C22H21N08.
Найдено, %: С 61,67; Н 4,94; N 3,27.
Спектр 1Н-ЯМР(СОС1з, (5): 3,35(д.д., 1Н, 3,4 Гц, 12,4 Гц), 3,71 (д.д., 1Н, 12,5 Гц, 5.8 Гц), 3,74 (С..6Н), 3,78 (с.,ЗН), 4,55 (д.,1Н, 5,7 Гц), 4,98 (д., 1 Н, 3,2 Гц), 5,94 (м., 2Н), 6,11 (с., 2Н), 6,41 (с., 1Н), 6,86 (с., Ж).
ИК-спектр (KBг, ), 3490, 2920. 2240. 1750, 1590, 1500, 1485, 1240, 1130, 1035.
П р и м е р 2. В суспензию НА (1,40 г, 3,23 ммоль) в метаноле (200 мл) вводят ни- кель Ренея ( 1,0 см3) и гидрогенизируют в аппарате Парра в течение 2 ч при начальном давлении водорода 3,5 кг/см2. Катализатор отфильтровывают через диатомую землю, растворитель выпаривают в вакууме. Вод- ный раствор подкисляют 6 н. соляной кислотой и экстрагируют 10%-ным метанолом в хлористом метилене. Органические экстракты высушивают над сульфатом магния и выпаривают. Получают аморфное твердое вещество (0,8 г. 60%), спектр н-ЯМР которого идентичен спектру ША, полученного в примере 1.
П р и м е р 3. В суспензию НБ (R1 и R2 вместе - ОСН2О; R3 и R5 - ОСНз; К4 - СНз; R6 - Br; R7 - CaHs) (0,106 г, 0.2- ммоль) в этилацетате, насыщенную водой (20 мл) и метанолом {.15 мл), вводят борную кислоту (36 мг, 0.6 ммоль), а затем никель Ренея («0,1 см3). Суспензию гидрогенизируют в аппарате Парра при давлении водорода 2,8 кг/см3 в течение 6 ч. Анализ методом ТСХ (5% этилацетата в хлористом метилене) показывает, что кроме исходного эфира с Rf 0,61, имеется компонент с Rf 0,15. Катализа- тор отфильтровывают, фильтрат концентрируют до получения твердого вещества, которое хроматографируют на колонке с си- ликагелем, элюируя смесью 5% и 10% эти- лацетата с хлористым метиленом. Получают твердое аморфное вещество (54 мг) с Rf 0,15. После перекристаллизации из 95%-ного зтанола выделяют dl-(1«, la, 3/3, 4/ }-этил- 1,2,3,4-тетрагидро-3-циан-4-окси-1-(3,4,5триметоксифенил) -нафталин-2-карбокси- лат(И|Б, где R1 и R2 вместе - ОСНаО; R3 и R5 - ОСНз; R4 - СНз: R7 - С2Н5), т.пл. 215- 216°С.
Вычислено, %: С 63,29; Н 5,53; N 3,08.
C24H25N08.
Найдено, %: С 63,16; Н 5,59; N 3,02.
Спектр 1Н-ЯМР (CDCI3,): 1.17(т.. ЗН. 7,3 Гц), 2,62 (д., 1 Н, 4,4 Гц), 3,44 (д.д., 1 Н, 3,3 Гц, 12,4 Гц), 3,74 (м., 1Н), 3,74 (с., 6Н), 3,80 (с.. ЗН), 4,06 (к., 2Н, 7,1 Гц), 4,53 (д., 1Н, 5,9 Гц). 5,07 (т., 1Н, 3,8 Гц), 5,97 (д,д., 2Н), 6,03 (с., 2Н), 6,42 (с, 1Н), 6,85 (с., 1Н).
ИК-спектр (КВг, п,акс), 3560, 2245, 1725,1590,1230,1128.
Пример 4. Раствор ПБ (64 мг, 0,12 ммоль) в обезвоженном бензоле (5 мл) в атмосфере азота обрабатывают гидридом трибутилолова (0,12 мл, 0.45 ммоль) и 2,2- азобисизобутиронитрилом (2 мг). Смесь кипятят 6 ч с обратным холодильником, перемешивают при комнатной температуре в течение ночи, выпаривают в вакууме и остаток хроматографируют на колонке с си- ликагелем, элюируя смесью 5% и 15% этилацетата с хлористым метиленом. Соответствующие фракции соединяют и выпаривают в вакууме, получая ШБ. спектр 1Н-ЯМР которого идентичен спектру продукта, полученного в примере 3.
Пример 5. Суспензию НЕ. (106 мг, 0,2 ммоль) в 90%-ном водном метаноле (10 мл), содержащем концентрированную соляную кислоту (0;08 мл) и 10%-ный палладий на угле (10мг, 55% воды), гидрогенизируют при давлении водорода 1 атм в течение 24 ч, затем выдерживают пять дней. Катализатор отфильтровывают через диатомовую землю, нейтрализуют фильтрат (рН 7) насыщенным раствором бикарбоната натрия и упаривают в вакууме. Остаток хроматографируют в колонке с силикагелем, элюируя смесью 20% этилацетата с хлористым метиленом, и получают II(Б (40 мг). идентичный продукту, полученному в примере 3.
Пример 6. В раствор I д (92 мг, 0,2 ммоль) в смеси метанола (36 мл), хлористого метилена (10 мл) и воды (4 мл) вводят борид никеля (30 мг) и гидрогенизируют в аппарате Парра при начальном давлении водорода 2,8 кг/см в течение 16 ч.1 Катализатор отфильтровывают через диатомовую землю, упаривают фильтрат в вакууме и получают ША (90 мг), идентичный продукту, полученному в примере 1.
Пример 7. Раствор ША (0,50 г, 1,2 ммоль) в обезвоженном тетрагидрофуране (15 мл) вводят в атмосфере азота при 0°С и перемешивании в суспензию литийалюминийгйдрида (0,16 г, 4,2 ммоль) в тетрагидро- фуране (20 мл). После выдержки в течение 16 ч при комнатной температуре избыток литийалюминийгидрида разлагают водой (0,16 мл), 15%-ным раствором гидроокиси натрия (0,16 мл) и снова водой (0,48 мл).
Осадок отфильтровывают, тетрагидро- фуран удаляют в вакууме, водный раствор подкисляют до рН 6 добавлением 0,1 н. соляной кислоты и экстрагируют хлористым метиленом. Объединенные экстракты высушивают над сульфатом магния и выпаривают, получая dHlct ,2а ,3/, ,2,3,4-тетрагид- ро-3-аминометил-4-окси-1-(3,4,5-триметок- сифенил) -нафталин-2-карбоновую кислоту (IVA, где R1 и R2 вместе - ОСНаО; R3 и R5 - ОСНз: R4 - СНз; R7 - Н) (0,12 г, 24%). Часть продукта растворяют в смеси метанол-хлористый метилен (1:4) и пропускают через колонку с силикагелем. Колонку промывают метанолом (4 мл) и аминокислоту элюируют 10%-ной уксусной кислотой в метаноле (2 ил). Растворитель выпаривают, твердый остаток высушивают в глубоком вакууме при 78°С и получают целевое соединение в форме соли уксусной кислоты.
Вычислено, %: С 56,57; Н 6,13: N 2,75.
C22H25N08 СНзСООН Н2О.
Найдено, %: С 56,85; Н 6,28; N 2,68.
Спектр 1Н-ЯМР (CDCb, 3): 6.83 (с., 1Н), 6,32 (с., 1Н), 6,05 (с., 2Н). 5,88 (д.. 2Н), 4,86 (ш.п., 1Н), 4,10 {ш.п„ 1Н), 3,79 (с„ ЗН), 3,73 (с., 6Н), 3,26 (ш.п., 2Н), 3,13 (м., 1Н), 2,60 м., 1Н).2,30(м., 1Н).
Пример 8. В раствор НА (200 мг, 0,43 ммоль) в смеси метанол - вода - хлористый метилен (7:1:3, 100 мл) вводят борид никеля (60 мг, 0,86 ммоль) и гидрогенизируют в аппарате Парра при давлении водорода 2,8 кг/см2 в течение 18 ч. В раствор вводят окись платины (200 мг, 0,88 ммоль) и гидрогенизируют пр,и давлении 2,8 кг/см2 еще 2 ч. Анализ методом ТСХ (5% метанола в хлористом метилене) показывает отсутствие исходной кислоты (Rt 0,48) и наличие высокополярного компонента (Rf 0,07). Катализаторы отфильтровывают через диатомовую землю, фильтрат выпаривают, часть полученного сиропообразного продукта обрабатывают, как в примере 7, и получают соединение, идентичное соединению, указанному в примере 7, в виде аддитивной соли уксусной кислоты. Остаток сиропообразного продукта растворяют в 50%-ной уксусной кислоте (7 мл), добавляют раствор
нитрита натрия (200 мг, 2,9 ммоль) в воде (8 мл). После перемешивания при комнатной температуре в течение 4 ч осторожно добавляют насыщенный водный раствор бикарбоната натрия (20 мл) и экстрагируют
хлористым метиленом (5 х 30 мл). Объедит ненные экстракты высушивают над сульфатом натрия, фильтруют и выпаривают, получая светло-желтое твердое вещество (84 мг). которое по данным ТСХ представляет собой однородный продукт - df-эпиподо- филлотоксин (А, где R1 и R вместе -ОСН2О; R3 и R5 - ОСНз; R - СНз).
Спектр Н-ЯМР (CDCI3, 5): 2,86 (м.. 1Н), 3,29 (д.д., 1Н, 5,1 Гц, 14,1 Гц), 3,75 (с., 6Н),
3,81 (с., ЗН), 4,38 (м., 2Н), 4,63 (д.. 1Н, 6,1 Гц), 6,00(д., 2Н), 6,29 (с., 2Н), 6,56{с.. Ж), 6,89 (с., 1Н).
Указанные характеристики согласуются с данными эпиподофиллотоксина.
П р и м е р 9. Раствор 1Нд (0,25 г, 0,58 ммоль) в обезвоженном тетрагидрофуране (7 мл) вводят в атмосфере азота в охлажденный раствор литийалюминийгидрида (0,08 г, 2 ммоль) в тетрагидрофуране (20 мл), перемешивают 16 ч при комнатной температуре и добавляют раствор уксусной кислоты в воде (10 мл) в объемном отношении 1:1. Тет- рагидрофуран выпаривают в вакууме, добавляют к остатку раствор нитрата натрия
(200 мл, 2,9 ммоль) в воде (1 мл), перемешивают 1 ч при комнатной температуре, нейтрализуют насыщенным водным раствором бикарбоната натрия и экстрагируют хлористым метиленом. Объединенные органичёские экстракты высушивают над сульфатом магния и выпаривают, получая эпиподофил- лотоксин (0,21 г, 87%) в виде светло-коричневой пены. Спектр Н-ЯМР этого продукта идентичен спектру эпиподофиллотоксина,
полученного в примере 8.
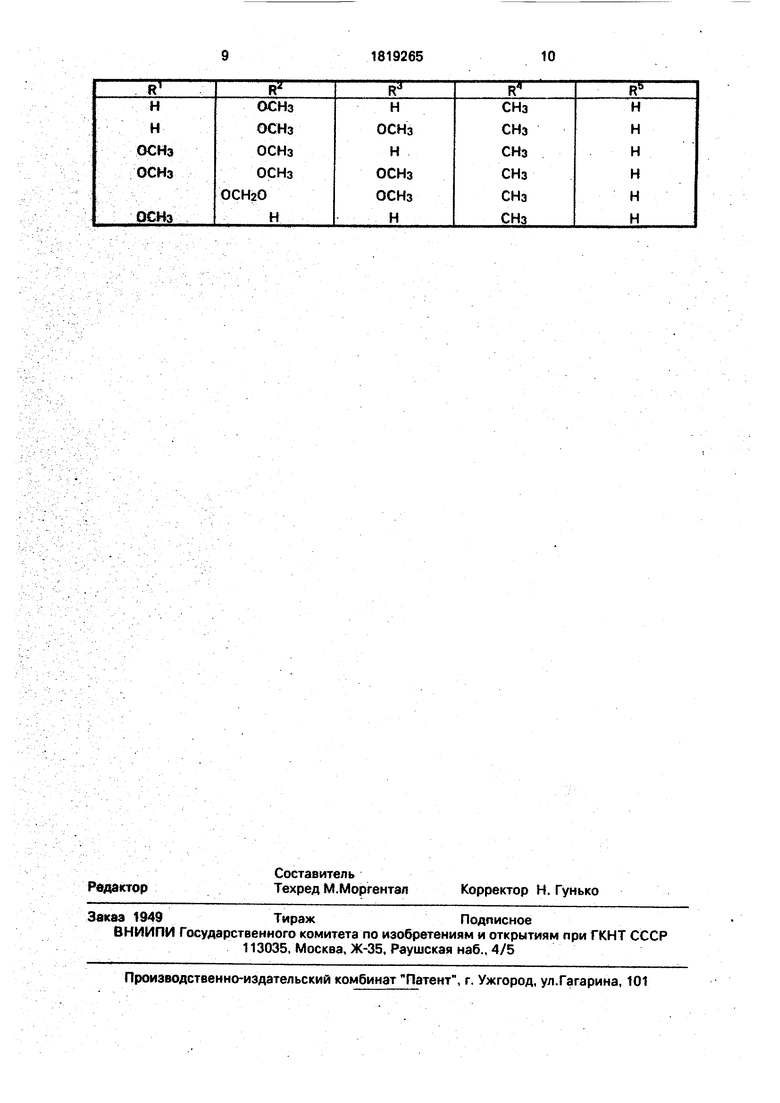
Пример 10. Аналогично получают соединения формулы f, перечисленные в таблице.
Предлагаемый способ позволяет получить соединения формулы I по более простой технологии, т.е. сократить число стадий до 4 против II в известном способе.

| - Org | |||
| Chem., т | |||
| Способ очистки нефти и нефтяных продуктов и уничтожения их флюоресценции | 1921 |
|
SU31A1 |
| УСТРОЙСТВО ДЛЯ ЗАЩИТЫ ПОДВАЛЬНЫХ СТЕН ОТ СЫРОСТИ | 1925 |
|
SU4004A1 |
| J | |||
| Org | |||
| Chem., т | |||
| Железобетонный фасонный камень для кладки стен | 1920 |
|
SU45A1 |
| Способ получения фтористых солей | 1914 |
|
SU1980A1 |
| Устройство для замачивания кукурузы | 1925 |
|
SU4538A1 |
Авторы
Даты
1993-05-30—Публикация
1986-04-11—Подача