сл
с

Сущность изобретения: продукт: 1-фе- нил-4, 5-бис-(4-нитробензоилоксиметил Н, 2,3-триазол,БФС24Н1708М5. Выход: 85%, т. пл, 188-189° С. Реагент 1:1, 4-бис-(4-нит- робензоилокси)-бутин-2, реагент 2: фенила- зид, Условия реакции1 в среде толуола при температуре кипения 1 табл
Данное изобретение относится к синтезу новых производных 1, 2, 3-триазола, в частности к синтезу 1-фенил-4, 5-бис(4-нит- робензоилоксиметил)-1.2, 3-триазол формуЛЫ1 ,-Л
о
,-о-с- оУыоо
обладающему противовоспалительной активностью.
Целью изобретения является синтез нового производного 1, 2. 3-триазола, обладающий большой активностью, чем известные структурные аналоги подобного действия.
Поставленная цель достигается получением 1-фенил-4, 5-бис-(4-нитробензоилок- симетил)-1, 2, 3-триазола.
Пример 1. Нижеследующий пример иллюстрирует способ получения нового соединения: э круглодонную колбу со шлифом помещают 4,99 (0,01 г-моль) 1, 4-бис(4-нит- робензолилокси}-бутин-2, растворенного в 20 мл сухого толуола, затем добавляют 1,309 г (0,011 моля) сзжеперегнанного фенилази- да. Соединив колбу с обратным водяным холодильником, снабженным хлоркальцие- вой трубкой, нагревают при температуре кипения реакционной смеси Ход реакции контролируют тонкослойной хроматографией. После окончания реакции (нагревают в течение 5 часов), растворитель упаривают, остаток перекристаллизовывают в гептане Выход 5,25 г (85 %). Полученное вещестзо представляет собой кристаллы желтого цвета без запаха, не растворимые в органических растворителях.
Индивидуальность проверялась ТСХ на AljOa 11 ст. активности в системе эфир гек- сан(5 :3). Rf-0,41 Т пл 188 189° С
00 К) 00
IQO |о о
Строение доказано данными элементного анализа. ИК-спектроскопией. Найдено. %:
С 57,29 Н 3,31 N 13,98. Вычислено для C24Hi7NsOe, %:
57,21 3,33 13,96
С 57,25 Н 3,37 N 13,91
8 ИК-спектре полученного соединения имеются полосы поглощения, которые характерны колебаниям ароматических гетероциклических колец (3200. 1550, 1450, 1270,910см 1).
Изучение на противовоспалительную активность проводились на белых крысах (масса 175-200 г) смешанной популяции, воспаление вызывалось формалином, который вводили под апоневроз галеностопного суставе 0,2 мл 1 %-ного раствора. Объем лапки крыс измеряли онкометрически 3 раза до и через 3, 6, 24, 48 и 72 часа после введения формалина.
Испытуемое соединение вводилось через рот (перорально) с помощью металлического зонда в виде масляного раствора. 3-5% -ные раствора препараты вводились из расчета 0,1 мл на 100 г массы тела животного в дозах 25,50 и 100 мг/кг. Они вводились по определенной схеме: четыре раза до вызывания воспаления: т. е. за 72, 48, 24 часа и 2 часа до введения формалина.
Для сравнения были взяты известные противовоспалительные средства - амидопирин, бутадион, индометацин, вольтарен.
В результате проведенных исследований установлено, что препарат 1-фенил-4, 5-бис(4-нитробензоилоксиметил)-1,2,3-три- азол в дозе 25мг/кг снижает воспаление на 37,0 %, в дозе 50 мг/кг на 59,3 %, в дозе 100 мг/кг на 39,0 %. В то время как амидопирин в дозе 100 мг/кг снижает воспаление на 25 %, индометацин в дозе 100 мг/кг - 28,0 %, вольтарен в дозе 25 мг/кг 39,4 %, бутадион в дозе 100 мг/кг - 26,1 %. Эти препараты использовались в тех дозах при которых согласно литературным данным проявляют наибольшую активность.
Токсичность излучали на белых мышах обоего пола массой 18-23 г. Вещество вводили в виде 1-10 % маслянного раствора подкожно. Обьем вводимого раствора не превышал 1 мл. Значение средней смертельной дозы (ЛДзд) определяли по методу Литчифильда Уилкоксона при Р 0,04.
Установлено, что описываемое соединение малотоксично. Оно даже в дозе 2500 мг/кг не вызывало гибели животных, в то время как амидопирин имеет ЛДзд 225 мг/кг, бутадиен ЛДзд 430 (344-538) мг/кг,
индометэцин ЛДю 47 (344-525) мг/кг, вольтарен ЛДво 370 (247-555) мг/кг.
Из приведенных данных следует, что 1- фенил-4, 5-бис(4-нитробензоилоксиметил)- 1, 2, 3-триазол проявляет более высокую
противовоспалительную активность по сравнению с амидопирином, бутадиеном, индометацином, вольтареном (базовый обь- ) и со структурными аналогами, которые в дозе 100 мг/кг (соединение 2) снижает
формалиновое воспаление на 56 % и соединение 3 в дозе 100 мг/кг снижает формалиновое воспаление на 59,6 %,
Новое соединение имеет более высокий индекс терапевтической широты (50, чем соединение 2 (25), амидопирин (2,25), вольтарен (14,8), индометацин (4,7), бутадион (4,3, соединение 3 (35),
Формула изобретения 1-Фенил-4,5-бис-(4-нитробензоилокси
метил Т.З-триазол формулы
оо
(О)- С-0-СН-,- ,- О- СЧО)
г V-T9
45
обладающий противовоспалительной активностью,
51828860б
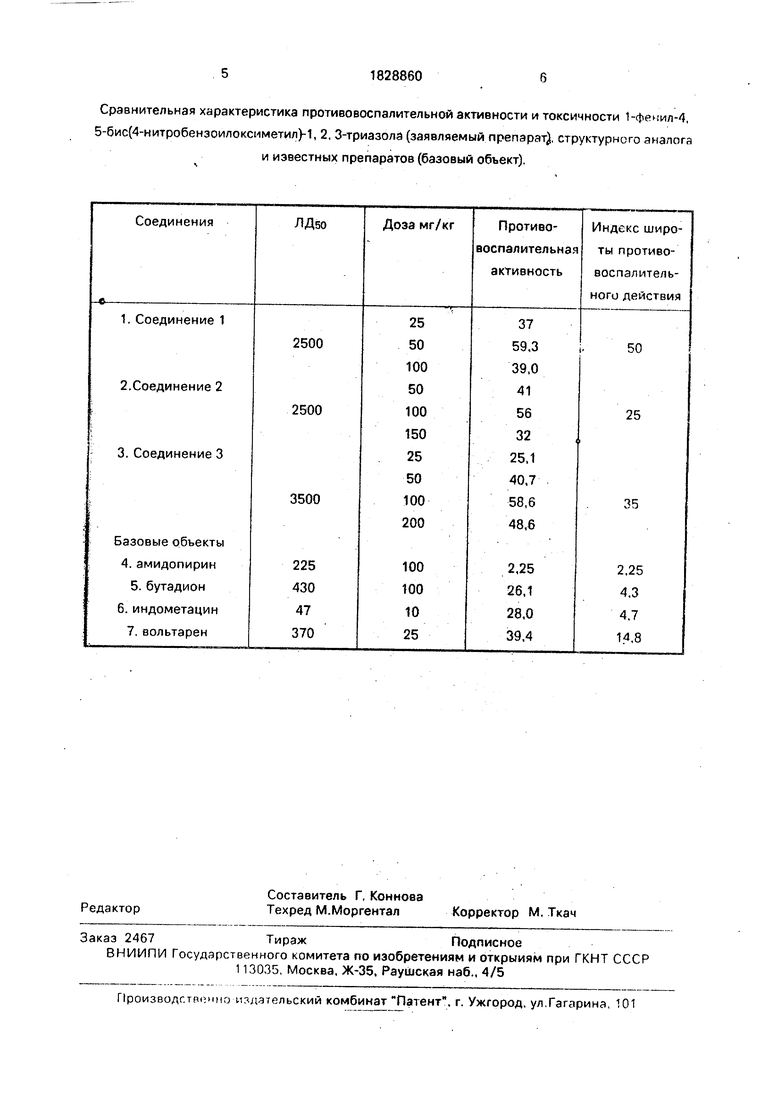
Сравнительная характеристика противовоспалительной активности и токсичности 1-фенил-4, 5-бис(4-нитробензоилоксиметил)-1, 2, 3-триазола (заявляемый препарат), структурного аналога
и известных препаратов (базовый обьект).
| Авторское свидетельство СССР №1334667, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Авторское свидетельство СССР № 1769517, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1993-07-23—Публикация
1990-12-04—Подача