Данное изобретение дает возможность получить группу соединений, которые могут представить интерес для изысканий новых полупродуктов и красителей.
Предлагается способ получения сульфидов 1,2-антрахинондиазолов общей формулы I,
О N-X
.0 R
где X-О или S; R-Н или галоид; А-ароматический или гетероциклический остаток, который может содержать различные заместители, например алкил-, карбокси-, галоид-, нитро-, ацилампногруппы, состоящий в том, что 1,2-антрахинондиазол общей формулы И
О Мгде R-Н или галоид, а Хп R имеют значения, указанные в формуле I, нагревают с меркаптаном в среде последнего или в подходящем органическом растворителе, например диметилформамиде или этиленгликоле, с последующей обработкой окислителем, например хлорным железом, азотистой или хромовой кислотой. Пример 1. В раствор 2,5 г антрахиноноксадиазола (II, X-О, R R-Н) в 40 мл диметилформамида добавляют 1,65 г тиофенола и кипятят 2 мин, после чего вливают 40 мл 20п/о-ного раствора хлорного железа. Образовавщуюся суспензию кипятят еще 2-3 мин,
охлаждают и фильтруют. Оранжево-красные иглы фенилсульфида формулы I X-О, R-Н, А-СбНз, 4-фенилтиоантра-(1,2-е)-(1,2,5)-оксадиазол-6,11-дион отфильтровывают и промывают спиртом. Выход 3,49 г (97о/о), т. пл.
255,5-256,5°С.
Пример 2. Раствор 2,56 г антрахинонтиадиазола (II, X-S, ) и 1,65 г тиофенола в 100 мл диметилформамида кипятят
3 мин, затем охлаждают до 100°С, вливают 25 мл 400/о-ного раствора хлорного железа и продоллсают кипячение еще 5 мин. По охлаждении фенилсульфид антрахинонтиадиазола (II, X-S, R-Н, ) отделяют и промывые иглы (из уксусной кислоты), т. пл. 270- 27ГС.
Прим ер 3. Раствор 2,9 г 4-хлорантрахинонтиадиазола (П, X-S, R-С1, R-Н) и 1,65 г тиофенола в 120 мл диметилформамида кипятят 5 MUH.J разбавляют 30 мл воды и охлаждают. Выход фенилсульфида (I, X-S, R-H, А-СбНз) 3,0 г (83о/о).
Пример 4. Смесь 2,5 г 4-хлорантрахиноноксадиазола (II, X-О, R-С1, R-Н), 75 мл этиленгликоля и 1,8 г л-тиокрезола нагревают при 160°С в течение 30 мин, охлаждают до 90°С и разбавляют горячей водой. Выход
сульфида (I, X-О, R-Н, А-rt-CHsCgHi) 3,0 г (84о/о).
Пример 5. Раствор 2,5 г антрахиноноксадназола (П, X-О, R-R H) кипятят с тисфенолом в растворе диметилформамида (см. пример 1), охлаждают до 100°С, разбавляют 20 мл 50/о-ной соляной кислоты и при кипячении по каплям приливают 5 мл ЗОа/О-ного раствора нитрита натрия. Осадок продукта (I, X-О, R-Н, А-СбНб) отделяют, промывают водой и спиртом. Выход 3,18 г условиях, описанных в примерах 1-5, получают также сульфиды антрахинондиазолов общей формулы I, указанные в таблице.
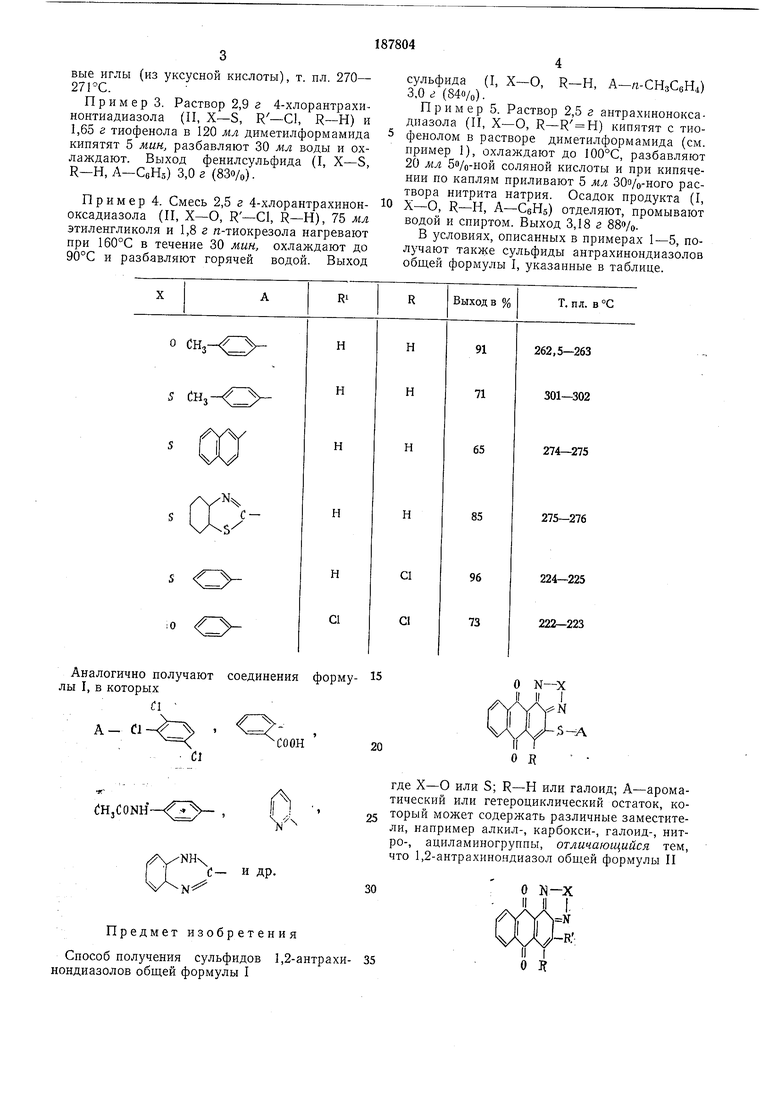

Аналогично получают соединения форму- 15 лы I, в которых .VNH С- и др. предмет изобретения 25 О N-X где X-О или S; R-Н или галоид; А-ароматический или гетероциклический остаток, который может содержать различные заместители, например алкил-, карбокси-, галоид-, нитРО-, ациламиногруипы, отличающийся тем, что 1,2-антрахинондиазол общей формулы II О N-X 5б
где R-Н или галоид, а X и R имеют значе-миде, этиленгликоле, с последующей обработния, указанные в формуле I, нагревают с мер-кой реакционной массы окислит лем, наприкаптаном в среде последнего или в органиче-мер хлорным железом, азотистой или хромоском растворителе, например диметилформа-вой кислотой.
187804 

Даты
1966-01-01—Публикация