Изобретение относится к области получения соединений, которые могут найти применение в качестве гербицидов.
Предлагается способ получения производных тиазола общей формулы
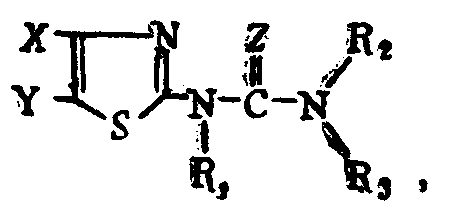
где X и Y - одинаковые или различные заместители и могут представлять собой водород, галоген, группу родана, циана, карбоксила, алкоксикарбонила, аминную, гидроксила, оксиалкила, алкила или алкоксила с содержанием С 1-4, причем эта группа может быть замещена или не замещена галогеном, группу арильную, арильную галогенированную, алкиларильную, алкоксиарильную, алкиларильную галогенированную, алкоксиарильную галогенированную, арилоксильную, арилоксильную галогенированную, алкиларилоксильную;
Z - кислород или сера;
R1 - водород, алкильная, алкоксильная, алкенильная, алкеноксильная или алкинильная группа с содержанием 1-4 атомов углерода;
R2 и R3 - каждый в отдельности водород, алкильная, алкоксильная алкенильная, алкеноксильная, алкинильная группа с С 1-4 или алкиларильный, алкиларильный галогенированный, арильный, арильный галогенированный или арилоксильный остаток. Способ заключается в том, что 2-аминотиазолы обрабатывают изоцианатами, изотиоцианатами либо галогенангидридами карбаминовой или тиокарбаминовой кислоты.
Пример 1. Синтез N-(5-хлортиазолил-2)-N′-метилмочевины.
К раствору 9,5 г 2-амино-5-хлортиазола в 35 мл диметилсульфоксида при интенсивном перемешивании приливают по каплям 4,8 г метилизоцианата. При этом температура возрастает примерно до 56°С. Когда смешение закончено, смесь охлаждают до 45°С и выдерживают при указанной температуре 1 час путем соответствующего нагревания. Затем отгоняют растворитель в вакууме, остаток растворяют в 500 мл кипящего ацетона в присутствии растительной черни и горячий раствор фильтруют, по охлаждении которого выпадают белые блестящие кристаллы. Это соединение отсасывают на нутч-фильтре и высушивают. Температура плавления его 271-271,5°С, выход около 50 вес. % по отношению к исходному амину.
C5H6ClN3OS.
Найдено, %: С 31,83; Н 3,19; Cl 18,39; S 16,70.
Вычислено, %: С 31,33; Н 3,15; Cl 18,50; S 16,73.
Пример 2. Синтез N-(5-хлор-4-метилтиазолил-2)-N1-фенилмочевины.
Растворяют 5 г 2-амино-5-хлор-4-метилтиазола в 50 мл ацетонитрила. К этому раствору приливают по каплям 4,1 г фенилизоцианата при комнатной температуре. Под конец приливания постепенно нагревают смесь до 50°С и выдерживают при этой температуре в течение 2 час. Смесь охлаждают и осадок отделяют на нутч-фильтре. Осадок перекристаллизовывают из ацетонитрила и обесцвечивают растительной чернью. Получают 6,75 г белого порошка с т.пл. 252°С и выходом 75 вес. %.
C11H10ClN3OS.
Найдено, %: С 49,34; Н 3,76; N 15,70; Cl 13 25.
Вычислено, %: С 49,46; Н 3,62; N 15,90; Cl 13,29.
Пример 3. Синтез N-(5-метилтиазолил-2)-N′-фенилмочевины.
К суспензии 7 г 2-амино-5-метилтиазола в 50 мл ацетонитрила приливают медленно 7,7 г фенилизоцианата. Температура постепенно возрастает до 48°С, причем амин полностью растворяется. Полученный раствор выдерживают 20 мин при 48°С, при этом вновь выпадает нерастворимое вещество. Наконец вся масса застывает. Ее оставляют на 4 час, отфильтровывают на нутч-фильтре, промывают кристаллы ацетонитрилом и высушивают в вакууме. Получают 12,45 г (87 вес. %) белого кристаллического порошка с т.пл. 195-196°С.
Пример 4. Синтез N-(тиазолил-2)-N′-фенилмочевины.
Так же, как это было описано в примере 3, получают N-(тиазолил-2)-N′-фенилмочевину в виде тонкого белого порошка. Выход сырого продукта 96%, т.пл. 171°С. После перекристаллизации из 50%-ной уксусной кислоты температура плавления возрастает до 173°С.
C19H9N3OS.
Вычислено, %: С 54,78; Н 4,14; N 19,16; S 14,62.
Найдено, %: С 54,77; Н 3,91; N 19,23; S 14,48.
Пример 5. Синтез N-(тиазолил-2)-N′-метилмочевины.
К суспензии 10 г 2-аминотиазола в 25 мл ацетонитрила с содержанием 2 капель триэтиламина медленно приливают 6 г метилизоцианата. Реакция слабо экзотермическая и температура возрастает до 66°С. После приливания смесь охлаждают до 50°С. Эту температуру выдерживают 1 час 15 мин, причем N-(тиазолил-2)-N′-метилмочевина выпадает в виде белого кристаллического осадка. Его отфильтровывают на нутч-фильтре и высушивают в вакууме. Выход сырого продукта 15,45 г (78%) т.пл. 215°С. После перекристаллизации из абсолютного спирта при - 30°С температура плавления возрастает до 218°С. Получают белые блестящие иглы с общим выходом 94%.
C5H7N3OS.
Найдено, %: С 37,77; Н 4,35; N 28,84; О 10,52; S 20,9.
Вычислено, %: С 38,2; Н 4,49; N 28,73; О 10,18; S 20,4.
Пример 6. Синтез N-(5-родантиазолил-2)-N′-метилмочевины.
В 580 мл ацетонитрила при 80°С растворяют 33,6 г 2-амино-5-родантиазола и приливают при энергичном перемешивании в этот раствор 17,1 г метилизоцианата. Перемешивание и нагревание продолжают еще 8 час так, чтобы температура держалась все время на 80°С. После охлаждения выпадает, замещенная мочевина в форме тонкого слабоокрашенного в розовый цвет порошка, который отфильтровывают на нутче и сушат. Выход сырого продукта 38,9 г (86,5%), т. пл. 225°С. Перекристаллизацией из метанола получают тонкие небольшие блестящие светло-желтые пластиночки с т.пл. 226°С.
C6H6N4O2S.
Найдено, %: С 33,42; Н 2,74; N 25,96; S 29,9.
Вычислено, %: С 33,63; Н 2,82; N 26,15; S 29,92.
Пример 7. Синтез N-(5-карбэтокси-4-метилтиазолил-2)-N1-метилмочевины.
Опыт проводят так же, как в примере 1, но с применением метилизоцианата и 2-амино-4-метил-5-карбэтокситиазола. Получают соединение, которое после перекристаллизации из этанола имеет т.пл. 262°С, выход 75,5%.
C9H13N3O3S.
Найдено, %: С 44,03; Н 4,83; N 17,44; О 19,92; S 43,5.
Вычислено, %: С 44,43; Н 5,38; N 17,27; О 19,72; S 13,17.
Пример 8. Синтез N-(4-метилтиазолил-2)-N-метилмочевины.
По примеру 5, но с применением метилизоцианата и 2-амино-4-метилтиазола как исходных веществ получают соединение, которое плавится после перекристаллизации из ацетонитрила при 212°С. Выход его 93%.
C6H9N3OS.
Найдено, %: С 41,81; Н 5,08; N 24,83; О 9,32; S 18,67.
Вычислено, %: С 42,09; Н 5,30; N 25,54; О 9,34; S 18,73.
Пример 9. Синтез N-(4-трифторметилтиазолил-2)-N1-метилмочевины.
По примеру 6, но с применением метилизоцианата и 2-амино-4-трифторметилтиазола в качестве реактивов получают соединение, которое после перекристаллизации из изопропилового спирта плавится при 254°С, выход 57%.
C6H6F3N3OS.
Найдено, %: С 32,23; Н 2,88; N 18,76; F 25,2; S 14,45.
Вычислено, %: С 32; Н 2,69; N 18,66; F 25,31; S 14,24.
Пример 10. Синтез N-[4-(n-хлорфенил)тиазолил-2]-N1-метилмочевины.
По примеру 5 получают, беря метилизоцианат и 2-амино-4-(n-хлорфенил)тиазол, соединение с т.пл. 232,5°С (после перекристаллизации из ацетонитрила) и выходом 97%.
C10H11ClN3OS.
Найдено, %: С 49,16; Н 3,64; Cl 13,30; N 15,52; S 11,96.
Вычислено, %: С 49,34; Н 3,76; Cl 13,24; N 15,69; S 11,97.
Пример 11. Синтез N-(5-хлор-4-метилтиазолил-2)-N′-метилмочевины.
Смешивают 6,1 г хлоргидрата 2-амино-5-хлор-4-метилтиазола и 25 мл пиридина и нагревают до 35-40°С. После этого добавляют 2,1 г метилизоцианата за 15 мин. Смесь перемешивают и нагревают 3 час при 50°С. После охлаждения быстро выливают смесь на лед. Выпавший осадок отделяют на нутч-фильтре и перекристаллизовывают из ацетонитрила. Получают конечный продукт в виде белого порошка с т.пл. 273°С и выходом 75%.
C6H8ClN3OS.
Найдено, %:С 35,06; Н 3,7; N 20,23; Cl 17,09; S 15,64.
Вычислено, %: С 35,04; Н 3,92; N 20,43; Cl 17,24; S 15,59.
Пример 12. Синтез N-(5-хлортиазолил-2)-N′-метилтиомочевины.
1,5 г метилизотиоцианата и 2,7 г 2-амино-5-хлортиазола растворяют в 42 г пиридина. Этот раствор нагревают 5 час с обратным холодильником и после охлаждения выливают в избыток воды. Образовавшийся осадок отфильтровывают, обильно промывают водой и высушивают. Полученная N-(5-хлортиазолил-2)-N′-метилтиомочевина после перекристаллизации из ацетона и обработки растительной чернью плавится при 199°С.
C5H6ClN3S2.
Найдено, %: С 29,56; Н 3; N 20,17; Cl 16,59; S 31,12.
Вычислено, %: С 20,91; Н 2,91; N 20,23; Cl 17,06; S 30,87.
Пример 13. Синтез N-(5-хлор-4-метилтиазолил-2)-N,N′-диметилмочевины.
Смесь 38,4 г пиридина и 22,7 г хлорангидрида диметилкарбаминовой кислоты охлаждают до 5°С и к смеси небольшими частями добавляют 29,7 г 2-амино-5-хлор-4-метилтиазола. Реакция слабоэкзотермическая и температура возрастает. Оставляют реакционную смесь на 1 час, а затем ее нагревают 3 час при 60°С. После охлаждения смесь выливают в 1 л ледяной воды при энергичном перемешивании так, чтобы продукт не осел. Образовавшиеся бурые кристаллы отсасывают на нутч-фильтре и перекристаллизовывают из 1,5 л 50%-ной уксусной кислоты. Их отфильтровывают и промывают водой до нейтральной реакции. Полученное соединение плавится при 163°С, выход 42,5%.
C7H10ClN3OS.
Найдено, % С 38,29; Н 4,22; Cl 16,15; S 14,59.
Вычислено, %: С 38,26; Н 4,59; Cl 16,15; S 14,59.
Пример 14. Синтез N-(4,5-диметилтиазолил-2)-N1-метилмочевины.
По примеру 5 из 2-амино-4,5-диметилтиазола и метилизоцианата получают соединение, которое плавится при 184,5°С после перекристаллизации из ацетона, выход 84%.
C7H11N3OS.
Найдено, %: С 45,33; Н 5,66; N 22,97; О 8,83.
Вычислено, %: С 45,38; Н 5,98; N 22,67; О 8,63.
Способ получения производных тиазола общей формулы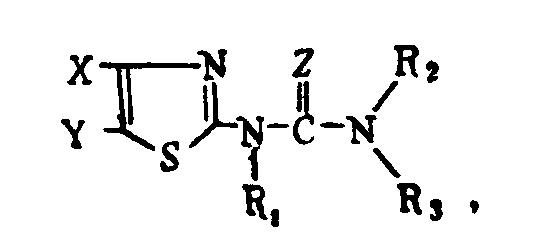
где X и Y являются одинаковыми или различными заместителями и могут представлять собой водород, галоген, группу родана, циана, карбоксила, алкоксикарбонила, аминную, гидроксила, оксиалкила, алкила или алкоксила с содержанием С 1-4, причем эта группа может быть замещена галогеном или не замещена, арильную, галогенированную арильную, алкиларильную, алкоксиарильную, алкиларильную галогенированную, алкоксиарильную галогенированную, арилоксильную, арилоксильную галогенированную или алкиларилоксильную группу; Z - кислород или сера; R1 - водород, алкоксильная, алкильная, алкенильная, алкеноксильная, алкинильная группы с С 1-4; R2 и R3 каждый в отдельности водород, алкильная, алкоксильная, алкенильная, алкеноксильная, алкинильная группа с С 1-4 или алкиларильный, алкиларильный галогенированный, арильный, арильный галогенированный или арилоксильный остаток, отличающийся тем, что 2-аминотиазол обрабатывают изоцианатом, изотиоцианатом или галогенангидридом карбамиловой либо тиокарбаминовой кислоты.
Авторы
Даты
1968-07-03—Публикация
1966-08-04—Подача