Известен способ получения адиподинитрила восстановительной димеризацией акрилонитрила в водной кислой среде при температуре 15-40°С в присутствии ацетона, ингибиторов полимеризации, таких как изатин, хинон, полифенол, в присутствии фосгена и солей железа.
Выход адиподинитрила при этом не превышает 74%.
По предлагаемому способу выход может быть увеличен практически до количественного.
Согласно изобретению предлагается процесс восстановительной димеризации способных к димеризации α, β-ненасыщенных олефиновых нитрилов, амидов или эфиров в одной фазе осуществлять в присутствии органического сульфоксида или сульфона следующего строения
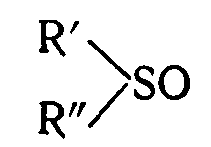
или
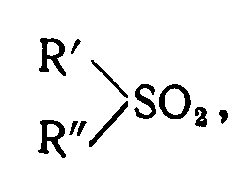
где R′ и R′′ представляют углеводные радикалы или их замещенные производные, в том числе алифатические, циклоалифатические, ароматические, аралкильные и алкарильные группы и водород, в которых R′ и R′′ могут быть одними и теми же или различными и могут быть соединены друг с другом связью, образуя гетероциклическое ядро, содержащее атом серы.
Сульфоксид или сульфон не должны мешать реакции гидродимеризации или подвергаться в нежелательной степени воздействию реакционной среды. Например, при гидродимеризации акрилонитрила с использованием амальгамного процесса, они не должны подвергаться восстановлению амальгамой или цианоэтилироваться акрилонитрилом.
Предпочтительно, чтобы сульфоксид или сульфон образовывали гомогенную реакционную смесь с другими компонентами смеси (например, жидкий совместный растворитель для акрилонитрила и воду). В качестве растворителей можно использовать, например, диметилсульфоксид, тетраметиленсульфон, диметилсульфон, дифенилсульфон.
Процесс, являющийся предметом настоящего изобретения, особенно полезен в приложении к α, β-олефиновым нитрилам с выходом алкиленовых динитрилов или их замещенных производных. В качестве примера можно привести восстановительную димеризацию акрилонитрила или способных к димеризации его замещенных производных до нитрила адипиновой кислоты или его замещенных производных.
Пропорции добавки к акрилонитрилу будут несколько изменяться в соответствии с детальными условиями процесса (например, в зависимости от эффективности добавки), однако добавки, по-видимому, будут полезны для реакции в широких границах соответствующих концентраций. Например, при восстановительной димеризации акрилонитрила в присутствии диметилсульфоксида хорошие результаты получаются, если вес диметилсульфоксида и вес акрилонитрила относятся приблизительно как 20:1, однако можно применять также весовые соотношения от 1:1 до 100:1 при некотором изменении выхода продукта.
Предпочтительно поддерживать соответствующие концентрации в таких границах, чтобы органическая часть реакционной смеси оставалась гомогенной. В гомогенную реакционную смесь, конечно, не включается амальгама или нерастворимые продукты, или отделяющиеся от нее продукты. При восстановительной димеризации акрилонитрила вес добавки берется обычно с избытком по отношению к акрилонитрилу. В реакционной смеси могут присутствовать и другие добавки, опять-таки в зависимости от деталей процесса. Например, при восстановительной димеризации α, β-олефиновых нитрилов процесс удобно проводить в присутствии цианистых алкилов, в частности ацетонитрила. Цианистый алкил добавляется произвольно и предпочтительно должен содержаться в исходных материалах (этот аспект изобретения не распространяется на случайное образование цианистых алкилов в качестве основных или побочных продуктов реакции, например пропионитрила). Восстановительная димеризация акрилонитрила в присутствии ацетонитрила, по-видимому, не только дает в некоторых случаях увеличение выхода продукта; имеется и другое экономическое преимущество, состоящее в том, что становится возможным использовать в качестве исходного материала сырой или лишь частично очищенный продукт какого-нибудь процесса получения акрилонитрила (например, из пропана, аммиака и кислорода в присутствии катализатора), вследствие чего отпадает необходимость в трудноосуществимой очистке акрилонитрила от ацетонитрила.
Реакция идет предпочтительно в присутствии замедлителя полимеризации, например N,N-диметил-n-нитрозоанилина.
Восстановительную полимеризацию можно осуществить, используя амальгаму щелочного или щелочноземельного металла в среде, способной порождать протоны. Обычно используется амальгама натрия или калия в водной среде. Хотя источником протонов обычно является водная среда, следует заметить, что нет необходимости в больших количествах воды, и на самом деле может оказаться более выгодным ограничить содержание воды до небольшой пропорции от общего количества реакционной смеси. Кроме того, могут быть использованы и другие источники протонов, такие как спирты или безводная кислота. При использовании амальгамы рН в реакционной среде стремится к увеличению по мере потребления амальгамы. Предпочтительно избегать экстремальных значений рН, хорошие выходы получаются при величине рН в пределах 2-13 и особенно в пределах 5-11. Величину рН можно регулировать различными известными способами, например, путем добавления кислот, таких как HCl, H2SO4 или углекислого газа, либо других неорганических и органических кислот в течение реакции, или посредством буферной системы, например водного раствора фосфата, бората, карбоната или бикарбоната.
Предпочтительнее охлаждать реакционную смесь, чтобы свести до минимума побочные реакции вроде полимеризации; хорошие результаты получаются, если восстановительная димеризация идет в температурном интервале от 0 до 30°С, при более низких температурах реакция замедляется, а при более высоких температурах уменьшается выход.
Величина давления не является критической для реакции, поэтому удобно применять атмосферное давление, но при желании для полимеризации акрилонитрила можно использовать повышенное давление. Предлагаемый процесс можно легко внедрять на установках, работающих как в непрерывном, так и в прерывистом режиме.
При использовании данного процесса было установлено, что восстановительная димеризация обеспечивает значительные выходы продукта. Например, при восстановительной димеризации акрилонитрила до нитрила адипиновой кислоты с использованием диметилсульфоксида выходы нитрила адипиновой кислоты в расчете на употребляемый акрилонитрил были улучшены, и при амальгамном способе были получены хорошие выходы нитрила адипиновой кислоты в пересчете на активный металл амальгамы.
Амальгамный способ удобен для проведения предложенного процесса в лабораторных условиях, когда амальгама добавляется с контролируемой скоростью в перемешиваемую реакционную смесь. Другие материалы тоже могут подаваться с контролируемой скоростью (например, кислота для регулирования величины рН или другие компоненты реакционной смеси для поддержания относительных пропорций этих компонентов на заданном уровне). Отделять продукты от реакционной смеси можно с помощью обычных средств. Например, при восстановительной димеризации акрилонитрила до нитрила адипиновой кислоты с использованием натриевой амальгамы и соляной кислоты для регулирования величины рН можно вначале отфильтровать из продукта неорганические соли натрия, а затем подвергнуть перегонке для удаления низкокипящих фракций вроде акрилонитрила, воды и любых побочных продуктов, например, нитрила, пропионовой кислоты, которые могут образоваться.
Затем под низким давлением подвергают перегонке остатки, чтобы отделить растворитель, например диметилсульфоксид, от нитрила адипиновой кислоты. Последний можно затем подвергнуть для очистки дальнейшей перегонке или иной процедуре, обычно используемой в этих целях.
Процесс, являющийся предметом данного изобретения, может быть также осуществлен в камере, расположенной рядом с электролитическим элементом или представляющей часть электролитического элемента для получения амальгамы. В одном из таких электролитических элементов катод имеет в качестве существенной детали слой ртути, расположенный на мембране, проницаемой для электролита, причем сам катод размещен между водным раствором щелочи или гидроксила щелочноземельного металла, или соли, которая содержит анод, и камерой, содержащей реакционную среду, в которой ведется процесс, являющийся предметом данного изобретения.
Ниже приводятся описания иллюстративных примеров.
Пример 1. В состав реакционной смеси входит 12 г акрилонитрила, 36 г тетрагидротиофена-1,1-двуокиси и 25 г водного раствора соляной кислоты (содержащих 2,25 г HCl).
К смеси при перемешивании при температуре 18-24°С в течение 15 мин добавляют 1550 г калиевой амальгамы (с содержанием калия 0,57 вес. %).
Реакционную смесь отделяют и подвергают анализу методом газо-жидкостной хроматографии на нитрил адипиновой кислоты, нитрил пропионовой кислоты и непрореагировавший акрилонитрил.
Молярный выход нитрила адипиновой кислоты в расчете на израсходованный акрилонитрил составил 74%. Молярный выход нитрила адипиновой кислоты в расчете на содержание калия в израсходованной амальгаме составил 50%.
Примеры 2-11. В таблице 1 приведены экспериментальные переменные величины и результаты для ряда экспериментов с димеризацией акрилонитрила в присутствии диметилсульфоксида. Эксперименты проводят в реакционном сосуде емкостью 2 л и реакционную смесь подвергают перемешиванию с интенсивностью 300 об/мин. Величину рН регулируют путем добавления соляной кислоты для нейтрализации гидроокиси, образующейся во время реакции.

Примеры 12-14. В таблице 2 приведены экспериментальные переменные величины и результаты для ряда восстановительных димеризаций акрилонитрила в присутствии диметилсульфоксида и ацетонитрила.
В примере 12, который приводится для сравнения, ацетонитрил отсутствовал. Применяются те же сокращения, что и в таблице 1. (MeCN - означает ацетонитрил).
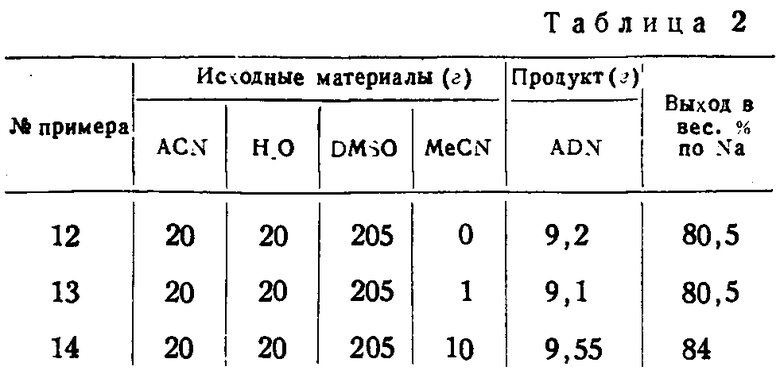
Натрий (4,85 г) добавляют в реакционную смесь в виде натриево-ртутной амальгамы (с содержанием натрия 0,3 вес. %) со скоростью 1 мл/мин. Величину рН регулируют в интервале 7-11 путем добавления водного 2 н. раствора соляной кислоты. Во всех экспериментах нитрил пропионовой кислоты образовывается лишь в незначительных количествах (следы). Присутствие ацетонитрила не ведет к уменьшению выхода нитрила адипиновой кислоты или эффективности в пересчете на натрий, а в одном случае, по-видимому, повышает выход. Поэтому очевидно, что присутствие ацетонитрила в реакционной смеси не является нежелательным.
Пример 15. Готовят реакционную смесь, состоящую из 250 г акрилонитрила, 100 г дифенилсульфоксида и 5 г воды. При перемешивании смеси, температуру которой поддерживают 0°С, в нее в течение 2 час добавляют 2000 г натриевой амальгамы (с содержанием натрия 0,1 вес. %); величину рН регулируют в интервале 8-10 2 н. раствором соляной кислоты. Вследствие низкой растворимости в воде дифенилсульфоксида в реакционной смеси образовывается два слоя. С помощью газо-жидкостной хроматографии установлено, что выход нитрила адипиновой кислоты составил 1,49 г, нитрила пропионовой кислоты - следы, что соответствует выходу в пересчете на акрилонитрил 99% и в пересчете на натрий 32%. В примерах 1-16 в качестве ингибитора полимеризации присутствует n-нитрозодиметиланилин в концентрации приблизительно 100 ч. на миллион (100 мг/л).
Пример 16. 100 мл 0,2%-ной натриевой амальгамы, приготовленной путем электролиза раствора хлористого натрия, в течение 1 час постепенно добавляют в раствор 25 г акриламида, 50 г воды и 100 г диметилсульфоксида. Температуру смеси поддерживают в интервале 0-10°С и величину рН регулируют в диапазоне 6-10 добавлением разбавленного раствора соляной кислоты. Раствор выдерживают в течение 30 мин, образовавшийся белый осадок диамида адипиновой кислоты отфильтровывают, промывают водой и высушивают. Вес образовавшегося адипамида составил 3 г, точка плавления 218°С, точка плавления в смеси с чистым диамидом адипиновой кислоты - 218°С.
Анализ.
Вычислено, %: С 50,0; Н 8,33; N 19,4; O 22,2.
Найдено, %: С 50,6; Н 8,21; N 19,1; О 22,1.
Пример 17. 100 мл 0,19%-ной натриевой амальгамы добавляют в перемешиваемый раствор 40 г этилакрилата в 50 г диметилсульфоксида и 10 г воды; величину рН регулируют в диапазоне 6-10 путем добавления двуокиси углерода.
Температуру смеси поддерживают ниже 10°С. Воду, этилакрилат и диметилсульфоксид отгоняют при пониженном давлении, а полученный остаток подвергают кипячению с эфиром. Эфирный экстракт отфильтровывают, высушивают и эфир выпаривают. Полученный в остатке раствор оранжевого цвета подвергают фракционированию и собирают фракцию, кипящую при 246-249°С. Вес полученного продукта 2 г.
Анализ для диэтиладипата.
Вычислено, %: С 59,4; Н 8,9; О 31,7.
Найдено, %: С 59,1; Н 8,7; О 31,0.
При использовании предлагаемого способа выход в пересчете на исходные материалы и к. п. д. использования тока выше, чем при известных способах, не использующих соединений, примененных в предлагаемом способе.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ НИТРИЛА АДИПИНОВОЙ КИСЛОТЫ | 1970 |
|
SU268291A1 |
| СПОСОБ ПОЛУЧЕНИЯ АДИПОДИНИТРИЛА | 1967 |
|
SU196649A1 |
| СПОСОБ ПОЛУЧЕНИЯ АДИПИНОВОЙ КИСЛОТЫ | 1971 |
|
SU315351A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИМЕРОВ | 1969 |
|
SU250764A1 |
| СПОСОБ ПОЛУЧЕНИЯ АДИПОНИТРИЛА | 1968 |
|
SU208571A1 |
| ТЕХНИЧЕСКАЯ '"^ БИБЛИОТЕКА | 1970 |
|
SU262008A1 |
| СПОСОБ ПОЛУЧЕНИЯ АДИПОНИТРИЛА | 1971 |
|
SU320114A1 |
| СПОСОБ ОЧИСТКИ АЦЕТОНИТРИЛА | 1995 |
|
RU2149867C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИМЕРОВ ПРОИЗВОДНЫХ АКРИЛОВОЙ КИСЛОТЫ | 1972 |
|
SU324741A1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОМЕРОВ И ИХ ПОЛИМЕРОВ | 2005 |
|
RU2390565C2 |
1. Способ получения динитрилов, диамидов или диэфиров алифатических дикарбоновых кислот общей формулы:
где R′ - СН3; Н;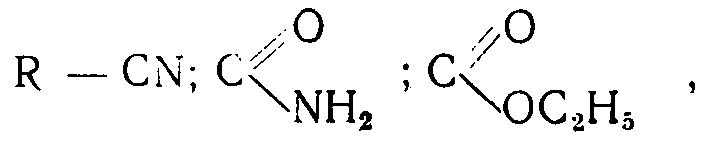
путем восстановительной димеризации α, β-ненасыщенных олефиновых нитрилов, амидов или эфиров общей формулы: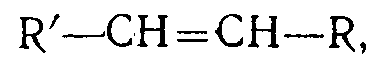
где R и R′ имеют вышеуказанные значения, амальгамой щелочного металла в водной среде при температуре 0-50°С с последующим выделением целевого продукта, отличающийся тем, что, с целью увеличения выхода продукта, процесс ведут при рН среды 2-13 в присутствии органических сульфоксида или сульфона в весовом отношении последнего к исходному олефину 1:1-100:1.
2. Способ по п. 1, отличающийся тем, что процесс ведут в присутствии ацетонитрила.
Авторы
Даты
1968-11-13—Публикация
1965-12-16—Подача