. 1
Изобретение касается способа получения нитрила адипиновой кислоты (адипонитрила) или ее эфиров восстановительной димеризацией акрилонитрила или эфира акриловой кислоты амальга.мой щелочного или щелочноземельного металла.
Известен способ гидродимеризации эфиров или нитрилов а,|3-мононенасыщенных низших карбоновых кислот, в частности акрилонитрила, восстановительной димеризацией амальгамой в присутствии воды, соли четвертичного аммония, ингибитора полимеризации и при рН среды 1,5-9,5. В реакционную среду молсет быть добавлеп полярный органический растворитель. В известном методе используют амальгаму натрия или калия и в качестве источника активного водорода - воду; приведены многочисленные примеры подходящих солей четвертичного аммония, например соли тетраалкиламмония, в которых атом азота связан по меньшей мере с двумя низшими алкильными группами, содержащими от I до 4, предпочтительно 2, атомов углерода. Величина любого радикала, не являющегося низшим алкильным радикалом, ограничивается тем условием, что соль четвертич.ного аммония должна оставаться заметно растворимой в водной среде. В качестве примеров приведены соли цетилтриметил- и тетраэткламмония, а также соли тетраметил- и
триметилэтиламмония. Считается, что природа аниона соли имеет второстепенное значение, но из соображений растворимости предпочитаются галогениды и п-толуолсульфонаты. Назначение соли четвертичного аммония состоит в подавлении нежелательного полного восстановления мономеров (например, акрилонитрила до пропионитрила) и предполагается, что это достигается благодаря ее адсорбции на поверхности амальгамы.
В большинстве примеров, изложенных в описании к известному методу, используется реакционная среда (исключая амальгаму), состоящая из акрилонитрила, воды и соли четвертичного аммония.
Известно, что в реакционную смесь можно прибавлять полярные апротонные растворители, например, для повышения растворимости катионообразующих солей и/или мономера. Подходящими растворителями являются, например, диоксан, ацетон, диметилформамид и этиленгликоль.
Изобретение относится к способу получения димеров акрилонитрила, метил- или этилакрилата или других а,р-мононенасыщенных нитрилов или сложных эфиров, основанному на взаимодействии амальгамы щелочного металла в гомогенной реакционной среде, состоящей из а,р-мононенась1щенного сложного эфира или нитрила, воды или метилового, или этилового спирта, соли четвертичного аммония, имеющей алкилрадикалы, связанные с атомом азота, и полярного апротонного органического растворителя, инертного в данной реакционной среде и по отношению к амальгаме, при кажущейся величине рН среды от 7 до 11,5, например 8-10. Реакционная смесь содержит ненасыщенный эфир или нитрил от 2,5 до 20 мол. %, источник протонов (предпочтительно воду, или метиловый, 10 или этиловый спирт) от 1 до 30 мол. %, предпочтительно от 2 до 20 мол. %, соль четвертичного аммония от 0,2 до 8 мол. % и полярный органический растворитель. В целях экономии по предлагаемому спосо- 15 бу применяют натриевую, (или, возможно, калиевую) амальгаму, из электрохимических соображений, однако для гидродимеризации а,р-мононенасыщенных сложных эфиров и нитрилов целесообразно использовать амаль- 20 гаму щелочноземельных металлов, содержащую активный металл (например, магний) с достаточно большим отрицательным окислительно-восстановительным потенциалом. Было исследовано влияние на ход реакции 25 кал ущейся величины рН реакционной средь(. Так, при кажущейся величине рН более 11,5 возникают реакции цианоэтилирования, при кажущейся величине рН менее 7 значительно усиливается образование полностью восста- 30 новленного мономера (т. е. пропионитрила). В качестве четвертичных солей аммония (например, хлорида или другого галогенида, или /г-толуолсульфоната) применяют соли тетраалкиламмония, например, содержащие 35 от 1 до 4 атомов углерода, связанных с атомом азота. Следует отметить, что требования относительно сохранения гомогенности реакционной среды могут обусловить некоторые ограничения при выборе соли четвертичного 40 аммония. Наилучшие результаты с точки зрения выхода гидродимера, например адипонитрила, из расчета на прореагировавший щелочной металл были получены при употреблении четвертичных солей аммония, обладаю- 45 щих достаточной растворимостью. Так, рекомендуется применять соли тетраэтиламмония и метилтриэтиламмония, хорошие результаты получают также при использовании солей тетра-н-бутиламмония, удовлетворительные - 50 солей триметилцетиламмония. Однако соли тетраметиламмония и триметилэтиламмония из числа солей тетраалкиламмония наименее растворимы в органических растворителях, что может затруднить их 55 использование ввиду необходимости сохранения гомогенности реакционной среды. Так, хлорид тетраметиламмония плохо растворяется Б обычных полярных растворителях, соответствующий л-толуолсульфонат несколько 60 лучще растворяется, л-толуолсульфонат триметилэтиламмония слегка растворяется даже в ацетонитриле, и при использовании этого растворителя могут быть применены растворы с концентрацией до 30 вес. %.65 5 При использовании йодидов четвертичного аммония выход адипонитрила на прореагировавший щелочной металл ниже чем в случае применения соответствующих хлоридов. Возможно применение соли фосфония, солей сульфония. Выбор подходящего органического полярного растворителя не представляет затруднений. Предлагаемый способ не очень чувствителен к изменению полярного растворителя, хотя оптимальные условия могут несколько меняться при использовании различных растворителей, необходимо чтобы растворитель был не реакционноспособен по отношению к другим компонентам реакционной среды и пе взаимодействовал с амальгамой. Кроме того, применяемый растворитель должен обеспечивать гомогенность реакционной среды и растворять требующееся количество соли четвертичного аммония. Из этих соображений используют полярные растворители. В качестве растворителей по предлагаемому способу могут быть применены ацетонитрил, адипонитрил, диоксан, диметилацетамид, диметилформамид, диметилсульфоксид и тетрагидрофуран. Являющийся продуктом реакции адипонитрил может быть также использован как растворитель. В непрерывной реакционной системе, включающей рециркуляцию органических реакционных жидкостей, в последних может присутствовать существенное количество адипонитрила, независимо от того, содерл ался ли в применяемом растворителе адипонитрил первоначально. Реакцию гидродимеризации проводить при любой температуре от 10 до 55°С, обычно реакцию проводят при температуре от 30 до 40°С, так как реакция экзотермическая, те.мпература свыше 55°С способствует полимеризации. В реакционную среду рекомендуется вводить агент, ингибирующий полимеризацию мономера под действием свободных радикалов, например Н,М-диметил-л-нитрозоанилин. Необходимо точно контролировать величину рН системы, интенсивно перемешивать амальгаму и органическую фазы. Для регулирования величины рН молсно использовать фосфатную буферную систему, рекомендуется для этих целей применять двуокись углерода, которая значительно лучше растворяется, например, в ацетонитриле, диметилформамиде, диметилсульфоксиде, диоксане и тетрагидрофуране, употребляемых в качестве полярных растворителей, чем в воде, Двуокись углерода может служить одновременно нейтрализующим агентом для образующейся в результате реакции щелочи. Получаемый бикарбонат натрия плохо растворяется в органической реакционной среде, и его отделяют в циклонах или центрифугированием, Кажущаяся величина рН насыщенного раствора двуокиси углерода в реакционной среде является устойчивой, например, в интервале от 8,5 до 9,5. При выполнении небольших работ хорошие результаты получают при использовании для регулирования величины рН газообразного хлористого водорода. В тех случаях когда необходимы высокие скорости реакции и низкое среднее время пребывания амальгамы в реакционной зоне, рекомендуется способ, близкий к способу с псевдоожиженным слоем, при котором амальгама диспергируется путем пропускания органической реакционной среды снизу вверх через зону, содержащую амальгаму (рекомендуется, чтобы амальгама представляла собой сплошную фазу), в которую непрерывно или периодически подают свежую амальгаму.
Скорость и способ подачи амальга.мы регулируют так, чтобы к сепаратору поступала только истощенная амальгама.
Для реакции можно применять трубчатый реактор, закрытый снизу пористой пластиной.
Ниже описан предлагаемый способ периодического процесса.
На прилагаемых графиках изображены кривые, отражающие зависимость выхода адипонитрила на прореагировавший щелочной металл в данных условиях температуры, рН и концентрации отдельных компонентов органической реакционной фазы от концентрации некоторых других компонентов реакции.
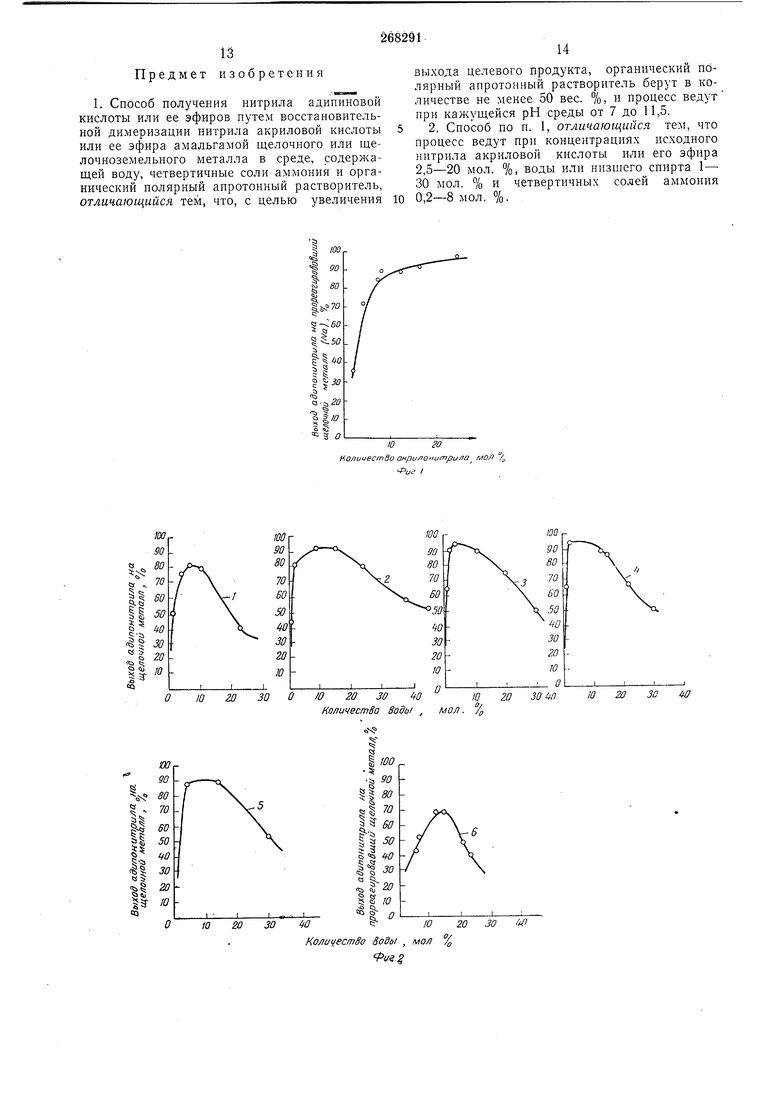
Кривая, изображенная на фит. 1, показывает выход адипонитрила (из расчета на прореагировавший щелочной металл, которым в данном случае являлся натрий), полученный при различном количестве акрилонитрила и постоянном содержании воды, соли четвертичного аммония и полярного растворителя. Количество воды составляло от 6 до 8 мол. %, содержание соли четвертичного аммония - примерно 2 мол. %. Растворителем служил ацетонитрил, а в качестве четвертичной соли был применен хлорид тетраэтиламмония Температуру поддерживали на уровие 35-40°С, а величину рН - в интервале от 8 до 9,5 путем добавления ДВУОКИСИ углерода.
Кривые 1-5 (см. фиг. 2) показывают значительное изменение выхода адипонитрила в зависимости от содержания воды в реакционной массе и нри концентрации четвертичной соли 0,5; 1,0; 2,5; 4 и 5 мол. % соответственно. Компоненты органической реакционной среды и условия реакции были такие же, как в опытах, результаты которых отображены кривой на фиг. 1.
Кривая 6 (см. фиг. 2) сходна с кривыми /- 5, но в этом случае для опыта было использовано 1,2 мол. % бромида триметилцетиламмония.
Кривые, изображенные на фиг. 3 и 4, показывают влияние на выход адипонитрила мопярной концентрации четвертичной соли. За исключением специально отмеченных случаев, природа и относительные концентрации ингредиентов органических реакционных сред, а также условия процесса, были такие же, как в опытах, результаты которых отображены кривыми на фиг. 2.
На основании кривой / (см. фиг. 1) можно сделать вывод, что выход адипонитрила улучшается при использовании большого количества акрилонитрила. Однако концентрации
свыше 20 мол. % непригодны в связи с образованием большого количества олигомера и полимера. Другими опытами было показано что степень образования олигомера имеет тенденцию уменьшаться при снижении рабочей
температуры. При этом выход адипонитрила уменьшается, а выход пропионитрила увеличивается.
Кривые /-5 (см. фиг. 2) показывают изменение выхода адипонитрила в зависимости от
количества воды примерно от О до 20-30 мол. %. Резкое новышение выхода адипонитрила при увеличении содержания воды в реакционной Л1ассе было отмечено во всех случаях. При дальнейшем увеличении концентрации воды выход заметно уменьшается. То же самое наблюдается при использовании вместо хлорида тетраэтиламмония 1,2 мол. % бромида триметилцетиламмония (см. фиг. 2, кривая 6. При применении этой четвертичной соли
выход ниже. Наименьший выход адипонитрила был получен при одновременно высокой молярной концентрации воды и низкой молярной концентрации соли четвертичного аммония.
На фиг. 3 изображены четыре кривые, полученные при различном содержании воды в реакционной среде: кривая 1-при б мол.%; 2 - при И; 3 - при 15 и 4 - при 20 мол. %. На фиг. 4 приведена кривая /, отображающая результаты опытов с хлоридом метилтриэтиламмония с 6 мол. 7о воды, кривая 2, показывающая сходные результаты для йодида метилтриэтиламмония. и кривая 5, полученная при использовании бролтида триметилцетиламмония и 5 мол. % воды.
На графиках, изображенных на фиг. 3 и 4, видно, что небольшие добавки четвертичных солей порядка 0.2-8 мол. % в несколько раз увеличивают выходы адипонитрила, при дальиейщем повышении концентрации четвертичных солей аммония выход постепенно снижается.
Целесообразно заметить, что соли четвертичного аммония, получаемые обычными методами, содержат кристаллизационную воду, эту воду следует учитывать при подсчете общего количества воды, присутствующей в органической реакционной среде, особенно при высоких К01щентрациях четвертичной соли.
Псследования показали, что при непрерывном процессе получения адипонитрила поддержание требующегося количества воды затруднено, когда концентрация соли четвертичного аммония в рециркулируемой жидкости превышает, примерно, 3-5 мол. %.
Примеры 1 и 2 приведены для случая применения хлористого водорода в качестве контроля величины рН среды.
строходиой мешалкой, капельной воронкой и широкогорлой вводной трубкой, загружают 40 г ацетонитрила, 5 г акрилонитрила, 1,75 г воды, 10 г моногидрата хлорида тетраэтиламмония и 100 мг индикатора тимолового синего. Всю аппаратуру охлаждают на ледяной бане до 5 -7°С.
В течение 30 мин к быстроперемешиваемому раствору медленно прибавляют 225 г амальгамы натрия, содержащей 0,675 г натрия. Через широкогорлую вводную трубку подают газообразный хлористый водород так, чтобы uBet индикатора оставался синим. Через 15 мин, быстрого перемешивания реакция прекращается. Органический слой отделяют от остаточной ртути, и содержимое анализируют методом газожид-костной хроматографии. Выход адипонитрила (из расчета на использованный натрий) 91% от теоретического.
Пример 2. В аппаратуре и по способу, .описанному в примере 1, проводят ряд опытов, изменяя концентрацию воды и моногидрата хлорида тетраэтиламмония..
Результаты приведены в табл. 1. Таблица 1 Были проведены опыты с другими полярными растворителями, солями четвертичного аммония и метиловым и этиловым спиртами. Во всех случаях температура реакции составляла 35-45°С, а величину рН поддерживали в интервале 8-10 двуокисью углерода. В качестве амальгамы применяли амальгаму натрия, в нескольких случаях - амальгаму калия, концентрация щелочного металла в амальгаме составляла 0,3%. . Реакционный сосуд представлял собой удлиненную стеклянную колбу (емкостью, например, 700 мл с прижатой пружиной съемной пятигорлой крышкой и с выходом в нижней части колбы. Рекомендуется сосуд снабжать направленным к его нижней части боковым отростком, через который вводят датчик прибора, регистрирующего величину рН, и мешалкой, пропускаемой через центральное
отверстие крышки. Два других отверстия в крышке служат для подачи двуокиси углерода и амальгамы внутрь сосуда, четвертое отверстие предназначено для термометра, а пятое - для холодильника, ведущего к ловушке для улавливания паров, увлекаемых двуокисью углерода, выходящей из холодильника.
Типовая загрузка ингредиентов следующая (в г): 120 ацетонитрила, 15 акрилонитрила (или 25 метилакрилата), 5 воды и 10 хлорида тетраэтиламмония, или 81; 7,3; 10 и 1,6 мол. %. Амальгама содержит 0,3% натрия.
скорость подачи
предпочтительна
ее 0,8 мл1мин.
Продолжительность реакции при периодическом процессе получения адипонитрила 1 час; по прошествии этого времени около /з мономера уже вступает в реакцию.
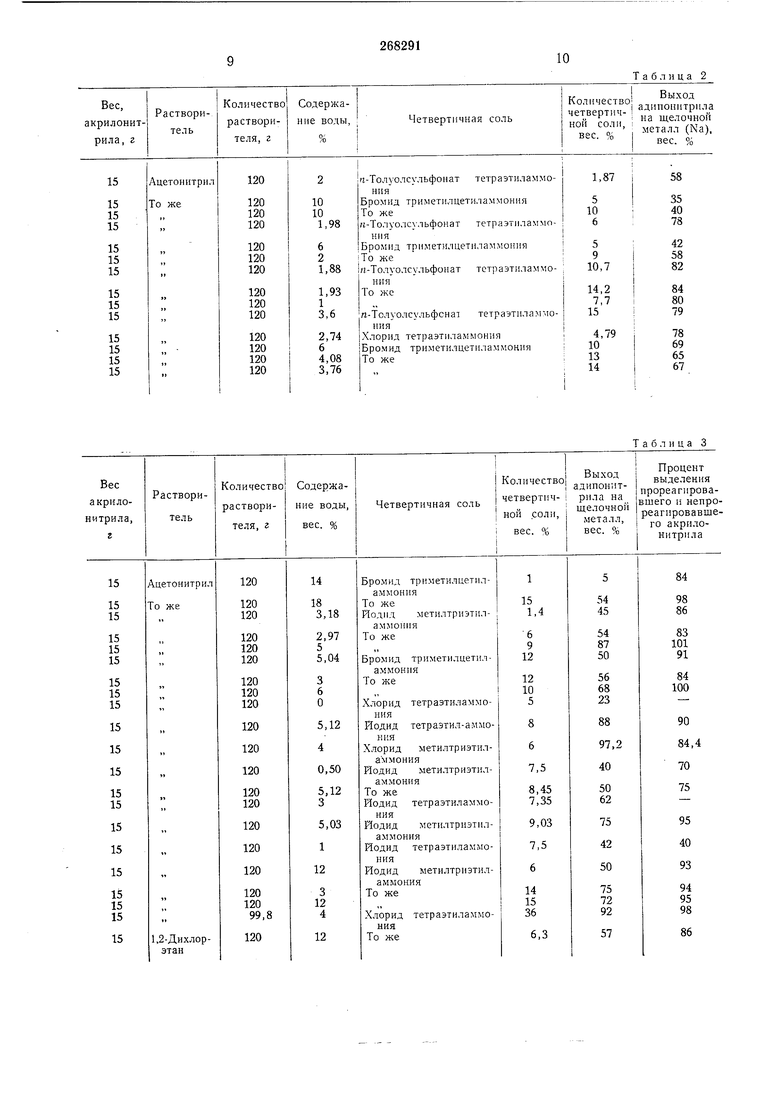
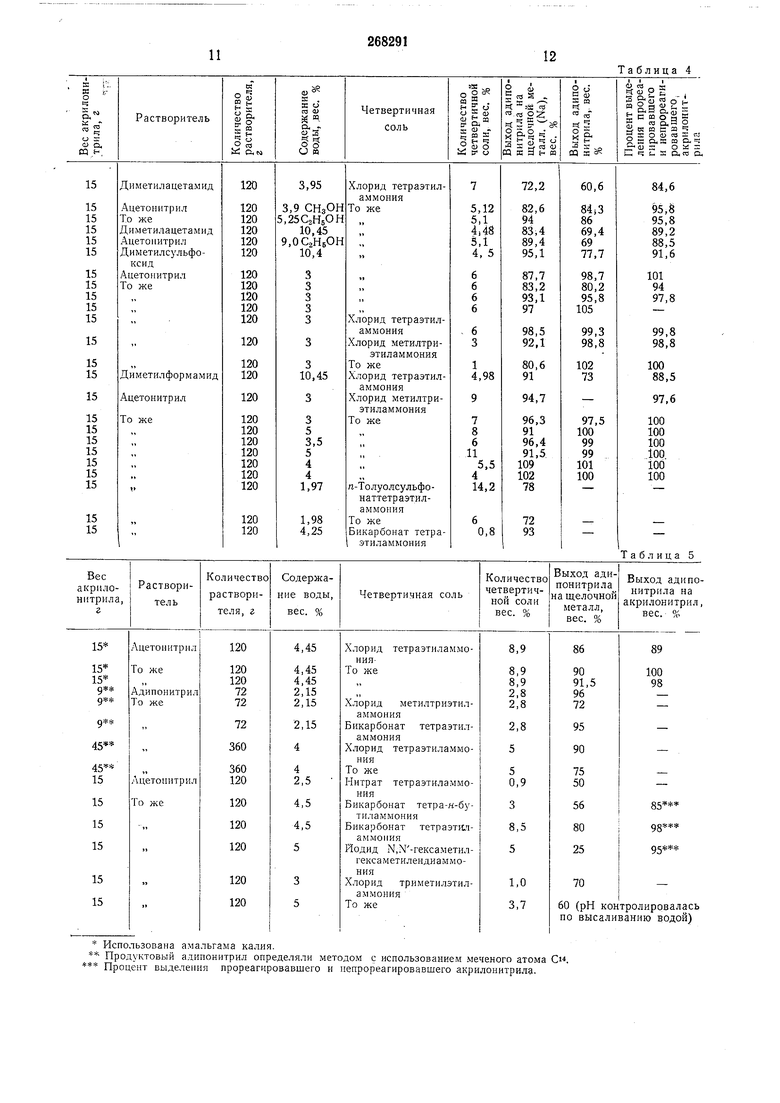
Во всех опытах применяют интенсивное перемешивание, из нижней части сосуда удаляют только амальгаму. Извлеченная амальгама не должна в основном содержать щелочной металл. В качестве органических полярных растворителей используют ацетонитрил и диметилформамид, однако с применением диметилформамида как растворителя обнаруживается меньшее влияние снижения концентрации четвертичной соли на выход адипонитрила. Во всех опытах вес растворителя (ацетонитрила или диметилформамида), загружаемого в сосуд, составлял 120 г, вес исходного эфира менялся в пределах от 24 до 40 г, количество вводимых воды и четвертичной соли таково, что концентрация воды в реакционном сосуде составляла от 0,5 до 12 вес. %. Эти относительные пропорции ингредиентов соответствуют содержанию воды, равному от 5 до 20 мол. %, и эфира от 5 до 12 мол. %. Выход диметил- или диэтиладипината составлял от 50 до 65 или 70% из расчета на прореагировавший натрий. Процесс протекает одинаково в случае применения как низших эфиров акриловой кислоты (в особенности, метил- и этилакрилат), так и акрилонитрила. В реакциях гидродимеризации при помощи амальгамы в.место воды можно применять метиловый или этиловый спирт, или даже циклогексанол. Результаты опытов приведены в табл. 2, 3, 4 и 5.
Таблица 3
II
268291
12
Таблица 4



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АДИПОНИТРИЛА | 1971 |
|
SU320114A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИМЕРОВ | 1969 |
|
SU250764A1 |
| СПОСОБ ПОЛУЧЕНИЯ АДИПОНИТРИЛА | 1968 |
|
SU208571A1 |
| СПОСОБ ПОЛУЧЕНИЯ АДИПОНИТРИЛА | 1969 |
|
SU258168A1 |
| Способ получения адипонитрила | 1967 |
|
SU500750A3 |
| СПОСОБ ПОЛУЧЕНИЯ ДИМЕРОВ ПРОИЗВОДНЫХ АКРИЛОВОЙ КИСЛОТЫ | 1972 |
|
SU324741A1 |
| СПОСОБ ПОЛУЧЕНИЯ АДИПОНИТРИЛА | 1972 |
|
SU332078A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИМЕРОВ а,р-МОНОНЕНАСЫЩЕННЫХ СОЕДИНЕНИЙ | 1971 |
|
SU298193A1 |
| Способ получения адипонитрила | 1968 |
|
SU461490A3 |
| Способ получения адипонитрила | 1973 |
|
SU784762A3 |

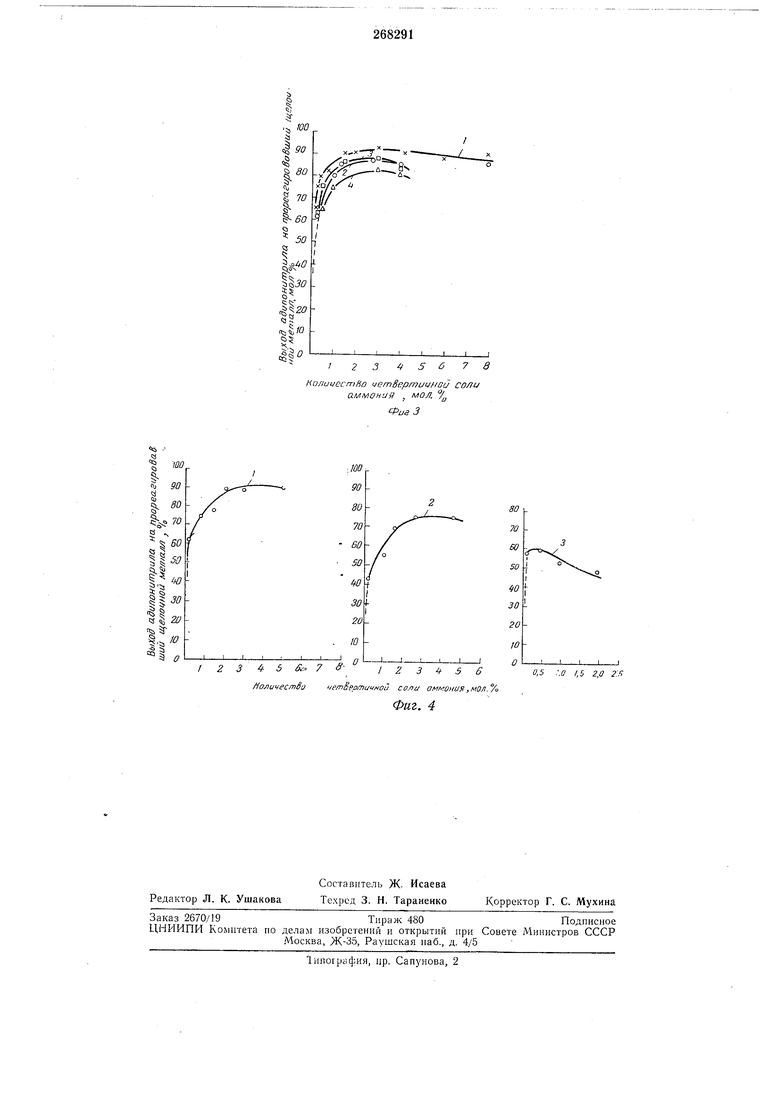

Таблица 5 Предмет изобретения 1. Способ получения нитрила адипиновой кислоты или ее эфиров путем восстановительной димеризации нитрила акриловой кислоты или ее эфира амальгамой щелочного или щелочноземельного металла в среде, содержащей воду, четвертичные соли аммония и органический нолярный анротонный растворитель, отличающийся тем, что, с целью увеличения
/00
so
80 70 60
§
.50
||ад
1|
|1;.
О 3
Количество af pu/JOfufnpa u мол / ю 20 30 О
го fue I /о 20 30 ffO Количество Водь/ , выхода целевого продукта, органический полярный апротонный растворитель берут в количестве не менее 50 вес. %, и процесс ведут при кажущейся рН среды от 7 до 11,5. 2. Способ по п. 1, отличающийся тем, что процесс ведут прп концентрациях исходного нитрила акриловой кислоты или его эфира 2,5-20 мол. %, воды или низшего спирта 1- 30 мол. % и четвертичных солей аммония 0,2-8 мол. %.
юо
90
%s 80 . 70
Р SO
§1 °
II °
S
tSl 30
«5 20
&
gi
О
«а
20 30
20 30 ffl
10
Количество 5оды , мол
°/ Ри.
4efr B p/nu f ou со.а )МОЛ.°/о
:.о /,5 2,0 2.к
Фиг. 4
Авторы
Даты
1970-01-01—Публикация