Изобретение касается получения галогенпроизводных фенокситриазина, которые обладают огнезадерживающим, фунгицидным, бактерицидным действием и могут найти применение в качестве средства для гидрофобизации, как шлифовальное средство в стекляной промышленности, текстильное вспомогательное сырье, для облагораживания поверхностей.
Известен способ получения галогенпроизводных фенокситриазнна путем взаимодействия цианурхлорида или соответствугош,его лор-5-триазина с солью щелочного металла галогеннронзводпого фенола в водно-ацетоновой среде при температуре 15-25° с последуюп им выделением продуктов.
Применение фенолята щелочного металла осложняет производство, так как требует эквивалентного количества щелочи для его приготовления, а также отделения хлористого натрия, образующегося в результате реакции, т. е. известный способ требует двух дополнительных стадий - приготовления фенолята п промывки и сущкн продукта.
Известен способ получения галогенпронзводных фенокситриазина общей формулы:
где X - галоид; /; 1 -5; У - остаток
Хп
где X и п имеют
вышеуказаппые
значения.
R, или группа-- N
где RI и Ro галогеR.,
иированный низший алкил, содержании до четырех атомов углерода, циклоалкил, содержании до 8 атомов углерода, или Ri - водород, а R2 - галогенирова ный низший , содержащий до 4 атомов углерода, Ц1 клоалкил, содержащий до 8 атомов углерода, арил, RI и.1и R2 вмесге могут быть составной часть() азотсодержащего гетерО,икла;
R,
/ - галоид или группа -N-R.
Ri в 5инеуказаппые значения.
По предложенному способу .хлорид или соответствующий хлор-5-триази 1 подвергают взапмодействию с галогеинроизводным фенола в нрисутствии каталитического количества третичного амнн.а К-моно-нли дизамещениого кислоты, взятого преимущественно в количестве 0,2-2% от применяемото S-триазина. Причем в качестве третичного амина-нредпочтительно применять триалкиламии или амии, содержаии Й 1 итрильную 200°С в среде инертного растворителя. Продукты выделяют известным способом. Выход количественный. В качестве катализатора пригодны однородные и смешанные третичные амины с алифатическими, циклоалифатическими и ароматическими радикалами нли их смеси, причем замещенные амины так же можно рассматривать как вид циклического третичного амина. Пригодными третичными аминами с алифатическими радикалами являются, например, триметиламин, тризтиламин, триизопропиламин, триизобутиламин, моноэтилдиизопропиламин, моноэтил-ди-н-бутила:мин, три-н-бутиламин, N, 1,,К-тетраметилбутандиамин(1,4), N,N, N, N-тетраметилэтилендиамин, в случае надобности замещенные третичные алифатические амины как р-хлорпропилдилропиламин, трис {р-этоКСиэтил)-ами1Н,метиламиноацетонитрил, N, N-ди-н-бутиламиноацетонитрил, N, N-диизопропиламиноацетонитрил, А -н-бутнл-К-метиламиноацетоиитрил, метиленаминоацетонитрил, N, 1 -диизобутр1ламинопропионнтрнл, N-днметиламинопропионитрил, диметиламиноацетонитрил, диметил - я-аминобензонитрил. Пз ряда аминов с циклоалифатическими радикалами может быть назван диметилциклогексиламин. Далее могут быть названы пригодные амины с ароматическими радикалами, такие как N, N-диалкиланилины (N, N-диметиланилин, N, Nдиэтиланилин и др.} л-бромфенилдиметиламии, 2, 4-динитрофенилдиметиламин, бензилдиметиламин, я-нитрофенил-ди-н-бутиламии, N-(2, 4-дихлорфеиил)-диэтиламин, N, N, N, ,-тетраметилбеизидин и др. Пригодными гетероциклическими третичными аминами являются, например, N-алкил-или 1 -арил-морфолин, как N-я-бутилморфолин, N-феннлморфолин, N- (л-метилфенил) -морфолин, морфолид морфолиноуксусной кислоты, N-арил-или Xалкилтетрагидрохинолии или N-тетрагидроизохииолин, как iN-н-проиилтетрагидрохинолин, 1 -феиилтетрагидроизохиноли11, N-алкил-илн N-арилиирролидины и их производные, например, N-метил пирролнднн, Л-к-бутил пиррол ндпп, .-фепилпирролидин п др. Лроматичсски.ми третичными аминами являются; шнрндин, пзохинолпп,пиразин, оксазин, хпназолин, оксадиазол, оксазол, боизтиазол и др. Для проведения предложсгыюго способа особенно хорошо Применять содержащие нитрил оные груп пы третичпые . N-MOHo нли диза1мещеипыми кислотными амидами являются амиды карбоповой кисло ты из одноосновных алифатических, аромати ческих и аралифатических карбоновых кислот с 1 до 18 С-атомов. Одноосновные кпслоты, та кие как муравьиная кислота, уксусная кисло та, нропноновая кислота, масляная кислота капроповая кислота, 2-этилгексановая кисло та, каприловая кислота, лауриновая кислота пальмитиновая кислота, стеариновая кислота бензойная кислота, фенилуксусная кислота фсиилмасляная кислота, могут иметь структу у прямых или разветвленных цепей или в алиловой цепи могут быть прерваны кетогруиой, как в иироБиноградной кислоте, ацетоукусной кислоте или левулиновой кислоте. В ачестве основной части соответствующих кислотных амидов берут аммиак или моно-или иамины. Предпочтительными являются нервичные или вторичные моио-или диамины, которые хмогут быть замещены радикалом ненасыщенного алифатического, ароматического, циклоалифатического ряда или ароматического ряда только с одним ароматическим кольцом. Например, метиламин, диметиламин, ди/i-или-изонроииламин, ди-я-или-изобутиламии, ди-2-.метилгексиламин, дилауриламин, этилендиамин, тетраметилендиамии, гексаметилендиамин, циклогекснламии, дициклогекснламнн, беизиламии, дибензиламин, анилин, метиланилин, толуидин, фенилендиамни и гексагидрофенилендиамии. Одна или обе алкиловые груины аминов могут быть также замещены феннловым или толуиловым радикалом или циклоалкиловыми груинами с 5-6 стоящими в кольце атомами углерода, которые могут быть замещены алкиловыми груинами, особенно одной или двумя метиловыми группами. В качечестве диаминов для нолучения амидов кислоты могут быть уиомяиуты такие, в которых обе аминовые группы замещены радикалом, содержащим от 1 до 8 метиленовых груни. Также в диаминах еще связанные с атомом азота атомы водорода могут быть по крайней мере до одного замещены, нанрнмер, алкило1и 1ми группами с 1-4 ато.мами углерода, феполовым или толуиловым радикалом или пяти или щестичленным циклоалкиловым радикалом. Подходящими амидами карбоновой кислоты, которые могут быть нрименены в качестве катализатора, могут быть ;азваны: формамид, метилформамид, диметилформамид, диэтилформамид, ацетамид, N, N-диметилацета.мид, N, N-ди-я-или изопронилбутирамид, N, 1 -ди-я-или-изобутилбутирамид, амид N-беизплмасляиой киелоты, амид N, N-дипропилэтил гексановой кислоты, N, N-ди-я-бутиламид ацетоуксусиой кислоты, анилид ацетоуксусной кислоты, бензилахмид беизойиой кислоты, амид ., Х-диметилбензойной кислоты и N, N-диформилгексаметилендиамин. Далее могут быть при-мепены также циклические амиды или а.миды кислоты. Используют также барбитуровые кислоты, которые могут быть замещены радикалами углеводорода, особеино метил-бис-нпли-изо-бутиловой или фениловой группой, как диметилбарбитуровая кислота, диэтилбарбитуро1 ая кислота, дипропилбдрбитуровая кислота, диаллилбарбитуровая кислота, ди-яб)тилбарбитуровая кислота и фенилэтилбарб1ггурОБая кислота. 0 По обязательно применять готовые амиды, можно также применять компоненты из которых онн построепы, например, смеси из одного первичного или вторичного моно-или диамина вышеназванного ряда и одной вышеуномя5 иутой .моно арбоновой кислоты или полученных из этих кислот хлоридов или ангидридов кислоты, так как при условиях реакции обиепного разложения образуются амиды кислоты. Сульфонамиды также являются подходящими катализаторами, например 4-сульфамоилацетанилин, N-амидипосульфаниламид, N-2-пиридилсульфаниламид.
Амиды фосфористой кислоты, как амид гексамеТилфосфористой кислоты, амид гексаметиЛфосфорной кислоты, амид гекса-н-илиизо-бутилфосфористой кислоты, триморфолид фосфористой кислоты могут быть применены как катализаторы. Триамиды фосфорной кислоты могут быть также использованы как катализаторы, однако их каталитическое действие слабее, чем действие фосфористой кислоты.
Амиды титановой и оловяной кислоты, как дипропоксититандиамид и ди-н-или-изо-бутилоловодиамид могут быть также использованы как катализаторы. Как катализаторы могут быть использованы смеси из вышеиазванных третичных аминов и амидов кислоты.
Реакция разложения может быть нроведена как в плаве, так и в инертном растворителе, причем инертный растворитель может иметь функции настоящего растворителя, а также функции диснергатора. Подходящими растворителями являются алифатические и ароматические углеводороды, а также простые и циклические эфиры. Из алифатических углеводородов могут быть названы однородные соединения, а также смеси их, как изооткап и бензиновые фракции, ианример,такие, область кипения которых 120-200°С. Могут быть применены также циклоалифатические соединения, как декагидронафталип. Бензол, толуол, ксилол, о-дихлорбензол и нитробензол служат примером подходящих ароматических углеводородов. Как эфиры пригодные для нроведения реакции могут быть названы: диизопропилэфир, диизоамилэфир, диметнлэфнр этиленового или диэтиленового гликоля, дифенилэфир, 1, 4-диоксан и т. д.
Таким образом, могут быть нрнменены как алифатические так и ароматические с открытой ценью эфиры. Однако могут быть применены также нолярные растворители, как днметилсульфоксид и диметилформамид.
Пример. 2-Анилнд-4, б-дн-(пентахлорфенокеи) -S-триазии.
В трехгорлую колбу, снабженную .мещалкой, холодильником и вводной трубкой, загружают 24,1 г 2-анилид-4, 6-дихлор-5-триазина, 53,3 г пентахлорфенола, 300 мл ксилола и 0,5 г N, N-ди-н-бутиламииоацетонитрила. Реакционную смесь размешивают нрн температуре кипения толуола. Образовавшийся ПС1-газ вытесняют азотом из реакционной смеси и поглощают в растворе NaOH, который по окончании реакции титруют. По истечении 24 час реакция заканчивается. Продукт выпадает в виде белого кристаллического осадка с ночти количественным выходом. Точка плавления 260- 264°С. Анализ:
Вычислено, %: С 35, 99; Н 0,86; X 7,99; CI 50,7.
Пайдено, %: С 36,64; Н0,82; N7,77; CI 49,3. Пример 2. 2-Хлор-4,,6-ди-(2,3,4,6-тетрахлорфеноксн) -S-триазин.
В трехгорлую колбу, снабженную мешалкой, холодильником и каиельиой воронкой, загружают 92,2 г хлористого цианура и 231,9с 2, 3, 4, 6-тетрахлорфенола, 1200 .мл ксилола и
1,5 г N-метнлпирролидина. Реакционную размешивают нри температуре кипения ксилола. Образовавшийся HCI-газ вытесияют азотом из реакцно)1)юй смеси н поглощают в растворе NaOH. По истеченнн 8 час реакция заканчивается. Продукт выпадает в виде белого, кристаллического осадка. Точка плавления 235°С. Выход приблизительно 95%. Анализ: Вычислено, %: С 31,3; Н 0,34; N 7,29; С 55 5
Пайдено, %: С 30,1; П 0,50; N 7,20; CI 54,9. Пример 3. 2-Хлор-4, 6-ди- (2,4,5-трихлорфенокси) -5-трназ11н.
В трехгорлую колбу, снабженную мещалкой, холодильником н каиельной воронкой, загружают 82 г хлористого циаиура, 176 г 2, 4, 5-трихлорфенола, 1000 мл ксилола н 1,0 г морфолида морфолниуксусной кислоты. Реакционную смесь размешивают нри температуре кипения ксилола. Образовавшийся HCI-газ
вытесняют азото.м из реакционной смеси и поглощают в растворе ХаОП. После окопчаиня выделения хлористого водорода реакционную смесь фильтруют. Продукт выпадает в виде белых кристаллов. Точка плавления 189-
. Выход 97%.
Пример 4. 2-Хлор-2, 6-дн-(иентахлорфе|10кси)-8-трназин. В трехгорлую колбу, снабженную мешалкой, холодильником н вводно1 | трубкой, загружают 18,44 г хлорнстого цианура, 53,3 г нентахлорфенола, 300 мл кснлола с 0,5 г трн-н-бутнламина. Реакционную смесь размешивают прп температуре кипения кснлола.Образовавшнйся HCI-газ вытесняют азотом нз реакционной смеси и ноглощают в растворе NaOH. По истечении нриблизительно 2 час реакция заканчивается. Продукт вынадает i виде белых к 1исталлов с выходом нриблизительно 98%. Точка плавления 325--327°С. Анализ:
Вычислено, %: С 27.95; X 6.52; CI 60,6.
Найдено, %: С 27,55 X 6,53; С1 59,88. Пример 5. 2-Хлор-4,6-дн-(2,4,6-трнбром(1)еноксп)-5-трназнн.
В трехгорлую колбу, снабженную мещалкой, холоднльником и 1чапелы1ой воронкой, загружают 18,44 г хлорнстого цианура, 66,16 г 2, 4. 6-трибромфенола, 300 мл кснлола и 0,5 г X, Х-диметиланилина. Реакционную смесь размешивают при температуре кнпения ксилола. Образовавщийся НС1-газ вытесняют азотом и: реакционной емесн н поглощают в растворе ХаОН. По окончании выделения хлористого водорода реакционную смесь фильтруют. Сырой продукт выпадает в виде белых криста; лов с почти количественным выходом. Точка
плавления 176-200°С. Перекристаллизовывают из бензина (область кипения 150-165°С). Точка плавления 200-204°С.
Пример 6. 2, 4-ди-(диэтиламин)-6-нентахлорфенокси-З-триазин.
В трехгорлую колбу, снабженную мешалкой, холодильником и вводной трубкой, загружают 19,79 г 2,4-ди-(диэтнламип)-6-хлор-5триазина, 20,4 г пентахлорфенола, 300 мл толуола н 0,5 мл три-н-бутиламина. Реакционную смесь размешивают при температуре кипения толуола.
Образовавшийся HCI-газ вытесняют азотом из реакционой смеси и ноглон ают в растворе NaOH. По истечении приблизительно, 24 час реакция заканчивается. Толуол нолиостью удаляют, а липкий остаток обрабатывают пеитаном, вследствие чего масса кристаллизуется. Точка плавления 107-- 12°С. После кристаллизации из цнклогексана точка нлавлепия 117--119°С.
Пример 7. 2-н-бутилал1ин-4, ()-ди-(нентах.юрфенокси) -S-три аз ИИ.
В трехгорлую колбу, снабженную мешалкой, холодильником и вводпой трубкой, загружают 22 г 2-н-бутнламииа-4, 6-дихлор-3-триазпна, 53 г пентахлорфенола, 0,5 мл N, N-днизобутиламипоанетоиитрила, 300 мл ксилола. Реакционную смееь размешивают при температуре кинення ксилола. Образовавшийся ITCi-газ вытееняют азотом из реакционной смееи. По истечении приблизительно 20 час реакция заканчивается. Вынавший осадок отфильтровывают. Точка плавления 240-241 С. Анализ:
Вычислено, %: С 33,7; Н 1,48; N 8,3; CI 51,7.
Найдено, %: С 33,5; 11 1,6; N 8,1; С1 51,3.
Приме-р 8. Аналогично нрнмеру 1 нод1 ергают взанмодействню 24,1 г 2-анилид-4,6-днхлор-З-триазина и 53.3 г нентахлорфенола в присутствии амина, N, К -дн-к-бутплбепзойпой кислоты в качестве катализатора. По нстеченнн приблизительно 24 час реакция заканчнвается. Точка плавления вынавн1его продукта 262°С. Выход 96%.
Пример 9. Апалогичио примеру 1 иодвергают взаимодействию 92,2 г цианурхлорида и 231 г тетрахлорфенола с 1,5 г амида N, X, N, К-тетра-/-/-бутиладнпиновой кислоты в качестве катализатора. Полученный продукт имеет точку плавления 235С. Выход 97%.
Пример 10. Аналогично нримеру 4 подвергают взаимодействию 18,44 г цианурхлорида и 53,3 г пеитахлорфенола с 0,5 г амида N. N-ди-н-пропилгексановой кислоты в качестве катализатора. Полученный нродукт имеет точку нлавлення . Выход 92%.
Пример 11. Аналогично примеру 4 нодвергают взанмодействню 18,4 г цианурхлорнда и 53,3 г нентахлорфенола в 300 мл ксилола с 0,5 г амнда гекеаметилфосфорпстой кислоты в качестве катализатора. По окоичаиии отнаепления ПС1 выпадает продукт в виде белого
осадка. Точка плавления 322°С, вы.код приблизительно 90%.
Пример 12. Аналогично примеру 3 подвергают взаимодействию 41 г цианурхлорида и 88 г 2, 4, 6-трихлорфенола с 0,5 г метиленаминоацетонитрила в качестве катализатора. По окоичании отщепления ПС1 реакционную смесь фильтруют. Продукт плавится при 188°С. Выход нриблнзительно 90%.
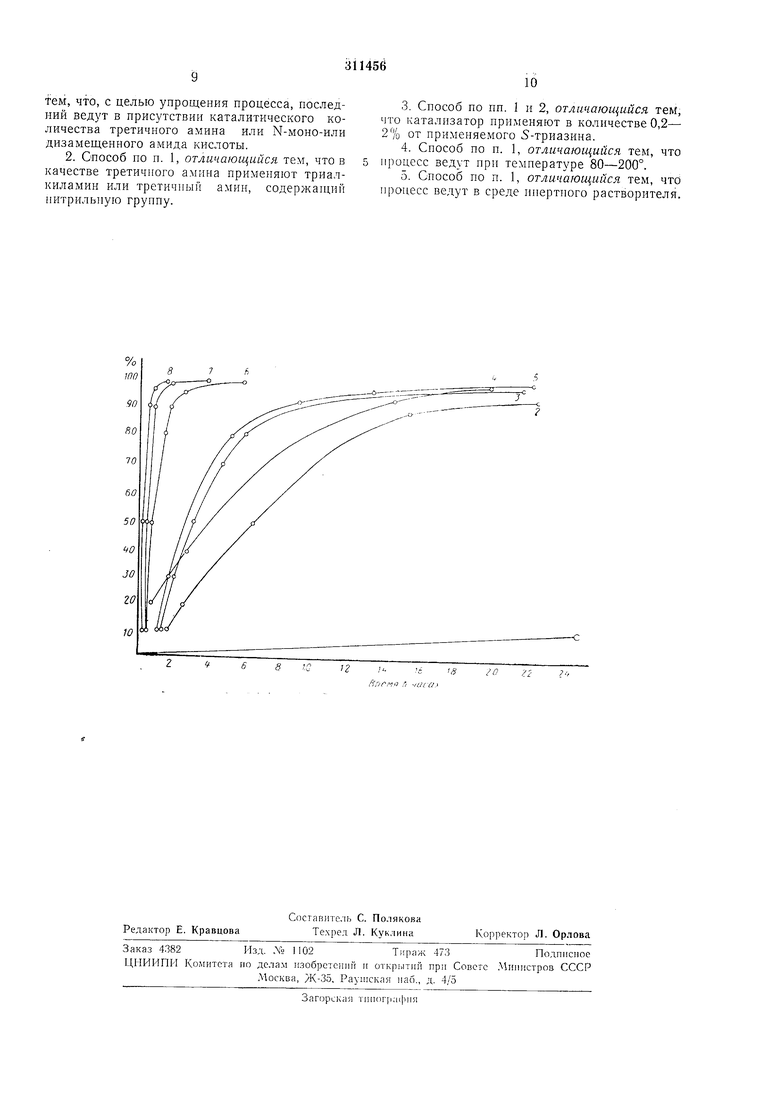
В нриложепной таблице кривая / показывает протекание выделеиия HCI в результате реакция 18,4 г хлористого цианура и 53,3 г пентахлорфенола в 200 мл ксилола при темнературе кинения раетворителя без добавления катализатора. Кривая 2 показывает время нротекания выделеиия в присутствии 1% дин-бутпламида бензойной кислоты, кривая 5-в нрпсутствии 1 % бенза.мида, кривая 4 - в присутствии 1 7о метиламииоцетонитрила, кривая
5 - в нрисутствни 1% N, N-диметиланилина, кривая 6 - в нрисутствии 1% амида N, N, N, X, 1, N-гекеаметил-фосфорпой кислоты, кривая 7 - в присутствии 1% три-н-бутиламииа, кривая - в присутствии 1% ннридина.
11 р е д м е т изобретен и я
1. Споеоб получеиия галогеннроидводных фенокситриазнна общей (1)ормул1,1:
галонд;
остаток
- С
где Х. // имеют вьпнеуказанные значения, и.Ш
грунна .Х
где н R2-галогепнрова1П1ЫЙ низшнй алкил, содержани1й до 4 атомов углерода, циклоалкил, содержаии-и до 8 атомов углерода, или RI - водород, а R2 - галогеннрованный низшн1 | алкил, содер каш,нй до 4 атомов углерода, никлоалкил, содержап1ий до 8 ато.мов углерода, арил, или RI н R2 в.месте могут быть составной частью азотсодержан1его гетероцикл а;
R, К,
Z га.юнд и.1И груииа - Х
() 1 где RI н имеют вышеуказанные значення,
тем, что, с целью упрощения процесса, последний ведут в присутствии каталитического количества третичного амина или N-моно-или дизамещенного амида кислоты.
2. Способ по н. 1, отличающийся тем, что в качестве третичного амина применяют триалкиламин или третичный амин, содержании питрильную грунну.
3.Способ по пп. 1 н 2, отличающийся тем, что катализатор нрименяют в количестве 0,2- 2% от применяемого 5-триазина.
4.Способ но п. 1, отличающийся тем, что процесс ведут нрн температуре 80-200°.
5.Способ но н. 1, отличающийся тем, что процесс ведут в среде ннертного растворителя.



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИАМИДОВ В МЕЛКОЗЕРНИСТОЙФОРМЕ | 1969 |
|
SU245685A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИСИЛАЗАНОВ | 1971 |
|
SU294355A1 |
| Способ получения 2-/2',2',2'-тригалогенэтил/-4-галогенциклобутан-1-онов | 1978 |
|
SU917695A3 |
| СПОСОБ ПОЛУЧЕНИЯ АЦИЛИРОВАННЫХ | 1970 |
|
SU266656A1 |
| СПОСОБ ПОЛУЧЕНИЯ АМИДОВ ИЛИ ПЕПТИДОВ N-АЦИЛ-а-АМИНОКИСЛОТЫ | 1972 |
|
SU328572A1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ДИАЗОТИПНЫХ КОПИЙ ПО ОДНОКОМПОНЕНТНОМУ МЕТОДУ | 1970 |
|
SU264285A1 |
| СПОСОБ ПОЛУЧЕНИЯ АКТИВНЫХ КРАСИТЕЛЕЙ | 1972 |
|
SU332636A1 |
| УЛУЧШЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ 2,4-ДИАМИНО-6-АЛКИЛТИО- S -ТРИАЗИНОВ | 1994 |
|
RU2162080C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ КАРБОНОВОЙ КИСЛОТЫ И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1994 |
|
RU2145959C1 |
| БИБЛИОТЕКА I | 1971 |
|
SU313356A1 |

юо
90 КО 10 60 50
40 JO
го

Авторы
Даты
1971-01-01—Публикация