Предлагается способ получения нового фенилового эфира оксим-О-угольной кислоты общей формулы 0-eo-o-N c где Ri - алкил с 1 - 4 атомами углерода, алкенил с 2 - 4 атомами углерода или фенил; Ra - алкил с 1 - 4 атомами углерода, алкенил с 2 - 4 атомами углерода, феНИЛ или водород, RI и Кг вместе означают алкилен с 4-И атомами углерода; Ra - низший алкил, галоген, фенил или алкоксикарбонил, или два рядом стоящих заместителя Rs означают вконденсироваиное ароматическое гетероциклическое кольцо; R4 означает Rs или алкилен; д О, 1, 2, 3, 4, который может найти применение в качестве соединения, обладающего биологической активностью. Известен способ получения производных угольной кислоты путем взаимодействия спирта с хлорпроизводным эфира угольной кислоты. Предлагаемый способ основан на известной химической реакции, однако, использование новых исходных соединений позволяет получить фениловый эфир оксим-О-угольной кислоты, обладающий улучшенными свойствами. Способ заключается в том, что фенол общей формулы где Rs, R4 и я имеют указанные значения, подвергают взаимодействию с хлоридом сложного эфира оксим-О-угольной кислоты общей формулы /«. C1-CO-0-NПроцесс проводят в инертном органическом растворителе, например в ацетоне, метилэтилкетоне, метиленхлориде, хлорбензоле, бензоле, толуоле, ацетонитриле, бензонитриле или этиловом эфире уксусной кислоты, цри минус 40-плюс 100°С, предпочтительно при минус 10-плюс 40°С, причем образовавшийся вб время реакции хлористый водород связывается при помощи основных веществ, например триэтиламина, диметилбензиламина, диметиланилина, пиридина, пиколина, хинолина, карбоната «алия, карбоната натрия, или же в реакцию непосредственно добавляют соли щелочного металла и фенолов.
Применяемые в качестве исходного материала хлориды сложного эфира оксим-0-угольной кислоты частично известны. Они могут быть получены, если, например, оксим в присутствии третичного амина, такого как диметиланилин, диэтиланилин, пиридин, пиколин, хинолин, триэтиламин или диметилциклогексиламин, в инертном органическом растворителе, таком как метиленхлорид, этиленхлорид, четыреххлористый углерод, лигроин, толуол или хлорбензол, при минус 20-плюс 50°С, предпочтительно при минус 10-плю-с 10° С, подвергарь реакции обменного разложения с фосгеном. От реакционной смеси гидрохлорид третичного амина, например, отфильтровывают или. отмывают холодной сильно разбавленной минеральной кислотой, в случае надобности сушат над сульфатом натрия и раствор контцентрируют. Нет необходимости хлориды сложного эфира оксим-О-угольной кислоты выделять в чистом виде, для реакции с фенолами могут быть взяты растворы хлоридов сложного эфира оксим-О-угольной кислоты.
Пример 1
Вг
СН,
(/ yo-co-o-N cC сснз
Вг
к смеси 72 г 3-хлор-2,4,6-трибромфенола (0,197 лголь), 17,4 г пиридина (0,22 моль
и 80 мл ацетонитрила при 23С прикапывают 27,1 г хлорида сложного эфира ацетоксим-Оугольной кислоты, растворенного в 27 г хлористого метилена. Реакционную смесь выдерживают в течение 7 час. при 40° С, затем добавляют к ней 30 мл хлористого метилена и размешивают при 0°С с раствором карбоната натрия. Раствор хлористого метилена два раза промывают водой, сушат над карбонатом
калия и упаривают. Выход сложного эфира 3-хлор-2,4,6-трибромфенилугольной кислоты составляет после сушки остатка 78 г (85% от теоретического), т. пл. 103,5-106°С. Перекристаллизованное из бутилацетата - петролейного эфира соединение плавится при 113,5°С. Пример 2
хСНэ 0 cO-0-N j
К 25,3 г 3-хлор-2,4,б-трийодфенола (0,05
моль} в 50 мл сухого ацетона при интенсивном размешивании добавляют 8,5 г порошкообразного карбоната калия (0,061 моль} и затем при 24° С прикапывают 0,06 моль хлорида сложного эфира ацетоксим-О-угольной кислоты в виде 34%Ного раствора в хлористом метилене. Смесь размешивают еще в течение 2 час при 25° С, затем добавляют к ней 600 жл хлористого метилена и 200 г льда. Раствор хлористого метилена два раза промывают ледяной водой, сушат над карбонатом калия и сильно упаривают. Путем добавки 300 мл петролейного эфира и охлаждения доО°С усиливают выделение кристаллов. Выход сложного эфира 3-хлор-2,4,6-трийодфенил-О-ацетоксимугольной кислоты после сушки составляет 23,5 г (77,5% от теоретического), т. пл. 196°С с разложением.
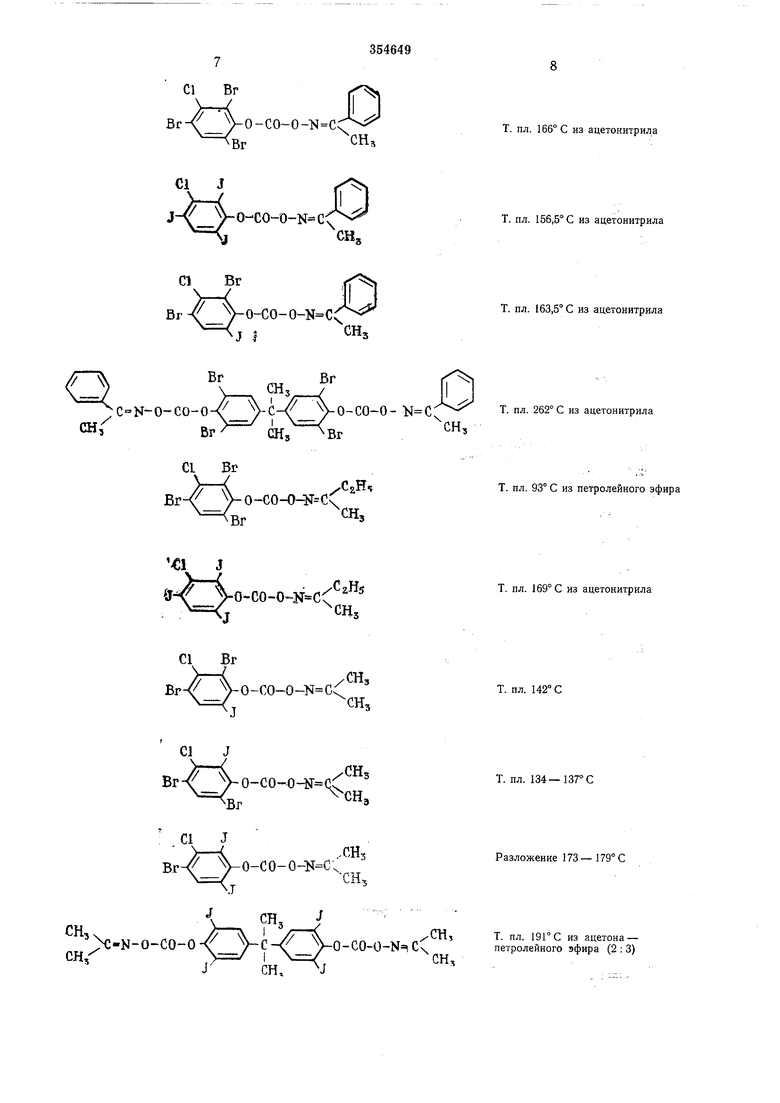
Аналогично описанному в рримерах 1 и 2 способу получены фениловые эфиры оксим-Оугольной кислоты, константы которых приведены ниже.
ci;,
Вг
0-CO-0-N C
CIL
Vo-co-o-N-cf
Cl
// Vn-i- - - 5
0-CO-O-N-C
СДз
С1 С1
/СНз
0-C(
CHj
Разложение при 95° С
Т. пл. 108- 115,5° С, разложение из ацетона
т. пл. 43,5° с из дибутилового эфира
т. пл. 156- 160° С из ацетона



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,1Л-ТРИХЛОРЭТАНА | 1972 |
|
SU353412A1 |
| ВПТБ10Й €51Д;Г.ТГ;!Г?5Т?ЯШ145ИСП511 | 1973 |
|
SU374825A1 |
| СПОСОБ ПОЛУЧЕНИЯ АМИНОФЕПИЛ-ЦИКЛОАМИДИНОВ ИЛИ ИХ СОЛЕЙ | 1973 |
|
SU404240A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОИДАНГИДРИДОВ Ы-ЗАМЕЩЕННОЙ АЦИЛКАРБАМИНОВОЙ КИСЛОТЫ | 1971 |
|
SU307566A1 |
| ЕИБЛ^--С | 1973 |
|
SU366602A1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛКАРБАМАТОВ | 1968 |
|
SU212178A1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЯД-ТРИАЗОЛОВ | 1973 |
|
SU408477A1 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННБ1Х ПОЛИМЕРОВ | 1973 |
|
SU400108A1 |
| СПОСОБ ПОЛУЧЕНИЯ 5-АЗАПИРИМИДИН-НУКЛЕОЗИДОВ | 1973 |
|
SU374828A1 |
| СПОСОБ ПОЛУЧЕНИЯ АМИДОВ ИЛИ ПЕПТИДОВ N-АЦИЛ-а-АМИНОКИСЛОТЫ | 1972 |
|
SU328572A1 |

./СНз
0-CO-0-N C
т. пл. 130,5° С из ацетона
С1
хСНз 0-CO-0-N-C ;
vJtlj
С1 Вг
СНз
СК/ )-0-СО-ОтК С CHs С1
/СНз
CO-0-N C ,
С1 Вг
т. пл. 85° с из петролейного эфира
т. пл. 102° с из петролейного эфира
т. пл. 141° с из петролейного эфира/хлористого метиленаCl Вг / Br 0-CO-0-N C Br Cl J - Vo-eo-o-N c
С1 Вг Вг - -0-CO-0-N C
Бг
Вг
СНз
N-0-CO-0-// 0-СО-0- N 0
н;
Вг Шз Вг
CL Вг
/CgH, 0-СО-0-№СС
Бг
СН,
с н
0-CO-0-N CC СНз
/СНз 0-CO-0-N C 354649
т. пл. 163,5° С из ацетонитрила
Т. пл. 262° С из ацетонитрила
сн.
т. пл. 93° С из петролейного эфира
т. пл. 169° с из ацетонитрила
Т. пл. 142° С т. пл. 166° с из ацетонитрила Т. пл. 156,5° С из ацетонитрила
Т. пл. 134-137°С
-СНз
-O-CO-O-K C-СН; сн, / сн,. I /г I C-N-0-CO-0 у-с ч/ с Ч -/
Разложение 173-179° С хСИ, т. пл. 191°с из ацетона - CO-0-N iC петролейного эфира (2 : 3) пн
// A
СО-0-К С
co-o-N c
сн, сн
5
O-K-CX
сн.
J
(/СНз СНз
УО-СО-О- С I
ел1
СНд
Вг
(/еНз СНз
O-CO-0-K G I
/Lrl2 v H.
сн,
Вг
СНз CHs
VO-CO-O-N C,
сн.
f л СН
С1-С УО-С(ЬО-К-С(
.
Предмет изобретения
Способ получения фенилового эфира оксимО-угольной кислоты общей формулы
:(Вз)«
т. пл. 166,5° С из этиленхлорида/легкого бензина
Т. пл. 144,5° С из хлористого метнлеиа
т. пл. 144° с из этилацетата
Т. пл. 64° С из легкого бензина
т. пл. 104° с из ацетона
Т. пл. 110° С из ацетона
Т. пл. 121° С из ацетона
т. пл. 157,5° с из хлористого метилена/легкого бензина
RI - алкил с 1 - 4 атомами углерода, алкенил с 2 - 4 атомами углерода или фенил;
Ra - алкил с 1 - 4 атомами углерода, алкенил с 2 - 4 атомами углерода, фенил или водород, Ra - НИЗШИЙ алкил, галоген, фенил или алкоксикарбонил, или два рядом стоящих заместителя Кз означают вконденсированное ароматическое или гетероциклическое кольцо; R4 означает Кз или алкилен; п О, 1, 2, 3, 4, отличающийся тем, что фенол общей формулы где Ra, и л имеют указанные значения, подвергают взаимодействию с хлоридом слож кого эфира оксим-О-угольной кислоты общей формулы С1-СО-0-№
где RI и R2 имеют указанные значения, с последующим выделением целевого продукта известным способом.

Авторы
Даты
1972-01-01—Публикация