1
Изобретение относится к способу получения йе описанных в литературе сложных эфиров циклопропанкарбоновой кислоты, которые Используются в качестве я-нсектицидов.
Известен способ получения эфиров циклопропанкарбоновой кислоты общей формулы
2 Н-З
4-Ri
М
й/
й
карбонойой кислоты со спиртом общей формулы
2 RS
Ri-fHbCH20H й/
где RI, Ra и Rs имеют вышеуказанные значения.
Предлагаемый способ получения сложных эфиров циклопронанкарбоновой кислоты общей формулы
где RI - всдород, галоген, алкил, алкенил, алкдиенил, бензил, фурфур.ил и тенил;
R2 и Rs - одинаковые или различные, водород, галоген, алкил, нричем если Ri и Ra - алкил, то они могут быть связаны алкиленовой группой;
Й4 - водород, метил;
R5-метил; если R4 - водород, то Ra - группа, включающая 2-метил-1-пропен1ИЛ, 2метоксикарбонил-1-нропенил или фенил, взаимодействием галоиданг.идрида циклопропанRI
X
О - сн с
Нг
R
с
Y
СНз СНз
20
где RI - водород, или метил;
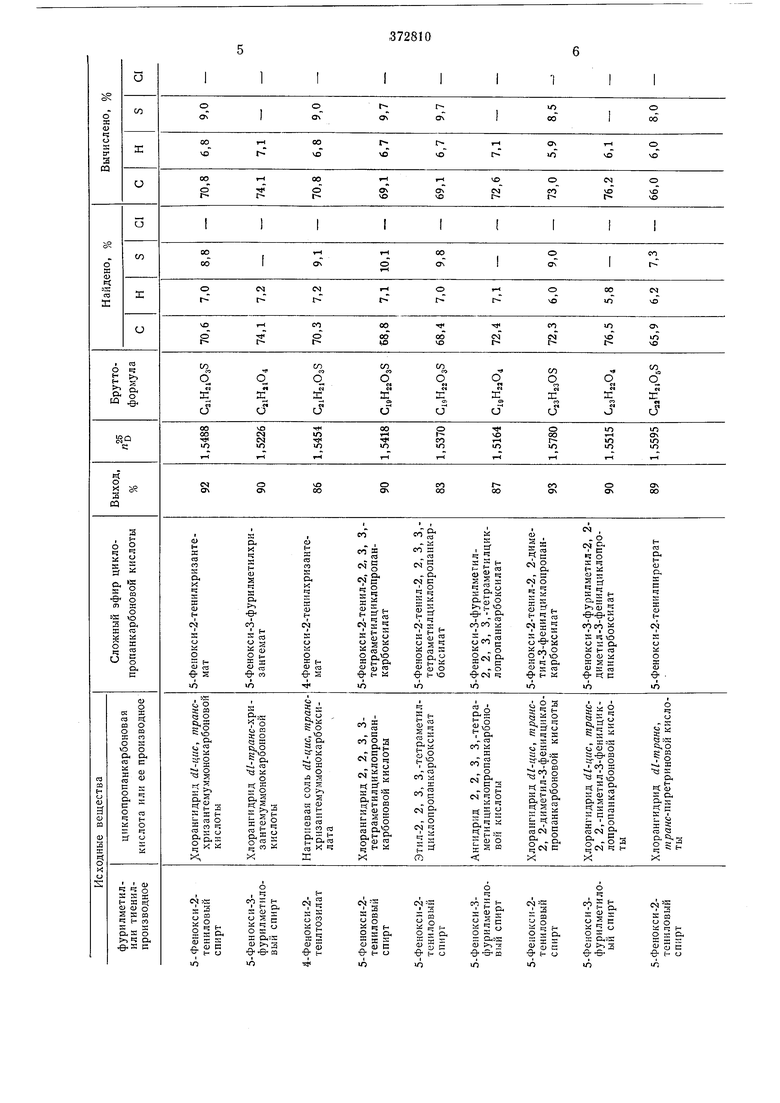
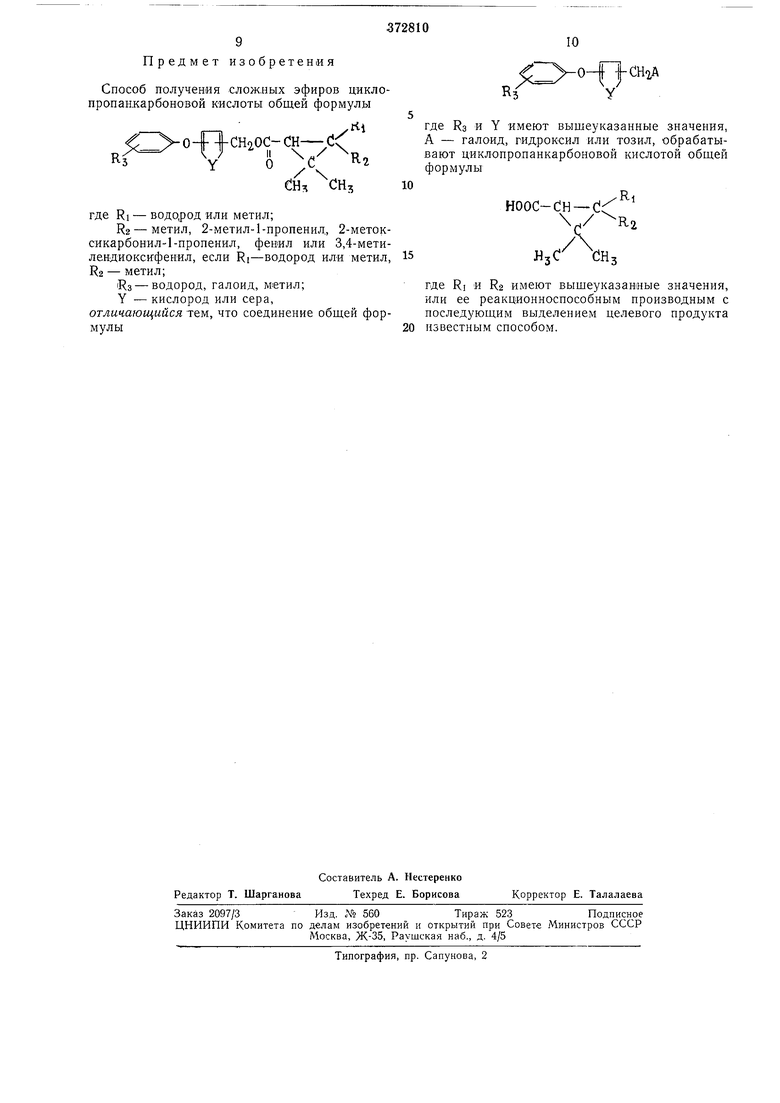
Ro-метил, 2-метил-1-нропенил, 2-метоксикарбонил-1-пропенил, фенил или 3,4-метилендиокснфенил; если Ri - водород или метил. Re - метил; Ra - водород; метил; Y - кислород или сера, состоит в том, что соединение общей формулы € -о-{П-й1аЛ ЪY где Кз и Y имеют вышеуказанные значения; А - галоид, гидроксил или тозил, обрабатывают циклоиропанкарбоновой кислотой общей формулы /RI шос-сн-ее ч/ Ri где RI и Кг имеют вышеуказанные значения, или ее функциоиальным производным последующим выделением целевого продукта .известным сиособом. При использовании кислоты реакцию проводят при нагревании, в присутствии катализатора дегидратации, например минеральной кислоты, я-толуолсульфокислоты, «ли азеотропного растворителя, такого, как бензол и толуол. Реакцию можно проводить ,в среде инертного растворителя, такого, как бензол или петролейный эфир, содержащего обезвоживающее средство, например дициклогексилкарбодиимид, при иагревании или без него. В случае применения галоидангидрида кислоты реакцию проводят при комнатной температуре в присутствии органического третичного амина, такого, как пиридин, триэтиламин, являющегося акцептором галоидводорода, и инертного растворителя, такого, как бензол, толуол, пиробенвол. Из галоидангидридов кислоты лучше применять хлорангидрид. При цспользовании низшего алкилового, например метилового, этилового, н-пропиловрго, изо-пропилО|Вого и н-бутилового, сложного эфира циклопропанкарбоновой кислоты реакцию проводят в присутствии основного катализатора, такого, как алкоголят натрия, при нагревании в инертном растворителе, например в бен13оле или толуоле. Пример 1. Взаимодействие спирта с галоидпроизводным карбоновой кислоты. К раствору 0,05 моль соответствующего спирта в 3-кратном объеме сухого бензола, добавляют 0,075 моль пиридина и раствор, содержащий 0,053 моль хлорангидрида карбоновой кислоты в 3-кратном объеме сухого бензола, выдерживают в условиях герметичности в течение иочи и приливают немного воды для растворения солянокислого пиридина. Образовавшийся водный слой отбрасывают. Органический слой последовательно промывают 5%-.ной соляной кислотой, насыщенным вод510 15 20 25 30 35 40 45 50 55 60 ным раствором бикарбоната натрия и насЫщенным раствором хлористого натрия, выс шивают над безводным сернокислым натрием и отгоняют бензол. Остаток хроматографируют на силикагеле и выделяют сложный эфир в виде светло-желтого масла. Пример 2. Взаимодействие спирта с карбоновой кислотой. К раствору 0,05 моль соответствующего спирта и 0,05 моль карбоновой кислоты в 3-кратном объеме бензола, добавляют при перемешивании 0,08 моль дициклогексилкарбодиимида, оставляют герметически закрытой .на всю ночь, на следующий день нагревают 2 час с обратным холодильником и извлекают эфир, как в примере 1. Пример 3. Взаимодействие спирта с ангидридом .карбоновой кислоты. К раствору 0,05 моль соответствующего спирта в 3-кратном объеме толуола добавляют 0,055 моль ангидрида карбоновой кислоты, нолученного из карбоновой кислоты и уксусного а 1гидрида, и нагревают 3 час при 100°С для завершения реакции. После охлаждения реакцион.ную смесь нейтрализуют 10%-ным едким натром при температуре не выше 10°С .и образующуюся кислоту извлекают из водного слоя в виде соответствующей натриевой соли. Органический слой обрабатывают, как указано в примере 1, и получают сложный эфир. Пример 4. Взаимодействие спирта с .низшим алкиловым сложным эфиром карбо.новой кислоты. К раствору 0,06 моль этилового эфира карбоновой кислоты и 0,05 моль спирта в 5-кратном объеме сухого толуола добавляют 0,005 моль этилата натрия, тщательно перемешивают и кипятят 10 час с обратным холодильником, здаляя образующийся этанол в виде азеотропа из голов.ной части ректификационной колонны. После осторожного удаления воды из органического слоя выделяют сложный эфир, применяя методику, указа.нную в примере 1. Пример 5. Взаимодействие галоидпроизводного с карбоновой кислотой. Раствор 0,05 моль соответствующего галоидпроизводного и 0,06 моль карбоновой кислоты в 3-кратном объеме ацетона нагревают при 15-20°С, прикапывают раствор 0,08 моль триэтиламина в 3-кратном объеме ацетона в течение 1 час при перемешиваиии, кипятят 2 час с обратным холодильником и охлаждают. Выделившийся солянокислый триэтиламин отфильтровывают, от фильтрата отгоняют ацето.н, к остатку добавляют 3-кратный объем бензола, обрабатывают органический слой по методике, указанной в примере 1, и получают сложный эфир. Полученные результаты приведены в таблице. Предмет изобретения Способ получения сложных эфиров циклопропанкарбоновой кислоты общей формулы .ос-сн Х СН, СНз где RI - водород или метил; Ra - метил, 2-метил-1-пропенид, 2-метоксикарбонил-1-пропенил, фенил или 3,4-метилендиоксифенил, если Ri-водород или метил, R2 - метил; iRa - водород, галоид, метил; Y - кислород или сера, отличающийся тем, что соединение общей формулы0-f|-CH A где Ra и Y имеют выщеуказанные значения, А - галоид, гидроксил или тозил, обрабатывают циклопропанкарбоновой кислотой общей формулы НООС-СН -0 ./ R2 Лнз где RI и R2 имеют выщеуказанные значения, или ее реакционноспособным производным с последующим выделением целевого продукта известным способом.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ ЦИКЛОПРОПАНКАРБОНОВОЙ КИСЛОТЫ | 1972 |
|
SU331540A1 |
| Способ получения эфиров замещенных циклопропанкарбоновой или фенилуксусной кислот | 1974 |
|
SU576911A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ТИОФЕНА | 1971 |
|
SU289593A1 |
| Способ получения циклопропанкарбоксилатов | 1974 |
|
SU577968A3 |
| Способ получения циклопропанкарбоксилатов | 1972 |
|
SU527133A3 |
| Способ получения замещенных эфиров хризантемовой кислоты | 1971 |
|
SU437273A1 |
| Способ получения производных уксусных кислот | 1973 |
|
SU627749A3 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ЭФИРОВ ЦИКЛОПРОПАНКАРБОНОВОЙ КИСЛОТЫ | 1969 |
|
SU253681A1 |
| Способ получения эфиров циклопропанкарбоновых кислот | 1973 |
|
SU584759A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БУТИРОФЕНОНА | 1973 |
|
SU404242A1 |


Авторы
Даты
1973-01-01—Публикация