Изобретение относится к способу получеиия Органических люминофоров .класса азометидов - производных о-тозилам,инобензальдепида ,о.бщен формулы где R - арил или алкил; , С1, Вг, ОСНз, NOs, которые 1могут найти применение в .народном Х|0зяйстве. Известен спосой получения органических люминофоров класса азометинов - производных салицилового альдегида, в частности сал.ид.илаль - N, N-диметил - «-фенилендиамина, при взаимодействии салицилового альдегида с N, N-диметил-ге-фенилендиамином в среде этилового сп.ирта. Однако при облучении лю-минофоров этого класса УФ-светом углубляется их Окраска и резко снижается интенсивлость свечения, что значительно сужает область их применения. С целью устранения указанного недостатка предлагается о-тозиламиноазометины получать при Обработке о-тозиламилобензальдегида или его 5-замещенных ароматическим или алифатическим амином в среде подходящего растворителя, например метанола или уксусной кислоты, с последующим выделением целевого продукта известными прие.мами. Приме р. ,К раствору 0,005 моль соответствующего й-тозиламинобелзальдегида в 25мл метанола, до-бавл яют раствор 0,005 моль соответстзующего ами1на в 5 мл Метанола, прибавляют 3-4 капл.и ледялой уксусной кислоты и кипятят 5 час. После отгопки половины растворителя охлаждают, отфильтровывают кристаллы и перекристалл.изовывают их из подходящего растворителя. Выход 60-80%. В таблице приведены основные люминесцентные характеристики получаемых люминофоров в кристаллическо.м состоянии, причем за 100% принята интенсивность свечения салицилаль-М,Ы-диметил-«-фелилендиамина, выпускаемого нащей промыщленностью как люмогел оранл-;евь Й 604-(613). Имея сра1В1Ни.мую с салицилальаиили1на.м-и, а в некоторых случаях и более высокую инте; сивность свечения, люминофоры предлагаемого класса отлич.аются от иих полным отсутствием фототропии .и, вследствие этого, очень высокой светостойкостью. Спектр и интенсивность излучения люминофоров ие изменяются после 6-8 час облучения нефильтрованным Уф-светом ртутнокварцевой ламлы .
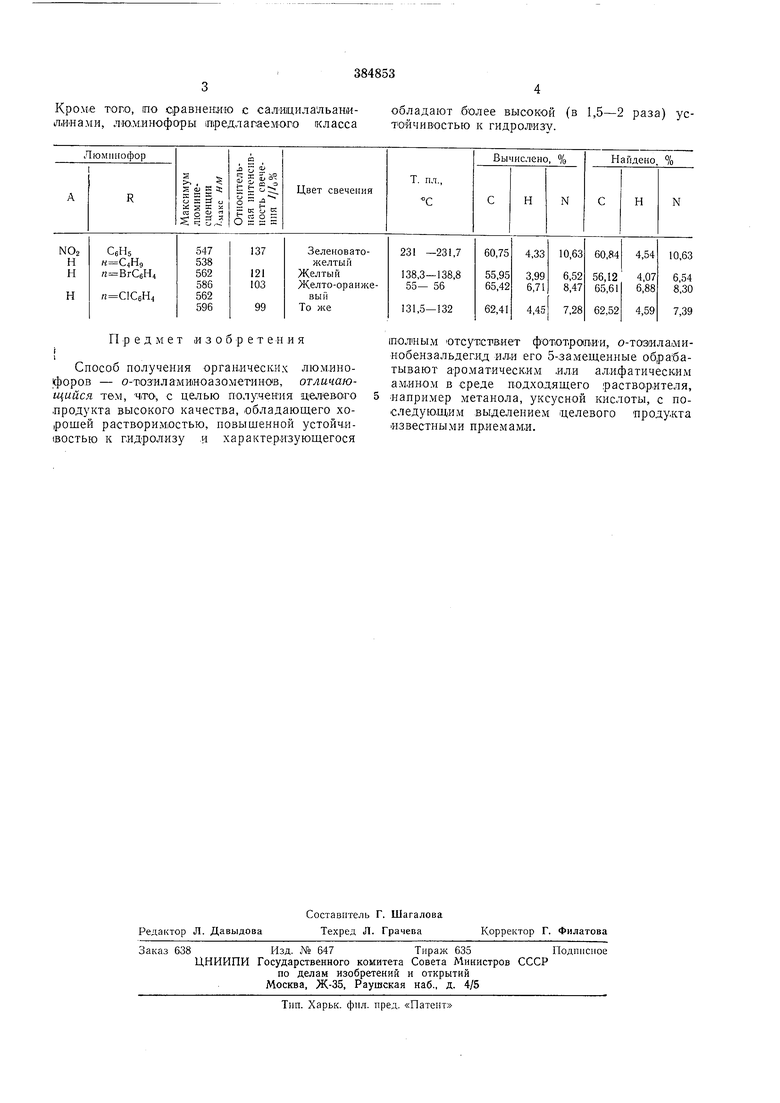
Кроме того, по сравнению с салицилальанил,и«ами, лю.минофоры ередлапаемого класса
обладают &олее высокой (в 1,5-2 раза) устойчивостью к гидролизу.
| название | год | авторы | номер документа |
|---|---|---|---|
| 7-АЛКОКСИ-8,9-ДИГИДРОКСАНТИЛИЕВЫЕ СОЛИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2100353C1 |
| ПРОИЗВОДНЫЕ 8,9-ДИГИДРОКСАНТЕНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2106350C1 |
| СОДЕРЖАЩАЯ АЛЬФА-СИЛАН ПОЛИУРЕТАНОВАЯ КОМПОЗИЦИЯ С АНИЗОТРОПНЫМИ СВОЙСТВАМИ МАТЕРИАЛА | 2009 |
|
RU2513108C2 |
| СОДЕРЖАЩАЯ ОРГАНОМЕТОКСИСИЛАН ПОЛИУРЕТАНОВАЯ КОМПОЗИЦИЯ С АНИЗОТРОПНЫМИ СВОЙСТВАМИ МАТЕРИАЛА | 2009 |
|
RU2513109C2 |
| КРАСЯЩАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ СОЕДИНЕНИЕ П-АМИНОФЕНОЛЬНОГО ИЛИ П-ФЕНИЛЕНДИАМИНОВОГО ТИПА, ЗАМЕЩЕННОЕ СИЛАНОВЫМ РАДИКАЛОМ | 2002 |
|
RU2237765C2 |
| ГИДРОКСИФЕНИЛТРИАЗИНЫ, СОДЕРЖАЩИЕ АРОМАТИЧЕСКУЮ КАРБОЦИКЛИЧЕСКУЮ КОНДЕНСИРОВАННУЮ КОЛЬЦЕВУЮ СИСТЕМУ | 2006 |
|
RU2418791C2 |
| Способ получения производных гексагидробензпираноксантенонов | 1979 |
|
SU927117A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПАРА-АМИНОФЕНОЛОВ | 2014 |
|
RU2567552C1 |
| СПОСОБ ПОЛУЧЕНИЯ N, N-БИС-АЦЕТОАЦЕТАРИЛАМИДОВ | 2005 |
|
RU2283300C1 |
| 1-(5-Фенилоксазолил-2)-4-[5-(X-пиридил)-1,3,4-оксадиазолил-2]бензолы в качестве люминесцирующих добавок органических сцинтилляторов | 1982 |
|
SU1063053A1 |

Пред м е т и з о б р е т е в и я
i I
Способ получения органлческих люминофоров - о-тозиламияоазометинов, отличающийся тем, -что, с целью получения щелев-ого .продукта высокого качества, обладающего хорошей растворимостью, повышенной устойч.и(востью к гидролизу .и характеризующегося
1ПОЛ1НЫМ отсутствиет фототроп.и-и, о-тозила1минобензальдегид иди его 5-замещенные обрабатывают ароматическим .или ал.ифатическим ам.ином в среде подходящего раствор.ителя, .например метанола, уксусной кислоты, с последую.Щ(Им выделением щелевого продукта .известными пр.иемам.и.
Авторы
Даты
1973-01-01—Публикация