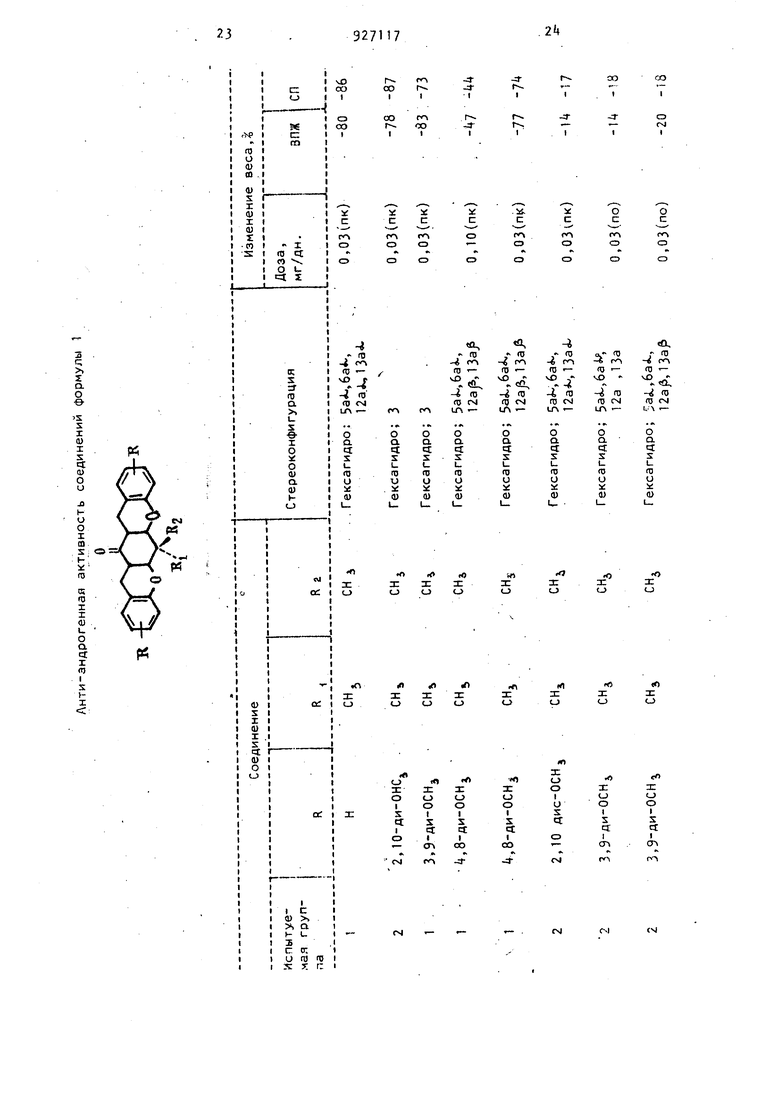
39 рая включает в себя соли щелочных ме таллов, соли четвертичных аммониевых оснований с содержанием атомов углерода в катионном остатке 10-28 или соли третичного амина с содержанием атомов углерода в катионном остатке 7-21. Исходные дигидробензпиранокстатеноны формулы 2 получаютвзаимодействием алкоксизамещенного 2-оксибензальдегида с , -диметил-2,5 Циклогексадиеном в присутствии пирролидина или его моно- или ди-замещенных производных в среде инертного органического растворителя при 0-б5°С. Электролитическое восстановление проводят путем растворения или сус- пендирования соответствующего дигид-. робензипираноксантенона в среде органического растворителя или в ере- 0 де, представляющей собой водно-органическую смесь. В качестве органи-: ческого растворителя используют раст ворители амидного типа, например М,М-диметилформамид и Н,Н-диметилацетамид, нитрилы, такие, например, как ацетонитрил, спирты, например метанол и этанол, ароматические угле водороды, такие как бензол и толуол, галоидированные углеводороды, такие как метиленхлорид и хлороформ и т.д. Предпочтительно используют в процессе амиды, нитрилы или спирты, такие как N N-диметилформамид, ацетонитрил или метанол. о В качестве электролита используют в частности различные соли, включая галогениды, тозилаты и перхлораты та ких щелочных металлов как литий, нат рий и калий или четвертичные аммоние вые соли, такие, например, как галогениды и перхлораты четвертичных аммониевых оснований, такие как тетраалкиламмоний, триалкиларалкиламмоний диалкилдиаралкиламмоний или алкилтриаралкиламмоний. Предпочтительно используют соль тетрабутиламмония. Другим классом электролитов являются соли третичных аминов и, в частности, галогенгидраты, тозилаты и перхлораты триалкиламинов, диалкиларалкиламинов,1алкилдиаракиламинов и триаралкиламинов, содержащие в катионной части в общем от 7 ДР 21 атома углерЪда. Предпочтительно используют соли трибутиламина и,в частности, п-толуолсульфонат (тозилат)трибутиламина. 7 В реакционную среду вводится также источник протонов. Наилучшие результаты дает использование сравнительно слабых карбоновых кислот, имеющих рКа в пределах от 2 до 6, и, в частности, бензойной кислоты и уксусной кислоты. При электролитическом восстановлении дигидробензпираноксантенона она присутствует в реакционной среде в количестве от примерно 1 до 15 мг на мл среды. Электролит используют в количестве 0,01 моля - 1,0 моля, а карбоновую кислоту - в количестве 1-5% по весу в расчете на объем реакционной среды. Полученную таким образом смесь приводят в контакт с катодом электролитической.ячейки.;На электроды этой ячейки подается потенциал, соответствующий точке фонового разряда. Этот потенциал определяется путем построения кривой зависимости ток - потенциал (сила тока - напряжение) для рабочих электродов в используемой среде перед проведением электролиза. Электролитические ячейки состоят из соответствующим образом подобранных катода и анода, разделенных мостиком. Катод, используемый в этом процессе, обычно является ртутным. К числу материалов, которые можно использовать для изготовления анода, относятся платина и углерод (графит) . Металлическая платина является наиболее предпочтительным материалом для изготовления анода, в особенности тогда, когда ему придают форму тонкой металлической сетки или проволочной ткани. Углерод, благодаря его низкой стоимости, представляет собой другой предпочтительный анодный материал. Мостик, соединяющий катод и анод, может быть обычным солевым мостиКом, таким, например, как А-процентная (s водная смесь, насыщенная хлористым калием. Таким мостиком может быть также подходящая пористая мембрана, например ионообменная мембрана, керамическая мембрана или мембрана,спеченная из стеклянной крошки, пористость которой может варьироваться от малой до средней пористости. Электролитическая ячейка состоит из снабженного термостатирующей рубашкой стеклянного цилиндрического катодного отделения, в котором под59вешивается стеклянное анодное отделение, одним из элементов которого является пористая стеклянная пластин ка, спеченная из порошкообразного стекла. Катод присутствует в ячейке в виде резервуара ртути, имеющего кольцевую форму. Анодное отделение обычно представляет собой пористый стеклянный цилиндр или кольцевую в поперечном сечении стеклянную трубку с двойными стенками, снабженную кольцевой стеклянной пористой пластинкой, изготовленной из спеченного стеклянного порошка и впаянной в ниж ней части упомянутой сте| лянной трубки. Анод представляет собой, как правило, платиновую проволочку,опущенную в ту же смесь органической или водно-органической среды и элект ролита, которая применяется для заполнения катодного отделения. Электролизная ячейка закрывается сверху колпачком, через который в ячейку вставляется деаэрирующая пластинка (воздушный фильтр), эталонный электрод-зонд и-термометр. Эталонный электрод-зонд представляет собой стеклянную трубку, содержащую волокнистую набивку, в которую вставляется насыщенный каломельный электрод. Электролитическое восстановление дигидробензпираноксантенонов осуществляется следующим образом в катодное пространство электролитической ячейки помещают соответствующим образом подобранную смесь, состоящую из органической или водно-органической среды, электролита и донора протонов. К этой смеси при перемешивани добавляют заранее рассчитанное количество (примерно 1-15 милиграмма/мл) соответствующего дигидробензпираноксантенона и затем устанавливают над лежащим образом относительно катода кольцевое анодное отделение, содержа щее, смесь органической или водно-органической среды и электролита, вместе с колпаком крышкой), накрывающим электролитическую ячейку .. Затем в ячейку через деаэрирующую фрит ту подают ток аргона, который пропус кают через перемешиваемую катодную dMecb. После завершения деаэрации (вытеснения воздуха аргоном), на что требуется обычно около 15 мин, деаэрирующую фритту-барботер поднимают и фиксируют в положении выше поверхности раствора в катодном отделении , продолжая в дальнейшем пропускать 7« ток аргона через ячейку над жидкостью. Затем к электродам ячейки.подводят заранее определенный электрический потенциал и поддерживают его до тех пор, пока количество тока, пропущенного через ячейку, не будет приблизительно соответствовать удвоенному числу Фарадея, требуемому дли четырехэлектронного восстановления. Подсчет количества электричества (в кулонах), пропущенного через систему, может ПРОИЗВОДИТЬСЯ с помощью кулонметра, причем протекание процесса в системе можно также контролировать с помощью, тонкослойной хроматографии или жидкостной хроматографии высокого давления. Любой из этих методов полезен для определения степени завершенности реакции восстановления. После завершения электролиза -катодный раствор собирают и подвергают обработке для выделения целевого продукта реакции. Обработку реакционной смеси осуществляют следующими методами: сначала производят удаление большей части органического или еодно-органического разбавителя, дпя чего используют упаривание реакционной смеси в вакууме. Полученный в результате упаривания сиропообразный остаток растворяют в этилацетате. Этилацетатный раствор промывают несколько раз, как правило, равными объемами воды с целью удаления электролита и донора протонов. Затем этилацетатную фазу высушивают над подходящим обезвоживающим агентом, таким, например, как безводный сульфат ма1 ния, и фильтруют с целью отделения осуи1ителя. Высушенный Этилацетатный раствор упаривают в вакууме с целью удаления растворителя, и остаток сушат атечение нескбльких часов в вакуумсушильном шкафу при 5 С. Для получения целевого гексагидробензпираноксантенона полученный остаток подвергают перекристаллизации из подходящего растворителя или системы растворителей. Природа катионатэлектролита имеет исключительно большое .значение для успешного осуществления реакции электролитического восстановления. Обнаружено, что стереоконфигурация гексагидробензпираноксантенона формулы 1 в значительной степени зависит от того, какой конкретно электролит используется для проведения процесса. 79 В том случае, когда электролит представляет собой соль, катион которой образует сильно ассоциированную ионную пару (к таким катионам можно отнести катионы лития, натрия или калия) в результате электролитического восстановления получается продукт, преимущественно состоящий из гексагидробензпираноксантеиона, имеющего 5aj..-, .ба ,, и 13а| гконфигурацию. Напротив, электролит, имеющий катион, который образует слабо ассоциированную ионную пару (например соль четвертичного аммониевого основания или соль третичного амина), на правляет электролитическое восстанов ление таким образом, что получается пpoдyкJ, преимущественно состоящий из гексагидробензпираноксантенона,им ющего 5aJv-, 6aL-, IZaJc-, и 13а Ь-конфигурацию. Поскольку в большинстве случаев (L, «К, J-j- HSOMep является более активным анти-андрогенным веществом, чем соответствующий Jv/,А,р,-изомер, в качестве электролита при проведении электролитического восстановления ди гидробензпираноксантенонов наиболее предпочтительно использовать соль че вертичного аммониевого основания или соль третичного амина г Пример 1 . Получение (Sai, ба..,) -6,6а-дигидро-6,6-диметил-5аН, 13Н-/1/-бензпираыо(3,2-Ь)ксантен-13 -она. Раствор 30 г (0,25 моля) салицилового альдегида в 150 миллилитрах бензола охлаждают под азотом (после того, как его обрабатывают.сначала 26,25 г 0,37 моля пирролидина) и затем добавляют к нему при перемешивании 15 мл (0,25 моля) уксусной кислоты. Спустя 15 мин -к полученной смеси при бавляют при комнатной температуре 15 г (0,125. моля) 4,А-диметил-2,5-циклогексадиенона и реакционную смес нагревают при бОС в течение ночи. После охлаждения смесь выливают.в большой объем ледяной воды. Органический. слой отделяют и дважды промывают в делительной воронке 1%-ным водным раствором уксусной кислоты, а затем три раза - 1 М раствором гид роокиси натрия. После заключательной промывки органической фазы-насыщен ны раствором хлористого натрия органический раствор сушат над безводным сульфатом натрия. Далее растворитель 78 удаляют и продукт, полученный в остатке, перекристаллизозывают из смеси бензол - гексан. Выход после двух перекристаллизации составляет 18,6 грамма {kf)°4 от теоретически возможного). Полученный целевой продукт имеет т.пл. 211-213 С и идентифицирован по данным элементного анализа, ИК-УФ- и ЯМР-спектроскопии. Элементный анализ: Найдено,: С 79,76; Н 5,б9. С 22 Н ,8 О J. Вычислено, %: С 79,98; Н 5,9Пример 2. Получение , ,6а-дигидро-2,10-диметокси-6,6-диметил-5зН, 13Н-/.1/-бензпирано (3,2-Ь)ксантен-13 она. Раствор 12,5 г (82 ммоля) 5 метоксисалицилового альдегида в 100 мл бензола охлаждают под азотом после добавления 8,73 г (123 ммоля) пирролидина и прибавляют к нему t,92 грамма (82 ммоля) уксусной кислоты. После перемешивания смеси при,комнатной температуре в течение нескольких минут к ней прибавляют 5,0-г () 4,-диметил-2,5 Циклогексадиенсжа, Затем реакционную смесь нагревают под азотом при 60 С в течение ночи,после чего смесь охлаждают и выливают в . большой объем ледяной воды. Полученный при этом органический слой отделяют в делительной воронке и промывают последовательно разбавленной уксусной кислотой, несколько разбавленным раствором гидроокиси натрия и насыщенным раствором хлористого натрия. Затем органический слой сушат над безводным сульфатом натрия и растворитель удаляют в вакууме.Остаток дважды перекристаллизовывают из смеси бензола и, гексана. В итоге получают г (23) целевого продукта, имеющего т.пл. 219-220 С. Элементный микроанализ: НайденоД: С 73,95, И 5,38. С.. Вычислено,: С 73,83, Н 5,68. Пример 3. Получение (5aJ- 6аА.)-6,6а-дигидро-3 ,9 Диметокси-6,6-диметйл-5аН,1ЗН-/1/-бензпирйно (3,2-6)ксантен-13 она. Приготовляют раствор И,35 г (9«,4 ммоля) 4-метоксиалицилоеого альдегида в 100 мл бензола.Этот раствор охлаждают и прибавляют к нему последовательно 10 г (И ммоль) пирролидина и 5,66 г (9, ммоля) уксус,9 ной кислоты. Через несколько минут полученной смеси прибавляют 5 г (1 ммоль) ,-диметил-2,5 циклогёк садиенона. Затем реакционный, раство нагревают в течение ночи при 55 в атмосфере азота. После охлаждения полученную реакционную смесь выливают в большой объем ледяной воды, органический слой отделяют и последовательно промывают разбавленной у уксусной кислотой, несколько раз разбавленным раствором гидроокиси натрия и в заключение - насыщенным раствором хлористого натрия. Затем органический слой сушат Над безводным сульфатом натрия и упаривают в вакууме с целью удаления растворите ля. Остаток перекристаллизовывают и смеси бензол-гексан и хроматографируют на силикате магния, используя бензол в качестве элюента. Результаты элементного микроанализа продукта: Найдено,: CJ3,79i Н 5-,78.. Cj,А Н gtOs. Вычислено,: ,83; Н 6,68. Пример . Получение (5а, 6а.)-6,6а-дигидро-, 8-диметокси-6,6 -диметил-5аН,1ЗН-/1/-бензпирано (3,2-Б)ксантен-13 Она. Раствор 100 г (0,66 моля) сисалицилового альдегида в ВОО мл бензола охлаждаюь в атмосфере азота и прибавляют к нему последовательно 80 г (1,15 моля) пирролидина и 60 г (1,0 моль) уксусной кислоты. Спустя 15 мин к полученной смеси прибавляют при комнатной температур Q г (0,33 моля) Ц,4-диметил-2,5-циклогексадиенона, и смесь нагрева ют при 55-бО С в течение ночи. После охлаждения реакционную смесь выливают в большой объем ледяной воды Органический слой отделяют и дважды промывают 1%-ным водным раствором уксусной кислоты, а затем три раза 1М водным раствором гидроокиси натрия. После заключительной промыбки органической фазы-насыщенным раство ром хлористого натрия раствор сушат над безводным сульфатом натрия и упаривают в вакууме с целью удаления растворителя. Остаток после упа ривания перекристаллизовывают из ем си бензола и гексана. В итоге получают 43 г (33 от теории) целевого соединения - (5а|К.,,6а-дигидро-4,8-диметокси-6,6-диметил-5аН,.1 ЗН710-/1/-бензпирано(3,2-6)ксантен-13-она, имеющего т.пл. 23Э-2 Гс. Элементный микроанализ: Найдено,: С 73,79; Н 5,62. гц гаО :Вычислено,J: С 73,83 Н 5,68. Пример 6. Получение (5ai/, )-6 ,6а-дигидро-,8-диэтокси 6 ,6-диметил-5аН,13Н-/1/-бензпирано (3,2-6)ксантен-13 она. Раствор 1,0 г (2,76 ммоля) (5аЛ/, ) -6,6а-дигидро-, 8-ДИОКСИ-6,6-димeтил-5aH,13H-/1/-бeнзпиpaнo(3,2-й) ксантен-13-она из примера 8 в 25 мл о сухого гексаметилфосфотриамида обрабатывают 1 г (7,25 ммоля) карбоната калия и 2 мл (2,9 г, 27 ммолей) бромистого этила. Полученную смесь нагревают в атмосфере азота при 70 С в течение ночи. После охлаждения реакционную смесь выливают s 200 мл холодной воды. Образовавшийся продукт собирают и перекристаллизовывают дважды из смеси этанол вода. В итоге получают 0,5 г.( от теории) целевого (5а,)-6,6а-дигидро-4 ,8-диэтокси-6,6-диметил- 5вН, 13Н-/1/-бензпирано(3,2-&)ксантен-13 -она с т.пл. 211-213 С. - Элементный микроанализ: НайденоД С 7,92 Н 6,51. Сгб гб зВычислено,%:. С 7,62; Н 6,26. Пример 7- Получение (5 aJy, ) -6 ,6а-яигидро-6р-метил-6-этил-ЗаН,1ЗН-/1/-бензпирано(3,2-Ь)ксантен-13-она. К 220 мл бензола последовательно прибавляют при охлаждении на ледяной бане 18,2 г (Й8 ммолей) салицилово-. го альдегида, 13,3 г пирролидина и 8,9 г уксусной .кислоты. Затем к полученному раствору прибавляют 10,0 г (73,5 ммоля) 4-этил-«-метил-2,5 циклогексадиенона. Полученную смесь оставляют перемешиваться при 55°С в атмосфере азота на период, равный в общей сложности 5 дн. Затем реакционную смесь охлаждают и выливают в большой объем ледяной воды. Образовавшийся органический слой отделяют и дважды промывают водным раствором уксусной кислоты, три раза - 1-нормальным водным раствором гидроокиси натрия и один раз насыщенным водным раствором хлористого натрия. Промытый органический слой сушат над безводным сульфатом натрия и затем упаривают на роторном испарителе в вакууме с 119 целью удаления бензола. Остаток посл упаривания перекристаллизовывают в смеси бензол-гексан, в результате ч jTo получают 4,6 г (18,2% от теории) целевого соединения, имеющего т.пл. 189-190C. Элементный микроанализ: НайденоД: С 80,8; Н 6, 4 % Вычислено,: С 80,21J Н 5,85П-р им е р 8. Получение (., 6а()-6,6а-дигидро- ,8-диметокс.и-б -метил-6 ч.-этил-5аН, 13Н-/1/-бензпира но(3,2-6)ксантен-13-она. К 180 мл бензола последовательно прибавляют при охлаждении 18,10 г (119 ммолей) Зметоксисалицилового альдегида, 10,64 г пирролидина и 7,12 г уксусной кислоты. К полученному раствору прибавляют 8,00 г (58,6 ммоля) 4-этил-4-метил-2, логексадиенона. Полученную-.смесь пе ремешивают в течение двух дней в ат мосфере азота при . Затем реакционную смесь охлаждают и выливают в большой объем ледяной воды. Органический слой отделяют и промывают последовательно: два раза водным раствором уксусной кислоты, три раза 1 N раствором гидроокиси натри и один раз насыщенным раствором хлорис того натрия.Промытый органический сло сушат над безводным сульфатом натрия и упаривают на роторном испарителе в вакууме с целью удаления бензола. Остаток после упаривания хроматогра фируют на колонке с силикагелем с целью выделения (5а,6а)6,6а-дигидро-4,8-диметокси-6 -метил-6А--этил -5аН,13Н-/1/-бензпиранокЗ,2-6) сантен-13 она. Перекристаллизация сыро го продукта из смеси хлороформа и метанола дает 2,18 г (9.2% от теории) чистого целевого соединения, имеющего т.пл. 203-205С. Элементный микроанализ: Найдено,%: С 7,46, Н 5,.s Eitt s Вычислено С 7,24; Н 5,98. П р и м е р 9. Получение (5аЦ ,6а-дигидроспиро- 5аН, 1 ЗН-/1/ -бензпирано()ксантен-б,V -цикл гексан -1 . К 85 мл бензола прибавляют 7.52 (61,6 ммоля) салицилового альдегида 5,5 г пирролидина и 3,7 г уксусной кислоты. Смесь охлаждают на ледяной бане и прибавляют к ней 5.00 г (30,8 ммоля) 4-циклогексанспиро-2,5 712 -циклогексадиенона. Затем смесь оставляют на два дня при перемешивании (в атмосфере азота), поддерживая ее температуру на уровне 55°С. После охлаждения смесь выливают в большой избыток ледяной воды, образовавшийся органический слой отделяют и дважды промывают водным раствором уксусной кислоты, а затем трижды - 1 N раствором гидроокиси натрия. После заключительной промывки насыщенным водным раствором хлористого натрия органический слой сушат над безводным сульфатом натрия и упаривают на роторном испарителе в вакууме с целью удаления бензола. Остаток после упаривания перекристаллиэовывают из метанола. Однако значительная часть продукта остается при этом в маточной жидкости. Поэтому маточный раствор концентрируют и остаток хроматографируют на колонке с силикагелем, используя бензол в качестве элюента. Объединенный продукт (перекристаллизованное вещество и вещество, выделенное в результате хроматографии на силикагеле) перекристаллизовывают из смеси хлороформ метанол, в результате чего получают 3,62 г (32% от теории) целевого соединения, имеющего т.пл. 1б2-1бЗ с. Элементный анализ: Найдено,%: С 81,13Г Н 6,12. Сг5 а г Вычислено,%: С 81,Об; Н 5.99Пример 10. Получение (5э, 6а(р -6,6а-дигидро-6,6-диметил-5аН, 13Н-/1/-бензпирано(3,2-6)ксантен-13-она. Раствор 8,72 г (71,t ммоля) салицилового альдегида в 60 мл бензола охлаждают на ледяной бане и прибавляют к нему сначала 8,2 г (115 ммолей) пирролидина, а затем 4,7 г уксусной кислоты. После перемешивания смеси в течении 15 мин к ней прибавляют 4,36 г (35,7 ммоля) 4,4-диметил-2,5-циклогексадиенона, и реакционный раствор перемешивают в атмосфере ; азота при в течение ночи. После охлаждения реакционную смесь выливают в холодную воду и экстрагируют бензолом. Бензольные экстракты промывают сначала разбавленным водным раствором гидроокиси натрия, а затем насыщенным раствором хлористого натрия. После сушки экстракта над безводным сульфатом натрия растворитель удаляют в.вакууме. Сырой продукт,по139лученный в остатке после упаривания, перекристаллизовывают из смеси бензол-гексан, получают при этом две порции кристаллов общим весом 4,3 г представляющих собой целевой -изомер. Маточную жидкость упаривают досуха и остаток чистят хроматографией на колонке, заполненной 100 г силикагеля 1-й степени активности, при использовании бензола в качестве элюента. В процессе хро 1втографии из колонки элюируют три основные фра ции: первая фракция содержит дополни тельно 0,18 г чистого и 6aiL-M3o мера, вторая фракция содержит 0,97 Т смеси (1:2) 5аА,- и ба -изомера и целевого , 6ар -изомера, а третья фракция содержит 0,66 г чистого целе вого соединения, т.е. (,)-6,6a -дигидpo-6 ,6-диметил-5аН,1ЗН-/1/-бензпирано(3,2-Ь)ксантен-13-она. Этот продукт кристаллизуют из гексана и получают аналитический образец, имеющий т.пл. С. Элементный микроанализ: Найдено-,1: С 80,24; Н 5,61. °ьВычислено,%: С 79,98; Н 5,. Пример 11. Получение (S, )-6,6а-дигидро-6,6-диметил-5аН, 12Н-/1/-бензпирано(3,2-6)ксантен-13 -она. Раствор 50 мГд ()-6,6a-дигидpo-6,6-димeтйл-5aH, 1ЗН-/1/-бензпирано(3,2-Б)ксантен-13-она в 5 мл толуола кипятят с обратным холодильником в атмосфере азота в течение ночи.. Анализ образца реакционного раствора, выполненный методом тонкослойной хроматографии, показывает, что превращение исходного соединения в целевой продукт идет полностью. После этого растворитель отгоняют в вакууме и остаток пропускают через J короткую хроматографическую колонку с силикагелем, используя бензол в качестве элюента. Продукт (kB мг), выделенный из бензольного элюата, перекристаллизовывают из смеси бензол- гёксан и получают в итоге 5 мг целевого соединения с т.пл. 183 l8t°C. Этот продукт снова перекристаллизовывают из смеси бензола и гек сана, получая в результате чистое целевое соединение с т.пл. 211212 С. Пример 12. Раство.р 100 г (0,66 моля) Зметоксисалицилового .альдегида в 800 мл толуола охлаждают в ледяной бане и прибавляют к нему последовательно 60 г (0,85 моля) пирролидина и 39, г {0,66 моля) уксусной кислоты. Смесь охлаждают при ниже О С и прибавляют к ней при перемешивании kO г (0,33 моля) ,-диметил-2,5 Циклогексадиенона. Полученную смесь перемешивают в атмосфере азота в течение ночи, после чего .постепенно доводят ее температуру до комнатной. Далее реакционную смесь выливают в ледяную воду и органический слой промывают последовательно двумя порциями Г -ного водного раствора уксусной кислоты, тремя порциями 1М водного раствора гидроокиси натрия, несколькими порциями 1М соляной кислоты (до исчезновения окраски) , более чем тремя порциями 1М раствора гидроокиси натрия и одной порцией насыщенного раствора хлористого натрия. В ходе проведения этих операций по экстракции к органической фазе в качестве сооастворителя добавляют метиленхлорид. После высушивания органического раствору над безводным сульфатом натрия растворители отгоняют в вакууме и получают в остатке кристаллическое вещество, которое промывают гексаном и сушат на воздухе до .постоянного веса. В результате, получают 1 г кристаллического продукта (выход 11%), имеющего т.пл. 175 180°С расплав вещества немедленно вновь закристаллизовывается, как только убирают нагрев. Спектральное изучение этого продукта показывает, что он представляет собой практически чистое целевое соединение, содержащее в качестве примеси менее 5 6аА.-изомера. Все попытки удалить эту примесь путем осторожной перекристаллизации из смеси бензол-гексан оказались безуспешными . Элементный микроанализ: Найдено,4: С 7з,97; Н 5,76. .05. Вычислено,: С 73,83, Н 5,68. Пример 13- Получение (5зА., 6aiJ)-6 .ба-дигидро- ,8-диметокси-6 ,6-диметил-5аН,1ЗН-/1/-бензпирано (3,2-8)ксантен-13-она. Раствор 100 мг (5а.,6а)-6,6а-дигидро-|,8-диметокси-6,6-диметил-5аН-1ЗН-/1/-бензпирано(3,2-)ксантен-13 она в 5 мл бензола кипятят с обратным холодильником в атмосфере азо15та в течение ночи. Анализ образца раствора методом тонкослойной хрома тографии показывает, что реакция эпимеризэции идет полностью. После этого растворитель отгоняют в вакуу ме и остаток хроматографируют через короткую колонку с силикагелем, испоЛьзуя смесь 10% этилацетата в бен золе в качестве элюента.. Из элюата выделяют 89 . мг продукта, который дважды перекристаллизовывают. из сме си бензол-гексан, в итоге получают чистое целевое соединение с т.пл. 237-239С. Пример И. Получение (, , 12aJs, 13аА.)-6,6а-12,12а, 13a7l Тексагидро-,8-диметокси-6,6-диметил-5аН,.13Н: /1/-бензпир.ано(3,2-Ь) ксантен-13 она.. К 75 мл ацетонитрила, содержащего 5 воды, прибавляют 15.0 г п-толуол сульфонататрибутиламина и Ц,0 г бензойной кислоты. К полученной смеси прибавляют 1,0 г (5aik.,6а)-6,6а-дигидро- ,8-диметокси-6,6-диметил-5аН,1ЗИ-/1/-бензпирано(3,2-)ксантен- 13-она. Растворимость субстрйта при 25°С составляет примерноЛг5.мг/м поэтому внесенное вещество остается в реакционной смеси в виде суспензии Эту смесь помещают в катодное отделе ние электролитической ячейки, имеющей ртутный катод (в виде резервуара iCO ртутью) и платиновый анод. К ячей ке прикладывают-потенц иал 1,6 В (в с(завнении с насыщенным эталонным каломельным электродом) и процесс электролиза продолжают до тех пор,по ка анализ пробы реакционного раствора, выполненный методом тонкослойной хроматографии, не показывает,что реакция восстановления идет до конца. После этого реакционную смесь удаляют из электролити-ческой ячейки и упаривают в вакууме с целью удаления растворителя. Остаток после упаривания растворяют в этилацетате и полученный раствор промывают после довательно; три раза IN соляной кислотой, три раза насыщенным водным раствором бикарбоната натрия, три раза 1 N соляной кислотой, два раза насыщенным водным раствором бикарбоната .натрия и один раз водой. Анализ продукта Методом жидкостной хроматографии высокого давления показывает, что .образуется 65 (За.Цба-, , . 13аА)-6,6а, 12,12а, 13а, Й-гексагидро- 4,8-диметокси-6 ,6-диметил-5аН, 1 ЗН7 6-/1/-бензпирано(3,2-Ь)ксантен-13-она. Этилацетат отгоняют в вакууме, а продукт, полученный в остатке, сушат до постоянного веса. Этот продукт перекристаллизовывают из смеси метанола и хлороформа, в результате чего получают с выходом 50 от теории целевой продукт, имеющий степень чистоты 90%. Пример 15- Получение (5аЯ, 6adL, 12а, 13aj2,) -6, 6а, 12,12а , 13а , U-гексагидро-,8-диметокси-6,6-диметил-5аН,13Н-/1/-бензпирано(3,2-Ь) ксантен-13 она. Используя методику, аналогичную описанной в примере 1, приготовляют смесь 0,8 г перхлората лития и,0мл ледяной уксусной кислоты в 75 мл ацетонитрила, содержащего в своем составе 5% воды. К полученной смеси прибавляют 1,0 г (.,,6a-дигидpo-,8-димeтoкcи-6,6-димeтил-5aH, 13Н-/1/-бензпирано(3,2-)ксаитен-13-она. Полученную таким образом смесь подвергают электролитическому восстановлению на ртутном катоде и платиновом аноде при 25 С и постоянном электрическом потенциале (1,5 В) установленном относительно насыщенного каломельного электрода, используемого в качестве, эталона. Контроль полноты протекания реакции электролитического восстановления осуществляют методом тонкослойной хроматографии. Дальнейшая обработка реакционной смеси с целью выделения продукта.восстановления и перекристаллизации этого продукта из .смеси хлороформ - метанол приводит к получению целевого (5aJv,, . , 12ajb, 13а/5.)-6, 6а, 12,12а, 13,1 -гeкcaгидpo-,8-димeтoкcи-6,6-димeтил-5aH,13H-/l/-бeнзпиpaнo(3,2-Б)кcaнген-13-она в виде пластинчатых кристаллов, имеющих кремовую окраску. Зыход продукта составляет 6S% от теоретически возможного, причем продукт имеет степень чистоты. Т.пл. этого продукта 235-2 5С. Пример. 16. Получение {5aJ, ,12ai, 13aJL.) -6,6а, 12 ,12а, 1 За, 14-гексагидро-,8-диметокси-6,6-диметил-5аН,13Н-/1/-бензпирано(3,2-8)ксан- . Тбн-13-она. Используя методику, аналогичную описанно.й в примере 2, к 50 мл N,N-диметилформамида, содержащего .5 воды прибавляют 2 г бензойной кислоты и такое количество перхлората тетрабутиламмония, которое достаточно для достижения 0,2 М концентрации раство179pa. Затем к полученной смеси прибавляют 100 мг (5at,6aA.)-6,6a-дигидpo-4,8-димeтoкcи-6,6-димeтил-5aH, 13Н-/1/-бензпирано(3,2-6)ксантен-13 она Полученную смесь подвергают электролитическому восстановлению на ртутном катоде при 25°С и постоянном (ра ном 1,5 в) электрическом потенциале (измеренном в сравнениис эталонным насыщенным каломельным электродом). Последующая обработка реакционной см си и перекристаллизация выделенного сырого продукта приводит к получению целевого (,, 12a(L, 1 3a.JO-6,6a, 12 12а, 13а, 1+-гексагидро-,8-диметокси-6,6-диметил-5аН,13Н-/1/-бензпирано (3, 2-6) ксантен-1 Зона с выходом 70%. Пример 17. Получение (SaJv, 6а J., , 1 ) -6,6а, 12 ,12а, 13а, 1 i -гексагидро-,8-диметокси-6,6-диметил-5аН,1ЗН-/1/-бензпирано(З,2-Ь) ксантен-13 она. , Используя методику,. аналогичную описанной в примере 1, к смеси 6О мл метанола и ,8 мл ледяной уксусной кислоты прибавляют тетрабутиламмоний хлорид в количестве, достаточном для достижения 0,1 М концентрации. Далее к полученной смеси прибавляют 100 мг ()-6.,6-дигидро-4,8-диметокси-6,6а-дигидро-4,8-диметокси-6,6-диме тил-5аН,1ЗН-/1/-бензпирано(3,2-Ь) ксантен-13 она. Приготовленную таким образ зм смесь подвергают электролити ческому восстановление на ртутном катоде при 25°С и постоянном 1,k В пот-.енциале (в сравнении со стандартным насыщенным каломельным электродом) . Последующая обработка реакцион ной смеси и перекристаллизация выделенного сырого продукта приводит к получению целевого (a,, .. )-6,6а, 12,12а, 13а, 14-гексагидр о-k,8-диметокси-6,6-димetил-5aH,1зП-/1/-бензпираио(3,2-6)ксантен-13 она с выходом 85% от теории. П р и м ер 18. Получение (5а(., 6а)-, 12aJL, 1 За -)-6, 6а-12,12а, 1 За, 1t-гексагидро-,8-диметокси-6,6 диметил-5аН,13Н-/1/-бензпирано(3,2-Ь)ксантен-13 она. Используя методику примера 1 , к смеси 75 мл ацетонитрила, содержащего 5% уксусной кислоты, прибавляют меТилтриоктиламмонийхлорид в количестве, достаточном для создания 0,1 М концентрации. К полученной ,; смеси прибавляют затем 200 мг ( .ба-дигидро- ,8-диметокси-6,6718-диметил-5аН,13Н-/1/-бензпирано (3,2-и)ксантен-13 она.Приготовленную таким образом смесь подвергают электролитическому восстановлению на ртутном катоде при и постоянном 1,6 В потенциале (в сравнении с эталонным насыщенным каломельным электродом) . Анализ реакционного раствора методом жидкостной хроматографии высокого давления показывает наличие в ней целевого (, баА,, , 13аА,) -6,6а-12,12а, 13а, Й-гексагидро-,8-диметокси-6,6-диметил-5аН,1ЗН-/1/-бензпирано(3,2-6)ксантен-13 она в количестве, соответствующем выхода. Пример 19. Получение . (, 6а J-, , )-6, 6а, 12,12а, 1 За , 1 it-гексагидро-, 8-диметокси-6 ,6-диметил-5аН,13Н-/1/-бензпиран©(3,2-6) ксантен-13 она. Используя методику примера 1, к смеси 67 мл ацетонитрила, содержащего 5% воды и 5,5% уксусной кислоты, при бавляют тозилат М,М-диизопропилзтиламина в количестве 0,1 М, далее к полученной смеси прибавляют 100 мг (5аЛ,6а)-6,6а-дигидро-А,8-диметокси-6,6-диметил-5аН,1ЗН-/1/-бензпирано (3,2- 6) ксантен- . Приготовленную таким образом смесь подвергают электролитическому восстановлению на ртутном катоде при и постоянном 1,5 В потенциале (в сравнении с эталонным насыщенным каломельным электродом). Анализ реакционной смеси методом жидкостной хроматографии высокого давления показывает присутствие в ней целевого (,6a(L, / , 13ai)-6,6a,12Л2a,13a,1 -гeкcaгидpo-4,8-диметокси-6,6-диметил-5аН, 13Н-/1/-бензпирано(3,2-&)ксантен-13 -она в количестве 60-65% от выхода. Пример 20. Получение (aji баЛ.) -6,6а-дигидро-3,9 дициано-6,6-диметил-5аН,1ЗН-/1/-бензпирано {3,2-6)ксантен-13 она. Аналогично примеру 1 проводят реакцию между -цианосалициловым альдегидом и 4, -диметил-2,5 циклогексадиеноном в присутствии пирролидина и уксусной кислоты. Продукт выделяют и очищают в соответствии с примером 1. Получают (5a()v.,,6a-дигидpo-3,9ДИЦиaнo-6,6-димeтил-5aH, 13Н-/1/-бензпирано 3,2- ксантен13-она с выходом 50% от теории. Пример 21. Получение (), 13ad)-6,6a,-12J2a, 13а, -гексагидро-4,8 диметокси-6,6-диметил-5аН,13Н-/1/-бензпирано(3,2-6) ксантен-13 она. Используя методику примера 1,приготовляют смесь 2,57 г перхлората тетрабутиламмония и 2,5 г бензойной кислоты в 50 мл толуола и 25 мл мета нола. К полученной смеси прибавляют 300 мг (5а(К.,,6а-дигидро-,8-ди метокси-6,6-диметил-5аН,1ЗН-/1/-бензпирано(3,2-6)ксантен-13 она. Приготовленную таким образом смес подвергают электролитическому восста новлению на ртутном катоде при 25С и постоянном 1,6 В потенциале в сравнении -с эталонным насыщенным каломельным электродом. Последующая обработка реакционной смеси и перекристаллизация выделенного сырого продукта приводит к получению целево го ., 12a.k;i3a v)-6,6a,12,12a, 13а,14-гексагидро-4,8-диметокси-6,6-диметил-5аН,13Н-/1/-бензпирано (3,2-6)ксантен-13-она с выходом 85% от теории. Пример 22, Получение (5аЛ,| 6а 12а/ За)-6,6а, 12,12а, 1 За , Й-гёксагидро-,8-диметокси-6,6-диметил-5аН, 13Н7/1/-бензпирано ( 3,2-й) ксантен-13-она. Используя .методику примера 1, к смеси 75 мл ацетонитрила, содержащего 5% уксусной кислоты и 5 воды, прибавляют тетра н-гек иламмонийхлорйд в количестве, достаточном для создания 0,1 М концентрации. Затем к полученной смеси прибавляют 200.мг (,) -6,6а-дигидро-и, 8-диметокси -6,6-диметил-5аН,1ЗН-/1/-бензпирано )ксантен-13-она, после чего эту смесь подвергают электролитическому восстановлению на ртутном катоде при и постоянном ,1,7 В потен циале (в сравнении с эталонным насыщенным каломельным электродом). Анализ реакционного раствора методом жидкостной хроматографии высокого . давления показывает присутствие в 4ней целевого (,, , 13а)-6,6 12,IZa,13а,1 -гексагидро-,8-диметок си-6,6-диметил-5аН,1ЗН-/1/-бензпирано (3,2- S) ксантен- 13 -она с выходом 65-701 от теории. Соединения формулы оказывают эффективное анти- андрогенное действие в дозах 0, мг на килограмм веса тела (имеется в виду дневная доза). Предпочтительно, чтобы лекарст720венные формы выпускались в такой до-: зировке, когда единица дозы (например одна таблетка или капсула) содержит 1-500 мг активного соединения. Наиболее предпочтительны, в частности, те единичныедозировки препарата, которые содержат 50-250 мг активного ингредиента. Предпочтительно соединения формулы 1 вводились перорально. Анти-андрогенная активность этих соединений иллюстрируется результатами стандартных биологических испытаний на крысах при использовании в качестве подопытных животных кастрированных неполовозрелых самцов крыс. Итак, биологические испытания проводятся при использовании неполовозрелых самцов крыс, обычно в возрасте 21 дн., которых подвергают двухсторонней (билатеральной) кастрации и оставляют без лечения на срок, равный трем дням. Это обеспечивает достаточное время для метаболизма эндогенных андрогенов и для атрофии вторичных половых органов (прежде всего). Далее кастрированных самцов крыс разделяют по крайней мере на три лечебные группы. Десяти крысам инъектируют подкожно, один раз в день, 0,02 мг пропионата тестостерона (ПТ), суспендированного в куку узном масле. Эти крысы служат в качестве контрольной группы животных, стимулированных андрогенным веществом, т.е. в качестве андроген-стимулированной контрольной группы. Другой группе из пяти крыс инъектируют подкожно, один раз каждый день (в течение всего срока эксперимента),чистое кукурузное масло, так что эта группа крыс составляет контрольную группу кастратов. Третья группа крыс, участвующих в испытаниях, состоит из пяти особей, каждая из которых получает подкожно 0,02 мг ПТ и соответствующее испытуемое соединение, либо пероральным путем, либо с помощью подкожной инъекции, один раз каждый день. Для проверки каждого соединения, подвергаемого испытанию на биологическую активность, и каждого уровня дозы используют отдельную группу подопытных животных. Всеживотные подвергаются указанной обработке без перерыва в течение семи дней. На восьмой день всех крыс, которым к этому дню исполняется 23 дн, умерщвляют (забивают)- и подвергают 219 вскрытию, в процеоре аутопсии (вскр тия) из трупов удаляют Именные пузырьки и вентральные предстательные железы, которые вз.вешивают. Вес семенных пузырьков (СП) и вентральных предстательных желез (ВПЖ) контрольной группы кастратов вычитается из веса СП и ВПЖ андроген стимулированной контрольной группы для того, чтобй определить степень андрогенной стимуляции, которая имела место в результате экзогеннного |Введения крысам контрольной группы ПТ.Все СП и ВПЙ каждой экспериментально группы животных, которым вводили испытуемые соединения, вычитается из веса СП и ВПЖ андроген-стимулированной группы крыс, и полученная раз ница делится на привес соответствующего органа, который имел место в ре зультате введения крысам одного тест стерон-прописЗната. Полученное частно 722 от деления выражают JB процентах и именуют степенью ингибирования или процентом ингибирования. Эффект от введения испытуемых соединений или, иначе говоря, влияние каждого введенного соединения на эффект андрогенной стимуляции, вызванной введением тестостерон-пропионата, доказывается и иллюстрируется отсутствием привеса эндокринных желез у крыс, которые наряду с андрогенным стимулятором (тестостерон-пропионатом) получали испытуемое соединение, проверяемое на анти-андрогенную активность, по сравнению с привесом тех. же органов у крыс, подвергшихся одной только андрогенной стимуляции тестостерон-пропионатои. Таблица демонстрирует андрогенингибирующую активность соединений формулы 2.
л
,
Z Q. О е5S
s г tt) I
u о о
о
о
I ffl
S :
H: ai
ПЗ
c;
fD
I
CJ
I.
о a
cr
r о
s
VI
О
«
сэ
-Л- I
т
(О
о
Ч)
сг
vO
ш
эе
-:Г I
0)
OQ
S
0)
I
W
о
о
I
т ct
rrv со rf
о
о L.
о
Z
-3ил
ГО
г I vO
г I
I
О LA
оо ил I
ts г- I 0
I
о
о
о
о
с
р о
гл
rf
CJ сэ
о о













ч
QX
г та
- ги
-« ( -г ГА
к
ПЗ гта -
, та 3-vD I
53-.
-ill
m о.
-6 ПЗ Т) N
та CN4
X LA ,ил -
оо о.
о о.
о
ct
ct
S
о
|
1 та о
0)
tD
о.
о i: и.
О)
4)
сЛ
з:
т: о о
rf
л X з:
t) о
л:
X
о
(-3
о
о
I
1:
S
ct
I оо
со
I
1с
(U
о.
НU2
СК
Ота та
SГ с
-
- та
г та л та
- ГА
- ГА
ГА
- та
-6 ОА
г та
-i ГА
- ГА
та -
та -
-
:-i
та - 1vO г
та -f
J--4 та - та - та
-i 3 та tvi
та fM
csi
та tsi ил - ил г-
та см ил -
ил -
О
О
о о.
а ее
о о.
о. ct ct ct з: | та о i:
S
S
S
и
tj о i:
Т)
о Si ш
та о i: а
О)
D
f
гО
X
пг
о
) -J
ё
«Л а:
Л1
л
ш: ( { ()
г X О
X
о о
S
ct
I
со
..4Г Формула -изобретения Способ получения производных гексагидробензпираиоксантенонов общей формулыУя, о „ Yt где ,R - Cj-С 1 -алкокси, причем оба ра дикала идентичны и расположены симметрично, R и R -метил, X , X , X , У и У - атомы водорода при условии, что X и X находятся в -конфигурации или в -конфигурации, а радикал R отличающийся тем,что,соед нение формулы 7 где R,R,R« Хс и Xd имеют указанные значения, подвергают электрохимическому восстановлению в органической или водноорганической среде при температуре окружающей среды на ртутном катоде в присутствии источника протонов с величиной рКа 2-6 и электролита,выбранного из группы, которая включает в себя соли щелочных металлов, соли четвертичных аммониевых оснований с содержанием атомов углерода в катионном остатке 10-25 или соли третичного амина с содержанием атомов углерода в катионном остатке . Источники информации, принятые во внимание при экспертизе 1. Эльдерфильд Р. Гетероциклические соединения. М., изд. И-Л. , Э5, т. 2, с. 271.
Авторы
Даты
1982-05-07—Публикация
1979-09-06—Подача